文章信息
- 何呈燕, 李依雯, 甘玲, 王珏, 薛海波
- HE Chengyan, LI Yiwen, GAN Ling, WANG Jue, XUE Haibo
- PI3K/AKT/mTOR信号通路通过调控Th17细胞分化参与EAT小鼠甲状腺自身免疫损伤
- PI3K/AKT/mTOR signaling pathway participates in thyroid autoimmune injury of EAT mice by regulating Th17 cells differentiation
- 中国医科大学学报, 2024, 53(11): 972-978
- Journal of China Medical University, 2024, 53(11): 972-978
-
文章历史
- 收稿日期:2023-11-23
- 网络出版时间:2024-11-21 14:32:22
自身免疫性甲状腺炎(autoimmune thyroiditis,AIT)是一种常见的器官特异性自身免疫性疾病,其主要特点为甲状腺内淋巴细胞浸润、滤泡细胞破坏及血清甲状腺自身抗体水平升高,最终进展为甲状腺功能减退[1]。AIT确切的发病机制尚未阐明,其中,B和T细胞亚群的功能异常被认为在破坏免疫稳态和启动自身免疫级联反应中发挥至关重要的作用[2]。然而,目前针对AIT尚无有效的治疗手段,常规治疗以激素替代为主。Th17细胞为一种新型CD4+辅助性T细胞亚群,可分泌多种细胞因子,介导针对细胞外细菌和真菌的免疫反应[3]。研究[4]发现,桥本甲状腺炎(hashimoto thyroiditis,HT)患者外周血中Th17细胞比例及白细胞介素(interleukin,IL)-17A浓度显著升高,并与疾病的严重程度呈正相关,提示Th17细胞可能参与AIT的发病。磷脂酰肌醇-3-激酶/蛋白激酶B/雷帕霉素靶蛋白(phosphatidylinositol 3-kinase/protein kinase B/mechanistic target of rapamycin kinase,PI3K/AKT/mTOR)信号通路是细胞内关键的信号转导途径,在细胞的生长、转移、存活、代谢等生物学过程中扮演重要角色[5]。研究[6]发现,PI3K/AKT/mTOR信号通路通过调控Th17细胞分化参与多种自身免疫性疾病的发生发展。目前,甲状腺球蛋白(thyroglobulin,Tg)诱导的实验性自身免疫性甲状腺炎(experimental autoimmune thyroiditis,EAT)是HT的理想动物模型[7],模型成功的指标包括血清中以甲状腺球蛋白抗体(thyroglobulin antibody,TgAb)为代表的高水平自身抗体的存在及甲状腺组织中大量淋巴细胞浸润。本研究通过给予EAT小鼠模型PI3K抑制剂LY294002阻断PI3K/AKT/mTOR信号通路,探讨PI3K信号通路对EAT小鼠Th17细胞表达及甲状腺自身免疫损伤的影响。
1 材料与方法 1.1 实验动物雌性C57BL/6小鼠(6~8周,体质量18~20 g)购自济南朋悦实验动物繁育有限公司,生产许可证号:SCXK(鲁)20190003,饲养于滨州医学院附属医院SPF级动物房,进食饮水自由,环境温度为19~22 ℃,湿度维持在50%左右。适应性喂养1周后开始实验。本研究获得滨州医学院附属医院动物伦理委员会批准(20220128-73)。
1.2 主要试剂和仪器猪甲状腺免疫球蛋白(porcine thyroid immnunoglobulin,pTg)、完全弗氏佐剂(complete freund’s adjuvant,CFA)、不完全弗氏佐剂(incomplete freund’s adjuvant,IFA)购自美国Sigma-Aldrich公司;LY294002购自美国MedChemExpress公司;小鼠TgAb ELISA试剂盒购自武汉华美生物工程有限公司;小鼠IL-17A酶联免疫吸附试验(enzyme linked immunosorbent assay,ELISA)试剂盒购自武汉伊莱瑞特生物科技股份有限公司;小鼠脾脏组织单个核细胞(spleen mononuclear cells,SMCs)分离液试剂盒购自天津灏洋生物制品科技有限责任公司;苏木素-伊红(hematoxylin and eosin,HE)染色试剂盒、4%多聚甲醛、中性树胶、RIPA裂解液、PMSF蛋白酶抑制剂、BCA蛋白浓度测定试剂盒、TBST缓冲液、佛波酯、布雷非德菌素A、钙离子霉素购自北京索莱宝科技有限公司;APC-CD4、PE-IL-17A单克隆抗体购自美国Biolegend公司;兔二步法检测试剂盒、DAB显色试剂盒购自北京中杉金桥生物技术有限公司;BSA、Tris、甘氨酸、SDS均购自德国biofroxx公司;p-AKT(Thr308)、p-AKT(Ser473)、p-mTOR(Ser2448)、S6K1、S6K2、IL-17A、β-actin抗体均购自美国Cell Signaling Technology公司;超敏ECL化学液购自大连美仑生物技术有限公司;Multiskan TMFC酶标仪购自美国Thermo Fisher Scientific公司;FACS Calibur流式细胞仪购自美国BD公司。
1.3 方法 1.3.1 实验动物分组24只雌性C57BL/6小鼠被随机分为正常对照(NC)组、EAT组和LY294002干预组(LY294002 25 mg/kg、50 mg/kg),每组6只。
1.3.2 EAT模型的建立将pTg溶于PBS中配成母液(2 mg/mL),EAT组及LY294002干预组小鼠第1周给予100 μL CFA充分乳化的pTg多点皮下注射,第2~8周给予IFA乳化的再次免疫制剂加强免疫,不同浓度LY294002干预组小鼠自造模第5周于免疫制剂皮下注射前30 min给予LY294002(25 mg/kg、50 mg/kg)腹腔注射,2次/周,共给药4周。所有小鼠在第8周末麻醉处死。
1.3.3 小鼠甲状腺组织HE染色取小鼠甲状腺组织,于4%多聚甲醛中固定、脱水、透明、包埋、制作4 μm厚度切片,根据HE染色试剂盒进行染色,拍照。根据淋巴细胞浸润程度进行炎症严重程度评分。0,正常;1,1%~10%;2,> 10%~30%;3,> 30%~50%;4,> 50%。
1.3.4 小鼠甲状腺组织免疫组织化学染色小鼠甲状腺组织制备成4 μm石蜡切片,梯度乙醇脱蜡后用抗原液进行修复,PBS洗涤,分别加入CD4、IL-17A抗体4 ℃孵育过夜,PBS洗涤3遍,二抗室温孵育20 min,最后DAB显色,拍照。为排除组织内源性物质引起的假阳性反应,设置了Control组,除不加一抗用PBS代替外,处理方法与其他待测切片一致。
1.3.5 血清TgAb滴度及IL-17A水平的ELISA检测小鼠心脏取血,室温静置30 min,离心,收集上清,按照小鼠TgAb及IL-17A ELISA试剂盒说明书的操作步骤进行检测和计算。
1.3.6 脾指数计算称量小鼠体重及脾脏重量,计算脾指数,脾指数(mg/g)=脾脏重量/体重。
1.3.7 小鼠SMCs悬液的制备取小鼠新鲜脾脏,按照小鼠SMCs分离液试剂盒说明书进行操作,最后将细胞重悬于2 mL RPMI 1640培养基中(含10%FBS),调整细胞密度为1×106/mL。
1.3.8 SMCs中Th17细胞比例的流式细胞术检测取SMCs悬液1 mL加入12孔板,用含有佛波酯、钙离子霉素的1 mL细胞培养基重悬细胞,于37 ℃、5%CO2培养箱中培养1 h,加入布雷非德霉素A,培养4 h后收集细胞。APC-CD4抗体进行表面染色,固定破膜后用PE-IL-17A抗体核内染色,上机检测。
1.3.9 脾脏组织中p-AKT(Thr308)、p-AKT(Ser473)、p-mTOR(Ser2448)、S6K1、S6K2、IL-17A蛋白表达水平的Western blotting检测取0.1 g小鼠脾脏组织,加入RIPA裂解液以及PMSF、磷酸酶抑制剂Ⅱ、磷酸酶抑制剂Ⅲ研磨提取总蛋白,BCA法测定蛋白浓度,将各组蛋白浓度调至一致。煮沸变性,SDS-PACE电泳分离蛋白、转膜、封闭,加入p-AKT(Thr308)(1∶1 000)、p-AKT(Ser473)(1∶1 000)、p-mTOR(Ser2448)(1∶1 000)、S6K1(1∶1 000)、S6K2(1∶1 000)、IL-17A(1∶1 000)、β-actin(1∶10 000)一抗4 ℃孵育过夜,TBST洗膜,二抗室温孵育45 min,洗膜、显影,采用ImageJ软件进行灰度值比较。
1.4 统计学分析采用SPSS 24.0统计学软件与GraphPad Prism 8.0分析数据。符合正态分布且方差齐的计量资料以x±s表示,多组间均数采用ANOVA单因素方差分析进行比较,组间两两比较采用LSD检验,采用Pearson相关分析检测不同指标间的相关性。P < 0.05为差异有统计学意义。
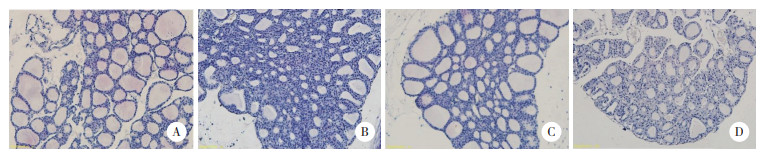
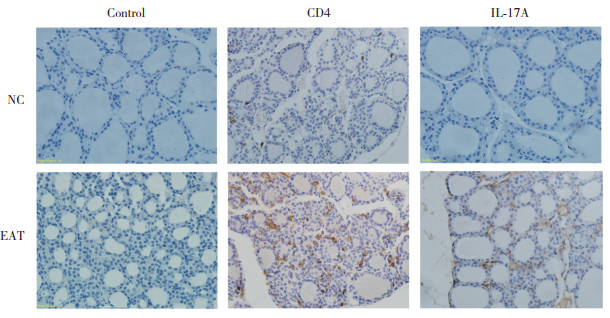
2 结果 2.1 小鼠甲状腺组织炎症程度评估显微镜下观察,NC组小鼠甲状腺组织滤泡大小较为均一,结构完整,无明显炎症细胞浸润;EAT组小鼠甲状腺组织可见滤泡萎缩、破坏,大小差异明显且不规则,间质纤维组织明显增生,并有不同程度的淋巴细胞浸润。LY294002干预组小鼠甲状腺滤泡萎缩程度减轻,淋巴细胞浸润面积减少,并呈浓度依赖性(图 1)。进一步分析EAT组和NC组小鼠甲状腺组织免疫组织化学染色结果,发现EAT组小鼠甲状腺组织中CD4和IL-17A的表达明显高于NC组,证实EAT组小鼠甲状腺组织中有Th17细胞浸润(图 2)。
|
| A,the thyroiditis score of the NC group is 0;B,the thyroiditis score of the EAT group is 4;C,the thyroiditis score of the LY294002 25 mg/kg group is 3;D,the thyroiditis score of the LY294002 50 mg/kg group is 2. 图 1 各组代表性小鼠甲状腺组织HE染色结果 ×200 Fig.1 Representative HE staining results of thyroid tissue in the different groups ×200 |
|
| 图 2 各组代表性甲状腺组织免疫组化染色结果 ×400 Fig.2 Representative immunohistochemical staining results of thyroid gland in different groups ×400 |
2.2 各组小鼠脾指数比较
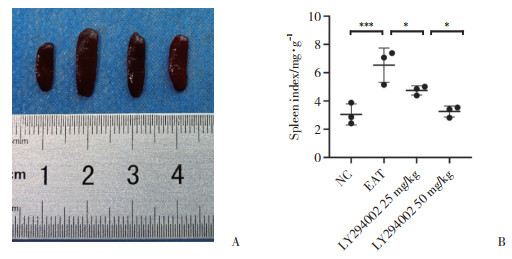
与NC组小鼠相比,EAT组小鼠脾脏体积显著增大,而LY294002组小鼠脾脏体积较EAT组减小(图 3A)。计算各组脾指数,结果显示,EAT组小鼠脾指数显著高于NC组(P < 0.001),LY294002干预后,脾指数明显下降,LY294002 25 mg/kg组小鼠脾指数与EAT组及LY294002 50 mg/kg组相比,均有统计学差异(P < 0.05,图 3B)。
|
| A,spleen volume of mice;B,spleen index of mice. *P < 0.05,***P < 0.001. 图 3 各组小鼠脾脏体积及脾指数 Fig.3 Spleen volume and spleen index of mice in different groups |
2.3 各组SMCs中Th17细胞比例比较
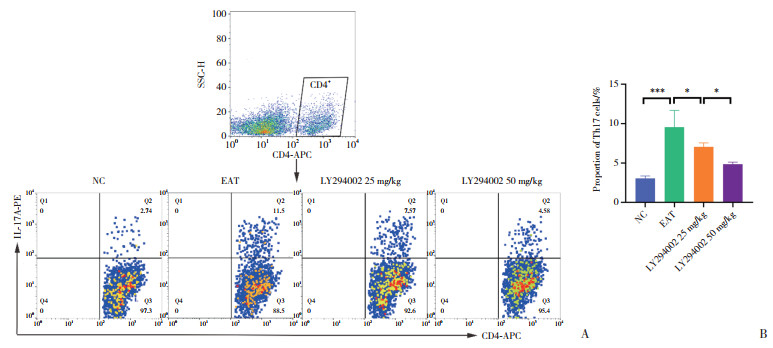
与NC组相比,EAT组SMCs Th17细胞比例显著升高(P < 0.001);与EAT组相比,LY294002 25 mg/kg组Th17细胞比例下降,有统计学差异(P < 0.05),且随着LY294002浓度升高Th17细胞比例下降更明显,LY294002 25 mg/kg组与LY294002 50 mg/kg组Th17细胞比例有统计学差异(P < 0.05),见图 4。
|
| A,representative flow cytometry analysis charts of SMCs in different groups;B,proportion of Th17 cells in SMCs in different groups. *P < 0.05,***P < 0.001. 图 4 各组SMCs中Th17细胞比例 Fig.4 The proportion of Th17 cells in SMCs in different groups |
2.4 各组血清TgAb、IL-17A水平的比较
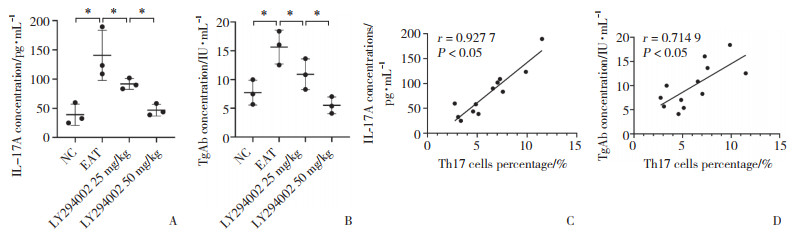
ELISA分析结果显示,EAT组IL-17A(图 5A)及TgAb(图 5B)浓度均较NC组显著升高(P均 < 0.05),LY294002 25 mg/kg组IL-17A及TgAb浓度较EAT组下降(P均 < 0.05),LY294002 50 mg/kg组浓度下降更明显,且与LY294002 25 mg/kg组有统计学差异(P均 <0.05)。将所有实验小鼠血清中IL-17A浓度及TgAb滴度与SMCs中Th17细胞比例进行相关性分析,结果表明两者均与Th17细胞比例呈正相关(图 5C、5D,r = 0.927 7和r = 0.714 9)。
|
| A,concentrations of serum IL-17A in different groups;B,concentrations of serum TgAb in different groups;C,correlation between the proportion of Th17 cells in SMCs and serum IL-17A concentrations;D,correlation between the proportion of Th17 cells in SMCs and serum TgAb concentrations. *P < 0.05. 图 5 血清IL-17A及TgAb浓度及其与SMCs中Th17细胞比例相关性分析 Fig.5 The concentrations of serum IL-17A and TgAb, and their correlation with the proportion of Th17 cells in SMCs |
2.5 各组小鼠脾脏组织p-AKT(Thr308)、p-AKT(Ser473)、p-mTOR(Ser2448)、S6K1、S6K2、IL-17A蛋白表达水平的比较
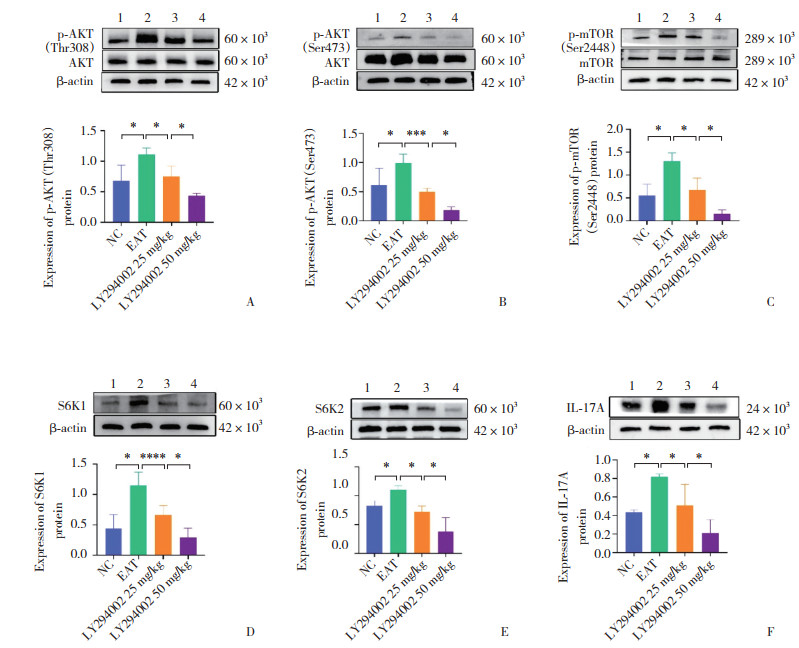
EAT组小鼠脾脏组织p-AKT(Thr308)、p-AKT(Ser473)、p-mTOR(Ser2448)、S6K1、S6K2、IL-17A蛋白相对表达水平明显高于NC组(P均 < 0.05)。与EAT组比较,LY294002 25 mg/kg组上述蛋白表达下降,有统计学差异(P均 < 0.05)。与LY294002 25 mg/kg组比较,LY294002 50 mg/kg组p-AKT(Thr308)、p-AKT(Ser473)、p-mTOR(Ser2448)、S6K1、S6K2、IL-17A蛋白表达水平下降更加明显(P均 < 0.05)。见图 6。
|
| A,p-AKT(Thr308);B,p-AKT(Ser473);C,p-mTOR(Ser2448);D,S6K1;E,S6K2;F,IL-17A. 1,NC group;2,EAT group;3,LY294002 25 mg/kg group;4,LY294002 50 mg/kg group. *P < 0.05,**P < 0.01,***P < 0.001. 图 6 各组小鼠脾脏组织信号通路相关分子蛋白表达水平 Fig.6 Expression levels of signaling pathway-related proteins in spleen tissue of mice from each group |
3 讨论
AIT为常见的自身免疫性甲状腺疾病。目前,Tg联合佐剂诱导EAT小鼠因造模方法简单、模型成功率较高、结果稳定而被广泛认可。Th17细胞为一种新型CD4+ Th细胞亚群,可分泌IL-17A、IL-17F、IL-21、IL-22等多种细胞因子[8],目前已被证明与银屑病、类风湿性关节炎、炎症性肠病等多种自身免疫性疾病的发病相关[3, 9-10]。本课题组前期研究[4, 11]发现Th17细胞参与AIT发病,并与疾病的严重程度呈正相关。另有研究[12]发现IL-17促进了AIT患者甲状腺组织的间质纤维化。因此,Th17细胞及其效应细胞因子IL-17A在AIT自身免疫损伤的发病机制中发挥重要作用。
PI3K/AKT/mTOR信号通路是控制细胞基本功能最关键的细胞内信号通路之一,此通路的异常激活可见于肿瘤、自身免疫性疾病、纤维增生性疾病等多种疾病[13]。PI3K属于脂质激酶家族,包括Ⅰ、Ⅱ、Ⅲ 3种类型。LY294002是一种PI3K的广谱抑制剂[14]。目前对Ⅰ类PI3K的研究较多,当感应到细胞外生长因子和细胞因子时,PI3K被招募到质膜上,并被受体酪氨酸激酶或G蛋白偶联受体激活,磷酸化磷脂酰肌醇第3位羟基,催化磷脂酰肌醇-4,5-二磷酸(phosphatidylinositol-4,5-bisphosphate,PIP2)转化为磷脂酰肌醇-3,4,5-三磷酸(phosphatidylinositol-3,4,5-trisphosphate,PIP3)。PIP3充当第二信使,收集含有PH结构域的分子,并将其携带至细胞膜上,包括3-磷酸肌醇依赖性蛋白激酶1(3-phosphoinositide-dependentproteinkinase-1,PDK1)和AKT [15]。第10号染色体磷酸酶和张力蛋白同源丢失性基因编码的产物-同源性磷酸酶-张力蛋白是PI3K/AKT信号通路的负调控因子,能够将PIP3去磷酸化生成PIP2 [16]。AKT是丝氨酸苏氨酸激酶的一种,结构上含有PH结构域,未活化的AKT通过其PH结构域与PIP3结合被招募到细胞膜上,而后PDK1和mTORC2分别将AKT的Thr308和Ser473位点磷酸化,最终彻底激活AKT[17]。mTOR是一种进化上高度保守的苏氨酸/丝氨酸蛋白激酶,参与细胞增殖、存活、自噬、代谢和免疫等多种生物过程[18]。PI3K/AKT/mTOR信号通路可以通过多种不同的途径调控Th17细胞分化,包括缺氧诱导因子1α表达、生长因子独立性1下调以及RORγt通过S6K1/S6K2途径的核转位[19]。
本研究结果显示,EAT组小鼠脾脏组织p-AKT(Thr308)、p-AKT(Ser473)、p-mTOR(Ser2448)、S6K1、S6K2信号通路分子蛋白表达水平异常增高,提示AIT中存在PI3K/AKT/mTOR信号通路的过度激活。然而,在应用LY294002阻断PI3K信号通路后小鼠脾脏组织p-AKT(Thr308)、p-AKT(Ser473)、p-mTOR(Ser2448)、S6K1、S6K2、IL-17A的蛋白表达水平、SMCs中Th17细胞比例及血清IL17-A浓度均明显下降,且呈浓度依赖性,提示在EAT小鼠模型中PI3K信号通路可以调控Th17细胞的分化及其效应因子IL-17A的表达。与此同时,LY294002干预组小鼠甲状腺组织滤泡破坏程度及淋巴细胞浸润程度明显减轻,血清TgAb滴度降低,相关性分析表明小鼠体内Th17细胞的比例与血清TgAb及IL-17A浓度呈正相关,进一步证明了Th17细胞参与了EAT小鼠甲状腺的免疫损伤和甲状腺炎的发生和发展。因此,PI3K/AKT/mTOR信号通路可能通过影响Th17细胞的分化和功能参与AIT的发生和发展。
综上所述,本研究初步证实了PI3K/AKT/mTOR信号通路可能通过调控Th17细胞分化,促进EAT小鼠IL-17A表达,参与其甲状腺组织自身免疫损伤。目前,LY294002因其水溶性差、不良反应较大的缺点尚未纳入临床用药开发中,但是本研究阐明了PI3K/AKT/mTOR信号通路参与AIT发病的机制,为靶向治疗AIT提供了新的思路。
| [1] |
LI YZ, TENG D, BA JM, et al. Efficacy and safety of long-term universal salt iodization on thyroid disorders: epidemiological evidence from 31 provinces of Mainland China[J]. Thyroid, 2020, 30(4): 568-579. DOI:10.1089/thy.2019.0067 |
| [2] |
RALLI M, ANGELETTI D, FIORE M, et al. Hashimotoos thyroiditis: an update on pathogenic mechanisms, diagnostic protocols, therapeutic strategies, and potential malignant transformation[J]. Autoimmun Rev, 2020, 19(10): 102649. DOI:10.1016/j.autrev.2020.102649 |
| [3] |
LEE GR. The balance of Th17 versus Treg cells in autoimmunity[J]. Int J Mol Sci, 2018, 19(3): 730. DOI:10.3390/ijms19030730 |
| [4] |
XUE HB, YANG YH, ZHANG Y, et al. Macrophage migration inhibi- tory factor interacting with Th17 cells may be involved in the pathogenesis of autoimmune damage in Hashimotoos thyroiditis[J]. Mediators Inflamm, 2015, 2015: 621072. DOI:10.1155/2015/621072 |
| [5] |
YU L, WEI J, LIU PD. Attacking the PI3K/Akt/mTOR signaling pathway for targeted therapeutic treatment in human cancer[J]. Semin Cancer Biol, 2022, 85: 69-94. DOI:10.1016/j.semcancer.2021.06.019 |
| [6] |
WANG P, ZHANG Q, TAN L, et al. The regulatory effects of mTOR complexes in the differentiation and function of CD4+ T cell subsets[J]. J Immunol Res, 2020, 2020: 3406032. DOI:10.1155/2020/3406032 |
| [7] |
BEDULEVA L, SIDOROV A, TERENTIEV A, et al. Reduction in experimental autoimmune thyroiditis by IgG Fc fragments bearing regRF epitopes[J]. Immunol Res, 2023, 71(1): 83-91. DOI:10.1007/s12026-022-09337-1 |
| [8] |
BUNTE K, BEIKLER T. Th17 cells and the IL-23/IL-17 axis in the pathogenesis of periodontitis and immune-mediated inflammatory diseases[J]. Int J Mol Sci, 2019, 20(14): 3394. DOI:10.3390/ijms20143394 |
| [9] |
ABDEL-MONEIM A, BAKERY HH, ALLAM G. The potential pathogenic role of IL-17/Th17 cells in both type 1 and type 2 diabetes mellitus[J]. Biomed Pharmacother, 2018, 101: 287-292. DOI:10.1016/j.biopha.2018.02.103 |
| [10] |
YANG P, QIAN FY, ZHANG MF, et al. Th17 cell pathogenicity and plasticity in rheumatoid arthritis[J]. J Leukoc Biol, 2019, 106(6): 1233-1240. DOI:10.1002/JLB.4RU0619-197R |
| [11] |
LIU H, LI YW, ZHU YJ, et al. Notch signaling pathway promotes Th17 cell differentiation and participates in thyroid autoimmune injury in experimental autoimmune thyroiditis mice[J]. Mediators Inflamm, 2023, 2023: 1195149. DOI:10.1155/2023/1195149 |
| [12] |
LI DP, CAI WQ, GU RX, et al. Th17 cell plays a role in the pathogenesis of Hashimotoos thyroiditis in patients[J]. Clin Immunol, 2013, 149(3): 411-420. DOI:10.1016/j.clim.2013.10.001 |
| [13] |
LAWRENCE J, NHO R. The role of the mammalian target of rapamycin (mTOR) in pulmonary fibrosis[J]. Int J Mol Sci, 2018, 19(3): 778. DOI:10.3390/ijms19030778 |
| [14] |
FERGUSSON AD, ZHANG R, RIFFLE JS, et al. Encapsulation of PI3K inhibitor LY294002 within polymer nanoparticles using ion pairing flash nanoprecipitation[J]. Pharmaceutics, 2023, 15(4): 1157. DOI:10.3390/pharmaceutics15041157 |
| [15] |
JANKU F, YAP TA, MERIC-BERNSTAM F. Targeting the PI3K pathway in cancer: are we making headway?[J]. Nat Rev Clin Oncol, 2018, 15(5): 273-291. DOI:10.1038/nrclinonc.2018.28 |
| [16] |
CHEN CY, CHEN JY, HE LN, et al. PTEN: tumor suppressor and metabolic regulator[J]. Front Endocrinol, 2018, 9: 338. DOI:10.3389/fendo.2018.00338 |
| [17] |
COSTA RLB, HAN HS, GRADISHAR WJ. Targeting the PI3K/AKT/mTOR pathway in triple-negative breast cancer: a review[J]. Breast Cancer Res Treat, 2018, 169(3): 397-406. DOI:10.1007/s10549-018-4697-y |
| [18] |
SUTO T, KARONITSCH T. The immunobiology of mTOR in autoimmunity[J]. J Autoimmun, 2020, 110: 102373. DOI:10.1016/j.jaut.2019.102373 |
| [19] |
REN WK, YIN J, DUAN JL, et al. mTORC1 signaling and IL-17 expression: defining pathways and possible therapeutic targets[J]. Eur J Immunol, 2016, 46(2): 291-299. DOI:10.1002/eji.201545886 |
 2024, Vol. 53
2024, Vol. 53