文章信息
- 孙诗涵, 马一诺, 王群, 李鑫, 巴微, 李婉明
- SUN Shihan, MA Yinuo, WANG Qun, LI Xin, BA Wei, LI Wanming
- 基于核酸适配体和量子点的胃癌靶向成像研究
- Targeted imaging of gastric cancer based on aptamer and quantum dots
- 中国医科大学学报, 2023, 52(6): 499-504
- Journal of China Medical University, 2023, 52(6): 499-504
-
文章历史
- 收稿日期:2022-12-31
- 网络出版时间:2023-05-25 16:12:32
胃癌是全球范围内常见癌症之一,通过遗传和表观遗传改变的积累而发展,分子改变在癌前病变发展前就已发生[1],致使胃癌通常在晚期才被确诊,死亡率极高[2]。目前,胃癌的发现和诊断仍高度依赖于内镜检查[3]、磁共振成像(magnetic resonance imaging,MRI) [4]、正电子发射计算机断层显像(positron emission computed tomography,PET) 等影像学检查方法,由于这些方法的特异度与灵敏度较低,对肿瘤的早期诊断难以实现。随着新的肿瘤标志物不断被发现以及检测方法不断创新,荧光成像成为了癌症靶向成像的工具之一,最终有望实现肿瘤早期诊断。核酸适配体是一种短的单链核酸(ssDNA或RNA),在针对肿瘤的分子成像研究中是一类理想的成像探针。量子点(quantum dots,QD)也被称为纳米级半导体晶体[5],可以长时间对标志物进行稳定观察。
本研究基于W3以及QD的多种特性,将两者偶联制备探针,用于针对胃癌细胞的靶向成像,并探讨其应用于临床的可能性。
1 材料与方法 1.1 材料 1.1.1 细胞和主要试剂胃腺癌细胞系SGC-7901、正常人胃黏膜上皮细胞GES-1购自上海中科院细胞库,链霉亲和素标记的QD605购自QD-SA,武汉珈源量子点技术有限公司,胰蛋白酶及胎牛血清购自美国HyClone公司,RPMI 1640培养基购自美国Gibco公司,BSA购自中国Biosharp公司,鲱鱼精DNA购自德国Sigma公司,Cell-TrackerTMGreen CMFDA购自美国Invitrogen公司,DAPI购自中国Tiangen公司,核酸适配子W3序列和原文库购自美国Library,W3筛选时的随机寡核苷酸文库和序列购自中国上海生工生物公司。
1.1.2 实验动物4周龄健康雌性BALB/c裸鼠购自中国北京维通利华实验动物技术有限公司。
1.1.3 组织标本选取中国医科大学附属第一医院经病理学确诊、术前未行放化疗的胃癌患者的癌旁组织和癌组织。本研究获得我校医学伦理委员会批准。
1.2 方法 1.2.1 细胞培养SGC-7901和GES-1细胞均用含10%胎牛血清的DMEM培养基,在37 ℃、5%CO2饱和湿度孵箱中进行培养,取对数生长期细胞进行实验。
1.2.2 核酸适配体的前处理将合成的W3或Library溶于结合缓冲液(PBS+10%BSA+1%鲱鱼精DNA) 中,95 ℃加热变性5 min,然后置于冰上10 min,于-20 ℃中保存待用。
1.2.3 流式细胞术检测W3-QD探针对不同细胞系的结合情况取对数生长期GES-1细胞与SGC-7901细胞,利用EDTA消化,制备单细胞悬液。加入终浓度为250 nmol/L的FAM-W3或FAM-Library,与细胞4 ℃孵育30 min;1 000 r/min离心5 min,弃去上清;加入QD-SA室温孵育20 min,1 000 r/min离心5 min,加入300 μL PBS重悬细胞,流式细胞仪检测细胞的荧光信号。
1.2.4 荧光显微镜观察W3-QD探针对细胞的靶向成像利用0.25%胰蛋白酶消化对数生长期的SGC-7901细胞和GES-1细胞并吹打成单细胞悬液,细胞计数后接种于内置盖玻片的6孔板中,过夜培养。加入Biotin-W3 (终浓度为250 nmol/L),分别与上述2种细胞4 ℃孵育30 min;加入QD-SA (1∶200稀释) 室温孵育20 min;DAPI复染细胞核5 min;荧光显微镜观察并拍照。
取对数生长期的GES-1细胞,加入Cell-tracker (绿色,1∶1 000稀释) 37 ℃孵育30 min,并吹打成单细胞悬液;取对数生长期SGC-7901细胞并吹打成单细胞悬液;细胞计数后取活染成绿色的GES-1细胞与SGC-7901细胞以1∶1进行混合,混匀后接种于6孔板中(内置盖玻片)过夜培养。如上述步骤进行W3-QD的标记。
取对数生长期的SGC-7901细胞,消化吹打成单细胞悬液,均匀接种于6孔板的2孔中(内置盖玻片)过夜培养;分别加入FAM-W3和W3-QD如上述步骤进行标记,并于第0天和第7天观察染色结果。
1.2.5 荷瘤裸鼠模型的建立4周龄雌性BALB/c裸鼠在SPF级条件下饲养。取对数生长期SGC-7901细胞,胰酶消化,细胞数浓度调整为1×107/mL。裸鼠右前腋下经皮下注射200 µL细胞悬液,观察肿瘤的生长情况。4周后取出肿瘤块。
1.2.6 W3-QD探针对胃癌组织的特异性标记裸鼠皮下移植瘤和临床患者病理组织常规包埋后制备成厚度为5 μm的石蜡切片,60 ℃烤片4 h。100%二甲苯脱蜡2次,15 min/次;梯度入水,100%乙醇2次,10 min/次,95%、90%、85%、75%和50%乙醇各5 min;PBS清洗3次,5 min/次;切片置于0.01 mol/L枸椽酸钠修复液中高压修复100 s,自然冷却至室温;PBS洗3次,5 min/次;加入封闭液(洗涤缓冲液+1%BSA+10%FBS) 4 ℃封闭60 min;PBS洗涤2次后加入Biotin-W3或Biotin-Library,终浓度为250 nmol/L,4 ℃孵育60 min;PBS洗涤2次后,加入QD-SA室温孵育20 min;PBS洗涤后荧光显微镜观察并拍照。
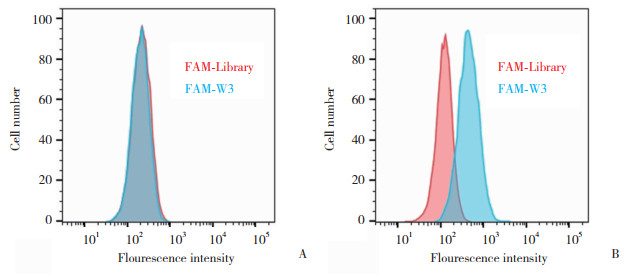
2 结果 2.1 核酸适配体W3与SGC-7901细胞的特异性结合流式细胞术结果显示,适配体W3与SGC-7901细胞孵育后的荧光结合峰明显右移,与之相比,与GES-1细胞孵育后的荧光结合峰没有明显移动,提示核酸适配体W3能够与SGC-7901细胞发生结合,而与GES-1细胞不结合。见图 1。
|
| A, GES-1;B, SGC-7901. 图 1 W3结合SGC-7901细胞的流式细胞术检测 Fig.1 W3 and SGC-7901 cells detected with flow cytometry |
2.2 W3-QD探针对SGC-7901细胞的靶向成像
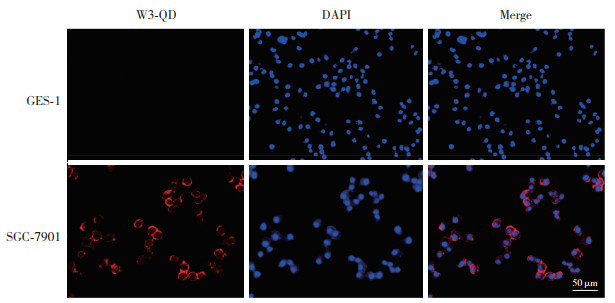
荧光显微镜结果显示,与W3-QD探针孵育后,SGC-7901细胞表面能观察到明显的特异性红色荧光,而GES-1细胞表面没有观察到任何荧光信号(图 2),表明W3-QD探针可以实现胃癌细胞的靶向成像。
|
| 图 2 W3-QD探针对SGC-7901细胞的荧光显微镜成像图 Fig.2 Fluorescence microscope image of SGC-7901 cells by W3-QD probe |
2.3 W3-QD探针对混合培养细胞中胃癌细胞SGC-7901的靶向成像
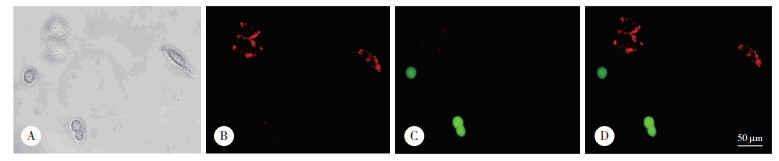
为了确定W3-QD具有对靶细胞的特异性识别能力,利用Cell-tracker活体荧光染料对GES-1正常细胞进行活细胞染色,再将染色后的细胞与SGC-7901胃癌细胞进行混合培养24 h。之后对混合细胞用W3-QD进行识别检测,荧光显微镜结果显示,被染色后的GES-1细胞表面没有识别到荧光信号,但胃癌细胞SGC-7901的细胞膜表面可以特异性地识别红色荧光信号(图 3),表明在与正常细胞混合培养的情况下,W3-QD探针仍然保持其对胃癌细胞的特异性,能够对胃癌细胞实现靶向成像。
|
| A, bright; B, W3-QD-SGC-7901;C, green-GES-1;D, merge. 图 3 W3-QD探针对混合培养细胞中SGC-7901靶向成像的荧光显微镜成像图 Fig.3 Fluorescence microscope image of targeting SGC-7901 in mixed culture cells by W3-QD probe |
2.4 QD探针具有更高的灵敏度和光稳定性
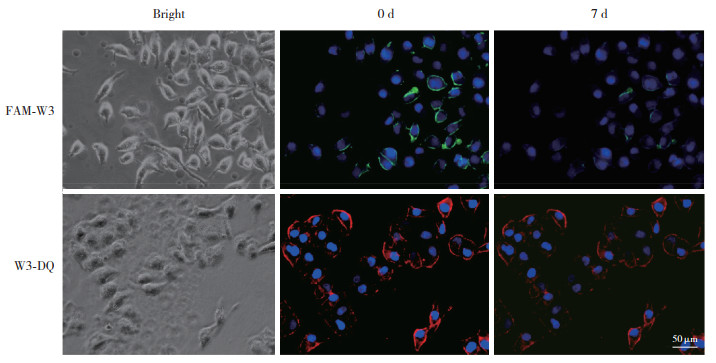
为了探究QD对靶细胞的灵敏度和光稳定性,对SGC-7901细胞进行FAM-W3和W3-QD的识别检测,使其表面分别带有特异性绿色荧光和红色荧光。并分别于第0天和第7天观察染色结果,相较于FAM-W3,W3-QD探针能识别更多的胃癌细胞,具有更高的灵敏度;而且在第7天时仍有大面积红色荧光被保留下来,但绿色荧光几乎全部淬灭(图 4)。以上结果表明,QD相较于有机染料对靶细胞的成像具有更高的灵敏度和光稳定性。
|
| 图 4 W3-QD和FAM-W3对SGC-7901靶向成像的荧光显微镜检测 Fig.4 Fluorescence microscopy detection of SGC-7901 targeting imaging by W3-QD and FAM-W3 |
2.5 W3-QD探针对荷瘤裸鼠肿瘤组织的靶向成像
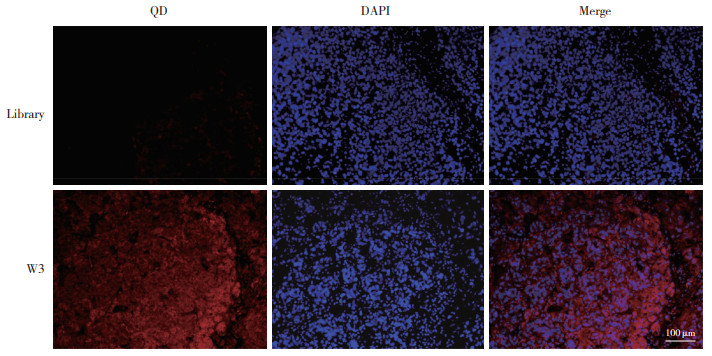
在细胞水平上,W3-QD探针可以对特定的肿瘤细胞系靶向成像已被证实,下一步为了验证W3-QD探针对体内环境下的肿瘤细胞能否靶向成像,建立了SGC-7901的荷瘤裸鼠模型,获取肿瘤组织制备石蜡切片,进行W3-QD的识别。组织免疫荧光实验结果显示,与Library处理组相比,W3-QD探针处理的裸鼠皮下移植瘤组织能观察到明显的红色荧光信号,表明W3-QD探针能够对裸鼠皮下移植瘤组织进行靶向成像。见图 5。
|
| 图 5 Library-QD和W3-QD对胃癌组织靶向成像的荧光显微镜成像图 Fig.5 Fluorescence microscope image of Library-QD and W3-QD targeted imaging of gastric cancer tissue |
2.6 W3-QD探针对临床胃癌病理切片的靶向成像
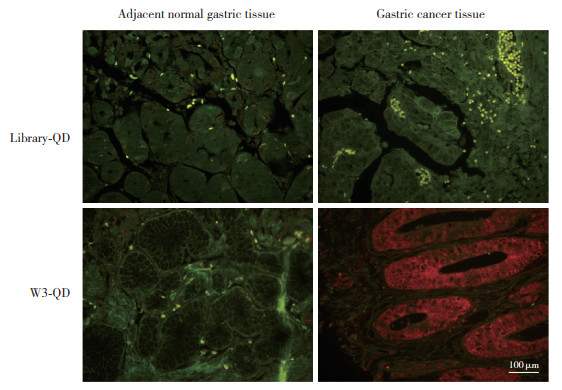
为了验证W3-QD探针对于临床胃癌组织切片的靶向成像能力,利用W3-QD对临床收集到的胃癌组织及癌旁组织进行特异性成像检测。荧光显微镜观察显示,经过W3-QD探针处理组的癌旁组织观察不到任何红色荧光信号,而在肿瘤组织的切片上特异性红色荧光信号清晰可见于肿瘤细胞的细胞膜表面;相比之下,经Library-QD进行标记时均无任何特异性荧光信号(图 6)。以上结果可以显示W3-QD有优良的对胃癌靶向成像特异性。
|
| 图 6 W3-QD探针对胃癌病理切片的靶向成像图 Fig.6 Target imaging of W3-QD probe on pathological section of gastric cancer |
3 讨论
与传统的医学影像方法相比,分子影像技术特异识别肿瘤相关标志物的靶向分子,对肿瘤的早期诊断更精准。单克隆抗体作为针对胃癌的靶向分子,已经相对成熟,但其仍存在着诸多缺点,如高免疫原性,在人体内清除时间长,可检测的靶标有限等。
核酸适配体是一种新型的分子标志物及靶向配体,能够折叠成特定的三维结构,对靶标分子具有很高的亲和力[6]和特异性[7]。与抗体相比,核酸适配体具有高特异性[8-9]、低免疫原性[10]、低成本、易修饰[11]、结构稳定、快速组织渗透性等优点,在现实使用中功能更为优越。QD在紫外光激发下可发出不同波长的荧光。相较于传统有机荧光染料,QD尺寸小[12-13],且具有独特的光学性质如高光漂白稳定性[14]、荧光间歇性[15]和宽而连续的激发光谱,更有利于成像检测。本研究将QD与适配体结合使用,并与传统染色方法做对比。前期研究[16]显示多种转移性肿瘤细胞可以被适配体W3特异性识别出来,并用于对具有转移潜能的肿瘤细胞实现靶向成像。
ZENG等[17]利用靶向CD30的适配体对淋巴瘤组织进行免疫染色,发现CD30适配体比CD30抗体具有更高的灵敏度和特异度。本研究利用前期Cell-SELEX筛选获得的核酸适配体W3作为靶向成像分子探针,首先在细胞水平上实现了胃癌细胞的靶向成像,并且在混合细胞中也能够特异性识别胃癌细胞;其次在组织水平上对裸鼠体内皮下移植瘤的胃癌细胞具有良好的靶向成像功能。进一步探讨临床胃癌组织的成像情况,发现核酸适配体W3具有良好的肿瘤特异性,有可能成为胃癌诊断的靶向成像分子探针。
本研究基于QD的优良特性和核酸适配体的靶向性,构建的W3-QD探针,实现了胃癌细胞的靶向成像,且7 d后与FAM-W3探针相比,W3-QD探针的荧光仍有良好的稳定性,具有更优良的实际应用价值。免疫组化是应用最广泛的对临床样本成像的方法,但其仍受到一定的限制[18],QD可以在一定程度上替代传统的免疫组化成像,应用到诸如癌症诊断、发病机制研究、治疗、分子病理学和癌症生物标志物结合的异质性等方面。本研究采用QD进行成像检测,有利于对靶标进行长时间而稳定的观察。
综上所述,以核酸适配体W3偶联QD制备量子点探针W3-QD,实现胃癌细胞系和临床胃癌组织的靶向成像,有可能为胃癌的早期诊断提供新的分子工具。
| [1] |
SMYTH EC, NILSSON M, GRABSCH HI, et al. Gastric Cancer[J]. Lancet, 2020, 396(10251): 635-648. DOI:10.1016/S0140-6736(20)31288-5 |
| [2] |
WATARI J, CHEN N, AMENTA PS, et al. Helicobacter pylori associated chronic gastritis, clinical syndromes, precancerous lesions, and pathogenesis of gastric cancer development[J]. World J Gastroenterol, 2014, 20(18): 5461-5473. DOI:10.3748/wjg.v20.i18.5461 |
| [3] |
YAO KS, NAGAHAMA T, MATSUI T, et al. Detection and characterization of early gastric cancer for curative endoscopic submucosal dissection[J]. Dig Endosc, 2013, 25(Suppl 1): 44-54. DOI:10.1111/den.12004 |
| [4] |
ZHANG YJ, YU JC. The role of MRI in the diagnosis and treatment of gastric cancer[J]. Diagn Interv Radiol, 2020, 26(3): 176-182. DOI:10.5152/dir.2019.19375 |
| [5] |
BRUCHEZ M Jr, MORONNE M, GIN P, et al. Semiconductor nanocrystals as fluorescent biological labels[J]. Science, 1998, 281(5385): 2013-2016. DOI:10.1126/science.281.5385.2013 |
| [6] |
刘婷先, 张娜. 适配体在肿瘤治疗方面的应用[J]. 生命的化学, 2013, 33(5): 503-508. DOI:10.13488/j.smhx.2013.05.006 |
| [7] |
NI SJ, ZHUO ZJ, PAN YF, et al. Recent progress in aptamer discoveries and modifications for therapeutic applications[J]. ACS Appl Mater Interfaces, 2021, 13(8): 9500-9519. DOI:10.1021/acsami.0c05750 |
| [8] |
ZAMAY GS, IVANCHENKO TI, ZAMAY TN, et al. DNA aptamers for the characterization of histological structure of lung adenocarcinoma[J]. Mol Ther Nucleic Acids, 2017, 6: 150-162. DOI:10.1016/j.omtn.2016.12.004 |
| [9] |
BING T, SHANGGUAN DH, WANG YS. Facile discovery of cell-surface protein targets of cancer cell aptamers[J]. Mol Cell Proteomics, 2015, 14(10): 2692-2700. DOI:10.1074/mcp.M115.051243 |
| [10] |
ZHU GZ, CHEN XY. Aptamer-based targeted therapy[J]. Adv Drug Deliv Rev, 2018, 134: 65-78. DOI:10.1016/j.addr.2018.08.005 |
| [11] |
MATEA CT, MOCAN T, TABARAN F, et al. Quantum dots in ima-ging, drug delivery and sensor applications[J]. Int J Nanomedicine, 2017, 12: 5421-5431. DOI:10.2147/IJN.S138624 |
| [12] |
KARGOZAR S, HOSEINI SJ, MILAN PB, et al. Quantum dots: a review from concept to clinic[J]. Biotechnol J, 2020, 15(12): e2000117. DOI:10.1002/biot.202000117 |
| [13] |
UPRETY B, ABRAHAMSE H. Semiconductor quantum dots for photodynamic therapy: recent advances[J]. Front Chem, 2022, 10: 946574. DOI:10.3389/fchem.2022.946574 |
| [14] |
SOUZA SO, LIRA RB, CUNHA CRA, et al. Methods for intracellular delivery of quantum dots[J]. Top Curr Chem (Cham), 2021, 379(1): 1. DOI:10.1007/s41061-020-00313-7 |
| [15] |
LE N, ZHANG M, KIM K. Quantum dots and their interaction with biological systems[J]. Int J Mol Sci, 2022, 23(18): 10763. DOI:10.3390/ijms231810763 |
| [16] |
LI WM, BING T, WEI JY. Cell-SELEX-based selection of aptamers that recognize distinct targets on metastatic colorectal cancer cells[J]. Biomaterials, 2014, 35(25): 6998-7007. DOI:10.1016/j.biomaterials.2014.04.112 |
| [17] |
ZENG ZH, ZHANG P, ZHAO NX, et al. Using oligonucleotide aptamer probes for immunostaining of formalin-fixed and paraffin-embedded tissues[J]. Mod Pathol, 2010, 23(12): 1553-1558. DOI:10.1038/modpathol.2010.151 |
| [18] |
SUN JZ, CHEN C, JIANG G, et al. Quantum dot-based immunofluorescent imaging of Ki67 and identification of prognostic value in HER2-positive (non-luminal) breast cancer[J]. Int J Nanomedicine, 2014, 9: 1339-1346. DOI:10.2147/IJN.S58881 |
 2023, Vol. 52
2023, Vol. 52