文章信息
- 白雪莹, 刘正华
- BAI Xueying, LIU Zhenghua
- 3D与2D单孔胸腔镜肺叶切除术的疗效比较
- Comparison of the therapeutic effects of 3D and 2D single-port thoracoscopic surgery for pulmonary lobectomy
- 中国医科大学学报, 2023, 52(3): 277-281
- Journal of China Medical University, 2023, 52(3): 277-281
-
文章历史
- 收稿日期:2022-11-17
- 网络出版时间:2023-03-16 09:19:43
近年来,随着全球范围内肺癌发病率的上升,其已成为发病率和致死率均居第一位的恶性肿瘤。并且随着肺癌肿瘤标志物广泛普及,薄层CT和高分辨率CT被广泛用于临床,早期肺癌可以被及时发现并通过手术根治,从而提高了肺癌的治愈率[1]。在胸腔镜技术尚未普及时,肺癌手术以开胸手术为主,开胸手术不仅会影响胸廓的完整性,还会造成肋间神经损伤,导致患者胸廓容量下降、呼吸功能受限,术后出现顽固性肋间神经痛等情况[2]。胸腔镜技术在近20年迅速发展,相较于传统的开胸手术,多孔胸腔镜手术极大改善了术后呼吸功能的恢复,有效规避了肋间神经损伤。而单孔胸腔镜在多孔胸腔镜的基础上,能够更好地改善术后疼痛,患者恢复更快,为快速康复外科奠定了基础[3]。受手术技术和设备的限制,目前许多中心仍以2D胸腔镜为主要手术方式。但2D胸腔镜手术存在一些弊端,如手术视野失真、切割缝合过程中在二维平面进行操作时纵深感差、对初学者学习曲线不友好等[4]。我院胸外科自2019年1月开始逐步开展3D单孔胸腔镜手术,本研究通过比较3D单孔胸腔镜手术与传统2D单孔胸腔镜手术在手术时间、术中出血量、术后并发症、术后引流量、D-二聚体水平、住院时间等方面的差异,评价3D单孔胸腔镜肺叶切除术的疗效。
1 材料与方法 1.1 研究对象和分组收集2019年1月至2022年1月间我院胸外科收治的158例接受单孔胸腔镜肺叶及肺段切除术患者的临床资料,其中接受3D单孔胸腔镜手术(3D组)80例,接受2D单孔胸腔镜手术(2D组)78例。纳入标准:(1)术后病理诊断为肺癌;(2)术前临床分期为Ⅰ~ⅢA期,可耐受手术;(3)既往未接受放疗或化疗等其他治疗。排除标准:(1)术中因各种原因转为开胸手术的患者;(2)术前接受过辅助化疗或放疗的患者;(3)肺部肿物考虑为其他脏器肿瘤转移的患者。本研究获得我院伦理委员会批准,所有患者均签署知情同意书。
1.2 术前检查和准备158例患者入院前均完善肺部增强CT三维重建,入院后完善血常规、血型、凝血四项、肝肾功能、血离子、肺癌相关肿瘤标志物、D-二聚体、乙型肝炎等传染病、血气分析等实验室检查。完善心肺功能检查,并进行术前麻醉评估。常规进行肝胆脾泌尿系统超声、颅脑CT检查,必要时完善PET-CT检查,除外肺部肿瘤为其他脏器肿瘤转移。
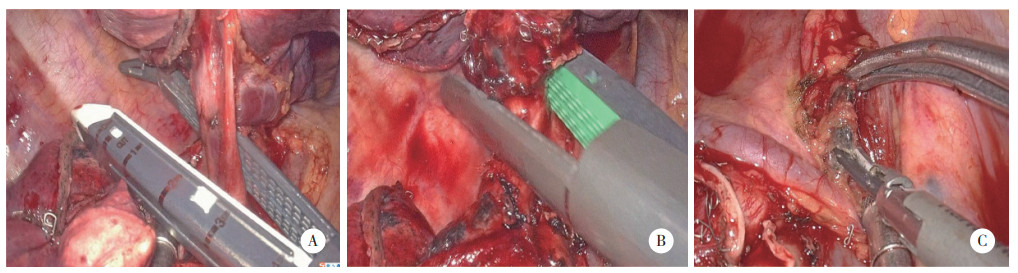
1.3 手术过程手术设备均采用日本Olympus胸腔镜系统,手术均由同一组医生完成,3D组术者和器械护士需佩戴3D眼镜。麻醉成功后,患者取侧卧位,术区常规消毒铺单。采用单孔手术方式。利用超声刀、电钩、吸引器分离黏连,探查胸腔,根据肿物位置游离下肺韧带,显露肺静脉和肺动脉及其分支,利用45或60 mm腔镜切割闭合器进行切断。显露支气管及其分支,随后嘱麻醉师膨肺,确认肺复张后,切断支气管,同时避免损伤膈神经、迷走神经、心包等重要毗邻解剖结构。常规进行淋巴结清扫术。3D组手术过程见图 1。
|
| A,离断静脉;B,离断支气管;C,清扫淋巴结. 图 1 3D单孔胸腔镜肺叶切除术手术过程 |
1.4 观察指标 1.4.1 一般资料
记录患者的性别、年龄以及肺部肿瘤的位置、大小、病理类型、分期。
1.4.2 术中观察指标记录手术时间、术中出血量和术中淋巴结清扫数量。
1.4.3 术后观察指标记录术后第1~3天D-二聚体水平的变化、术后引流量、引流管留置时间、住院时间和术后并发症的发生率。
1.5 统计学分析应用SPSS 22.0软件进行数据分析。计量资料用x±s表示,组内比较采用独立样本t检验,组间比较采用配对样本t检验。计数资料用率表示,组间比较采用χ2检验或Fisher确切概率法。P < 0.05为差异有统计学意义。
2 结果 2.1 一般资料的比较3D组和2D组比较,患者的年龄、性别构成比、肿瘤位置和大小、肿瘤病理类型、肿瘤分期均无统计学差异(P > 0.05)。见表 1。
| 项目 | 3D组(n = 80) | 2D组(n = 78) | t /χ2 | P |
| 年龄(岁) | 52.9±18.5 | 47.9±18.8 | 1.660 | 0.090 |
| 性别[n(%)] | 0.913 | 0.339 | ||
| 男 | 56(70.00) | 49(62.82) | ||
| 女 | 24(30.00) | 29(37.18) | ||
| 肿瘤位置[n(%)] | 0.970 | 0.914 | ||
| 左肺上叶 | 17(21.25) | 14(17.95) | ||
| 左肺下叶 | 15(18.75) | 13(16.67) | ||
| 右肺上叶 | 20(25.00) | 22(28.21) | ||
| 右肺中叶 | 16(20.00) | 14(17.95) | ||
| 右肺下叶 | 12(15.00) | 15(19.22) | ||
| 肿瘤直径(mm) | 18.0±7.5 | 18.6±7.3 | 1.100 | 0.290 |
| 病理类型[n(%)] | 0.468 | 0.784 | ||
| 鳞状细胞癌 | 28(35.00) | 31(39.74) | ||
| 腺癌 | 43(53.75) | 40(51.29) | ||
| 其他 | 9(11.25) | 7(8.97) | ||
| 肿瘤分期[n(%)] | 1.941 | 0.809 | ||
| ⅠA | 42(52.50) | 38(48.72) | ||
| ⅠB | 18(22.50) | 19(23.75) | ||
| ⅡA | 11(13.75) | 10(12.82) | ||
| ⅡB | 9(11.25) | 9(11.54) | ||
| ⅢA | 0(0.00) | 2(2.56) |
2.2 术中和术后观察指标的比较
患者术后均常规应用抗生素抗炎,低分子肝素抗凝,避免发生下肢静脉血栓和肺栓塞。3D组手术时间较2D组明显缩短(P < 0.05),而2组比较术中出血量、淋巴结清扫数量无统计学差异(P > 0.05)。3D组术后第1~3天D-二聚体水平明显低于2D组(P < 0.05),住院时间明显短于2D组(P < 0.05),2组比较术后引流量、引流管留置时间和各种并发症发生率均无统计学差异(P > 0.05)。见表 2。
| 项目 | 3D组(n = 80) | 2D组(n = 78) | t /χ2 | P |
| 手术时间(min) | 106.2±13.2 | 112.5±12.3 | 3.01 | 0.002 |
| 术中出血量(mL) | 52.0±12.3 | 58.2±14.1 | 3.87 | 0.140 |
| 淋巴结清扫数量 | 6.4±1.5 | 6.9±2.1 | 1.56 | 0.140 |
| D-二聚体(mg/L) | ||||
| 术后第1天 | 5.8±2.2 | 7.8±1.9 | 1.56 | 0.043 |
| 术后第2天 | 3.8±2.6 | 4.4±2.1 | 1.43 | 0.042 |
| 术后第3天 | 2.2±1.8 | 3.2±2.0 | 1.33 | 0.038 |
| 术后引流量(mL) | 216.0±52.1 | 211.1±61.7 | 4.92 | 0.820 |
| 术后引流管留置时间(d) | 3.9±1.1 | 4.3±1.1 | 1.67 | 0.080 |
| 住院时间(d) | 7.4±1.6 | 8.0±1.7 | 2.29 | 0.020 |
| 并发症[n(%)] | ||||
| 肺炎 | 3(3.75) | 8(10.00) | 2.581 | 0.108 |
| 肺栓塞 | 1(1.25) | 1(1.25) | 8.012 | 0.992 |
| 低氧血症 | 2(2.50) | 4(5.00) | 0.097 | 0.755 |
| 心律失常 | 0(0.00) | 2(2.50) | 2.078 | 0.149 |
| 乳糜胸 | 2(2.50) | 4(5.00) | 8.012 | 0.992 |
3 讨论 3.1 胸腔镜手术较开胸手术的优势
近年来,受吸烟人数、大气环境等影响,早期肺小结节患者筛查率逐年升高。TOGAMI等[5]对155例肺癌患者进行回顾性研究,发现行胸腔镜肺癌切除术的患者与行开胸手术的患者相比,5年生存率无明显差异,但术后并发症发生率更低,术后引流量更少,住院时间更短。肺癌往往伴随着肺部多组淋巴结转移,淋巴结转移是影响肺癌患者预后的重要因素,但早期肺癌患者术中是否行淋巴结清扫仍存在巨大争议[6]。大量研究将淋巴结升期作为评判淋巴结清扫是否彻底的重要指标,而许多学者对胸腔镜下肺淋巴结清扫术能否最终准确评估肺部肿瘤淋巴结转移情况存在质疑。研究[7]显示,开胸手术相较于胸腔镜手术,具有更高的淋巴结升期率。随着胸腔镜的普及,胸外科医生手术技术的提高,这种担忧正在逐渐消失。MATSUURA等[8]对193例行开胸和胸腔镜淋巴结清扫的患者进行回顾性研究,发现胸腔镜手术与开胸手术比较,淋巴结升期、5年无进展生存期无明显差异。随着越来越多的中心进行胸腔镜手术与开胸手术的随机对照试验,更多的证据表明胸腔镜手术较开胸手术具有多方面的优势。
开胸手术由于创伤大,术后患者容易出现严重疼痛,这种疼痛剧烈且持续时间长,往往与手术切口大小、肌肉撕裂、胸膜损伤、引流管刺激等有关[9]。BENDIXEN等[10]进行了一项随机对照研究,结果显示,胸腔镜组无论是在术后24 h内数字分级评分法疼痛评分≥3分方面还是在术后52周的中重度疼痛程度方面均优于开胸组,因此胸腔镜手术在早期肺癌手术中更应被推广。尽管胸腔镜手术具有创伤小、恢复快、术后生活质量高等优势,但对于复杂病例的治疗,开胸手术仍是重要的治疗方式。
3.2 3D胸腔镜与2D胸腔镜相比的优缺点由于初期的硬件技术限制,3D电视胸腔镜手术(video-assisted thoracoscopic surgery,VATS)的成像质量欠佳,导致术者在手术过程中出现严重的头疼、视觉疲劳,因此未被广泛推广。随着3D VATS硬件的进步,为术者提供了更好的纵深感,术者能够更加准确地定位,为切割、止血、吻合带来了更好的体验[11]。同时,术者在手术学习过程中无需在2D和3D影像间进行转换,能够带来更平滑的学习曲线和更高的容错率,保障了手术的安全。本研究表明,3D VATS可以明显缩短手术时间,减少出血量,降低D-二聚体水平,从而明显改善患者的血流动力学,降低静脉血栓发生的概率。
尽管3D VATS技术存在上述优势,但在临床实践中仍有一些问题有待解决。首先,无论何种3D VATS技术,其成像原理均是通过3D眼镜形成视觉错觉,通过术者大脑分析后提供景深信息。术者手术过程中必须全程佩戴3D眼镜,而3D眼镜尤其是偏光眼镜,会不同程度降低手术视野的亮度,导致术者视觉疲劳。其次,手术过程中,需要术者与助手更默契配合,由于3D VATS的腔镜镜头通常不可调节角度,在镜头移动过程中术者需要不停适应切换的镜头,如果术者与助手配合不够默契,容易造成术者出现头晕、疲劳等情况[12]。最后,3D胸腔镜手术设备价格高昂,不能在各级医院普遍推广,且患者需要承担更高的医疗费用。
3.3 胸腔镜技术的发展越来越先进的腔镜技术正在逐步用于临床,裸眼3D VATS和更加先进的机器人辅助胸外科手术(robot-assisted thoracic surgery,RATS)正在高速发展。裸眼3D VATS作为传统3D VATS的改良技术,摒弃了术者需要佩戴3D眼镜的需求,不仅缩短了手术的学习曲线,也为术者提供了更加明亮的手术视野。同时配合裸眼3D系统的面部和眼部定位技术,可以在任何角度为术者提供实时的3D视野。目前,裸眼3D VATS仍处于早期临床研究阶段,人们对该技术存在较大争议。LI等[13]进行了一项裸眼3D VATS与2D胸腔镜手术的比较研究,发现前者术中出血更少,术后住院时间更短。未来应进行大规模的随机对照试验,对该技术进行进一步评估。
达芬奇机器人系统于2002年首次用于临床,并于2014年推出带有激光指引技术的达芬奇机器人Xi系统。传统VATS由于操作角度、视野等方面的设计缺陷,一定程度上提高了术者的学习曲线难度,而RATS在设计之初,就以机械臂操控系统、高清的3D成像技术等技术优势为切入点,提高了胸腔镜手术的精准度,减轻了术者的疲劳感[14]。在一项纳入6 593例肺癌患者的网状meta分析中,对32个中心的RATS与VATS及开胸手术进行对比,结果发现,RATS与VATS具有相似的手术时间、中转开胸率、术后死亡率和住院时间,尽管RATS与开胸手术相比手术时间较长,但却能明显缩短住院时间[15]。随着机器人手术普及率的增加,随着5G技术和LifDAR技术的发展,机器人辅助胸腔镜技术无论在硬件层面还是在术者技术层面,都将迎来长足的发展,并将远程手术操作变为可能。
综上所述,3D单孔胸腔镜近年来逐步用于胸外科手术,相较于传统2D单孔胸腔镜,具有更好的操作纵深感,能够显著缩短手术时间,提高手术安全性,可广泛用于肺癌治疗。
| [1] |
BADE BC, DELA CRUZ CS. Lung cancer 2020:epidemiology, etiology, and prevention[J]. Clin Chest Med, 2020, 41(1): 1-24. DOI:10.1016/j.ccm.2019.10.001 |
| [2] |
李立彬, 牛学瑞, 李栋, 等. 胸腔镜肺叶切除术与常规开胸手术治疗肺癌的疗效及并发症发生情况[J]. 实用癌症杂志, 2020, 35(1): 91-93, 103. DOI:10.3969/j.issn.1001-5930.2020.01.025 |
| [3] |
赵子聪, 洪志鹏. 外科胸腔镜的发展现状[J]. 中华肺部疾病杂志(电子版), 2018, 11(5): 618-620. DOI:10.3877/cma.j.issn.1674-6902.2018.05.026 |
| [4] |
朱国勇, 姜杰, 于修义. 不同年度3D与2D胸腔镜肺癌根治术的对比研究[J]. 中国医师杂志, 2017, 19(12): 1807-1809. DOI:10.3760/cma.j.issn.1008-1372.2017.12.014 |
| [5] |
TOGAMI S, KAWAMURA T, YANAZUME S, et al. Comparison of survival outcomes between laparoscopic and open surgery in patients with low-risk endometrial cancer[J]. Jpn J Clin Oncol, 2020, 50(11): 1261-1264. DOI:10.1093/jjco/hyaa116 |
| [6] |
VAN DER WOUDE L, WOUTERS MWJM, HARTEMINK KJ, et al. Completeness of lymph node dissection in patients undergoing minimally invasive- or open surgery for non-small cell lung cancer: a nationwide study[J]. Eur J Surg Oncol, 2021, 47(7): 1784-1790. DOI:10.1016/j.ejso.2020.11.008 |
| [7] |
MERRITT RE, HOANG CD, SHRAGER JB. Lymph node evaluation achieved by open lobectomy compared with thoracoscopic lobectomy for N0 lung cancer[J]. Ann Thorac Surg, 2013, 96(4): 1171-1177. DOI:10.1016/j.athoracsur.2013.05.044 |
| [8] |
MATSUURA Y, ICHINOSE J, NAKAO M, et al. Outcomes of nodal upstaging comparing video-assisted thoracoscopic surgery versus open thoracotomy for lung cancer[J]. Lung Cancer, 2021, 152: 78-85. DOI:10.1016/j.lungcan.2020.12.017 |
| [9] |
KALIA H, PRITZLAFF S, LI AH, et al. Application of the novel NaluTM Neurostimulation System for peripheral nerve stimulation[J]. Pain Manag, 2022, 12(7): 795-804. DOI:10.2217/pmt-2021-0050 |
| [10] |
BENDIXEN M, JØRGENSEN OD, KRONBORG C, et al. Postope- rative pain and quality of life after lobectomy via video-assisted thoracoscopic surgery or anterolateral thoracotomy for early stage lung cancer: a randomised controlled trial[J]. Lancet Oncol, 2016, 17(6): 836-844. DOI:10.1016/S1470-2045(16)00173-X |
| [11] |
XIN N, DING X, HUANG K, et al. Three-dimension versus twodimension video-assisted thoracoscopic surgery for esophageal cancer: a meta-analysis[J]. Transl Cancer Res, 2021, 10(7): 3448-3457. DOI:10.21037/tcr-21-644 |
| [12] |
JIAO P, WU QJ, SUN YG, et al. Comparative study of three-dimensional versus two-dimensional video-assisted thoracoscopic two-port lobectomy[J]. Thorac Cancer, 2017, 8(1): 3-7. DOI:10.1111/1759-7714.12387 |
| [13] |
LI X, CUI F, XING T, et al. Glasses-free 3D versus 2D video-assisted thoracoscopic thymectomy: a single-center short-term comparative study[J]. Ann Transl Med, 2019, 7(23): 761. DOI:10.21037/atm.2019.11.96 |
| [14] |
陈天翔, 吴晗, 罗清泉. 机器人辅助肺癌手术的淋巴结清扫研究进展[J]. 中华胸部外科电子杂志, 2022, 9(1): 29-34. DOI:10.3877/cma.j.issn.2095-8773.2022.01.04 |
| [15] |
HU J, CHEN Y, DAI J, et al. Perioperative outcomes of robot-assisted vs video-assisted and traditional open thoracic surgery for lung cancer: a systematic review and network meta-analysis[J]. Int J Med Robot, 2020, 16(5): 1-14. DOI:10.1002/rcs.2123 |
 2023, Vol. 52
2023, Vol. 52




