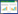文章信息
- 李红英, 张会军, 王军, 穆秀娥, 李红方
- LI Hongying, ZHANG Huijun, WANG Jun, MU Xiu'e, LI Hongfang
- lncRNA SNHG1靶向miR-145-5p/PDCD4轴对缺氧/复氧诱导的心肌细胞凋亡的影响
- Effect of lncRNA SNHG1 targeting miR-145-5p/PDCD4 axis on hypoxia/reoxygenation-induced cardiomyocyte apoptosis
- 中国医科大学学报, 2023, 52(10): 904-909, 916
- Journal of China Medical University, 2023, 52(10): 904-909, 916
-
文章历史
- 收稿日期:2022-11-17
- 网络出版时间:2023-10-16 19:46:59
急性心肌梗死(acute myocardial infarction,AMI)是一种常见的心血管疾病,死亡率高,及时、有效的再灌注是减少AMI后心肌损伤的重要治疗选择[1]。研究[2]报道,心肌细胞凋亡、氧化应激参与了AMI的发病机制。心肌缺氧/复氧(hypoxia/reoxygenation,H/R) 损伤与心血管外科手术高度相关[3],预防H/R诱导的心肌细胞凋亡可能为AMI提供新的治疗策略。越来越多的研究表明,长链非编码RNA (long noncoding RNA,lncRNA) 在包括AMI在内的心血管疾病的生理和病理过程中发挥重要作用。核内小RNA宿主基因1 (small nucleolar RNA host gene 1,SNHG1) 作为一种lncRNA,已有研究[4]显示,下调SNHG1可以抑制心肌缺血/再灌注损伤小鼠的心肌细胞凋亡。但其具体分子机制尚不完全明确。研究[5]显示,过表达miR-145通过靶向下调程序性细胞死亡因子4 (programmed cell death 4,PDCD4) 抑制H/R诱导心肌细胞凋亡。生物信息学分析显示,SNHG1与miR-145-5p存在靶向关系。而SNHG1能否通过调控miR-145-5p/PDCD4轴影响H/R诱导的心肌细胞凋亡尚不明确。因此,本研究主要探讨了SNHG1对H/R诱导的心肌细胞凋亡的影响及其作用的分子机制。
1 材料与方法 1.1 材料 1.1.1 细胞大鼠心肌细胞H9c2购自浙江美森细胞科技有限公司。
1.1.2 主要试剂SNHG1小干扰RNA (si-SNHG1) 及其阴性对照(si-NC)、miR-145-5p模拟物(miR-145-5p mimic) 及其阴性对照(mimic NC)、miR-145-5p抑制物(miR-145-5p inhibitor) 及其阴性对照(inhibitor NC),均购自赛默飞世尔科技(中国) 有限公司;CCK-8试剂盒,购自上海继和生物科技有限公司;Annexin V-FITC/PI细胞凋亡试剂盒,购自无锡云萃生物科技有限公司;大鼠超氧化物歧化酶(superoxide dismutase,SOD)、丙二醛(malondialdehyde,MDA) 试剂盒,购自上海广锐生物科技有限公司;兔源一抗PDCD4、caspase 3、Bcl-2、Bax、GAPDH及过氧化物酶标记的羊抗兔IgG二抗,均购自英国Abcam公司。
1.2 方法 1.2.1 细胞培养、H/R细胞模型的构建及实验分组将H9c2细胞在含有10%胎牛血清的DMEM培养基中培养,培养条件为37 ℃和5%CO2。
H/R细胞模型的构建[6]: 将H9c2细胞在缺氧培养箱(37 ℃、94%N2、1%O2、5%CO2) 中培养24 h,再在复氧培养箱(37 ℃、95%空气、5%CO2) 中复氧1 h。
将H9c2细胞分为H/R组、si-NC组、si-SNHG1组、mimic NC组、miR-145-5p mimic组、si-SNHG1+inhibitor NC组、si-SNHG1+miR-145-5p inhibitor组。上述各组细胞进行相应的转染处理48 h后,再进行缺氧24 h、复氧1 h。si-NC组、si-SNHG1组、mimic NC组、miR-145-5p mimic组H9c2细胞分别转染si-NC、si-SNHG1、mimic NC、miR-145-5p mimic,si-SNHG1+inhibitor NC组H9c2细胞同时转染si-SNHG1和inhibitor NC,si-SNHG1+miR-145-5p inhibitor组H9c2细胞同时转染si-SNHG1和miR-145-5p inhibitor。同时取正常培养的H9c2细胞作为对照组(NC组)。上述处理结束后,收集各组细胞用于后续实验。
1.2.2 实时定量PCR (real-time quantitative PCR,qRT- PCR) 检测细胞中SNHG1、miR-145-5p表达使用TRIzol试剂提取H9c2细胞中的总RNA,将总RNA逆转录为cDNA,以cDNA为模板进行定量PCR。GAPDH、U6分别作为SNHG1、miR-145-5p内参。采用2-ΔΔCt法计算SNHG1、miR-145-5p相对表达量。引物序列: GAPDH,正向5’-CACCATTGGCAATGAGCGGTTC-3’,反向5’-CACCATTGGCAATGAGCGGTTC-3’;SNHG1,正向5’-AACTTCCCATAACTCCACTTC-3’,反向5’-ACAACCAACACAGCAACAC-3’;miR-145-5p,正向5’-TCGGCAGGGTCCAGTTTTCCCA-3’,反向5’-CTCAAC TGGTGTCGTGGA-3’;U6,正向5’-CTCGCTTCGGCAGCACA-3’,反向5’-AACGCTTCACGAATTTGCGT-3’。
1.2.3 CCK-8检测细胞增殖将各组H9c2细胞以1×104/孔的密度接种到96孔板中,培养48 h后,将10 μL CCK-8试剂添加到96孔板的每个孔中,将96孔板在37 ℃下孵育1.5 h,使用酶标仪在450 nm处读取光密度值(optical density,OD)。
1.2.4 流式细胞术检测H9c2细胞凋亡将各组H9c2细胞用预冷的PBS洗涤2次,重悬于1×结合缓冲液中,然后在室温下依次与5 μL Annexin V-FITC、5 μL碘化丙啶在黑暗条件下孵育5 min。使用流式细胞仪检测细胞凋亡。
1.2.5 试剂盒检测H9c2细胞中SOD活性、MDA含量按照试剂盒说明书检测H9c2细胞中SOD活性、MDA含量。
1.2.6 Western blotting检测H9c2细胞中PDCD4、Bcl-2、caspase 3、Bax蛋白表达RIPA裂解缓冲液裂解H9c2细胞并提取蛋白质,蛋白质经定量、电泳、转膜、封闭后,将膜与一抗PDCD4 (1∶2 000)、Bcl-2 (1∶2 000)、caspase 3 (1∶2 000)、Bax (1∶1 000)、GAPDH (1∶2 000) 在4 ℃下孵育过夜。随后,将膜与辣根过氧化物酶标记的山羊抗兔二抗(1∶1 000) 在室温下孵育1 h,再次用TBST缓冲液洗涤膜3次,加入ECL试剂,观察蛋白质条带,使用ImageJ分析蛋白灰度值。
1.2.7 双荧光素酶报告基因实验分别构建SNHG1野生型质粒(SNHG1-WT) 和突变型质粒(SNHG1- MUT),将SNHG1-WT和SNHG1-MUT分别与mimic NC或miR-145-5pmimic共转染于H9c2细胞,48 h后观察荧光素酶活性变化。
分别构建PDCD4野生型质粒(PDCD4-WT) 和突变型质粒(PDCD4-MUT),将PDCD4-WT和PDCD4-MUT分别与mimic NC或miR-145-5pmimic共转染于H9c2细胞,48 h后观察荧光素酶活性变化。
1.3 统计学分析采用SPSS 22.0软件处理数据。计量资料以x±s表示,多组数据的比较采用单因素方差分析,进一步2组数据的比较采用SNK-q检验。P < 0.05为差异有统计学意义。
2 结果 2.1 各组H9c2细胞中SNHG1、miR-145-5p、PDCD4蛋白表达比较与NC组比较,H/R组H9c2细胞中SNHG1、PDCD4蛋白表达升高,miR-145-5p表达降低(P < 0.05)。与H/R组、si-NC组比较,si-SNHG1组H9c2细胞中SNHG1、PDCD4蛋白表达降低,miR-145-5p表达升高(P < 0.05)。与H/R组、mimic NC组比较,miR-145-5p mimic组H9c2细胞中SNHG1表达变化的差异无统计学意义(P > 0.05),miR-145-5p表达升高,PDCD4蛋白表达降低(P < 0.05)。与si-SNHG1组、si-SNHG1+inhibitor NC组比较,si-SNHG1+miR-145-5p inhibitor组H9c2细胞中SNHG1表达变化的差异无统计学意义(P > 0.05),miR-145-5p表达降低,PDCD4蛋白表达升高(P < 0.05)。见图 1、表 1。
|
| 1, NC group; 2, H/R group; 3, si-NC group; 4, si-SNHG1 group; 5, mimic NC group; 6, miR-145-5p mimic group; 7, si-SNHG1+inhibitor NC group; 8, si-SNHG1+miR-145-5p inhibitor group. 图 1 Western blotting检测各组细胞中PDCD4蛋白的表达 Fig.1 PDCD4 protein expression detected by Western blotting in each study group |
| Group | SNHG1 | miR-145-5p | PDCD4 |
| NC | 1.00 ±0.00 | 1.00 ±0.00 | 0.35 ±0.03 |
| H/R | 2.32 ±0.161) | 0.21 ±0.021) | 1.54 ±0.131) |
| si-NC | 2.30 ±0.14 | 0.22 ±0.01 | 1.56 ±0.14 |
| si-SNHG1 | 1.26 ±0.132),3) | 0.83 ±0.072),3) | 0.62 ±0.052),3) |
| mimic NC | 2.31 ±0.15 | 0.20 ±0.01 | 1.53 ±0.11 |
| miR-145-5p mimic | 2.29 ±0.13 | 0.96 ±0.082),5) | 0.51 ±0.042),5) |
| si-SNHG1+inhibitor NC | 1.24 ±0.12 | 0.85 ±0.08 | 0.60 ±0.04 |
| si-SNHG1+miR-145-5p inhibitor | 1.23 ±0.11 | 0.33 ±0.034),6) | 1.12 ±0.084),6) |
| 1) P < 0.05 vs NC group;2) P < 0.05 vs H/R group;3) P < 0.05 vs si-NC group;4) P < 0.05 vs si-SNHG1 group;5) P < 0.05 vs mimic NC group;6) P < 0.05 vs si-SNHG1+inhibitor NC group. | |||
2.2 各组H9c2细胞增殖能力比较
NC组、H/R组、si-NC组、si-SNHG1组、mimic NC组、miR-145-5p mimic组、si-SNHG1+inhibitor NC组、si-SNHG1+miR-145-5p inhibitor组H9c2细胞OD450值分别为0.87±0.07、0.31±0.02、0.29±0.01、0.69±0.05、0.30±0.03、0.72±0.06、0.70±0.06、0.38±0.03。与NC组比较,H/R组H9c2细胞OD450值降低(P < 0.05);与H/R组、si-NC组比较,si-SNHG1组H9c2细胞OD450值升高(P < 0.05);与H/R组、mimic NC组比较,miR-145-5p mimic组H9c2细胞OD450值升高(P < 0.05);与si-SNHG1组、si-SNHG1+inhibitor NC组比较,si-SNHG1+miR-145-5p inhibitor组H9c2细胞OD450值降低(P < 0.05)。
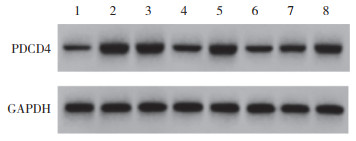
2.3 各组H9c2细胞凋亡能力比较NC组、H/R组、si-NC组、si-SNHG1组、mimic NC组、miR-145-5p mimic组、si-SNHG1+inhibitor NC组、si-SNHG1+miR-145-5p inhibitor组H9c2细胞凋亡率分别为(3.79±0.14) %、(18.86±1.15) %、(18.72±1.12) %、(6.78±0.34) %、(18.80±1.07) %、(5.49±0.26) %、(6.69±0.29) %、(13.34±1.17) %。与NC组比较,H/R组H9c2细胞凋亡率升高(P < 0.05);与H/R组、si-NC组比较,si-SNHG1组H9c2细胞凋亡率降低(P < 0.05);与H/R组、mimic NC组比较,miR-145-5p mimic组H9c2细胞凋亡率降低(P < 0.05);与si-SNHG1组、si-SNHG1+inhibitor NC组比较,si-SNHG1+miR-145-5p inhibitor组H9c2细胞凋亡率升高(P < 0.05)。见图 2。
|
| A, NC group; B, H/R group; C, si-NC group; D, si-SNHG1 group; E, mimic NC group; F, miR-145-5p mimic group; G, si-SNHG1+inhibitor NC group; H, si-SNHG1+miR-145-5p inhibitor group. 图 2 流式细胞术检测H9c2细胞凋亡 Fig.2 H9c2 cell apoptosis detected by flow cytometry |
2.4 各组H9c2细胞中SOD活性、MDA含量比较
与NC组比较,H/R组H9c2细胞中SOD活性降低,MDA含量升高(P < 0.05);与H/R组、si-NC组比较,si-SNHG1组H9c2细胞中SOD活性升高,MDA含量降低(P < 0.05);与H/R组、mimic NC组比较,miR-145-5pmimic组H9c2细胞中SOD活性升高,MDA含量降低(P < 0.05);与si-SNHG1组、si-SNHG1+inhibitor NC组比较,si-SNHG1+miR-145-5p inhibitor组H9c2细胞中SOD活性降低,MDA含量升高(P < 0.05)。见表 2。
| Group | SOD (U/mL) | MDA (mmol/mL) |
| NC | 68.83 ±2.34 | 322.27 ±14.42 |
| H/R | 17.74 ±0.861) | 754.66 ±32.241) |
| si-NC | 17.65 ±0.82 | 758.81 ±31.77 |
| si-SNHG1 | 49.66 ±2.552),3) | 382.24 ±16.642),3) |
| mimic NC | 17.42 ±0.73 | 760.63 ±33.44 |
| miR-145-5p mimic | 53.36 ±2.752),5) | 359.91 ±14.432),5) |
| si-SNHG1+inhibitor NC | 50.51 ±2.48 | 380.33 ±15.59 |
| si-SNHG1+miR-145-5p inhibitor | 30.22 ±1.514),6) | 576.34 ±27.724),6) |
| 1) P < 0.05 vs NC group;2) P < 0.05 vs H/R group;3) P < 0.05 vs si-NC group;4) P < 0.05 vs si-SNHG1 group;5) P < 0.05 vs mimic NC group;6) P < 0.05 vs si-SNHG1+inhibitor NC group. | ||
2.5 各组H9c2细胞中Bax、Bcl-2、caspase 3蛋白表达比较
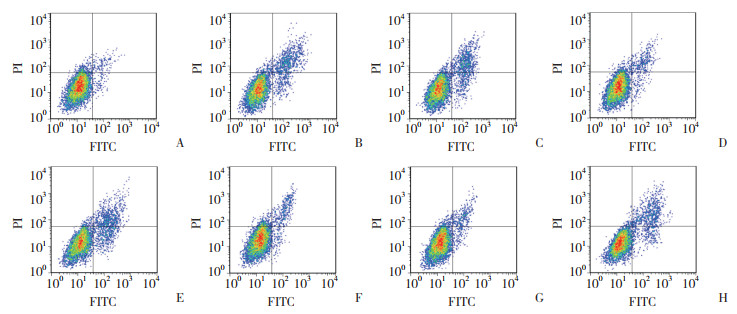
与NC组比较,H/R组H9c2细胞中Bax、caspase 3蛋白表达升高,Bcl-2蛋白表达降低(P < 0.05);与H/R组、si-NC组比较,si-SNHG1组H9c2细胞中Bax、caspase 3蛋白表达降低,Bcl-2蛋白表达升高(P < 0.05);与H/R组、mimic NC组比较,miR-145-5p mimic组H9c2细胞中Bax、caspase 3蛋白表达降低,Bcl-2蛋白表达升高(P < 0.05);与si-SNHG1组、si-SNHG1+inhibitor NC组比较,si-SNHG1+miR-145-5p inhibitor组H9c2细胞中Bax、caspase 3蛋白表达升高,Bcl-2蛋白表达降低(P < 0.05)。见图 3、表 3。
|
| 1, NC group; 2, H/R group; 3, si-NC group; 4, si-SNHG1 group; 5, mimic NC group; 6, miR-145-5p mimic group; 7, si-SNHG1+inhibitor NC group; 8, si-SNHG1+miR-145-5p inhibitor group. 图 3 Western blotting检测各组细胞中Bax、Bcl-2、caspase 3蛋白的表达 Fig.3 Bax, Bcl-2, and caspase 3 protein expression detected by Western blotting by study group |
| Group | Bax/GAPDH | Bcl-2/GAPDH | caspase 3/GAPDH |
| NC | 0.27 ±0.02 | 1.32 ±0.11 | 0.32 ±0.03 |
| H/R | 0.95 ±0.081) | 0.42 ±0.041) | 1.43 ±0.121) |
| si-NC | 0.97 ±0.09 | 0.44 ±0.03 | 1.45 ±0.11 |
| si-SNHG1 | 0.38 ±0.032),3) | 0.97 ±0.082),3) | 0.59 ±0.042),3) |
| mimic NC | 0.96 ±0.07 | 0.43 ±0.03 | 1.44 ±0.10 |
| miR-145-5p mimic | 0.35 ±0.022),5) | 1.13 ±0.102),5) | 0.67 ±0.052),5) |
| si-SNHG1+inhibitor NC | 0.39 ±0.02 | 0.99 ±0.08 | 0.60 ±0.05 |
| si-SNHG1+miR-145-5p inhibitor | 0.65 ±0.054),6) | 0.68 ±0.054),6) | 0.96 ±0.084),6) |
| 1) P < 0.05 vs NC group;2) P < 0.05 vs H/R group;3) P < 0.05 vs si-NC group;4) P < 0.05 vs si-SNHG1 group;5) P < 0.05 vs mimic NC group;6) P < 0.05 vs si-SNHG1+inhibitor NC group. | |||
2.6 SNHG1靶向调控miR-145-5p/PDCD4轴
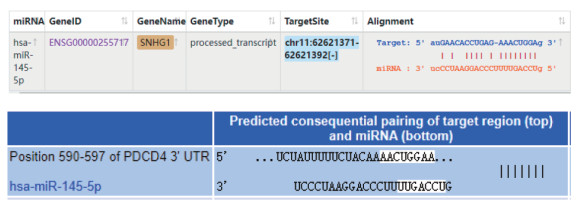
在Starbase (http://starbase.sysu.edu.cn/)、Target Scan (https://www.targetscan.org/vert_72/) 网站分别预测lncRNA SNHG1与miR-145-5p、miR-145-5p与PDCD4的结合位点,见图 4。与mimic NC和SNHG1-WT共转染组比较,miR-145-5p mimic和SNHG1-WT共转染组的荧光素酶活性降低(分别为1.05±0.12和0.23±0.01,P < 0.05);与mimic NC和SNHG1-MUT共转染组比较,miR-145-5p mimic和SNHG1-MUT共转染组荧光素酶活性无显著变化(分别为1.03±0.11和1.02±0.10,P > 0.05);与mimic NC和PDCD4-WT共转染组比较,miR-145-5p mimic和PDCD4-WT共转染组的荧光素酶活性降低(分别为1.03±0.10和0.29±0.02,P < 0.05);与mimic NC和PDCD4-MUT共转染组比较,miR-145-5p mimic和PDCD4-MUT共转染组荧光素酶活性无显著变化(分别为0.97±0.08和1.01±0.09,P > 0.05)。
|
| 图 4 Starbase、TargetScan网站分别预测lncRNA SNHG1与miR-145-5p、miR-145-5p与PDCD4的结合位点 Fig.4 Binding sites of lncRNA SNHG1 and miR-145-5p as well as of miR-145-5p and PDCD4 predicted at Starbase and TargetScan websites |
3 讨论
AMI是冠状动脉急性闭塞引起的心肌损伤,严重威胁人类生命健康。尽管AMI的诊断和治疗在过去几十年中有所进展,但全世界其发病率和死亡率仍在上升[7]。因此,早期发现和干预对于减少心肌损伤和改善患者预后是必要的。
SNHG1是一种新发现的lncRNA,研究[8]报道,沉默SNHG1可抑制脓毒症小鼠心肌损伤;敲低SNHG1可抑制脂多糖诱导的PC12细胞凋亡[9]。以上研究表明,SNHG1在调控细胞凋亡和心肌损伤方面具有重要作用。SOD和MDA是氧化应激的标志物;Bax、Bcl-2、caspase 3是常用于评估细胞凋亡的蛋白,Bcl-2是一种抗凋亡蛋白,而Bax、caspase 3是促凋亡效应蛋白。本研究显示,SNHG1在H/R诱导的H9c2细胞中高表达,沉默SNHG1可抑制H/R诱导的H9c2细胞凋亡和氧化应激,提示SNHG1可能是治疗AMI的潜在有效靶点。
lncRNA可通过海绵化微RNA (microRNA,miRNA) 发挥作用。本研究通过生物信息学分析和双荧光素酶报告基因实验,证实SNHG1与miR-145-5p存在靶向关系。miR-145-5p作为一种miRNA,已有研究报道,下调miR-145-5p可加重心肌梗死小鼠心肌损伤[10],过表达miR-145-5p可减轻心肌缺血/再灌注损伤中的细胞凋亡[11]。以上研究表明,miR-145-5p在AMI进展中发挥重要调控作用。本研究结果与上述研究结果一致,本研究显示,miR-145-5p在H/R诱导的H9c2细胞中低表达,过表达miR-145-5p可抑制H/R诱导的H9c2细胞凋亡和氧化应激。此外,本研究还发现沉默SNHG1可上调H/R诱导的H9c2细胞中miR-145-5p表达,推测沉默SNHG1可能通过上调miR-145-5p抑制H/R诱导的H9c2细胞凋亡和氧化应激。为了验证这一推测,本研究在沉默SNHG1的基础上应用miR-145-5p inhibitor干预H/R诱导的H9c2细胞,结果显示,miR-145-5p inhibitor减弱了沉默SNHG1对H/R诱导的H9c2细胞凋亡和氧化应激的影响。本研究证实了这一推测,即沉默SNHG1可能通过上调miR-145-5p抑制H/R诱导的H9c2细胞凋亡和氧化应激。
miRNA是一类非编码RNA,通过与其靶基因mRNA的3’非翻译区结合,在转录后水平负调控基因表达。本研究证实了PDCD4为miR-145-5p的靶基因。PDCD4基因定位于染色体10q24上[12]。研究显示,沉默PDCD4能够减弱H/R诱导的心肌细胞凋亡和氧化应激损伤[13],抑制PDCD4可抑制阿霉素诱导的大鼠心肌细胞凋亡[14]。以上研究表明,PDCD4在调控心肌细胞凋亡和氧化应激方面发挥重要作用。本研究显示,PDCD4蛋白在H/R诱导的H9c2细胞中高表达,沉默SNHG1后,H/R诱导的H9c2细胞中miR-145-5p表达升高,而PDCD4蛋白表达降低,双荧光素酶报告基因实验证实了SNHG1与miR-145-5p、miR-145-5p与PDCD4存在靶向关系。证实了沉默SNHG1可能通过调控miR-145-5p/PDCD4轴,抑制H/R诱导的H9c2细胞凋亡和氧化应激。
综上所述,沉默SNHG1可能通过上调miR-145-5p来抑制PDCD4表达,进而抑制H/R诱导的H9c2细胞凋亡和氧化应激。本研究尚存在不足之处,仅进行了体外实验,未进行体内实验探究SNHG1对H/R诱导的H9c2细胞凋亡的影响,后期将进行进一步体内研究。
| [1] |
HIEDA M, GOTO Y. Cardiac mechanoenergetics in patients with acute myocardial infarction: from pressure-volume loop diagram related to cardiac oxygen consumption[J]. Heart Fail Clin, 2020, 16(3): 255-269. DOI:10.1016/j.hfc.2020.02.002 |
| [2] |
刘蕾, 赵雪东, 王智彬. 北五味子多糖对缺氧/复氧心肌细胞氧化应激损伤的保护作用[J]. 中西医结合心脑血管病杂志, 2022, 20(12): 2174-2179. DOI:10.12102/j.issn.1672-1349.2022.12.010 |
| [3] |
OUYANG M, LU J, DING Q, et al. Knockdown of long non-coding RNA PVT1 protects human AC16 cardiomyocytes from hypoxia/ reoxygenation-induced apoptosis and autophagy by regulating miR-186/Beclin-1 axis[J]. Gene, 2020, 754: 144775. DOI:10.1016/j.gene.2020.144775 |
| [4] |
杨涛, 李小玲, 阳承艳, 等. lncRNA SNHG1调控PI3K/AKT/NF-κB信号通路对小鼠心肌缺血/再灌注损伤的影响[J]. 广西医科大学学报, 2022, 39(7): 1054-1060. DOI:10.16190/j.cnki.45-1211/r.2022.07.005 |
| [5] |
张朝华, 刘旭帮, 朱银川, 等. miR-145通过调控PDCD4表达抑制缺氧/复氧所诱导的心肌细胞凋亡[J]. 中国循证心血管医学杂志, 2021, 13(10): 1194-1197. DOI:10.3969/j.issn.1674-4055.2021.10.11 |
| [6] |
徐敏, 岳峰, 宋勃, 等. miR-25通过TGF-β1途径降低缺氧/复氧诱导的心肌细胞凋亡[J]. 中国老年学杂志, 2022, 42(12): 3045-3048. DOI:10.3969/j.issn.1005-9202.2022.12.053 |
| [7] |
CHEN M, GUO Y, SUN Z, et al. Long non-coding RNA SENCR alleviates hypoxia/reoxygenation-induced cardiomyocyte apoptosis and inflammatory response by sponging miR-1[J]. Cardiovasc Diagn Ther, 2021, 11(3): 707-715. DOI:10.21037/cdt-20-1037 |
| [8] |
ZHANG R, NIU Z, LIU J, et al. LncRNA SNHG1 promotes sepsisinduced myocardial injury by inhibiting Bcl-2 expression via DNMT1[J]. J Cell Mol Med, 2022, 26(13): 3648-3658. DOI:10.1111/jcmm.17358 |
| [9] |
ZHOU J, LI Z, ZHAO Q, et al. Knockdown of SNHG1 alleviates autophagy and apoptosis by regulating miR-362-3p/Jak2/stat3 pathway in LPS-injured PC12 cells[J]. Neurochem Res, 2021, 46(4): 945-956. DOI:10.1007/s11064-020-03224-7 |
| [10] |
ZHOU W, JI L, LIU X, et al. AIFM1, negatively regulated by miR-145-5p, aggravates hypoxia-induced cardiomyocyte injury[J]. Biomed J, 2022, 45(6): 870-882. DOI:10.1016/j.bj.2021.11.012 |
| [11] |
TAN L, LIU L, YAO J, et al. miR-145-5p attenuates inflammatory response and apoptosis in myocardial ischemia-reperfusion injury by inhibiting (NADPH) oxidase homolog 1[J]. Exp Anim, 2021, 70(3): 311-321. DOI:10.1538/expanim.20-0160 |
| [12] |
CAI Q, YANG HS, LI YC, et al. Dissecting the roles of PDCD4 in breast cancer[J]. Front Oncol, 2022, 12: 855807. DOI:10.3389/fonc.2022.855807 |
| [13] |
尤其, 郭辉. lncRNA SNHG6调控miR-335-3p/PDCD4途径对缺氧复氧诱导的心肌细胞损伤的影响[J]. 心电与循环, 2021, 40(4): 355-361. DOI:10.12124/j.issn.2095-3933.2021.4.2021-4260 |
| [14] |
梁丽英, 刘欢, 张永琴, 等. miR-21靶向调控PDCD4在四逆汤减轻大鼠心肌细胞损伤中的意义[J]. 山东医药, 2019, 59(23): 14-18. DOI:10.3969/j.issn.1002-266X.2019.23.003 |
 2023, Vol. 52
2023, Vol. 52