文章信息
- 李俞羲, 路遥, 田野
- LI Yuxi, LU Yao, TIAN Ye
- HOXA10基因敲低对非小细胞肺癌安罗替尼敏感性的影响
- Effect of HOXA10 knockdown on the sensitivity of non-small cell lung cancer cells to anlotinib
- 中国医科大学学报, 2022, 51(6): 508-512
- Journal of China Medical University, 2022, 51(6): 508-512
-
文章历史
- 收稿日期:2021-10-22
- 网络出版时间:2022-06-02 9:58
2. 中国医科大学附属第四医院胸外科,沈阳 110032
2. Department of Thoracic Surgery, The Fourth Affiliated Hospital of China Medical University, Shenyang 11003, China
肺癌是全球发病率和死亡率最高的恶性肿瘤[1],严重威胁人类健康。非小细胞肺癌(non-small cell lung cancer,NSCLC) 是肺癌的最常见类型,约占确诊肺癌的80%~85%[1]。目前,NSCLC的治疗手段主要包括外科手术、放疗、化疗、靶向治疗和免疫治疗。尽管近年来NSCLC的治疗方法不断进步,但是由于多数NSCLC患者确诊时已属临床Ⅳ期,无法采用外科手术切除,而以铂类为基础的化疗存在耐药性[2]。目前NSCLC患者的5年生存率仅为10%~15%[1],因此寻找更有效的临床治疗方法对提高患者生存率十分重要。
安罗替尼是小分子多靶点酪氨酸激酶抑制剂,能够有效抑制血管内皮生长因子受体、血小板源生长因子受体和成纤维生长因子受体等[3]。临床研究[4-5]表明,安罗替尼作为三线药物可以显著延长NSCLC患者的总生存期和无进展生存期。RNA高通量测序和分析发现同源异型盒基因A10 (homeobox A10,HOXA10) 与NSCLC对安罗替尼的耐药性相关[6],然而具体的作用机制尚未阐明。研究抗肿瘤药物的耐药机制有利于改善治疗效果,进一步优化治疗方案。因此,本研究通过敲低HOXA10,探讨HOXA10对NSCLC细胞安罗替尼敏感性的影响。
1 材料与方法 1.1 材料人胚肺成纤维细胞MRC-5、人肺癌细胞A549和PC-9购自中国科学院上海细胞库。安罗替尼购自美国MCE公司。DMEM培养基、胎牛血清、HOXA10小干扰RNA (small interfering RNA,siRNA)、对照siRNA和Lipofectamine 2000转染试剂购自美国Thermo Fisher公司。CCK-8试剂、Annexin V凋亡检测试剂盒购自碧云天公司。HOXA10、GAPDH抗体购自美国Santa Cruz公司。Transwell小室购自美国康宁公司。
1.2 细胞培养和转染人肺癌细胞A549和PC-9培养于含10%胎牛血清的DMEM培养基内,培养液内含有青霉素100 U/mL、链霉素100 μg/mL。细胞均置于含5% CO2的37℃培养箱内培养,0.25%胰酶-EDTA消化传代,细胞处于对数生长期时用于实验。当细胞生长融合度为70%~80%时,按照Lipofectamine 2000试剂说明书转染si-NC (对照组)或si-HOXA10。
1.3 RNA提取和实时定量PCR采用TRIzol提取细胞总RNA,用QuantiTect ReverseTranscription试剂盒反转录为cDNA,随后使用SYBR Green PCR Master Mix进行实时定量PCR。引物序列:HOXA10,正向5’-CTCGCCCATAGACCTGTGG-3’,反向5’-GTTCTGCGCGAAAGAGCAC-3’;GAPDH,正向5’-TGTGGGCATCAATGGATTTGG-3’,反向5’-ACACCATGTATTCCGGGTCAAT-3’。采用2-ΔΔCt法计算目的基因表达。
1.4 蛋白提取和Western blotting采用RIPA裂解液提取细胞总蛋白,BCA法测定蛋白浓度。取各样本等量蛋白进行SDS-聚丙烯酰胺凝胶电泳,湿转将蛋白转移至PVDF膜。5%脱脂奶粉室温封闭1 h后,分别孵育HOXA10 (1∶500) 或者GAPDH (1∶1 000) 一抗4 ℃过夜。洗膜后,室温孵育耦联HRP的二抗1 h。采用ECL发光液检测蛋白条带,GAPDH为内参。
1.5 CCK-8法采用CCK-8法检测细胞增殖活性,以评估安罗替尼细胞毒性。将转染后的A549和PC-9细胞接种于96孔培养板中,以不同浓度(1、2、4、8、10、15、25、50、95 μg/mL) 安罗替尼处理细胞。安罗替尼处理24 h后,每孔加入10 μL CCK-8试剂,37 ℃孵育1 h。酶标仪检测450 nm吸光度。每组设置至少3个复孔。
1.6 克隆形成实验A549和PC-9细胞转染24 h后,以0.25%胰酶-EDTA消化,用含10%胎牛血清的DMEM培养基重悬并接种至6孔板,细胞密度为800/孔。继续培养14 d,4%多聚甲醛固定后进行0.1%结晶紫染色,拍照记录克隆数。
1.7 Transwell法检测细胞迁移和侵袭能力细胞迁移实验不需预包被Transwell小室,细胞侵袭实验前需用Matrigel包被Transwell小室。将转染后的A549和PC-9细胞悬液加入Transwell上室无血清培养,Transwell下室加入含10%胎牛血清的DMEM培养液。Transwell上室和下室中均含4 μg/mL安罗替尼,细胞在含5% CO2的37℃培养箱内培养48 h,用棉签擦去Transwell上室细胞。4%多聚甲醛固定后以0.1%结晶紫染色。随机选取5个视野,计数每个视野中的迁移或侵袭细胞数。
1.8 流式细胞术检测细胞凋亡采用Annexin V/碘化丙啶染色,经流式细胞术检测细胞凋亡率。转染后的细胞用8 μg/mL安罗替尼处理24 h。细胞以胰酶消化,用PBS洗涤3次后重悬于binding buffer,加入Annexin-V-FITC和碘化丙啶溶液避光染色30 min。用流式细胞仪检测细胞凋亡率,Annexin V阳性为早期凋亡细胞,Annexin V和碘化丙啶双阳性为晚期凋亡细胞。
1.9 统计学分析采用SPSS 22.0软件进行统计分析。计量资料以x±s表示,多组间比较采用单因素方差分析,2组间比较采用t检验。P < 0.05为差异有统计学意义。
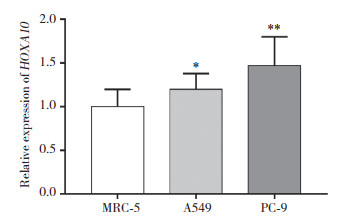
2 结果 2.1 HOXA10在NSCLC中呈高表达与人胚肺成纤维细胞MRC-5相比,HOXA10在人肺癌细胞A549和PC-9中呈高表达,差异有统计学意义(P = 0.030 3,P = 0.001 2),表明HOXA10在NSCLC细胞中呈高表达。见图 1。
|
| * P < 0.05 vs MRC-5 cells; ** P < 0.01 vs MRC-5 cells. 图 1 HOXA10在NSCLC细胞中的表达水平 Fig.1 Expression of HOXA10 in NSCLC cell lines |
2.2 敲低HOXA10降低安罗替尼在A549和PC-9细胞中的半数抑制浓度(half-maximal inhibitory concentration,IC50)
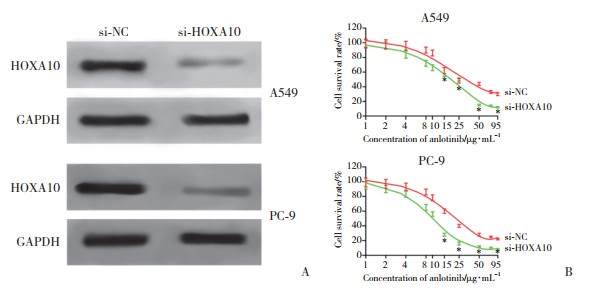
为了进一步研究HOXA10对安罗替尼药物敏感性的影响,分别将si-NC和si-HOXA10转染至A549和PC-9细胞。细胞转染后48 h,采用Western blotting检测HOXA10表达水平。与转染si-NC的A549和PC-9细胞相比,转染si-HOXA10的细胞中HOXA10表达水平显著降低,见图 2A。
|
| A, HOXA10 expression after HOXA10 knockdown detected using Western blotting; B, half-maximal inhibitory concentration (IC50) of anlotinib after HOXA10 knockdown detected using the CCK-8 assay. * P < 0.05 vs si-NC. 图 2 敲低HOXA10降低安罗替尼在A549和PC-9细胞中的IC50 Fig.2 Half-maximal inhibitory concentration (IC50) of anlotinib after HOXA10 knockdown in A549 and PC-9 cells |
将转染后的细胞以不同浓度(1、2、4、8、10、15、25、50、95 μg/mL) 安罗替尼处理24 h,采用CCK-8法检测细胞增殖活性,结果显示,敲低HOXA10的A549和PC-9细胞的生存率显著低于对照组(P < 0.05),说明安罗替尼对敲低HOXA10的细胞增殖有抑制作用。见图 2B。此外,敲低HOXA10会降低安罗替尼在A549和PC-9细胞中的IC50,si-NC-A549细胞和si-HOXA10-A549细胞中安罗替尼的IC50分别为(35.29±3.24) 和(18.33±2.07) μg/mL,si-NC-PC-9细胞和si-HOXA10-PC-9细胞中安罗替尼的IC50分别为(24.32±4.06) 和(10.31± 2.83) μg/mL,差异均有统计学意义(P < 0.001)。
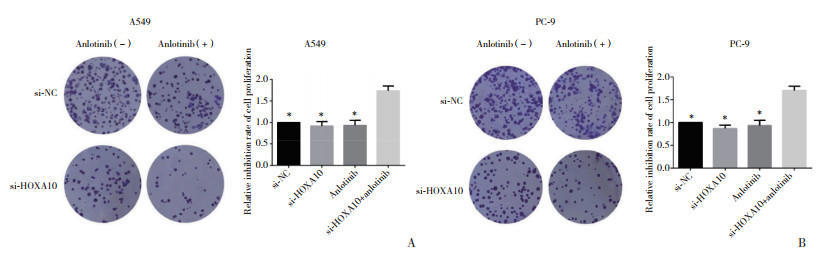
2.3 敲低HOXA10后安罗替尼对细胞增殖的抑制作用增强克隆形成实验结果表明,A549和PC-9细胞中,未经处理的转染si-NC的细胞(si-NC组)、未经处理的转染si-HOXA10的细胞(si-HOXA10组)、经4 μg/mL安罗替尼处理的细胞(Anlotinib组) 比较,细胞增殖抑制率的差异无统计学意义(均P > 0.05),经4 μg/mL安罗替尼处理的转染si-HOXA10的细胞(si-HOXA10+anlotinib组) 与上述3组细胞比较,细胞增殖抑制率明显增高(均P < 0.05),说明敲低HOXA10后安罗替尼对细胞增殖的抑制作用增强。见图 3。
|
| A, inhibition of cell proliferation by anlotinib is enhanced after HOXA10 knockdown in A549 cells; B, inhibition of cell proliferation by anlotinib is enhanced after HOXA10 knockdown in PC-9 cells. * P < 0.05 vs si-HOXA10+anlotinib. 图 3 敲低HOXA10后安罗替尼对细胞增殖抑制作用增强 Fig.3 Inhibition of cell proliferation by anlotinib is enhanced after HOXA10 knockdown |
2.4 敲低HOXA10后安罗替尼对细胞迁移和侵袭的抑制作用增强
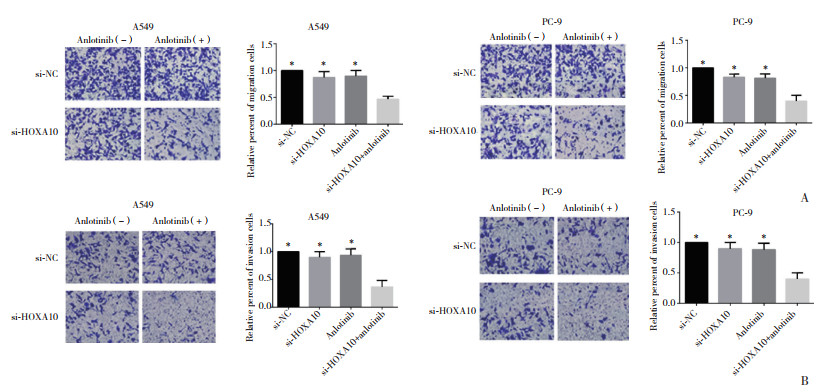
Transwell细胞迁移和侵袭实验表明,A549和PC-9细胞中,未经处理的转染si-NC的细胞(si-NC组)、未经处理的转染si-HOXA10的细胞(si-HOXA10组)、经4 μg/mL安罗替尼处理的细胞(Anlotinib组) 比较,细胞迁移和侵袭相对数量的差异无统计学意义(均P > 0.05),经4 μg/mL安罗替尼处理的转染si-HOXA10的细胞(si-HOXA10+anlotinib组) 与上述3组细胞比较,细胞迁移和侵袭相对数量明显降低(均P < 0.05),说明敲低HOXA10后安罗替尼对细胞迁移和侵袭的抑制作用增强。见图 4。
|
| A, Transwell migration assay (×400);B, Transwell invasion assay (×400). * P < 0.05 vs si-HOXA10+anlotinib. 图 4 敲低HOXA10后安罗替尼对细胞迁移和侵袭抑制作用增强 Fig.4 Anlotinib-induced inhibition of cell migration and invasion is enhanced after HOXA10 knockdown |
2.5 敲低HOXA10促进安罗替尼诱导的细胞凋亡
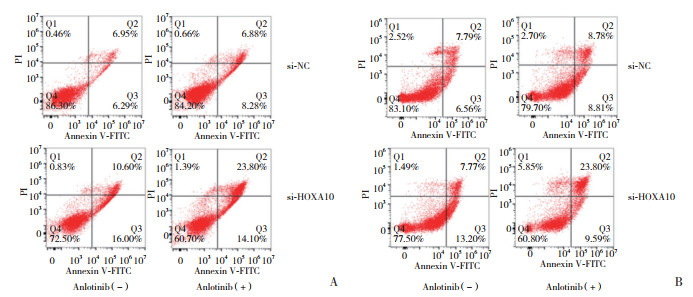
流式细胞术结果(图 5) 显示,8 μg/mL安罗替尼诱导转染si-NC的A549或PC-9细胞凋亡。未经处理的si-NC-A549细胞凋亡率为(14.14±3.9) %;经安罗替尼处理的si-NC-A549细胞凋亡率为(15.11±4.2) %;未经处理的si-HOXA10-A549细胞凋亡率为(18.63±3.8) %;经安罗替尼处理的si-HOXA10-A549细胞凋亡率为(36.9±4.5) %;未经处理的si-NC-PC-9细胞凋亡率为(16.31±4.2) %;经安罗替尼处理的si-NC-PC-9细胞凋亡率为(16.59±3.7) %;未经处理的si-HOXA10-PC-9细胞凋亡率为(20.78±3.8) %;经安罗替尼处理的si-HOXA10-PC-9细胞凋亡率为(32.31±3.9) %。与对照组相比,相同浓度安罗替尼显著上调敲低HOXA10的A549或PC-9细胞的凋亡率,差异有统计学意义(均P < 0.001)。结果表明,敲低HOXA10促进安罗替尼诱导的细胞凋亡。
|
| A, anlotinib-induced apoptosis is enhanced after HOXA10 knockdown in A549 cells; B, anlotinib-induced apoptosis is enhanced after HOXA10 knockdown in PC-9 cells. 图 5 敲低HOXA10促进安罗替尼诱导的细胞凋亡 Fig.5 Anlotinib-induced apoptosis is enhanced after HOXA10 knockdown |
3 讨论
肿瘤耐药性在晚期NSCLC患者的治疗中几乎无法避免。尽管第一代酪氨酸激酶抑制剂吉菲替尼、厄洛替尼和埃克替尼等被证明能够有效治疗NSCLC,但研究[7]发现,在中位治疗时间10个月后患者会出现耐药问题。近年来研究发现,肿瘤耐药是多种基因共同作用的结果,鉴定相关耐药分子并阐明其作用机制,对增加肿瘤细胞药物敏感性、提高临床疗效十分重要。
HOXA10属于同源异型盒基因家族,该家族成员多为转录因子,以高度保守的DNA结合结构域调控下游目的基因表达[8]。HOX基因家族许多成员在肿瘤中异常表达,参与调控肿瘤的发生、发展。HOXA10在多种恶性肿瘤中发挥促癌基因功能[9-10]。研究[11]发现,HOXA10在NSCLC中高表达,然而其作用机制尚不清楚。本研究通过实时定量PCR检测NSCLC细胞中HOXA10表达水平,结果表明HOXA10在NSCLC细胞中呈高表达,与最新临床样本分析[12]结果一致。
临床研究[4-5]证实,安罗替尼作为三线抗肿瘤药物可有效提高晚期NSCLC患者的总生存期。机制研究[13]发现,安罗替尼通过抑制趋化因子CCL2而抑制血管生成,血清CCL2水平是潜在的NSCLC预后指标。基于RNA测序技术的转录组学分析[6]发现,肺癌细胞中CXC趋化因子配体2 (C-X-C motif ligand 2,CXCL2) 与安罗替尼耐药性相关。在安罗替尼敏感的NCI-H1975细胞中,安罗替尼可以显著下调CXCL2水平;而在耐药细胞中,安罗替尼对CXCL2表达水平无明显影响。后续功能实验[6]验证了CXCL2对安罗替尼耐药性的影响。值得注意的是,转录组学分析[6]也发现HOXA10在安罗替尼敏感细胞中可被安罗替尼显著下调,而在耐药细胞中无明显变化,提示HOXA10与NSCLC安罗替尼敏感性相关。
与NCI-H1975细胞相比,A549和PC-9细胞对安罗替尼的敏感性相对较差。因此,本研究选择了这2个细胞系用于研究安罗替尼耐药性。本研究通过敲低HOXA10,首次探讨了其与安罗替尼药物敏感性的关系。由于本研究使用了浓度较低的安洛尼替处理细胞,在对照组未观察到安罗替尼对细胞增殖、迁移、侵袭和凋亡的明显抑制作用。而CCK-8和克隆形成实验证实,敲低HOXA10显著增加安罗替尼的细胞毒性,增强其抑制细胞增殖的作用。Transwell实验发现,在HOXA10低表达细胞中,安罗替尼抑制细胞迁移和侵袭的能力明显增强。此外,流式细胞术结果表明,敲低HOXA10促进安罗替尼诱导的细胞凋亡。由此可见,敲低HOXA10可提高A549和PC-9细胞对安罗替尼的敏感性。由于肿瘤细胞耐药机制比较复杂,后续还需要通过动物体内实验进一步验证。
综上所述,本研究发现HOXA10在NSCLC中对增强安罗替尼敏感性起关键作用,为提高安罗替尼治疗效果提供了新的思路。
| [1] |
SIEGEL RL, MILLER KD, JEMAL A. Cancer statistics, 2020[J]. CA Cancer J Clin, 2020, 70(1): 7-30. DOI:10.3322/caac.21590 |
| [2] |
SMIT E, MORO-SIBILOT D, CARPEÑO J, et al. Cisplatin and carboplatin-based chemotherapy in the first-line treatment of non-small cell lung cancer: analysis from the European FRAME study[J]. Lung Cancer, 2016, 92: 35-40. DOI:10.1016/j.lungcan.2015.11.022 |
| [3] |
LIN B, SONG X, YANG D, et al. Anlotinib inhibits angiogenesis via suppressing the activation of VEGFR2, PDGFRβ and FGFR1[J]. Gene, 2018, 654: 77-86. DOI:10.1016/j.gene.2018.02.026 |
| [4] |
HAN B, LI K, WANG Q, et al. Effect of anlotinib as a third-line or further treatment on overall survival of patients with advanced non-small cell lung cancer: the ALTER 0303 phase 3 randomized clinical trial[J]. JAMA Oncol, 2018, 4(11): 1569-1575. DOI:10.1001/jamaoncol.2018.3039 |
| [5] |
HAN B, LI K, ZHAO Y, et al. Anlotinib as a third-line therapy in patients with refractory advanced non-small-cell lung cancer: a multicentre, randomised phaseⅡtrial (ALTER0302)[J]. Br J Cancer, 2018, 118(5): 654-661. DOI:10.1038/bjc.2017.478 |
| [6] |
LU J, XU W, QIAN J, et al. Transcriptome profiling analysis reveals that CXCL2 is involved in anlotinib resistance in human lung cancer cells[J]. BMC Med Genomics, 2019, 12(Suppl 2): 38. DOI:10.1186/s12920-019-0482-y |
| [7] |
CAMIDGE DR, PAO W, SEQUIST LV, et al. Acquired resistance to TKIs in solid tumours: learning from lung cancer[J]. Nat Rev Clin Oncoly, 2014, 11(8): 473-481. DOI:10.1038/nrclinonc.2014.104 |
| [8] |
CARNESECCHI J, PINTO PB, LOHMANN I. Hox transcription factors: an overview of multi-step regulators of gene expression[J]. Int J Dev Biol, 2018, 62(11/12): 723-732. DOI:10.1387/ijdb.180294il |
| [9] |
HAN Y, LU S, WEN YG, et al. Overexpression of HOXA10 promotes gastric cancer cells proliferation and HOXA10+/CD44+ is potential prognostic biomarker for gastric cancer[J]. Eur J Cell Biol, 2015, 94(12): 642-652. DOI:10.1016/j.ejcb.2015.08.004 |
| [10] |
LIU C, GE M, MA J, et al. Homeobox A10 promotes the proliferation and invasion of bladder cancer cells via regulation of matrix meta- lloproteinase-3[J]. Oncol Lett, 2019, 18(1): 49-56. DOI:10.3892/ol.2019.10312 |
| [11] |
GUO YN, LUO B, CHEN WJ, et al. Comprehensive clinical implications of homeobox A10 in 3, 199 cases of non-small cell lung cancer tissue samples combining qRT-PCR, RNA sequencing and microa- rray data[J]. Am J Transl Res, 2019, 11(1): 45-66. |
| [12] |
郑彭玮, 程淑芳, 吴天斌, 等. 非小细胞肺癌的CT表现及其诊断价值研究[J]. 中国现代医生, 2020, 58(3): 137-139. |
| [13] |
CRINÒ L, METRO G. Therapeutic options targeting angiogenesis in nonsmall cell lung cancer[J]. Eur Respir Rev, 2014, 23(131): 79-91. DOI:10.1183/09059180.00008913 |
 2022, Vol. 51
2022, Vol. 51