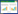文章信息
- 胡晓莹, 张跃骜, 崔志强, 顾颖, 杨拓, 张文强, 张慧予
- HU Xiaoying, ZHANG Yueao, CUI Zhiqiang, GU Ying, YANG Tuo, ZHANG Wenqiang, ZHANG Huiyu
- 跨膜蛋白16F对阿尔茨海默病细胞模型铁死亡的调控作用
- Effect of transmembrane protein 16F on ferroptosis in an Alzheimer disease cell model
- 中国医科大学学报, 2022, 51(5): 395-400
- Journal of China Medical University, 2022, 51(5): 395-400
-
文章历史
- 收稿日期:2021-12-22
- 网络出版时间:2022-05-23 14:19
2. 中国医科大学临床一系2020级82班,沈阳 110122;
3. 中国医科大学附属第四医院老年病科,沈阳 110032
2. Class 82, Grade 2020, The First Clinical Department of China Medical University, Shenyang 110122, China;
3. Department of Gerontology, The Fourth Affiliated Hospital of China Medical University, Shenyang 110032, China
阿尔茨海默病(Alzheimer disease,AD) 是一种以渐进性记忆障碍、认知功能障碍、人格改变及语言障碍等神经精神症状为主要临床特征的慢性进行性中枢神经系统变性疾病。其病理特征主要包括β淀粉样蛋白(β-amyloid protein,Aβ) 沉积导致的淀粉样斑块和Tau蛋白过度磷酸化导致的神经纤维缠结[1]。近年来认为大脑中铁的异常沉积能加重AD的病理进程[2]。铁死亡是一种铁依赖性的由脂质过氧化引起的调节性细胞死亡,在形态、生化、遗传上区别于细胞凋亡、自噬及程序性坏死[3]。研究[4-6]表明,铁死亡与帕金森病、癫痫、脑出血等神经系统疾病密切相关。在AD病理过程中,也存在铁异常积累、脂质过氧化等铁死亡表象。因此,研究AD病理进程中潜在的铁死亡机制有利于寻找AD的治疗靶点。
跨膜蛋白16F (transmembrane protein16F,TMEM16F) 是一种具有10个跨膜片段的蛋白质[7],存在于多种组织细胞(淋巴细胞、巨噬细胞、肠上皮细胞、血小板细胞、脊髓运动神经元) 中,主要发挥离子通道及磷脂翻转两方面作用。磷脂翻转即位于质膜内部小叶的磷脂酰丝氨酸(phosphatidylserine,PS) 通过催化作用暴露于质膜外部,从而导致质膜中脂质重新分布。有研究[8]认为PS外翻可能是质膜修复程序。也有研究[9]认为PS外翻是细胞死亡的信号。OUSINGSAWAT等[10]证明了在质膜磷脂过氧化过程中发生铁死亡会激活TMEM16F。SIMÕES等[11]发现,活性氧(reactive oxygen species,ROS) 水平上调时TMEM16F激活,导致细胞发生铁死亡。TMEM16F对脂质的调控可能与铁死亡病理进程有关[12],提示TMEM16F是细胞发生铁死亡过程中的重要组成部分。目前,AD中TMEM16F的相关研究甚少,因此,本研究通过沉默TMEM16F基因,探讨其对AD神经元铁死亡的影响,以期寻找AD治疗的新靶点。
1 材料与方法 1.1 材料SH-SY5Y神经母细胞瘤细胞(中国医学科学院基础医学研究所基础细胞研究中心),胎牛血清(德国Sera Pro公司),细胞培养基DMEM-F12 (美国Hyclone公司),纯度 > 99%的Aβ25-35 (美国APExBIO公司),BCA蛋白定量试剂盒、ECL化学发光试剂盒(中国碧云天生物科技公司),酰基辅酶A合成酶长链家族成员4 (acyl-CoA synthetase long-chain family member 4,ACSL4)、谷胱甘肽过氧化物酶4 (glutathione peroxidase 4,GPX4) 抗体(美国Abcam公司),溶质载体家族40成员1[solute carrier family 40 member 1,SLC40A1,又称铁转运蛋白1 (ferroportin 1,Fpn1)]抗体(美国Proteintech公司),Aβ抗体(中国Wanleibio公司),p-Tau抗体(美国Affinity公司),ROS检测试剂盒(中国碧云天生物科技公司),lipofectamine3000 (美国ThermoFisher Scientific公司),siRNA (中国JTSbio公司)。
1.2 方法 1.2.1 细胞培养SH-SY5Y神经母细胞瘤细胞培养于含有DMEM-F12和10%胎牛血清、1%青链霉素的培养基,在37 ℃、5%CO2的细胞培养箱中培养,2~3 d后换液,5~7 d后消化混悬,按1:2~1:3的比例传代。将同时段培养处于对数生长期的细胞分为Control组(0 μmol/L Aβ25-35)、Model组(20 μmol/L Aβ25-35处理12 h)。
1.2.2 细胞转染将siRNA阴性对照和siRNA-TMEM16 (序列信息为F链GGUGGCAAGAUCAUAAUGUTT,R链ACAUUAUGAUCUUGCCACCTT) 分别转染至SH-SY5Y细胞中,转染48 h后继续用20 μmol/L Aβ25-35处理12 h,设为siRNA-nc组和siRNA-TMEM16F组。
1.2.3 CCK-8法将细胞铺于96孔板(2 000/孔)。孵育1 d后,实验组分别加入不同体积1 mol/L Aβ25-35 (终浓度分别为5、10、20、40、80 μmol/L),空白组、对照组加入等量基础培养基。分别培养6、12、24、48 h后加入CCK-8,4 h后酶标仪450 nm处测吸光度值,计算细胞存活率。
1.2.4 Western blotting收集细胞,加入含有蛋白酶抑制剂和磷酸酶抑制剂的蛋白裂解液,4 ℃孵育30 min,4 ℃、12 000 r/min离心15 min,保留上清液。BCA蛋白定量,行SDS-PAGE电泳(浓缩胶80 V,分离胶120 V);200 mA下将分离的蛋白转移至PVDF膜上;5%脱脂奶粉封闭1 h,TBST洗膜(5 min/次,3次);加入一抗(Aβ 1:1 000、p-Tau 1:1 000、ACSL4 1:10 000、GPX4 1:1 000、Fpn1 1:600、GAPDH 1:20 000) 4℃孵育过夜,TBST洗膜(10 min/次,3次);加入二抗孵育1 h,TBST洗膜(5 min/次,3次);ECL发光显色。应用ImageJ软件分析目的条带和内参GAPDH的灰度值,用二者之比表示目的蛋白的相对表达量。
1.2.5 免疫荧光染色各组细胞在共聚焦小皿中培养至70%,多聚甲醛固定20 min,PBS洗涤(5 min/次,3次),Triton通透20 min,PBS洗涤(5 min/次,3次),5%BSA封闭1 h,一抗4 ℃孵育过夜,PBS洗涤(5 min/次,3次),避光加入二抗FITC孵育,PBS洗涤(5 min/次,3次),加入DAPI孵育30 min,PBS洗涤(5 min/次,3次) 后,倒置荧光显微镜拍摄。
1.2.6 ROS检测各组细胞经处理后加入荧光探针DCFH-DA,终浓度为10 μmol/L,置于37 ℃细胞培养箱内孵育20 min,洗涤细胞3次,用倒置荧光显微镜直接观察。
1.3 统计学分析每个实验至少重复3次,数据用x±s表示。采用GraphPad Prism 8软件分析数据。2组间比较采用t检验,多组间比较采用单因素方差分析。P < 0.05为差异有统计学意义。
2 结果 2.1 Aβ25-35对SH-SY5Y细胞活力的影响利用CCK-8法检测Aβ25-35对SH-SY5Y细胞生存率的影响,将Aβ25-35浓度梯度设为0、5、10、20、40、80 μmol/L,时间梯度设为6、12、24、48 h。结果显示,Aβ25-35作用时间为6 h时,Aβ25-35浓度≤40 μmol/L组细胞生存率与对照组相比无统计学差异。当Aβ25-35作用时间为12 h时,Aβ25-35浓度≥20 μmol/L组细胞生存率随Aβ25-35浓度增加而降低(P < 0.001),因此,选用20 μmol/L作为细胞造模的有效处理浓度,12 h作为细胞造模的有效处理时间。见图 1。
|
| ***P < 0.001, ****P < 0.000 1 vs 0 h. 图 1 梯度浓度时间Aβ25-35对SH-SY5Y细胞存活率的影响 Fig.1 Effect of concentration and time gradients of Aβ25-35 on the viability of SH-SY5Y cells |
2.2 TMEM16F在AD神经元中的表达情况
Western blotting结果显示,Aβ25-35诱导的Model组中,TMEM16F蛋白表达显著上调(P < 0.05)。见图 2。提示TMEM16F可能参与促进AD的发生发展。

|
| ** P < 0.01 vs control group. n = 3. 图 2 TMEM16F蛋白表达情况 Fig.2 The expression of TMEM16F protein |
2.3 TMEM16F对AD神经元病理指标的影响
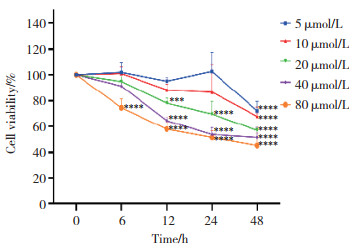
Western blotting结果显示,与Control组相比,Model组中Aβ、p-Tau蛋白表达明显上调;与siRNA-nc组相比,siRNA-TMEM16F组中Aβ、p-Tau蛋白表达显著下降,差异均有统计学意义(均P < 0.05),见图 3。
|
| * P < 0.05, **** P < 0.000 1. n = 3. 图 3 AD相关指标蛋白表达情况 Fig.3 The relative expression of AD-related indictors protein |
2.4 TMEM16F对AD神经元铁死亡的作用
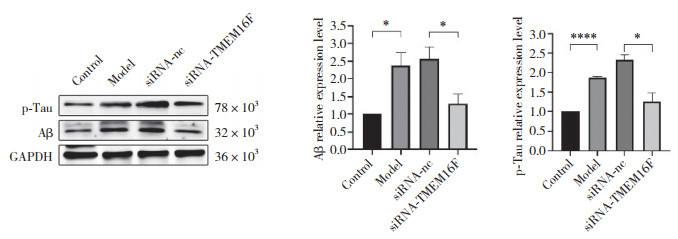
Western blotting结果显示,与Control组相比,Model组中ACSL4蛋白表达增加,GPX4、Fpn1表达降低;与siRNA-nc组相比,siRNA-TMEM16F组中ACSL4蛋白表达下降,GPX4、Fpn1表达明显增加,差异均有统计学意义(均P < 0.05),见图 4A。免疫荧光染色结果显示,Model组中ACSL4表达较Control组明显增加,siRNA-TMEM16F组较siRNA-nc组显著降低,差异有统计学意义(P < 0.01),见图 4B。
|
| A, the relative expression of Fpn1, ACSL4, GPX4 detected by Western blotting (n = 3);B, the expression of ACSL4 detected by immunofluorescence (n = 3). Scale bar =50 μm. * P < 0.05, ** P < 0.01. 图 4 TMEM16F对SH-SY5Y细胞铁死亡的影响 Fig.4 The effect of TMEM16F on the ferroptosis of SH-SY5Y cells |
2.5 TMEM16F对AD神经元ROS的影响
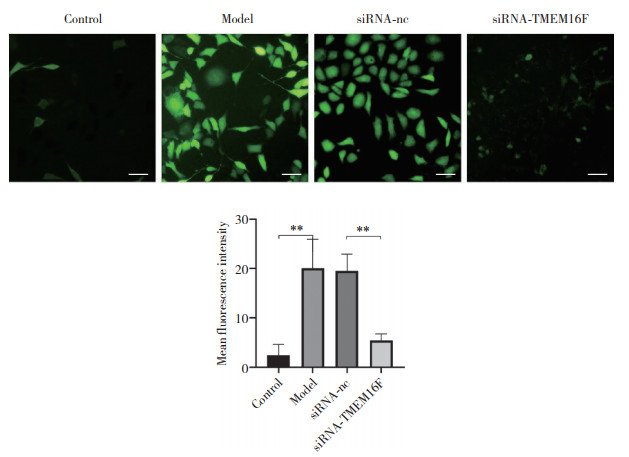
结果显示,与Control组相比,Model组ROS水平明显增加;与siRNA-nc组相比,siRNA-TMEM16F组ROS水平明显下降,差异有统计学意义(P < 0.01),见图 5。
|
| The ROS level detected by fluorescence microscope. Scale bar=100 μm ** P < 0.01. n = 6. 图 5 TMEM16F对SH-SY5Y细胞ROS的影响 Fig.5 The effect of TMEM16F on the ROS of SH-SY5Y cells |
3 讨论
AD发病机制不明,其典型病理特征表现为Aβ沉积和Tau蛋白过度磷酸化。此外,还有研究[13]发现AD患者早期大脑铁沉积现象。动物实验[2]证明,铁过载能导致学习和记忆功能下降,铁稳态与AD发生密切相关。铁死亡是一种铁依赖性的、由脂质过氧化引起的调节性细胞死亡,铁积累与脂质过氧化是其2个特征,均与AD病理过程密切相关。目前认为铁死亡和神经退行性疾病有关[14],但铁死亡如何参与AD病理过程尚不可知。基于此,本研究首先探索了AD细胞模型中铁死亡相关指标的变化。Fpn1是一种铁输出蛋白,能介导铁离子从细胞中输出,从而维持铁稳态平衡。ACSL4能将多不饱和脂肪酸合成磷脂,提供脂质过氧化的原料[15]。GPX4作为抗氧化系统的重要成员,能将脂质过氧化物还原为脂质醇,从而减轻氧化损伤。而ROS过度增加能氧化不同生物分子,包括核酸、蛋白质、脂质,导致氧化应激损伤。本研究通过Aβ25-35诱导的AD细胞模型发现,AD细胞中Fpn1蛋白水平明显降低,推测神经细胞内铁输出蛋白减少,细胞内铁离子含量可能增加。此外,还发现AD中ROS明显增加,ACSL4蛋白表达水平显著增高,而GPX4蛋白表达水平明显下降,提示可能发生了脂质过氧化。因此,认为神经元在AD病理过程中发生铁死亡的可能性较大。
TMEM16F作为磷脂翻转酶,在细胞内钙水平升高导致的磷脂翻转中起重要作用。ZHANG等[16]发现,TMEM16F能通过增加神经元PS翻转暴露,介导神经元的小胶质细胞吞噬作用,从而加重神经元损伤。SOULARD等[17]发现在肌萎缩侧索硬化小鼠模型中,抑制脊髓运动神经元TMEM16F能显著调节运动阻力延迟疾病发作。ZHAO等[18]发现小鼠脊髓损伤后TMEM16F上调,抑制TMEM16F能减弱小胶质细胞促炎症反应,改善小鼠运动功能。此外,既往研究表明TMEM16F有助于不同形式的调节性细胞死亡。本研究首先证实了TMEM16F在AD神经元中的表达量高于正常神经元,提示TMEM16F高表达可能导致AD病理指标Aβ和p-Tau表达增加,加重神经元损伤。然后利用RNA干扰技术,在Aβ25-35诱导的SH-SY5Y细胞中沉默了TMEM16F,证明了其在AD神经元铁死亡中的作用,即沉默TMEM16F可抑制AD神经元的铁死亡,减轻AD神经元损伤。
综上所述,TMEM16F在AD神经元中高表达,沉默TMEM16F能抑制AD神经元发生铁死亡。但TMEM16F在AD神经元中介导铁死亡的具体作用机制尚需进一步研究。虽然AD病理标志物Aβ沉积和Tau蛋白高度磷酸化现已明确,但针对二者的治疗情况尚不理想,因此,寻找新的靶向标志物尤为重要。本研究提示TMEM16F可能成为AD治疗的新靶点,以及铁死亡是AD发生发展的重要环节。
| [1] |
TIWARI S, ATLURI V, KAUSHIK A, et al. Alzheimer's disease: pathogenesis, diagnostics, and therapeutics[J]. Int J Nanomedicine, 2019, 14: 5541-5554. DOI:10.2147/IJN.S200490 |
| [2] |
WAN WB, CAO L, KALIONIS B, et al. Iron deposition leads to hyperphosphorylation of tau and disruption of insulin signaling[J]. Front Neurol, 2019, 10: 607. DOI:10.3389/fneur.2019.00607 |
| [3] |
DIXON SJ, LEMBERG KM, LAMPRECHT MR, et al. Ferroptosis: an iron-dependent form of nonapoptotic cell death[J]. Cell, 2012, 149(5): 1060-1072. DOI:10.1016/j.cell.2012.03.042 |
| [4] |
MAHONEY-SÁNCHEZ L, BOUCHAOUI H, AYTON S, et al. Ferroptosis and its potential role in the physiopathology of Parkinson's disease[J]. Prog Neurobiol, 2021, 196: 101890. DOI:10.1016/j.pneurobio.2020.101890 |
| [5] |
CHEN S, CHEN YM, ZHANG YK, et al. Iron metabolism and ferroptosis in epilepsy[J]. Front Neurosci, 2020, 14: 601193. DOI:10.3389/fnins.2020.601193 |
| [6] |
BAO WD, ZHOU XT, ZHOU LT, et al. Targeting miR-124/ferroportin signaling ameliorated neuronal cell death through inhibiting apoptosis and ferroptosis in aged intracerebral hemorrhage murine model[J]. Aging Cell, 2020, 19(11): e13235. DOI:10.1111/acel.13235 |
| [7] |
SUZUKI J, UMEDA M, SIMS PJ, et al. Calcium-dependent phospholipid scrambling by TMEM16F[J]. Nature, 2010, 468(7325): 834-838. DOI:10.1038/nature09583 |
| [8] |
WU N, CERNYSIOV V, DAVIDSON D, et al. Critical role of lipid scramblase TMEM16F in phosphatidylserine exposure and repair of plasma membrane after pore formation[J]. Cell Rep, 2020, 30(4): 1129-1140.e5. DOI:10.1016/j.celrep.2019.12.066 |
| [9] |
SEGAWA K, NAGATA S. An apoptotic'eat me' signal: phosphatidylserine exposure[J]. Trends Cell Biol, 2015, 25(11): 639-650. DOI:10.1016/j.tcb.2015.08.003 |
| [10] |
OUSINGSAWAT J, SCHREIBER R, KUNZELMANN K. TMEM16F/anoctamin 6 in ferroptotic cell death[J]. Cancers, 2019, 11(5): 625. DOI:10.3390/cancers11050625 |
| [11] |
SIMÕES F, OUSINGSAWAT J, WANITCHAKOOL P, et al. CFTR supports cell death through ROS-dependent activation of TMEM16F (anoctamin 6)[J]. Pflugers Arch, 2018, 470(2): 305-314. DOI:10.1007/s00424-017-2065-0 |
| [12] |
SCHREIBER R, OUSINGSAWAT J, WANITCHAKOOL P, et al. Regulation of TMEM16A/ANO1 and TMEM16F/ANO6 ion currents and phospholipid scrambling by Ca2+ and plasma membrane lipid[J]. J Physiol, 2018, 596(2): 217-229. DOI:10.1113/JP275175 |
| [13] |
ACOSTA-CABRONERO J, BETTS MJ, CARDENAS-BLANCO A, et al. In vivo MRI mapping of brain iron deposition across the adult lifespan[J]. J Neurosci, 2016, 36(2): 364-374. DOI:10.1523/JNEUROSCI.1907-15.2016 |
| [14] |
STOCKWELL BR, ANGELI JPF, BAYIR H, et al. Ferroptosis: a regulated cell death Nexus linking metabolism, redox biology, and disease[J]. Cell, 2017, 171(2): 273-285. DOI:10.1016/j.cell.2017.09.021 |
| [15] |
DOLL S, PRONETH B, TYURINA YY, et al. ACSL4 dictates ferroptosis sensitivity by shaping cellular lipid composition[J]. Nat Chem Biol, 2017, 13(1): 91-98. DOI:10.1038/nchembio.2239 |
| [16] |
ZHANG YJ, LI HY, LI X, et al. TMEM16F aggravates neuronal loss by mediating microglial phagocytosis of neurons in a rat experimental cerebral ischemia and reperfusion model[J]. Front Immunol, 2020, 11: 1144. DOI:10.3389/fimmu.2020.01144 |
| [17] |
SOULARD C, SALSAC C, MOUZAT K, et al. Spinal motoneuron TMEM16F acts at C-boutons to modulate motor resistance and contributes to ALS pathogenesis[J]. Cell Rep, 2020, 30(8): 2581-2593.e7. DOI:10.1016/j.celrep.2020.02.001 |
| [18] |
ZHAO J, GAO QY. TMEM16F inhibition limits pain-associated behavior and improves motor function by promoting microglia M2 polarization in mice[J]. Biochem Biophys Res Commun, 2019, 517(4): 603-610. DOI:10.1016/j.bbrc.2019.07.070 |
 2022, Vol. 51
2022, Vol. 51