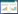文章信息
- 孙倩, 刘盛力, 马钰, 杜莉
- SUN Qian, LIU Shengli, MA Yu, DU Li
- 长链非编码RNA SLC25A25-AS1对喉癌细胞侵袭和迁移的影响及其机制
- Effects of long noncoding RNA SLC25A25-AS1 on invasion and migration of laryngeal carcinoma cells and its mechanism
- 中国医科大学学报, 2022, 51(4): 324-328
- Journal of China Medical University, 2022, 51(4): 324-328
-
文章历史
- 收稿日期:2021-12-06
- 网络出版时间:2022-04-29 10:42
喉癌是头颈部第二常见的恶性肿瘤,占头颈部肿瘤的13.9%,鳞状细胞癌是其主要病理类型。喉癌的具体病因尚不确定,可能与吸烟、饮酒等不良生活习惯以及病毒感染、环境、放射线等因素有关[1]。喉癌治疗以手术方法为主,放疗、化疗和新型靶向治疗在临床中应用也较多[2]。但即使在积极治疗后,晚期喉癌患者死亡率也极高[3]。患者术后出现呼吸、发音以及进食困难,生活质量受到很大影响。肿瘤的形成和发展受多种生物分子的调控,如癌基因、肿瘤抑制基因和非编码RNA等,这是一个复杂的过程[4-5]。长链非编码RNA(long noncoding RNA,lncRNA)是一类无蛋白编码功能的RNA,其在表观遗传学修饰、转录调控、染色质修饰、转录后加工、核易位过程、细胞增殖和凋亡等多种生物过程中发挥重要作用[6]。研究[7]发现,lncRNA SLC25A25的反义RNA1(lncRNA SLC25A25-AS1)在结肠癌、宫颈癌、胃癌的发展中具有肿瘤抑制作用。本研究探讨了SLC25A25-AS1在喉癌细胞中的表达水平及其对细胞侵袭、迁移能力的影响,探讨其对肿瘤作用的分子机制。
1 材料与方法 1.1 材料人鼻咽上皮细胞NP69和喉癌细胞TU-212、TU-177购自NTCC典型培养物保藏中心,喉癌细胞Hep-2购自中国医学科学院基础医学研究所细胞资源中心,MTT试剂盒购自碧云天公司,RNA提取试剂TRIzol和脂质体Lipofectamine 3000购自美国Invitrogen公司,实时荧光定量PCR引物购自南京金斯瑞公司,逆转录试剂盒和SYBR试剂盒购自北京Genstar公司,信号转导及转录激活因子3(signal transduction and activator of transcription 3,STAT3)抗体、磷酸化STAT3(p-STAT3)抗体和血管内皮生长因子(vascular endothelial growth factor,VEGF)抗体购美国Proteintech公司,GAPDH多克隆抗体购自杭州贤至公司,HRP标记山羊抗兔IgG购自美国Thermo公司,BCA蛋白浓度检测试剂盒、SDS上样缓冲液和ECL发光液购自北京Genstar公司。
1.2 细胞培养和转染NP69细胞置于Defined Keratinocyte SFM培养基中,TU-212和TU-177细胞置于RPMI 1640培养基中,Hep-2细胞置于EMEM培养基中。培养条件均为37℃、5%CO2,常规换液。过表达组用脂质体Lipofectamine 3000将pcDNA3.1-SLC25A25-AS1转染至Hep-2细胞,NC组转染pcDNA3.1的空载体,对照组进行常规培养。48 h后检测SLC25A25-AS1表达水平。
1.3 总RNA提取和实时荧光定量PCR转染48 h后,收集每组细胞,用TRIzol试剂提取细胞的总RNA,随后按逆转录试剂盒操作步骤将提取的RNA反转录成cDNA。以cDNA为模板进行实时荧光定量PCR。反应条件:95 ℃ 30 s;95℃ 10 s,65 ℃ 10 s,30个循环。SLC25A25-AS1、STAT3和VEGF的表达以GAPDH为内参,采用2-ΔΔCt法计算目的基因的相对表达量。引物序列:SLC25A25-AS1,上游5’-GTAATGAGCGTGCCGAGA-3’,下游5’-CCCGAGTGCTAATCAGACC-3’;STAT3,上游5’-GGGTCTGGCTGGACAAT-3’,下游5’-GCTTAGTGCTCAAGATGGC-3’;VEGF,上游5’-GGAACACCGACAAACCC-3’,下游5’-AATCCCCAAAGCACAGC-3’;GAPDH,上游5’-GCCAACGTGTCAGTGGTG-3’,下游5’-AAGGTGGAGGAGTGGGTGT-3’。
1.4 Western blotting检测蛋白水平取转染48 h后的细胞,RIPA裂解液裂解后提取细胞总蛋白。随后用BCA蛋白浓度试剂盒检测各组总蛋白纯度,将蛋白提取液进行SDS-PAGE电泳,转膜封闭,滴加一抗(稀释度为1∶1 000)4 ℃过夜孵育,次日二抗(稀释度为1∶10 000),室温下孵育2 h,以GAPDH为内参,用ECL发光液显影,曝光显色后用ImageJ图像分析系统测量灰度值。目的条带灰度值/GAPDH条带灰度值为目标蛋白相对表达量。
1.5 MTT法检测细胞增殖活性取对数生长期的对照组、NC组、过表达组Hep-2细胞,接种至96孔板,5×103/孔,37 ℃、5%CO2培养24、48、72 h后,每孔加入5 mg/mL MTT溶液,37 ℃、5%CO2培养4 h。弃上清,加DMSO溶解MTT甲臜沉淀,测492 nm波长下的吸光度值,评估细胞活力。
1.6 划痕实验检测细胞迁移能力将转染后的细胞悬液接种于6孔板,1×105/孔,培养过夜,待细胞完全融合后开始划痕实验。用20 μL移液管尖端划伤细胞单层,细胞碎片用PBS冲洗,倒置显微镜下0和24 h时拍照并记录。
1.7 Transwell实验检测细胞侵袭能力转染后的Hep-2细胞置于EP管中,制成1×105/mL浓度的悬浮液,将细胞悬液加入Matrigel胶覆盖的Transwell小室上室,保证其均匀铺满小室底,室温过夜,下室加入15%胎牛血清的培养基,在恒温培养箱中培养24 h后,擦除小室内细胞,以甲醇固定,0.5%结晶紫染色,冲洗封片。
1.8 统计学分析使用GraphPad Prism 6.0软件进行统计学分析。计量资料以x±s表示,两两比较采用t检验,多重比较采用单因素方差分析。P < 0.05为差异有统计学意义。
2 结果 2.1 喉癌细胞的SLC25A25-AS1水平与NP69细胞相比,TU-212、TU-177、Hep-2喉癌细胞的SLC25A25-AS1水平均显著下降(P < 0.05)。本研究后续实验选取SLC25A25-AS1水平最低的Hep-2细胞。过表达组Hep-2细胞的SLC25A25-AS1表达水平较对照组和NC组显著升高(P < 0.01),而对照组和NC组比较无统计学差异(P > 0.05)。见图 1。
|
| A, the relative expression of SLC25A25-AS1 in NP69, TU-212, TU-177, and Hep-2 cells; B, the relative expression of SLC25A25-AS1 in Hep-2 cells of control, NC, and overexpression groups. *P < 0.05 vs NP69 cell; **P < 0.01 vs control group; ## P < 0.01 vs NC group. 图 1 SLC25A25-AS1在喉癌细胞中的表达水平 Fig.1 Expression levels of SLC25A25-AS1 in laryngeal carcinoma cells |
2.2 过表达SLC25A25-AS1对Hep-2细胞增殖的影响
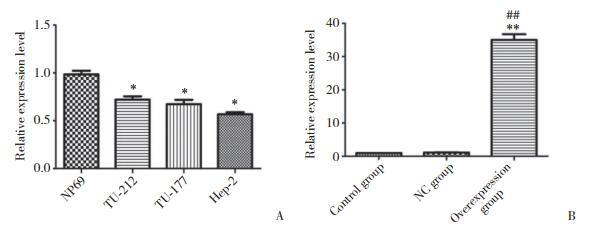
过表达组转染pcDNA3.1-SLC25A25-AS1载体48、72 h后,细胞增殖活性显著低于对照组和NC组(P < 0.05),而对照组和NC组比较无统计学差异(P > 0.05)。见图 2。
|
| *P < 0.05 vs control group; # P < 0.05 vs NC group. 图 2 对照组、NC组和过表达组的Hep-2细胞增殖曲线 Fig.2 Proliferation curves of Hep-2 cells in control, NC, and overexpression groups |
2.3 过表达SLC25A25-AS1对Hep-2细胞迁移的影响
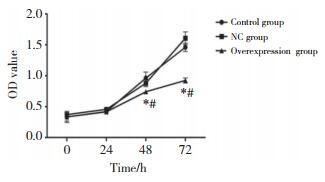
划痕实验结果表明,过表达组Hep-2细胞的划痕愈合率(25.23%)低于对照组(85.64%)和NC组(81.25%)(P < 0.05),而对照组与NC组比较无统计学差异(P > 0.05)。见图 3。
|
| 图 3 Hep-2细胞划痕实验×100 Fig.3 Results of scratch experiment of Hep-2 cells ×100 |
2.4 过表达SLC25A25-AS1对Hep-2细胞侵袭的影响
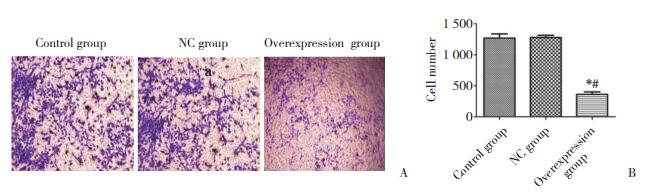
Transwell实验结果显示,过表达组Hep-2细胞的穿膜细胞数低于对照组和NC组(P < 0.05),而对照组与NC组比较差异无统计学意义(P > 0.05)。见图 4。
|
| A, results of Transwell assay (×200);B, number of invasive cells. *P < 0.05 vs control group; # P < 0.05 vs NC group. 图 4 Hep-2细胞侵袭实验 Fig.4 Results of Transwell assay of Hep-2 cells |
2.5 过表达SLC25A25-AS1对Hep-2细胞中STAT3/VEGF通路的影响
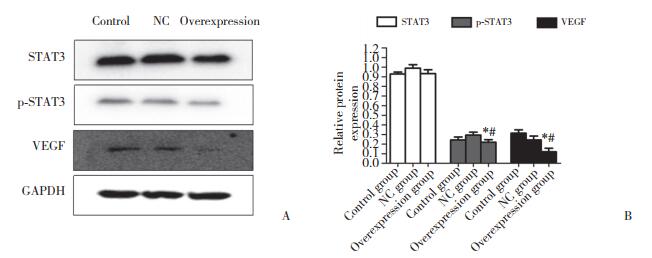
与对照组和NC组相比,过表达组Hep-2细胞的STAT3水平无变化(P > 0.05),p-STAT3和VEGF水平降低(P < 0.05);对照组和NC组比较,STAT3、p-STAT3和VEGF蛋白的表达水平均无统计学差异(P > 0.05)。见图 5。
|
| A, results of Western blotting; B, relative expression of STAT3, p-STAT3, and VEGF. *P < 0.05 vs control group; # P < 0.05 vs NC group. 图 5 Hep-2细胞中STAT3、p-STAT3和VEGF蛋白表达水平 Fig.5 Protein levels of STAT3, p-STAT3, and VEGF in Hep-2 cells |
3 讨论
非编码RNA是具有蛋白质功能的核酸分子,因缺乏完整的特异性开放阅读框,故无编码能力。根据核苷酸链长度分为两类,长度小于200 nt的为短链非编码RNA,长度大于200 nt的为lncRNA,lncRNA位于细胞核或细胞质内[8]。一般来说,lncRNA RNA聚合酶Ⅱ转录后,再剪接加工就得到lncRNA。lncRNA依靠二级结构和剪接模式上的功能保守性,即使初级结构保守性差,仍具有组织或细胞特异性。随着生物科学研究的不断深入,lncRNA参与表观遗传、转录和转录后调控等多种生物学过程,扮演着信号分子、诱饵分子、向导分子、骨架分子的角色,具有调控肿瘤生物活性的作用[9]。lncRNA可通过调控下游基因转录、干扰邻近基因表达、与编码蛋白基因的启动子区形成螺旋结构,阻断转录启动。此外,lncRNA可干扰mRNA的剪切,与微RNA等形成竞争性内源RNA,影响其靶基因的表达[10]。
全世界每年约有新发喉癌患者13万例,且95.0%以上的患者为鳞状细胞癌,临床多表现为声嘶、呼吸困难、吞咽困难和颈部淋巴结转移等[11]。HOTAIR、H19、MALAT1、NEAT1、SOX2-OT被证实在喉癌的发生、发展中发挥了重要的作用。本研究中的SLC25A25-AS1位于9q34.11,包含5个外显子,其转录方向与蛋白编码基因SLC25A25相反。SLC25A25是线粒体内膜的家族成员,参与线粒体载体蛋白的编码。LI等[12]的研究证明,SLC25A25-AS1通过MAPK信号传导通路,参与结肠癌的恶性增殖和上皮间质转化。研究[13]表明,SLC25A25-AS1过表达可以抑制宫颈癌细胞从上皮细胞向间充质的转化。目前,SLC25A25-AS1抑癌作用的研究集中在结肠癌、胃癌、宫颈癌,其在喉癌中的作用未见报道。本研究发现,SLC25A25-AS1在喉癌细胞中均表现为低表达,转染过表达质粒,可以抑制喉癌细胞增殖、侵袭、迁移。上述结果表明,SLC25A25-AS1与喉癌的发展密切相关,可能抑制癌细胞的侵袭和转移。
STAT3是STAT结合蛋白的一类,其作用广泛,参与许多生理功能调控[14]。VEGF主要在血管内皮细胞、肿瘤细胞中表达[15]。STAT3可以通过调节血管生成因子或缺氧诱导因子-1α等间接诱导VEGF的表达,而阻断VEGF的表达可以有效控制癌症的发生、发展。本研究发现,SLC25A25-AS1水平上调后,喉癌细胞中p-STAT3表达显著降低,同时VEGF的表达也减弱。由此得出,SLC25A25-AS1可能通过STAT3/VEGF信号对喉癌细胞的迁移和侵袭产生负调节作用。
综上所述,喉癌细胞中SLC25A25-AS1异常低表达可能通过抑制STAT3 /VEGF信号通路抑制喉癌细胞增殖、侵袭、迁移能力,发挥抑癌作用,这为喉癌发展和治疗提供了新思路。
| [1] |
ECHANIQUE KA, DESAI SV, MARCHIANO E, et al. Laryngeal verrucous carcinoma[J]. Otolaryngol Head Neck Surg, 2017, 156(1): 38-45. DOI:10.1177/0194599816662631 |
| [2] |
STEUER CE, EL-DEIRY M, PARKS JR, et al. An update on larynx cancer[J]. CA Cancer J Clin, 2017, 67(1): 31-50. DOI:10.3322/caac.21386 |
| [3] |
TAHARA M, KIYOTA N, YOKOTA T, et al. PhaseⅡtrial of combination treatment with paclitaxel, carboplatin and cetuximab (PCE) as first-line treatment in patients with recurrent and/or metastatic squamous cell carcinoma of the head and neck (CSPOR-HNO2)[J]. Ann Oncol, 2018, 29(4): 1004-1009. DOI:10.1093/annonc/mdy040 |
| [4] |
BHAN A, SOLEIMANI M, MANDAL SS. Long noncoding RNA and cancer: a new paradigm[J]. Cancer Res, 2017, 77(15): 3965-3981. DOI:10.1158/0008-5472.can-16-2634 |
| [5] |
ÁYEN Á, JIMÉNEZ MARTÍNEZ Y, BOULAIZ H. Targeted gene delivery therapies for cervical cancer[J]. Cancers, 2020, 12(5): 1301. DOI:10.3390/cancers12051301 |
| [6] |
LIU Y, ZHANG R, YING K. Long non-coding RNAs: novel links in respiratory diseases (review)[J]. Mol Med Rep, 2015, 11(6): 4025-4031. DOI:10.3892/mmr.2015.3290 |
| [7] |
魏琳琳, 张娜, 郭红, 等. 长链非编码RNA SLC25A25-AS1对胃癌细胞及对5-氟尿嘧啶耐药的作用[J]. 解剖科学进展, 2019, 25(3): 237-240. DOI:10.16695/j.cnki.1006-2947.2019.03.004 |
| [8] |
计红, 李悦, 牛春阳, 等. 长链非编码RNA生物学特性和功能研究进展[J]. 黑龙江八一农垦大学学报, 2019, 31(2): 28-32. DOI:10.3969/j.issn.1002-2090.2019.02.005 |
| [9] |
郑玲, 盛苗苗, 何吉祥, 等. 长链非编码RNA在乳腺癌中的研究进展[J]. 生命科学, 2020, 32(9): 937-944. DOI:10.13376/j.cbls/2020115 |
| [10] |
PARASRAMKA MA, MAJI S, MATSUDA A, et al. Long non-coding RNAs as novel targets for therapy in hepatocellular carcinoma[J]. Pharmacol Ther, 2016, 161: 67-78. DOI:10.1016/j.pharmthera.2016.03.004 |
| [11] |
MARCHIANO E, CHIN OY, FANG CH, et al. Laryngeal adenoid cystic carcinoma: a systematic review[J]. Otolaryngol Head Neck Surg, 2016, 154(3): 433-439. DOI:10.1177/0194599815621884 |
| [12] |
LI Y, HUANG SK, LI Y, et al. Decreased expression of lncRNA SLC25A25-AS1 promotes proliferation, chemoresistance, and EMT in colorectal cancer cells[J]. Tumour Biol, 2016, 37(10): 14205-14215. DOI:10.1007/s13277-016-5254-0 |
| [13] |
CHEN J, GAO C, ZHU W. Long non-coding RNA SLC25A25-AS1 exhibits oncogenic roles in non-small cell lung cancer by regulating the microRNA-195-5p/ITGA2 axis[J]. Oncol Lett, 2021, 22(1): 529. DOI:10.3892/ol.2021.12790 |
| [14] |
高楠, 温博, 桑力轩, 等. miR-125b通过靶向STAT3抑制胃癌细胞SGC-7901的侵袭迁移能力[J]. 解剖科学进展, 2018, 24(2): 159-162. DOI:10.16695/j.cnki.1006-2947.2018.02.014 |
| [15] |
安南, 陈子琦, 黄敏. 血管内皮细胞代谢与肿瘤血管新生研究进展[J]. 药学学报, 2020, 55(7): 1373-1381. DOI:10.16438/j.0513-4870.2020-0134 |
 2022, Vol. 51
2022, Vol. 51