文章信息
- 李晓娜, 何苗, 梁洪玥, 史瑞雪, 付钰, 顾宇婧, 李艾凝, 郭凤
- LI Xiaona, HE Miao, LIANG Hongyue, SHI Ruixue, FU Yu, GU Yujing, LI Aining, GUO Feng
- 瞬时受体电位通道7参与匹鲁卡品诱导的癫痫体外模型凋亡的调控
- Role of transient receptor potential melastatin 7 in the modulation of apoptosis in epilepsy in an in vitro model induced by pilocarpine
- 中国医科大学学报, 2022, 51(4): 289-293
- Journal of China Medical University, 2022, 51(4): 289-293
-
文章历史
- 收稿日期:2021-09-06
- 网络出版时间:2022-04-29 10:32
2. 中国医科大学药学院药物毒理学教研室, 沈阳 110122
2. Department of Pharmaceutical Toxicology, School of Pharmacy, China Medical University, Shenyang 110122, China
癫痫是由大脑神经元异常放电引发的慢性脑部疾病,是最常见的神经系统疾病之一。癫痫本质上是“离子通道病”,即电压门控和配体门控离子通道功能突变引发癫痫[1]。钠、钾、钙等经典离子通道在癫痫发病机制中的作用早已被证实,随着越来越多离子通道的结构和功能被解析,研究者对新型离子通道研究也越来越深入,这为癫痫机制与治疗的研究提供了新思路。
瞬时受体电压(transient receptor potential,TRP)通道是位于细胞膜上的一组非选择性阳离子通道。TRP通道的Melastatin亚家族,特别是瞬时受体电位通道7(transient receptor potential melastatin 7,TRPM7),在神经系统广泛表达。已有大量文献表明,神经退行性疾病如阿尔茨海默病[2]、帕金森病[3]和肌萎缩侧索硬化症[4]等的发生和发展都与TRPM7介导的病理过程有关。然而,目前对TRPM7在癫痫中的变化尚未阐明,在匹鲁卡品(pilocarpine,PILO)诱导的癫痫持续状态大鼠模型中发现TRPM7蛋白表达增加,抑制TRPM7可以减少神经细胞死亡[5]。
细胞凋亡是半胱氨酸天冬氨酸蛋白酶3(caspase-3)介导的程序性细胞死亡[6],其是神经疾病中神经细胞死亡的主要发病机制[7]。研究[8-9]发现TRPM7参与调控凋亡以及神经系统疾病的发生与发展。截至目前为止,TRPM7是否参与PILO诱导的癫痫体外模型凋亡尚无报道。因此,本研究旨在阐明TRPM7在PILO诱导的癫痫模型凋亡中的作用,为癫痫发病机制靶点的探寻提供新角度与新思路。
1 材料与方法 1.1 材料 1.1.1 细胞小鼠脑神经瘤细胞(Neuro-2A细胞),由中国科学院上海细胞生物学研究所提供。
1.1.2 试剂PILO购自美国APE*BIO公司;CCK-8试剂盒、BCA蛋白浓度测定试剂盒和TUNEL细胞凋亡检测试剂盒购自中国碧云天生物技术研究所;GAPDH上下游引物和TRPM7上下游引物购自上海生工生物工程股份有限公司;TRPM7 siRNA和GP-transfect-Mate转染试剂购自苏州吉玛基因股份有限公司;扩增、反转录试剂盒购自日本TaKaRa公司;兔抗caspase-3、兔抗Bcl-2相关X蛋白(Bax)、兔抗细胞色素C蛋白(cytochrome C,Cyt C)、兔抗β肌动蛋白(β-actin)和辣根过氧化物酶标记的山羊抗兔IgG二抗购自美国Abcam公司。
1.1.3 仪器电泳仪购自美国Bio-Rad公司;凝胶成像分析仪购自以色列DNR生物影像系统有限公司;酶标仪购自美国BIOTEK公司;荧光定量基因扩增仪购自美国Thermo Fisher Scientific公司;CO2培养箱购自日本SANYO公司;倒置荧光显微镜购自日本Olympus公司。
1.2 方法 1.2.1 细胞培养和转染 1.2.1.1 细胞培养接种Neuro-2A细胞于含10%胎牛血清的DMEM高糖培养基中,5%CO2、37℃、饱和湿度培养箱培养,当细胞密度达80%以上时进行消化传代。
1.2.1.2 siRNA转染以1×105/孔的细胞密度将Neuro-2A细胞接种于6孔板中,当细胞密度达到80%左右时按照GP-transfect-Mate说明书进行转染。设置对照组、PILO模型组和PILO+siRNA组进行实验,其中对照组和PILO模型组转染无序序列,PILO+siRNA组转染TRPM7 siRNA。转染48 h后,应用终浓度为20 mmol·L-1的PILO处理PILO模型组和PILO+siRNA组,对照组加入等量培养基继续培养24 h。siRNA无序序列(NC-siRNA):上游5’-UUCUUCGAACGUGUCACGUTT-3’,下游5’-ACGUGACACGUUCGGAGAATT-3’;TRPM7 siRNA序列:上游5’-GGAGUAAGCAUGCAUAAAUTT-3’,下游5’-AUUUAUGCAUGCUUACUCCTT-3’。
1.2.2 CCK-8法检测细胞毒性取处于对数生长期Neuro-2A细胞,消化后调整细胞浓度为4×104 /mL,接种100 μL细胞悬液到96孔板于培养箱中培养24 h。用不同浓度的PILO(0、2、4、16、64和128 mmol·L-1)处理24 h。细胞毒性活力(%)=[吸光度(加药)-吸光度(空白)] / [吸光度(对照)-吸光度(空白)] ×100。
1.2.3 蛋白质印迹法检测凋亡相关蛋白的表达水平将Neuro-2A细胞接种于6孔板中,当细胞密度达到80%左右时进行给药处理。药物处理结束后,RIPA试剂提取细胞总蛋白,BCA法测定蛋白浓度。以30 μg/孔进行十二烷基硫酸钠-聚丙烯酰胺凝胶电泳,电泳条件为70 V恒压30 min,110 V恒压120 min;用湿转法将分离的目标蛋白完全转移至聚偏氟乙烯膜(polyvinylidene fluoride,PVDF)上,转膜条件为300 mA恒流120 min;并于5%脱脂奶粉封闭1.5 h。分别加入caspase-3(1∶1 000)、Bax(1∶10 000)、Cyt C(1∶5 000)和β-actin(1∶10 000)一抗,4 ℃孵育过夜。加相应的辣根过氧化物酶标记的二抗,4 ℃孵育1.5 h。加化学发光试剂,避光显影,曝光拍照。以β-actin作为内参,采用Image J图像分析软件分析各条带灰度值。
1.2.4 实时定量PCR法检测基因表达将Neuro-2A细胞接种于6孔板中,当细胞密度达到80%左右时进行给药处理。药物处理结束后,应用TRIzol法提取细胞总RNA,并应用酶标仪检测RNA纯度,以光密度(optical density,OD)260/OD280值在1.8~2.2为合格。按照PrimeScriptTM RT Master Mix试剂盒逆转录合成cDNA。按照TB Green® Premix Ex TaqTM Ⅱ说明书以cDNA为模板进行PCR扩增,扩增条件及参数为95 ℃预变性60 s;95 ℃变性15 s,57 ℃退火30 s,72 ℃延伸45 s,重复40个循环。以GAPDH为内参基因,应用2-ΔΔCt法计算目的基因的相对表达量。相关序列见表 1。
| Gene | Primer sequence(5’-3’) | Product length(bp) |
| Mouse TRPM7 | F:TTTGGTGTTCCCAGAAAAGC | 175 |
| R:ACCAAGTTCCAGGACCACAG | ||
| Mouse GAPDH | F:GCTACACTGAGGACCAGGTTGTC | 135 |
| R:AGCCGTATTCATTGTCATACCAGG |
1.2.5 TUNEL染色
将Neuro-2A细胞接种于6孔板中,当细胞密度达到80%左右时按1.2.1.2进行处理。给药结束后,严格按照TUNEL染色明书进行染色,DAPI复染细胞核。在荧光显微镜下观察成像,TUNEL阳性细胞为绿色,随机选取4个视野观察凋亡情况。采用Image J图像分析软件分析。
1.3 统计学分析采用GraphPad Prism 6进行统计学分析,数据以x±s表示,2组比较采用t检验,多组数据比较采用单因素方差分析,P < 0.05为差异有统计学意义。
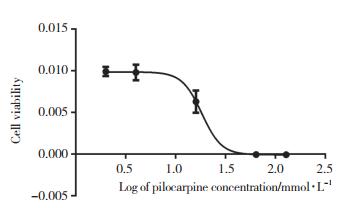
2 结果 2.1 PILO能够抑制Neuro-2A细胞存活率CCK-8实验结果显示,不同浓度的PILO作用于Neuro-2A细胞24 h后,随着药物浓度升高,细胞存活率下降,并通过计算得到PILO的半数抑制浓度(half maximal inhibitory concentration,IC50)为18.27 mmol·L-1,见图 1。应用20 mmol·L-1的PILO进行后续实验。
|
| 图 1 不同浓度PILO对Neuro-2A细胞活力的影响 Fig.1 Cell viability in different concentrations of PILO-treated Neuro-2A cells |
2.2 PILO诱导Neuro-2A细胞出现凋亡
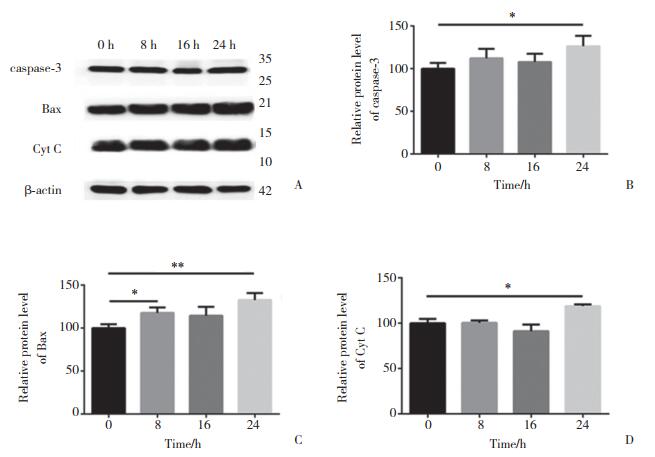
应用20 mmol·L-1 PILO处理Neuro-2A细胞24 h后,与对照组相比,凋亡相关蛋白caspase-3、Bax和Cyt C表达水平明显升高(P < 0.05),见图 2。提示应用20 mmol·L-1 PILO处理Neuro-2A细胞24 h后,凋亡发生。因此,应用20 mmol·L-1 PILO处理Neuro-2A细胞24 h进行后续实验。
|
| A, the expression of caspase-3, Bax, and Cyt C in different groups; B, statistical analysis of caspase-3; C, statistical analysis of Bax; D, statistical analysis of Cyt C.*P < 0.05, **P < 0.01. 图 2 PILO处理Neuro-2A细胞不同时间后凋亡相关蛋白表达 Fig.2 The expression of apoptotic-related proteins in Neuro-2A cells induced by PILO at different times through Western blotting |
2.3 PILO诱导Neuro-2A细胞中TRPM7高表达
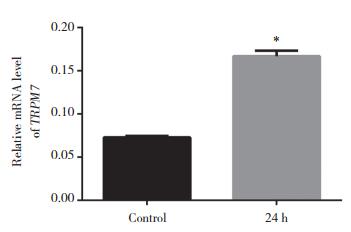
应用PILO处理24 h后,与对照组(7.285%±1.587%)相比,PILO模型组TRPM7 mRNA表达(16.700%±1.587%)显著增加(P < 0.000 1),见图 3。提示PILO处理Neuro-2A细胞24 h后,TRPM7表达增加。
|
| *P < 0.000 1 vs control group. 图 3 PILO处理Neuro-2A细胞中TRPM7 mRNA表达 Fig.3 The mRNA expression of TRPM7 in the PILO-treated group |
2.4 干扰TRPM7表达抑制PILO诱导的细胞模型出现凋亡
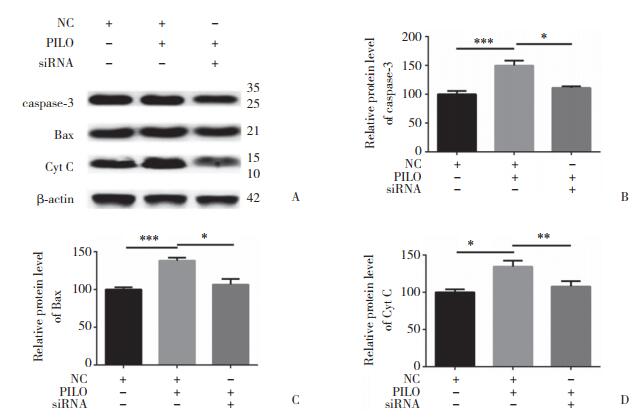
应用PILO处理Neuro-2A细胞24 h后,与PILO模型组相比,PILO+siRNA组凋亡相关蛋白caspase-3,Bax和Cyt C表达显著下降(均P < 0.05),见图 4,表明敲除TRPM7基因后,凋亡相关蛋白表达下调。
|
| A, the expression of caspase-3, Bax, and Cyt C in different groups; B, statistical analysis of caspase-3; C, statistical analysis of Bax; D, statistical analysis of Cyt C.*P < 0.05, **P < 0.01, ***P < 0.001. 图 4 干扰TRPM7对PILO诱导的细胞模型凋亡相关蛋白的影响 Fig.4 Effect of interference with TRPM7 on apoptotic-related proteins in the PILO-treated cell model |
2.5 干扰TRPM7表达对PILO诱导的细胞模型凋亡形态学的影响
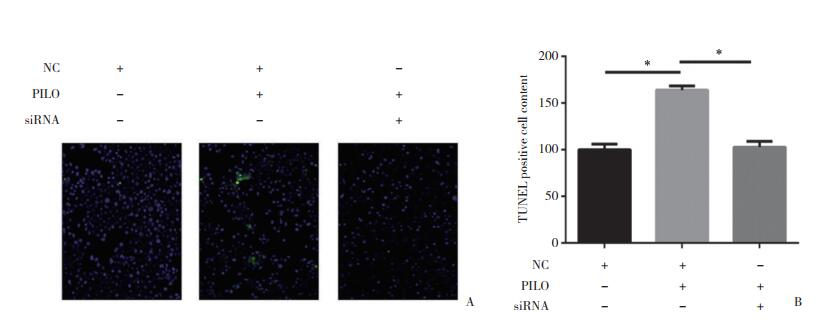
应用TUNEL染色后,与对照组相比,PILO诱导Neuro-2A细胞凋亡率显著增加(P < 0.01);与PILO模型组相比,PILO+siRNA组细胞凋亡率显著减少(P < 0.05),见图 5。
|
| A, the result of TUNEL staining in different groups; B, statistical analysis of TUNEL staining. The blue dots represent the cell nucleus, and the green dots represent the TUNEL-positive cells. Scale bar=100 μm. *P < 0.01. 图 5 干扰TRPM7对PILO诱导的细胞模型凋亡形态学的影响 Fig.5 Effect of interference with TRPM7 on the apoptotic morphology of the cell model induced by PILO by TUNEL staining |
3 讨论
癫痫是一种常见的神经系统疾病,其具体发生机制仍未可知。研究[1]表明,离子通道参与癫痫的发生并发挥重要作用。TRPM7是非选择性阳离子通道,介导多种神经系统疾病的发生与发展。目前,许多离子通道都被证明参与了癫痫的发生,而TRPM7在癫痫中的作用研究较少。TRPM7抑制剂降低了癫痫发作诱导的TRPM7过度表达、细胞内锌积累和活性氧生成;氧化应激、神经胶质细胞活化和血脑屏障破坏也受到抑制。此外,TRPM7抑制剂可显著降低癫痫发作后的凋亡神经元死亡[5]。然而,TRPM7在癫痫体外模型中对细胞死亡的作用尚未报道。
凋亡是一种经典的细胞死亡方式,是帕金森病、阿尔茨海默病和亨廷顿病等慢性神经退行性疾病中神经细胞死亡的主要原因[7]。研究[10]发现,应用特异性siRNA敲除TRPM7或采用TRPM7非特异性抑制剂2-氨基乙基联苯基硼酸酯和钆(Gd3+)作用于高糖处理的NS20Y神经细胞细胞后,凋亡受到抑制;而过表达TRPM7基因后,凋亡增加;这表明TRPM7参与凋亡发生。在帕金森病模型中应用TRPM7特异性microRNA(miR-22)抑制TRPM7表达会减少细胞凋亡[3]。到目前为止,癫痫体外模型中TRPM7与凋亡的关系仍不清楚。
本研究首次表明TRPM7参与介导PILO体外模型的凋亡。采用蛋白质印迹法和实时荧光定量PCR发现PILO诱导的体外癫痫模型导致凋亡相关蛋白(caspase-3、Bax和Cyt C)和TRPM7基因表达上调,而沉默TRPM7引起凋亡相关蛋白表达下降,表明TRPM7参与介导PILO体外模型的凋亡。本研究为癫痫机制的阐明与治疗提供了新靶点,但在癫痫状态下,TRPM7调控凋亡的具体机制仍需进一步探究。
| [1] |
ZHENG F. TRPC channels and epilepsy[J]. Adv Exp Med Biol, 2017, 976: 123-135. DOI:10.1007/978-94-024-1088-4_11 |
| [2] |
ZHU DH, SU YC, FU BM, et al. Magnesium reduces blood-brain barrier permeability and regulates amyloid-β transcytosis[J]. Mol Neurobiol, 2018, 55(9): 7118-7131. DOI:10.1007/s12035-018-0896-0 |
| [3] |
YANG CP, ZHANG ZH, ZHANG LH, et al. Neuroprotective role of microRNA-22 in a 6-hydroxydopamine-induced cell model of Parkinson's disease via regulation of its target gene TRPM7[J]. J Mol Neurosci, 2016, 60(4): 445-452. DOI:10.1007/s12031-016-0828-2 |
| [4] |
FREY D, SCHNEIDER C, XU L, et al. Early and selective loss of neuromuscular synapse subtypes with low sprouting competence in motoneuron diseases[J]. J Neurosci, 2000, 20(7): 2534-2542. DOI:10.1523/jneurosci.20-07-02534.2000 |
| [5] |
JEONG JH, LEE SH, KHO AR, et al. The transient receptor potential melastatin 7(TRPM7) inhibitors suppress seizure-induced neuron death by inhibiting zinc neurotoxicity[J]. Int J Mol Sci, 2020, 21(21): 7897. DOI:10.3390/ijms21217897 |
| [6] |
KAWAMOTO Y, NAKAJIMA YI, KURANAGA E. Apoptosis in cellular society: communication between apoptotic cells and their neighbors[J]. Int J Mol Sci, 2016, 17(12): 2144. DOI:10.3390/ijms17122144 |
| [7] |
GHAVAMI S, SHOJAEI S, YEGANEH B, et al. Autophagy and apoptosis dysfunction in neurodegenerative disorders[J]. Prog Neurobiol, 2014, 112: 24-49. DOI:10.1016/j.pneurobio.2013.10.004 |
| [8] |
CASTIGLIONI S, ROMEO V, LOCATELLI L, et al. The simultaneous downregulation of TRPM7 and MagT1 in human mesenchymal stem cells in vitro: effects on growth and osteogenic differentiation[J]. Biochem Biophys Res Commun, 2019, 513(1): 159-165. DOI:10.1016/j.bbrc.2019.03.178 |
| [9] |
ZHOU DM, SUN LL, ZHU J, et al. miR-9 promotes angiogenesis of endothelial progenitor cell to facilitate thrombi recanalization via targeting TRPM7 through PI3K/Akt/autophagy pathway[J]. J Cell Mol Med, 2020, 24(8): 4624-4632. DOI:10.1111/jcmm.15124 |
| [10] |
HUANG Y, LENG TD, INOUE K, et al. TRPM7 channels play a role in high glucose-induced endoplasmic reticulum stress and neuronal cell apoptosis[J]. J Biol Chem, 2018, 293(37): 14393-14406. DOI:10.1074/jbc.RA117.001032 |
 2022, Vol. 51
2022, Vol. 51