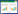文章信息
- 崔梦旭, 郑阳, 王晓明
- CUI Mengxu, ZHENG Yang, WANG Xiaoming
- 新生猪缺氧缺血性脑损伤后脑内髓鞘相关蛋白表达的变化
- Changes in the expression of myelin-associated proteins after hypoxic-ischemic brain injury in neonatal piglets
- 中国医科大学学报, 2022, 51(3): 199-202
- Journal of China Medical University, 2022, 51(3): 199-202
-
文章历史
- 收稿日期:2021-04-26
- 网络出版时间:2022-01-14 8:39
新生儿缺氧缺血性脑病(hypoxic-ischemic encephalopathy,HIE)可引起新生儿围产期脑功能损伤,包括髓鞘损伤[1]。髓鞘碱性蛋白(myelin basic protein,MBP)在中枢神经系统由少突胶质细胞合成,在婴幼儿时期表达量较高,其表达量减少说明髓鞘发生一定程度的损伤。髓鞘相关糖蛋白(myelin-associated glycoprotein,MAG)位于髓鞘膜的最内层,与轴突膜保持密切接触。它在外周神经系统中的施万细胞和中枢神经系统中的少突胶质细胞表达[2]。髓鞘少突胶质细胞糖蛋白(myelin oligodendrocyte glycoprotein,MOG)位于髓鞘外膜,与其他主要的髓鞘蛋白相比,MOG的表达延迟24~48 h,且在少突胶质细胞表面表达,因此MOG是成熟少突胶质细胞的一个很好的标志物[3]。本研究观察新生猪缺氧缺血性(hypoxic-ischemic,HI)脑损伤模型在不同时间点MBP、MOG、MAG表达的变化,探究HI脑损伤对中枢神经系统髓鞘和少突胶质细胞的影响。
1 材料与方法 1.1 实验动物和分组选用28头健康新生约克夏猪,平均体质量1.0~1.5 kg,3~5日龄,雌雄不限,随机分为对照组(n = 4)和HI模型组(n = 24)。根据HI后的存活时间,将HI模型组分为6个亚组(n = 4),分别为0~2 h、2~6 h、6~12 h、12~24 h、24~48 h、48~72 h亚组。本研究获得我院伦理委员会审批,所有实验动物的处理遵守《实验动物管理条例》和《实验动物许可证管理办法》。
1.2 动物模型制作HI模型组新生猪使用速眠新注射液(长春军事医学院兽医研究所)按0.6 mL/kg剂量肌肉注射麻醉,在28~30 ℃室温下操作,麻醉后行气管插管(直径2.5 mm),使用TKR-200C小动物呼吸机(江西特力麻醉呼吸设备中国有限公司)机械通气(100%氧气),使用Tuff Sat手掌式脉搏血氧仪(美国GE公司)监测心率和血氧饱和度。消毒颈部皮肤,取颈部正中切口,游离双侧颈总动脉,置于保温箱内约30 min,待其状态稳定,用动脉夹夹闭双侧颈总动脉,同时机械通入6%含氧浓度的氮氧混合气(大连大特气体有限公司),HI状态持续40 min后撤去动脉夹,改为机械通入100%氧气。操作完成后,缝合切口,新生猪恢复自主呼吸后停用呼吸机。全程密切监控心率和血氧饱和度。对照组新生猪仅游离双侧颈总动脉,不进行HI操作。
1.3 免疫组化染色 1.3.1 染色过程HI造模完成后,根据分组在相应时间段处死动物,迅速取出脑组织,使用4%多聚甲醛固定,经脱水、二甲苯透明、石蜡包埋后,以冠状面切成4 mm厚的组织片,进行MBP、MOG、MAG(英国Abcam公司)免疫组化染色。置于37 ℃烤箱烤干切片,行常规脱水、透明、封片操作。用PBS代替一抗做阴性对照。
1.3.2 图像采集和结果分析使用日本Nikon Edipse E800显微镜和日本NIS-Elements F2.30图像采集软件,400倍光镜下观察,每张切片观察5~6个视野。镜下观察到棕黄色染色为阳性表达。使用Image Pro Plus6.0软件半定量分析免疫组化图像光密度(optical density,OD)值。对采集的数据进行统计学分析,判断各组中MBP、MOG、MAG的表达情况。
1.4 统计学分析采用SPSS 24.0软件进行统计学处理。计量资料经Kolmogorov-Smirnov检验均服从正态分布,以x±s表示。采用单因素方差分析比较各组间MBP、MOG、MAG的表达是否存在差异,两两比较使用LSD-t检验。采用双侧检验,P < 0.05为差异有统计学意义。
2 结果 2.1 MBP免疫组化染色结果和表达变化趋势MBP免疫组化染色结果(图 1)显示,与对照组相比,HI模型组0~2 h、2~6 h、6~12 h、12~24 h、24~48 h、48~72 h亚组染色均变浅。MBP的表达整体呈先降低后升高的趋势,6~12 h达到最低值,而后升高,24~48 h后再次降低。与对照组相比,HI模型组0~2 h、2~6 h、6~12 h、12~24 h、24~48 h、48~72 h亚组MBP的表达水平均降低,差异均有统计学意义(P < 0.05)。与HI模型组0~2 h亚组相比,HI模型组2~6 h、6~12 h、12~24 h、24~48 h、48~72 h亚组MBP的表达水平均降低,差异均有统计学意义(P < 0.05)。2~6 h亚组、6~12 h亚组、12~24 h亚组、24~48 h亚组、48~72 h亚组间两两比较,MBP的表达水平均无统计学差异(P > 0.05)。见表 1。
|
| 图 1 MBP、MOG、MAG免疫组化染色结果×400 Fig.1 Immunohistochemical staining of myelin basic protein(MBP), myelin oligodendrocyte glycoprotein(MOG), and myelin-associated glycoprotein(MAG) ×400 |
| Group | MBP | MOG | MAG |
| Control group | 0.039 3±0.004 2 | 0.022 4±0.003 73),4) | 0.050 8±0.004 5 |
| HI model group | |||
| 0-2 h | 0.033 2±0.003 31) | 0.022 5±0.002 73),4) | 0.044 9±0.004 21) |
| 2-6 h | 0.027 7±0.001 71),2) | 0.028 5±0.005 34) | 0.042 7±0.005 61) |
| 6-12 h | 0.025 9±0.002 91),2) | 0.036 0±0.004 4 | 0.041 1±0.006 91) |
| 12-24 h | 0.026 7±0.002 91),2) | 0.025 8±0.004 54) | 0.039 6±0.005 91) |
| 24-48 h | 0.027 4±0.003 31),2) | 0.023 6±0.002 94) | 0.041 4±0.002 61) |
| 48-72 h | 0.027 6±0.005 41),2) | 0.024 0±0.003 14) | 0.039 7±0.002 71) |
| 1)P < 0.05 vs control group;2)P < 0.05 vs 0-2 h;3)P < 0.05 vs 2-6 h;4)P < 0.05 vs 6-12 h. | |||
2.2 MOG免疫组化染色结果和表达变化趋势
MOG免疫组化染色结果(图 1)显示,MOG阳性表达为棕黄色颗粒。MOG表达整体呈先升高再降低再升高的趋势,6~12 h达到最高值,而后降低,24~48 h后略有升高。与HI模型组6~12 h亚组相比,对照组和HI模型组0~2 h、2~6 h、12~24 h、24~48 h、48~72 h亚组MOG的表达水平均降低,差异均有统计学意义(P < 0.05)。与HI模型组2~6 h亚组相比,对照组和HI模型组0~2 h亚组MBP表达水平均降低,差异有统计学意义(P < 0.05)。见表 1。
2.3 MAG的免疫组化染色结果及表达变化趋势MAG免疫组化染色结果(图 1)显示,MAG表达整体呈先降低后升高再降低的趋势,12~24 h达到最低值,而后升高,24~48 h后再次降低。与对照组相比,HI模型组0~2 h、2~6 h、6~12 h、12~24 h、24~48 h、48~72 h亚组MAG的表达水平均降低,差异均有统计学意义(P < 0.05);2~6 h亚组、6~12 h亚组、12~24 h亚组、24~48 h亚组、48~72 h亚组间两两比较,MAG的表达水平均无统计学差异(P > 0.05)。见表 1。
3 讨论既往对新生儿HI脑损伤的研究多集中于神经元的损伤和修复,较少关注髓鞘的损伤。事实上,少突胶质细胞作为中枢神经系统的髓鞘形成细胞,容易受到脑缺血的影响。
MBP是中枢髓鞘的一种结构性蛋白,约占髓鞘蛋白质总量的30%,具有中枢神经系统特异性,存在于有髓神经髓鞘的浆膜面,是中枢神经系统受损的标志物[4]。MBP起到维持髓鞘结构和功能、促进神经快速传导、维持神经传导绝缘的作用[5]。本研究中,HI模型组MBP的表达较对照组降低,提示HI后可能发生了髓鞘损伤,在6~12 h达到最低值后出现了小幅度升高,而后又降低,说明可能同时存在少突胶质细胞持续性损伤以及髓鞘再生。体外细胞研究[6]提示,缺氧可引起神经干细胞向少突胶质细胞和星形胶质细胞分化而抑制其向神经元分化。研究[7]表明,侧脑室下区的少突胶质细胞前体细胞在生理和缺血条件下可以分化为髓鞘形成的少突胶质细胞,但体内环境更加复杂,具体作用机制有待进一步明确。MBP具有强碱性,当发生大量髓鞘损伤时,MBP进入血液和脑脊液,并作为抗原激活免疫系统,诱导继发性炎症反应,导致神经细胞凋亡[8]。因此,进行早期干预保护神经胶质细胞,抑制脱髓鞘进程,促进中枢神经系统再髓鞘化,对改善HIE患儿的预后尤为重要。
MOG在中枢神经系统髓鞘和少突胶质细胞的外表面表达,因此更容易受到免疫系统攻击,被认为和一些自身免疫性疾病相关[9]。MOG的表达比其他髓鞘蛋白开始得晚,因此可以作为少突胶质细胞成熟的标志[10]。本研究中,对照组少突胶质细胞中MOG的表达量极少,HI模型组MOG的表达呈先升高后降低的趋势,在6~12 h达到最高值,其可能原因是MOG表达的时间较晚,在HI过程中成熟的少突胶质细胞逐渐增多,同时也存在少突胶质细胞损伤,在6~12 h前少突胶质细胞的生成大于缺失,MOG的表达增加可能会干扰受损神经的修复。在6~12 h后,少突胶质细胞的生成减弱,损伤加强,MOG的表达逐渐减少。
MAG在最内层髓磷脂膜包裹物上表达,直接包裹在轴突表面[11]。MAG具有双重特性,既是轴突生长因子,又能抑制轴突再生;在胎儿时期,MAG是一种刺激剂,当髓鞘形成完成时,MAG变成一种抑制剂。它可以增强轴突-髓鞘的长期稳定性,并调节轴突细胞骨架。除在轴突-髓鞘稳定方面的作用外,MAG还抑制损伤后轴突的再生[12]。MAG通过与特定的神经元糖脂(神经节苷脂)相互作用来维持髓鞘-轴突间距,抑制轴突再生并控制髓磷脂的形成。本研究中,HI模型组MAG的表达较对照组减少,但HI模型组各亚组间无统计学差异,说明在新生儿HIE中,会发生MAG丢失。
综上所述,新生猪HI后可发生脑白质损伤,其发病机制可能与氧化应激、兴奋性氨基酸积累、小胶质细胞激活有关。本研究使用新生猪HI模型,很好地模拟了新生儿HIE的病理生理过程。本研究中,HI后MBP、MAG的表达均降低,MOG的表达先升高再降低,说明HI可引起髓鞘和少突胶质细胞的损伤。这也提示临床在治疗新生儿HIE时,在挽救神经细胞的同时,还应该关注髓鞘的损伤,以及脱髓鞘改变对神经元的继发性损伤和对轴突再生的抑制作用。保护髓鞘、促进小胶质细胞对髓鞘裂解产物的清除、阻断介导MAG和MOG对神经轴突抑制作用的下游信号分子,对改善HIE患儿的远期预后也会起到一定作用。
| [1] |
BUSL KM, GREER DM. Hypoxic-ischemic brain injury: pathophysiology, neuropathology and mechanisms[J]. NeuroRehabilitation, 2010, 26(1): 5-13. DOI:10.3233/nre-2010-0531 |
| [2] |
QUARLES RH. Myelin-associated glycoprotein(MAG): past, pre-sent and beyond[J]. J Neurochem, 2007, 100(6): 1431-1448. DOI:10.1111/j.1471-4159.2006.04319.x |
| [3] |
JOHNS TG, BERNARD CC. The structure and function of myelin oligodendrocyte glycoprotein[J]. J Neurochem, 1999, 72(1): 1-9. DOI:10.1046/j.1471-4159.1999.0720001.x |
| [4] |
BOGGS JM. Myelin basic protein: a multifunctional protein[J]. Cell Mol Life Sci, 2006, 63(17): 1945-1961. DOI:10.1007/s00018-006-6094-7 |
| [5] |
HARAUZ G, LADIZHANSKY V, BOGGS JM. Structural polymorphism and multifunctionality of myelin basic protein[J]. Biochemistry, 2009, 48(34): 8094-8104. DOI:10.1021/bi901005f |
| [6] |
王雨晴, 陈志刚, 张斯佳, 等. 神经干细胞在缺氧后的分化情况及相关信号通路初探[J]. 中国比较医学杂志, 2021, 31: 7-15. DOI:10.3969/j.issn.1671-7856.2021.01.002 |
| [7] |
ZAWADZKA M, RIVERS LE, FANCY SP, et al. CNS-resident glial progenitor/stem cells produce Schwann cells as well as oligodendrocytes during repair of CNS demyelination[J]. Cell Stem Cell, 2010, 6(6): 578-590. DOI:10.1016/j.stem.2010.04.002 |
| [8] |
SUN X, WANG X, CHEN T, et al. Myelin activates FAK/Akt/NF-kappaB pathways and provokes CR3-dependent inflammatory response in murine system[J]. PLoS One, 2010, 5(2): e9380. DOI:10.1371/journal.pone.0009380 |
| [9] |
SALAMA S, KHAN M, PARDO S, et al. MOG antibody-associated encephalomyelitis/encephalitis[J]. Mult Scler, 2019, 25(11): 1427-1433. DOI:10.1177/1352458519837705 |
| [10] |
REINDL M, WATERS P. Myelin oligodendrocyte glycoprotein antibodies in neurological disease[J]. Nat Rev Neurol, 2019, 15(2): 89-102. DOI:10.1038/s41582-018-0112-x |
| [11] |
SCHNAAR RL, LOPEZ PH. Myelin-associated glycoprotein and its axonal receptors[J]. J Neurosci Res, 2009, 87(15): 3267-3276. DOI:10.1002/jnr.21992 |
| [12] |
MCKERRACHER L, ROSEN KM. MAG, myelin and overcoming growth inhibition in the CNS[J]. Front Mol Neurosci, 2015, 8: 51. DOI:10.3389/fnmol.2015.00051 |
 2022, Vol. 51
2022, Vol. 51