文章信息
- 黄鑫, 朱璐, 林梅青, 王继蕊, 商秀丽
- HUANG Xin, ZHU Lu, LIN Meiqing, WANG Jirui, SHANG Xiuli
- MEG8对阿尔茨海默病微环境下血脑屏障通透性的影响及其作用机制
- Effects of MEG8 on the blood-brain barrier permeability of Alzheimer disease microenvironment and its mechanism
- 中国医科大学学报, 2022, 51(12): 1069-1073
- Journal of China Medical University, 2022, 51(12): 1069-1073
-
文章历史
- 收稿日期:2022-06-29
- 网络出版时间:2022-12-08 15:04:58
2. 中国医科大学附属盛京医院康复中心, 沈阳 110136;
3. 中国医科大学附属第一医院神经内科, 沈阳 110001
2. Department of Rehabilitation, Shengjing Hospital of China Medical University, Shenyang 110136, China;
3. Department of Neurology, The First Hospital of China Medical University, Shenyang 110001, China
阿尔茨海默病(Alzheimer disease,AD)是慢性进展性中枢神经系统退行性疾病,其病理学标志包括β淀粉样蛋白(β-amyloid protein,Aβ)积聚、神经纤维缠结、神经元变性等[1]。神经血管功能障碍促进AD的发生发展。血脑屏障(blood-brain barrier,BBB)是中枢神经系统的重要组成部分[2]。生理条件下,BBB能选择性地限制毒素从外周血液进入中枢神经系统,调节新陈代谢,维持大脑微环境的稳态[3-4]。内皮细胞间的紧密连接蛋白是维持BBB生理功能的重要结构基础。研究[5]显示,AD发病早期就出现了BBB通透性增加和血管损伤等功能障碍。
长链非编码RNA(long non-coding RNA,lncRNA)是一类长度超过200 nt的非编码转录本,在多种生物学过程中发挥关键作用[6]。越来越多的研究[7]表明,lncRNA可对下游靶基因的染色质修饰、转录和转录后调控产生影响。研究[8]发现,lncRNA在许多神经系统疾病(癫痫、神经系统退行性疾病和遗传性疾病等)中表达失调。MEG8是小核仁宿主基因,定位于染色体14q32.3的基因簇中。MEG8通过吸附miR-181a-5p抑制氧化低密度脂蛋白诱导的血管平滑肌细胞增殖、迁移,并诱导细胞凋亡,参与对动脉粥样硬化进程的调控[9]。MEG8可通过与多梳抑制复合物2(EZH2)蛋白的增强子结合,诱导组蛋白H3甲基化并调节上皮-间质转化相关的细胞形态学变化[10]。目前,关于MEG8在AD微环境下BBB中调节作用的研究尚未见报道。
在体外AD微环境BBB的研究中,目前是以Aβ处理的人脑微血管内皮细胞模拟AD微环境下BBB来进行。本研究探讨MEG8对AD微环境下BBB通透性的作用,旨在为AD早期BBB的功能改变提供新的实验依据。
1 材料与方法 1.1 细胞培养人脑微血管内皮细胞hCMEC/D3由法国巴黎第五大学Couraud教授惠赠,EBM-2培养基培养。人脑正常星形胶质细胞(normal human astrocyte,NHA)购自上海中科院细胞库,DMEM(含10%胎牛血清)培养。所有细胞均于37 ℃、5% CO2的恒温培养箱中培养。每2~3 d细胞换液或者传代。Aβ(美国Sigma公司)溶解后加入细胞中共同孵育。
1.2 构建体外BBB模型并进行Aβ处理NHA细胞接种于6孔Transwell小室(0.4微孔膜)的下室,加入3 mL的DMEM完全培养基进行培养,待细胞长至约80%后,将2×105个Aβ处理的人脑微血管内皮细胞(Aβ-incubated human brain microvascular endothelial cells,AD-ECs)接种于鼠尾胶原预处理的Transwell小室的上室。上下室内均加入适量的EBM-2完全培养液。48 h后换液,培养4 d后体外BBB模型建立。
1.3 稳定转染沉默MEG8质粒及分组待细胞长至接近80%融合时,按照转染试剂Lipofectamine LTX说明书,应用Lipofectamine LTX试剂将MEG8沉默质粒及其阴性对照质粒转染至细胞中,48 h后显微镜下观察细胞带光情况。随后,应用G418筛选细胞,每隔24 h梯度(0.2 mg/mL)加药1次,最高至2 mg/mL筛选出稳定转染的AD-ECs。按照细胞处理方法分为:对照组、转染MEG8阴性对照组(sh-NC组)、转染MEG8沉默质粒组(sh-MEG8组)。
1.4 实时荧光定量PCR(real-time quantitative PCR,qRT-PCR)检测使用Trizol提取细胞中的总RNA,测定RNA浓度。获取的RNA应用染料法一步法试剂盒来检测MEG8的表达情况。以GAPDH为内参,以2-ΔΔCt计算相对表达量。
1.5 跨内皮阻抗(transendothelial electric resistance,TEER)值测定应用微孔电阻系统检测TEER值,在37 ℃恒温下检测各组TEER值的变化,每组样品读数减去空白Transwell小室的微孔膜背景电阻值,之后与Transwel小室表面积的乘积为最终TEER值(Ω·cm2)。
1.6 辣根过氧化物酶(horseradish peroxidase,HRP)含量测定应用转染细胞建立体外BBB模型后,将含有0.5 μmol/L HRP的无血清EBM-2培养基加入Transwell小室的上室中,收集下室的培养基并通过TMB显色法测量HRP含量(pmol/cm2)。
1.7 免疫荧光观察选取生长状态良好的细胞培养在含1%明胶包被的盖玻片上,待细胞生长融合至95%~100%时,PBS清洗3次。4%多聚甲醛(ZO-1)室温固定30 min后0.3% Trixton-100室温通透10 min,或甲醇(occludin无需通透)-20℃固定10 min,PBS清洗3次。5%BSA室温封闭2 h,PBS清洗3次。加入1%BSA稀释的一抗(ZO-1和occludin均1∶50稀释),4 ℃湿盒孵育过夜。复温45 min,PBST清洗3次,每次5 min。加入1%BSA稀释的Cy3标记荧光二抗山羊抗兔(1∶500)避光于抗体孵育盒中室温孵育1.5 h。PBST避光清洗3次,每次5 min。DAPI避光染核5~8 min,PBS避光清洗3次,每次5 min。抗荧光淬灭封片液封片,荧光显微镜下观察和拍照。
1.8 Western blotting检测搜集细胞样品,加入适量裂解液震荡混匀,置于冰上裂解45 min,超声粉碎,4 ℃ 17 000 r/min离心40 min,收集上清液。采用BCA法测定蛋白浓度,并计算上样量。等量的蛋白样品液(40~50 μg)经SDS-聚丙烯酰胺凝胶电泳后,将蛋白转至PVDF膜上,封闭后,按一定比例稀释一抗(ZO-1 1∶600;occludin 1∶600)4 ℃孵育过夜。HRP标记的二抗室温孵育1.5 h。GAPDH作为内参。ECL发光、拍照,结果以目的蛋白与GAPDH的相对整合密度值比值表示。
1.9 统计学分析采用SPSS 22.0统计软件,计量资料以x±s表示,2组间比较采用t检验,多组间比较采用单因素方差分析,P < 0.05为差异有统计学意义。
2 结果 2.1 MEG8在AD-ECs中的表达结果显示,人脑微血管内皮细胞和AD-ECs中MEG8的表达分别为1.00±0.00和2.05±0.29。与人脑微血管内皮细胞比较,MEG8在AD-ECs中表达显著升高(P < 0.01)。
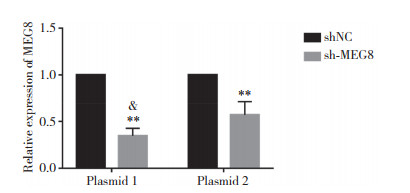
2.2 沉默MEG8的转染效率应用qRT-PCR检测沉默MEG8的转染效率。结果显示,在质粒1和质粒2中,与shNC组比较,sh-MEG8表达均显著降低(P < 0.01),质粒1中的转染效率更高(P < 0.05)。因此选择质粒1筛选的细胞进行后续实验。见图 1。
|
| **P < 0.01 vs shNC group in the same plasmid; & P < 0.05 vs the plasmid 2 in same group (n = 3, each group). 图 1 AD-ECs中沉默MEG8的转染效率比较 Fig.1 Comparison of transfection efficiency of deletion of MEG8 in AD-ECs |
2.3 沉默MEG8表达对AD微环境下BBB通透性的影响
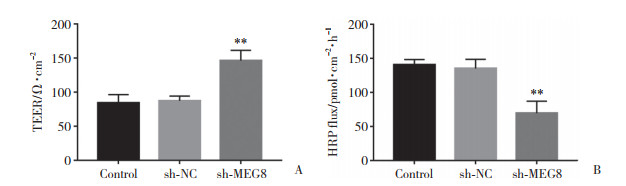
结果显示,与对照组比较,sh-NC组TEER值和HRP渗出量无显著变化(均P > 0.05);与sh-NC组比较,sh-MEG8组TEER值显著增加(P < 0.01),HRP渗出量显著降低(P < 0.01),提示沉默MEG8表达能够降低AD微环境下BBB的通透性。见图 2。
|
| Effects of deletion of MEG8 on TEER values (A) and HRP flux (B) in AD microenvironment. **P < 0.01 vs sh-NC group (n = 3, each group). 图 2 沉默MEG8表达对AD微环境BBB通透性的影响 Fig.2 Effects of deletion of MEG8 on the BBB permeability of AD microenvironment |
2.4 沉默MEG8对AD微环境下血管内皮细胞紧密连接相关蛋白ZO-1和occludin分布的影响
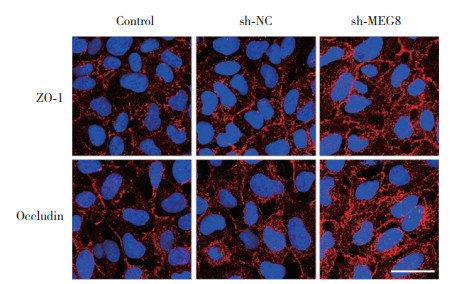
结果显示,与sh-NC组比较,sh-MEG8组紧密连接相关蛋白ZO-1和occludin呈现相对连续分布。见图 3。
|
| Immunofluorescence assays were used to determine ZO-1, and occludin (red) expression levels and distribution, respectively, and nuclei (blue) were labeled with DAPI. Scale bar = 30 μm. 图 3 沉默MEG8对AD微环境中紧密连接相关蛋白ZO-1和occludin分布的影响 Fig.3 Effects of deletion of MEG8 on the distribution of ZO-1 and occludin in AD microenvironment |
2.5 沉默MEG8表达对AD微环境下血管内皮细胞紧密连接相关蛋白ZO-1和occludin表达的影响
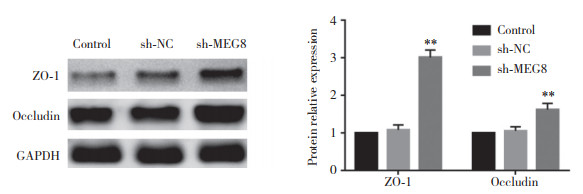
结果显示,与对照组比较,sh-NC组ZO-1和occludin的表达无统计学差异(均P > 0.05)。与sh-NC组比较,sh-MEG8组ZO-1和occludin表达显著升高(均P < 0.01),提示沉默MEG8表达能上调紧密连接相关蛋白ZO-1和occludin表达水平。见图 4。
|
| **P < 0.01 vs sh-NC group (n = 3, each group). 图 4 沉默MEG8表达对AD微环境下中ZO-1和occludin蛋白表达的影响 Fig.4 Effects of deletion of MEG8 on the expression of ZO-1 and occludin in AD microenvironment |
3 讨论
本研究首次证明了lncRNA MEG8在AD-ECs中高表达,沉默MEG8表达显著增加AD微环境下BBB的TEER值,降低HRP渗出量。此外,沉默MEG8表达使紧密连接相关蛋白ZO-1和occludin在AD-ECs中表达显著增加,同时在AD-ECs的边界上呈现相对连续的分布,提示MEG8可能通过影响紧密连接相关蛋白的表达和分布进而调控AD微环境下BBB的通透性。
BBB是调节中枢神经系统稳态的动态和复杂的界面,血管内皮细胞的紧密连接相关蛋白是BBB的主要物理屏障组分,通过细胞旁途径调节通透性。TEER值是检测BBB完整性的指标,HRP渗出量是检测BBB渗透性的指标,同时检测TEER值和HRP渗出量是目前公认的研究BBB通透性的指标。既往研究[11]表明,AD微环境下BBB的通透性增加,与本研究结果一致。MEG8在AD-ECs中高表达,沉默MEG8表达显著增加了AD微环境下BBB的TEER值,降低HRP渗出量,提示沉默MEG8表达可显著降低AD微环境下BBB的通透性。
在调节BBB通透性的细胞旁途径中,血管内皮细胞紧密连接相关蛋白ZO-1和occludin的分布与表达水平的变化直接影响BBB通透性[12-13]。在AD的发生发展进程中,特别是AD发病的早期,BBB通透性的改变发挥重要调节作用[14]。本研究结果发现沉默MEG8表达使AD-ECs边界的紧密连接相关蛋白ZO-1和occludin呈现相对连续的分布,显著增加了ZO-1和occludin的蛋白表达水平。有研究[15]报道,Aβ处理显著降低了血管内皮细胞紧密连接相关蛋白occludin和ZO-1的表达水平,损害了小鼠脑中BBB的完整性。上述研究结果均提示细胞旁途径的改变是AD早期BBB通透性变化的重要途径,而沉默MEG8表达可通过降低BBB的通透性发挥一定程度的保护作用。
近来研究[16]表明,lncRNA与PI3K-Akt、MTOR、AMPK等信号通路相互调节,调节AD的发生发展。lncRNA 17A在Aβ孵育的SH-SY5Y细胞中表达失调,过表达lncRNA 17A促进细胞自噬,诱导神经变性[17]。β-分泌酶1(beta-secretase 1,BACE1)与淀粉样蛋白沉积相关,研究[18]发现BEACE1反义链可通过调节BACE1的表达在AD的病理生理过程中发挥重要作用。本研究发现MEG8在AD-ECs中高表达。沉默MEG8表达使AD-ECs紧密连接相关蛋白ZO-1和occludin呈现相对连续的分布,ZO-1和occludin表达水平显著增加。提示沉默MEG8的表达可通过改变ZO-1和occludin的细胞分布,增加ZO-1和occludin的蛋白表达水平来降低AD微环境下BBB的通透性,从而发挥一定的保护作用。LINC00662在Aβ处理的人脑ECs中高表达,沉默LINC00662表达可通过改变ZO-1、occludin和Claudin-5的细胞分布,增加ZO-1、occludin和Claudin-5的蛋白表达水平来降低AD微环境下BBB通透性[12],与本研究结果类似。
综上所述,MEG8在AD-ECs中表达上调,沉默MEG8表达显著降低AD微环境下BBB的通透性,其作用机制可能是通过改变ZO-1和occludin的细胞分布,增加ZO-1和occludin蛋白表达实现的。MEG8在AD微环境下BBB的功能调节中可能发挥重要作用,但是,AD微环境下BBB的功能调节是多维度、多层次、多细胞、多分子共同参与的,因此,从不同层次的调控网络来探讨AD微环境下BBB通透性的变化,有望为AD的早期防治提供新策略。
| [1] |
ZHANG YL, WANG J, ZHANG ZN, et al. The relationship between amyloid-beta and brain capillary endothelial cells in Alzheimer's disease[J]. Neural Regen Res, 2022, 17(11): 2355-2363. DOI:10.4103/1673-5374.335829 |
| [2] |
ZLOKOVIC BV. Neurovascular pathways to neurodegeneration in Alzheimer's disease and other disorders[J]. Nat Rev Neurosci, 2011, 12(12): 723-738. DOI:10.1038/nrn3114 |
| [3] |
CARDOSO FL, BRITES D, BRITO MA. Looking at the blood-brain barrier: molecular anatomy and possible investigation approaches[J]. Brain Res Rev, 2010, 64(2): 328-363. DOI:10.1016/j.brainresrev.2010.05.003 |
| [4] |
KEANEY J, CAMPBELL M. The dynamic blood-brain barrier[J]. FEBS J, 2015, 282(21): 4067-4079. DOI:10.1111/febs.13412 |
| [5] |
ERICKSON MA, BANKS WA. Blood-brain barrier dysfunction as a cause and consequence of Alzheimer's disease[J]. J Cereb Blood Flow Metab, 2013, 33(10): 1500-1513. DOI:10.1038/jcbfm.2013.135 |
| [6] |
SHIBATA C, OTSUKA M, KISHIKAWA T, et al. Diagnostic and therapeutic application of noncoding RNAs for hepatocellular carcinoma[J]. World J Hepatol, 2015, 7(1): 1-6. DOI:10.4254/wjh.v7.i1.1 |
| [7] |
KUNG JTY, COLOGNORI D, LEE JT. Long noncoding RNAs: past, present, and future[J]. Genetics, 2013, 193(3): 651-669. DOI:10.1534/genetics.112.146704 |
| [8] |
LUO Q, CHEN YH. Long noncoding RNAs and Alzheimer's disease[J]. Clin Interv Aging, 2016, 11: 867-872. DOI:10.2147/CIA.S107037 |
| [9] |
ZHANG BY, DONG Y, ZHAO Z. LncRNA MEG8 regulates vascular smooth muscle cell proliferation, migration and apoptosis by targeting PPARα[J]. Biochem Biophys Res Commun, 2019, 510(1): 171-176. DOI:10.1016/j.bbrc.2019.01.074 |
| [10] |
TERASHIMA M, ISHIMURA A, WANNA-UDOM S, et al. MEG8 long noncoding RNA contributes to epigenetic progression of the epithelial-mesenchymal transition of lung and pancreatic cancer cells[J]. J Biol Chem, 2018, 293(47): 18016-18030. DOI:10.1074/jbc.RA118.004006 |
| [11] |
ZHU L, LIN MQ, MA J, et al. The role of LINC00094/miR-224-5p (miR-497-5p)/Endophilin-1 axis in Memantine mediated protective effects on blood-brain barrier in AD microenvironment[J]. J Cell Mol Med, 2019, 23(5): 3280-3292. DOI:10.1111/jcmm.14214 |
| [12] |
LIU QS, ZHU L, LIU XB, et al. TRA2A-induced upregulation of LINC00662 regulates blood-brain barrier permeability by affecting ELK4 mRNA stability in Alzheimer's microenvironment[J]. RNA Biol, 2020, 17(9): 1293-1308. DOI:10.1080/15476286.2020.1756055 |
| [13] |
HE JY, XUE YX, WANG QY, et al. Long non-coding RNA MIAT regulates blood tumor barrier permeability by functioning as a competing endogenous RNA[J]. Cell Death Dis, 2020, 11(10): 936. DOI:10.1038/s41419-020-03134-0 |
| [14] |
BALOYANNIS SJ. Brain capillaries in Alzheimer's disease[J]. Hell J Nucl Med, 2015, 18(Suppl 1): 152. |
| [15] |
WAN WB, CAO L, LIU LM, et al. Aβ(1-42) oligomer-induced leakage in an in vitro blood-brain barrier model is associated with up-regulation of RAGE and metalloproteinases, and down-regulation of tight junction scaffold proteins[J]. J Neurochem, 2015, 134(2): 382-393. DOI:10.1111/jnc.13122 |
| [16] |
YANG B, XIA ZA, ZHONG BW, et al. Distinct hippocampal expression profiles of long non-coding RNAs in an Alzheimer's disease model[J]. Mol Neurobiol, 2017, 54(7): 4833-4846. DOI:10.1007/s12035-016-0038-5 |
| [17] |
WANG XH, ZHANG M, LIU HF. LncRNA17A regulates autophagy and apoptosis of SH-SY5Y cell line as an in vitro model for Alzheimer's disease[J]. Biosci Biotechnol Biochem, 2019, 83(4): 609-621. DOI:10.1080/09168451.2018.1562874 |
| [18] |
SAYAD A, NAJAFI S, HUSSEN BM, et al. The emerging roles of the β-secretase BACE1 and the long non-coding RNA BACE1-AS in human diseases: a focus on neurodegenerative diseases and cancer[J]. Front Aging Neurosci, 2022, 14: 853180. DOI:10.3389/fnagi.2022.853180 |
 2022, Vol. 51
2022, Vol. 51




