文章信息
- 王辉, 李章富, 温行, 刘剑利, 李福才
- WANG Hui, LI Zhangfu, WEN Xing, LIU Jianli, LI Fucai
- 肽基脯氨酰顺反异构酶1对喉癌细胞系Hep-2细胞生物学行为的影响
- Effect of peptidylprolyl cis/trans isomerase NIMA-interacting 1 on the biological behavior of Hep-2 cells
- 中国医科大学学报, 2021, 50(8): 681-689
- Journal of China Medical University, 2021, 50(8): 681-689
-
文章历史
- 收稿日期:2020-09-06
- 网络出版时间:2021-07-28 9:05
喉癌是一种主要起源于喉黏膜上皮组织的恶性肿瘤。近年来研究[1]显示喉癌的5年存活率未见提高,且诊断缺乏分子水平临床特征。因此,阐明影响喉癌发生发展的分子生物学机制至关重要。肽基脯氨酰顺反异构酶1(peptidylprolyl cis/trans isomerase NIMA-interacting 1,Pin1)能特异地识别和结合蛋白质磷酸化丝/苏-脯氨酸基序,催化磷酸化丝/苏-脯氨酸肽键发生顺反异构[2]。研究[3]显示,人类多种癌症中Pin1蛋白高表达,进而上调癌蛋白表达,扰乱细胞周期进程。Pin1通过磷酸化依赖的泛素通路,催化它的底物结构发生顺反异构,从而避免癌蛋白降解[4]。除了稳定和激活癌蛋白之外,Pin1可以使大量肿瘤抑制因子和生长抑制因子失活。研究[5]显示乳腺癌组织中Pin1过表达与中心体扩增有关。在基因敲除的小鼠胚胎成纤维细胞中,Pin1过表达可促进中心体扩增,但Pin1调节中心体扩增的分子机制尚不清楚。
核转录因子-κB(nuclear transcription factor-kappa B,NF-κB)异常激活在人类许多癌症中均有发现[6]。肝癌细胞中Pin1通过介导NF-κB活化而促进肿瘤的发生[7]。NF-κB是可诱导的二聚体核转录因子,p50/p65异源二聚体为NF-κB家族的主要形式。前期研究[8]发现NF-κB可以特异性地结合细胞周期蛋白依赖性激酶2(cyclin-dependent kinase 2,CDK2)启动子区,增强CDK2表达,并调节中心体扩增。本研究探讨Pin1对喉癌细胞系Hep-2细胞中心体扩增以及生物学行为的影响,旨在为阐明喉癌发生发展的分子机制提供依据。
1 材料与方法 1.1 材料人喉癌细胞系Hep-2细胞购自中国科学院上海生命科学研究所。Pin1的小干扰RNA(small interfering RNA,siRNA)及阴性对照由广州锐博公司合成。其他材料包括RPMI 1640培养基(美国Gibeo公司),四季青胎牛血清(浙江天杭公司),细胞周期检测试剂盒(中国KeyGEN BionTECH公司),Annexin V FITC Apoptosis Detection Kit 1(美国BD公司),Cell Counting Kit-8(中国Dojindo公司),RNAiso Plus、SYBR Premix Ex TapⅡ、Primescript RT reagent kit(perfect real time)(日本TaKaRa公司),来源于鼠GTU-88杂交瘤抗γ微管蛋白单克隆抗体、NF-κB/p65抗体(美国Sigma公司),Pin1抗体、CDK2抗体、β-actin抗体(美国Proteintech公司),山羊抗兔二抗、山羊抗鼠二抗(北京中杉金桥生物技术有限公司),Alexa Flour-488标记抗小鼠IgG二抗(美国Invitogen公司)。
1.2 方法 1.2.1 细胞培养人喉癌细胞系Hep-2细胞接种于含10%胎牛血清的RPMI1640培养基(含100 U/mL青霉素、100 μg/mL链霉素),置于37 ℃、5% CO2及饱和湿度条件下培养,0.25%胰酶消化传代。
1.2.2 Pin1的siRNA构建、转染及分组Pin1的siRNA,靶序列5’-CATTTGAAGACGCCTCGTT-3’;正义链5’-CAUUUGAAGACGCCUCGUUdTdT-3’;反义链3’-dTdTGUAAACUUCUGCGGAGCAA-5’。细胞接种于6孔板中,在含10%小牛血清培养基中生长至60%~80%融合。采用脂质体转染法,按照脂质体说明书操作。Pin1过表达分为3组:转染pcDNA3.1组(NC组)、转染pcDNA3.1-Pin1组(Pin1组)、转染pcDNA3.1-Pin1后加NF-κB/p65抑制剂(BAY11-7082)组(Pin1+7082组)。Pin1干扰分为3组:转染阴性对照组(NC组)、转染siRNA组(Si-Pin1组)、转染siRNA后加NF-κB/p65激活剂(IL-1β)组(Si-Pin1+IL-1β组)。
1.2.3 免疫荧光检测各组细胞爬片,-20 ℃预冷甲醛溶液中固定20 min,预冷丙酮溶液-20 ℃再固定6 min,1%牛血清白蛋白(BSA)封闭0.5 h,分别加入1∶50稀释的γ-Tubulin抗体、p65抗体(1∶100),4 ℃湿盒孵育过夜,漂洗后加入Alexa Flour-488标记抗小鼠IgG二抗,37 ℃湿盒孵育0.5 h,结束后DAPI复染,10 min后荧光显微镜下观察细胞2极至多极中心体分裂情况、每组计数4张载玻片,中心体异常=2极以上分裂细胞数/总分裂细胞数×100%。
1.2.4 CCK-8检测各组细胞增殖情况常规细胞铺板并转染后,分别将各组细胞重悬,2×103/孔加入细胞悬液铺96孔板。每组5个复孔,每孔加入完全培养基补齐体积至100 μL,37 ℃孵育培养,每12 h测定1次,测试前每孔加入10 μL CCK-8试剂,混匀,37 ℃孵育2 h。酶标仪于450 nm处测定吸光度值(optical delnsity,OD)。
1.2.5 细胞凋亡检测常规细胞铺板并转染后48 h收集细胞,利用Annexin V FITC Apoptosis Detection Kit试剂盒检测细胞凋亡情况,每个样品抽取1×105个细胞进行流式细胞仪检测。
1.2.6 细胞周期测定胰酶消化细胞后离心,用含有PBS溶液(300 μL)重悬细胞,加入700 μL无水乙醇固定过夜,第2天离心并用PBS溶液清洗2遍,溴化丙啶染色后流式细胞仪检测。
1.2.7 Transwell检测各组细胞利用无抗生素、无血清培养基制成细胞悬液,接种于Transwell小室上室,5×104/孔,每组3个复孔。下室加入含10%小牛血清的RPMI1640培养基(600 µL)。培养24 h后将上室底部滤膜用4%甲醛固定30 min,苏木素染色40 s,伊红染色3 min。PBS洗涤风干后显微镜下拍照计数。
1.2.8 划痕实验药物处理前用200 μL移液管头在细胞板的中央做一划痕,立即在显微镜下观察并拍照记录,设定为0 h;药物处理24 h再次在显微镜下观察并拍照记录,设定为24 h,划痕的宽度分别为A0和A24,迁移距离=A24-A0。
1.2.9 克隆形成实验检测肿瘤细胞集落形成能力常规细胞铺板并转染后,分别将各组细胞重悬,将细胞浓度调整至3×104/mL后,移取100 μL至6孔板内,加2 mL新鲜完全培养基摇匀后放入培养箱继续培养,待细胞团个数达到50个左右,固定并以苏木素染色。
1.2.10 实时PCR检测细胞中Pin1及CDK2 mRNA表达收获培养的细胞,提取细胞总RNA,将mRNA逆转录为cDNA,扩增PIN1、CDK2基因,同时以GAPDH基因作为内参照。引物序列为:GAPDH,上游,5’-TGCACCACCAACTGCTTAG-3’,下游,5’-GACGAGGGATGATGTTC-3’;Pin1,上游,5’-ATGGCGGACGAGGAGA-3’,下游,5’-TGGCTGGCGTTAGTGAT-3’;CDK2,上游,5’-GTGGGCCCGGCAAGATTTTAG-3’,下游,5’-GCCGAAATCCGCTTGTTAGGG-3’。采用2-ΔΔCt表示实验组目的基因相对于对照组原始拷贝数的倍数差异。
1.2.11 Western blotting检测总蛋白采用RIPA裂解液充分裂解细胞、提取蛋白。核蛋白按照Scientific Pierce NE-PER试剂盒说明书抽提核蛋白、胞质蛋白,均置于100 ℃变性5 min。配置5%的浓缩胶和12%的分离胶,待变性结束将样本加入点样孔中进行垂直电泳(80 V 20 min,120 V 80 min)和电转膜(350 mA 45 min)。转膜完成后取出硝酸纤维素膜并用5%脱脂牛奶封闭过夜(4 ℃),第2天取出膜TBST溶液洗涤3次,分别孵育Pin1、actin、CDK2、p65一抗,过夜后取出膜TBST溶液洗涤3次,然后用辣根过氧化物酶标记的第二抗体37 ℃孵育,2 h后再次TBST溶液洗涤3次。显影后计算蛋白条带的灰度值,以目的蛋白灰度值/内参蛋白灰度值作为蛋白含量,对照组蛋白含量作为1。
1.3 统计学分析应用SPSS 13.0统计软件进行统计分析,计量资料采用x±s表示,组间比较采用t检验,P < 0.05为差异有统计学意义。
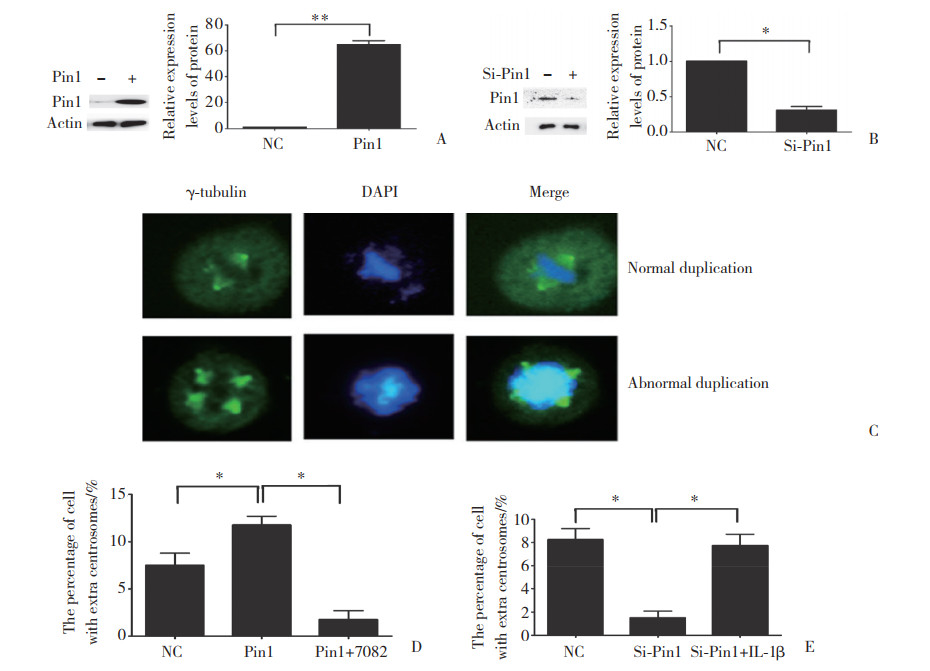
2 结果 2.1 Pin1经NF-κB/p65通路对细胞中心体异常扩增的影响在Hep-2细胞中分别转染pcDNA3.1-Pin1和siRNA来改变Pin1表达。结果显示,转染pcDNA3.1-Pin1能够使Pin1表达显著提高(图 1A),而转染siRNA能够有效降低Pin1表达(图 1B)。免疫荧光实验结果显示,中心体在Hep-2细胞中出现异常扩增(图 1C)。Pin1过表达中与NC组比较,Pin1组Hep-2细胞中心体异常扩增的细胞数目比例增加(P < 0.05),而BAY11-7082能够抑制Pin1过表达的上调作用(图 1D)。Pin1干扰中与NC组比较,Si-Pin1组中心体异常扩增的细胞比例显著降低(P < 0.05),IL-1β能够逆转此效应(图 1E)。提示Pin1能够通过NF-κB通路上调中心体异常扩增。
|
| A, Pin1 expression in Hep-2 cells transfected with pcDNA3.1-Pin1 after 48 h of culture; B, Pin1 expression in Hep-2 cells transfected with Pin1 siRNA after 48 h of culture; C, immunofluorescence showed abnormal centrosome amplification in Hep-2 cells (×400);D, Hep-2 cells transfected with pcDNA3.1 or pcDNA3.1-Pin1 and treated with BAY11-7082 or DMSO after 12 h, immunofluorescence showed abnormal centrosome amplification after 48 h of culture; E, Hep-2 cells transfected with Pin1 siRNA or a control and treated with IL-1β or BSA after 24 h, immunofluorescence showed abnormal centrosome amplification after 48 h of culture.*P < 0.05, **P < 0.01 vs NC or Pin1 or Si-Pin1 group. 图 1 Pin1经NF-κB/p65通路对细胞中心体异常扩增的影响 Fig.1 Effect of Pin1 on abnormal centrosome amplification via NF-κB/p65 pathway |
2.2 Pin1经NF-κB/p65对细胞增殖能力的影响
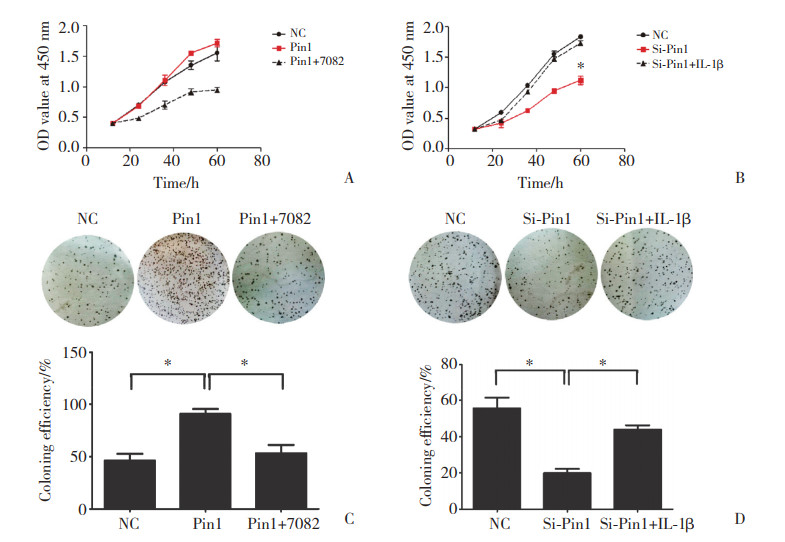
CCK-8实验检测细胞增殖能力结果显示,Hep-2细胞Pin1过表达中与NC组比较,Pin1组细胞增殖能力无统计学差异(P > 0.05);而BAY11-7082能够抑制细胞增殖能力(图 2A)。Pin1干扰中与NC组比较,Si-Pin1组细胞增殖能力显著减弱(P < 0.05),IL-1β能够逆转此效应(图 2B)。
|
| A, Hep-2 cells transfected with pcDNA3.1 or pcDNA3.1-Pin1 and treated with BAY11-7082 or DMSO after 12 h, the results of cell proliferation capacity was detected by CCK-8 assay; B, Hep-2 cells transfected with Pin1 siRNA or a control and treated with IL-1β or BSA after 24 h, the results of cell proliferation capacity was detected by CCK-8 assay; C, D, representative results of clone formation of Hep-2 cells. *P < 0.05 vs NC or Pin1 or Si-Pin1 group. 图 2 Pin1经NF-κB/p65通路对细胞增殖能力的影响 Fig.2 Effect of Pin1 on cell proliferation capacity via NF-κB/p65 pathway |
Hep-2细胞Pin1过表达中与NC组比较,Pin1组克隆形成数目显著增加,而BAY11-7082能够抑制Pin1过表达的上调作用(均P < 0.05,图 2C)。Hep-2细胞Pin1干扰中与NC组比较,Si-Pin1组克隆形成数目显著减少,IL-1β能够逆转这一效应(均P < 0.05,图 2D)。表明Pin1可通过NF-κB通路促进Hep-2细胞克隆形成。
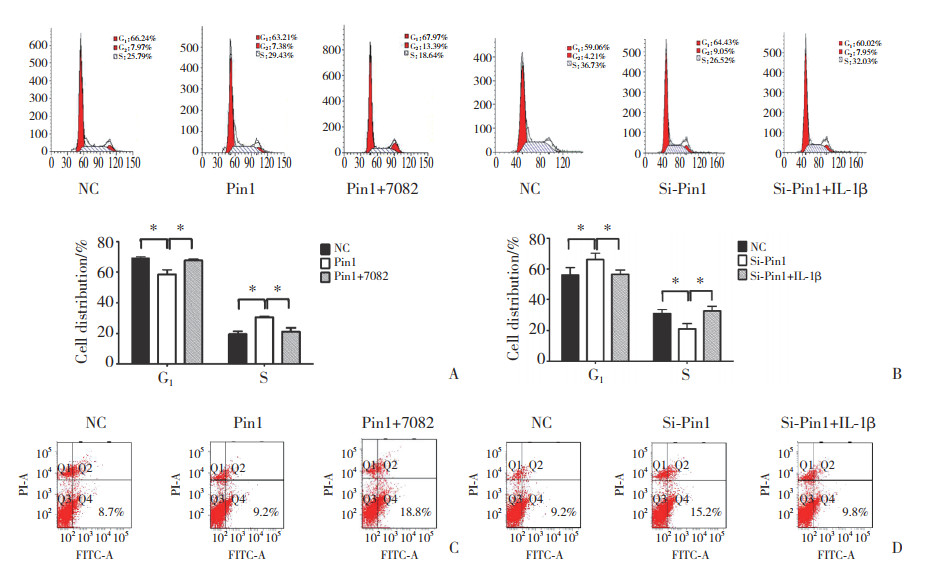
2.3 Pin1对细胞周期和凋亡的影响流式细胞仪检测细胞周期结果显示,Hep-2细胞Pin1过表达中与NC组比较,Pin1组G1期细胞减少,S期细胞增加,而BAY11-7082能够抑制Pin1过表达的调节作用(均P < 0.05,图 3A)。Pin1干扰中与NC组比较,Si-Pin1组G1期细胞增加,S期细胞减少,IL-1β能够逆转这一效应(均P < 0.05,图 3B)。提示Pin1能够通过NF-κB通路促进G1/S期的转化,而加入NF-κB/p65抑制可以消减G1/S期的转化作用,Pin1通过NF-κB通路对细胞周期产生影响。
|
| A, Hep-2 cells transfected with pcDNA3.1 or pcDNA3.1-Pin1 and treated with BAY11-7082 or DMSO, respectively, after 12 h, and cell cycle analysis of Hep-2 cells after 48 h transfection; B, Hep-2 cells transfected with Pin1 siRNA or a control and treated with IL-1β or BSA, respectively, after 24 h, and cell cycle analysis of Hep-2 cells cultured for 48 h after transfection; C, D, flow cytometric detection of cell apoptosis by using Annexin V FITC and propidium iodide staining. *P < 0.05 vs NC or Pin1 or Si-Pin1 group. 图 3 Pin1对细胞凋亡和周期的影响 Fig.3 Effect of Pin1 on cell cycle and apoptosis |
流式细胞仪检测Hep-2细胞凋亡结果显示,Hep-2细胞Pin1过表达中与NC组比较,Pin1组细胞凋亡无明显差异,而BAY11-7082使细胞凋亡增加(图 3C)。Hep-2细胞Pin1干扰中与NC组比较,Si-Pin1组细胞凋亡增加,IL-1β能够逆转这一效应(图 3D)。说明Pin1通过NF-κB/p65对细胞凋亡发挥作用。
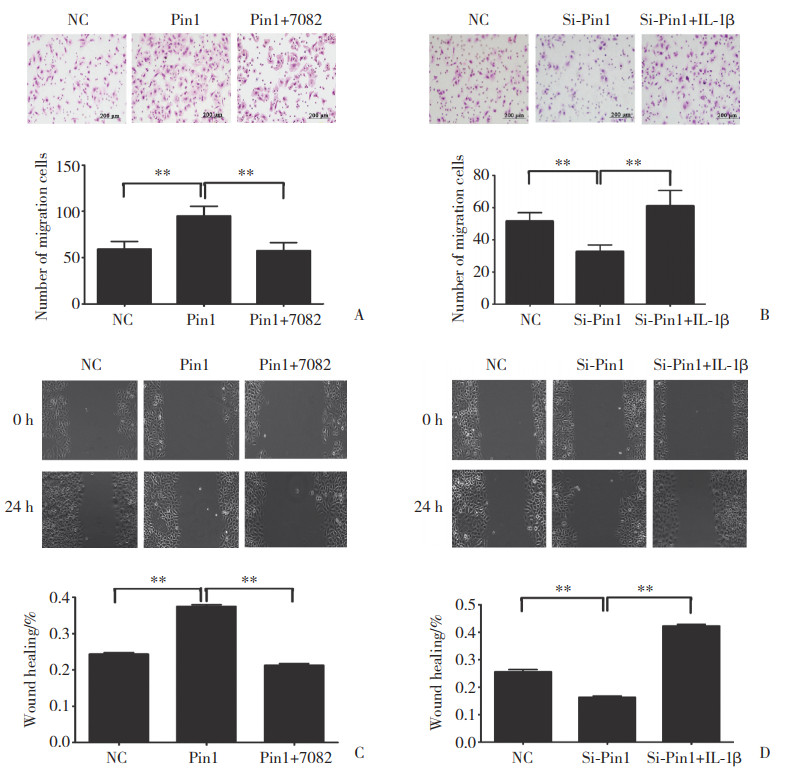
2.4 Pin1对细胞迁移的影响Transwell实验结果显示,Hep-2细胞Pin1过表达中与NC组比较,Pin1组穿过膜细胞数显著增加,而BAY11-7082能够抑制Pin1过表达的上调作用(均P < 0.01,图 4A)。Pin1干扰中与NC组比较,Si-Pin1组穿过膜细胞数减少,IL-1β能够逆转这一效应(均P < 0.01,图 4B)。
|
| A, migration ability determined by transwell chamber assay in Hep-2 cells after transfection with pcDNA3.1 or pcDNA3.1-Pin1 and treated with BAY11-7082 or DMSO, respectively, after 12 h (×100);B, migration ability determined by transwell chamber assay in Hep-2 cells after transfection with Pin1 siRNA or a control and treated with IL-1β or BSA, respectively, after 24 h (×100);C, D, migration ability determined by wound healing assay (×100). **P < 0.01 vs NC or Pin1 or Si-Pin1 group. 图 4 Pin1对细胞迁移的影响 Fig.4 Effect of Pin1 on cell migration |
划痕实验结果显示,Hep-2细胞Pin1过表达中与NC组比较,Pin1组细胞迁移距离显著增加,而BAY11-7082能够抑制Pin1过表达的上调作用(均P < 0.01,图 4C)。Pin1干扰中与NC组比较,Si-Pin1组迁移距离显著减少,IL-1β能够逆转这一效应(均P < 0.01,图 4D)。说明Pin1可通过NF-κB通路促进Hep-2细胞迁移。
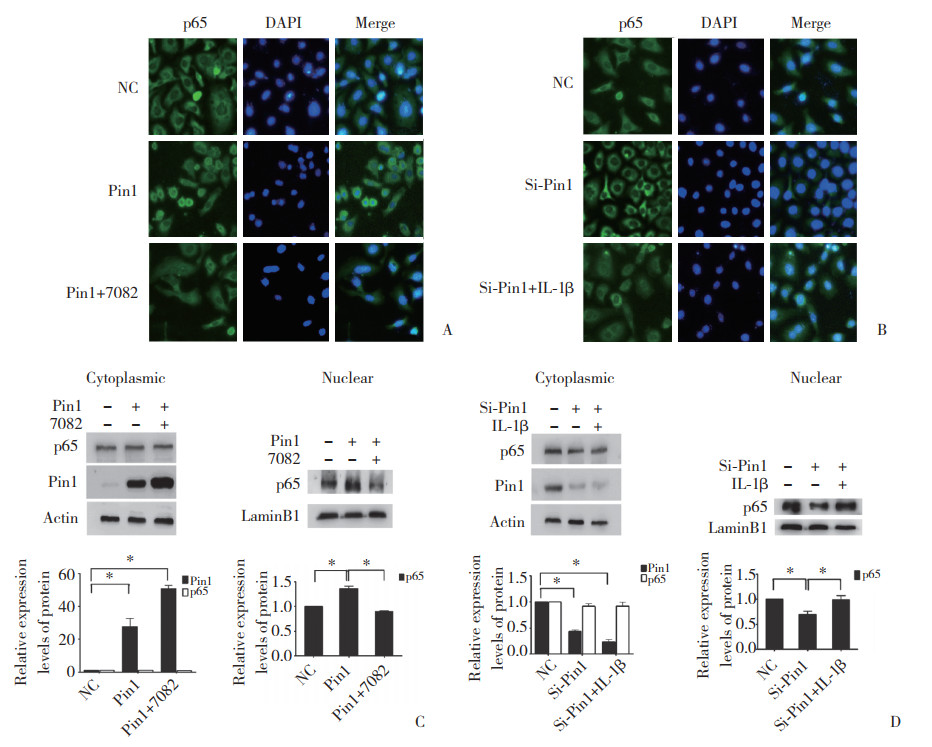
2.5 Pin1对NF-κB/p65核转位的影响免疫荧光结果显示,Hep-2细胞Pin1过表达中与NC组比较,Pin1组核中NF-κB/p65蛋白表达增加,而BAY11-7082能够抑制Pin1过表达的上调作用(图 5A);Pin1干扰中与NC组比较,Si-Pin1组核中NF-κB/p65蛋白表达减少;IL-1β能够逆转这一效应(图 5B)。
|
| A, Hep-2 cells transfected with pcDNA3.1 or pcDNA3.1-Pin1 and treated with BAY11-7082 or DMSO, respectively, after 12 h, and immunofluorescence detection of NF-κB/p65 protein expression in Hep-2 cells cultured for 48 h after transfection (×400);B, Hep-2 cells transfected with Pin1 siRNA or a control and treated with IL-1β or BSA, respectively, after 24 h, and immunofluorescence detection of NF-κB/p65 protein expression in Hep-2 cells cultured for 48 h after transfection (×400);C, D, NF-κB/p65 protein expression. *P < 0.05 vs NC or Pin1 or Si-Pin1 group. 图 5 Pin1对NF-κB/p65核转位的影响 Fig.5 Effect of Pin1 on nuclear translocation of NF-κB/p65 |
Western blotting检测结果显示,Hep-2细胞Pin1过表达中与NC组比较,Pin1组NF-κB/p65核内蛋白显著增多,而BAY11-7082能够抑制Pin1过表达的上调作用(均P < 0.05);而Pin1组、NC组及Pin1+7082组的细胞质中NF-κB/p65蛋白表达比较无统计学差异(均P > 0.05),见图 5C。Pin1干扰中与NC组比较,Si-Pin1组NF-κB/p65核内蛋白减少,IL-1β能够逆转这一效应(均P < 0.05,图 5D)。说明Pin1能够促进NF-κB/p65入核。
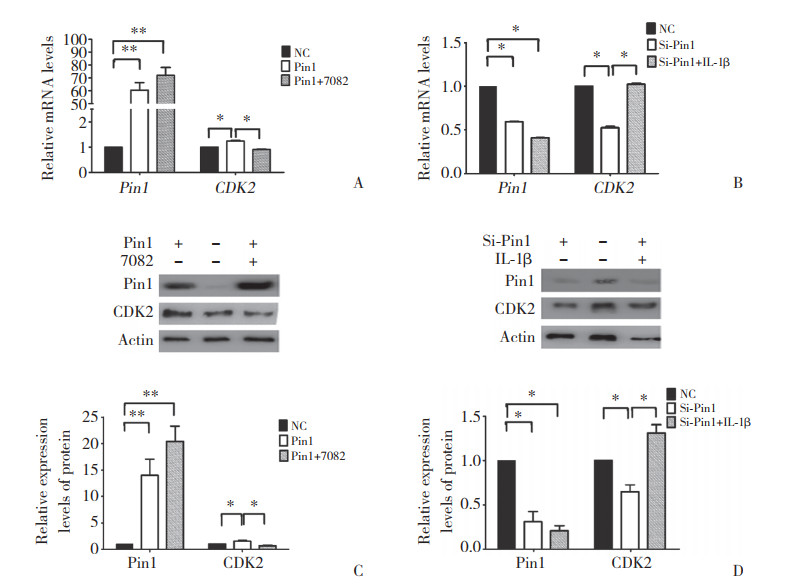
2.6 Pin1对CDK2表达的影响实时PCR检测结果显示,Hep-2细胞Pin1过表达中与NC组比较,Pin1组CDK2表达上调,而BAY11-7082能够抑制Pin1过表达的上调作用(均P < 0.05,图 6A)。Pin1干扰中与NC组比较,Si-Pin1组CDK2表达下调,IL-1β能够逆转这一效应(均P < 0.01,图 6B)。Western blotting蛋白检测结果与实时PCR检测结果一致,见图 6C、6D。提示Pin1促进NF-κB/p65核转位,上调CDK2的表达,可能通过NF-κB通路对CDK2表达产生影响。
|
| A, Hep-2 cells transfected with pcDNA3.1 or pcDNA3.1-Pin1 and treated with BAY11-7082 or DMSO, respectively, after 12 h, and Pin1 and CDK2 expression determined by RT-PCR in Hep-2 cells cultured for 48 h after transfection; B, Hep-2 cells transfected with Pin1 siRNA or a control and treated with IL-1β or BSA, respectively, after 24 h, and Pin1 and CDK2 expression determined by RT-PCR in Hep-2 cells cultured for 48 h after transfection; C, D, Pin1 and CDK2 protein expression. *P < 0.05, **P < 0.01 vs NC or Pin1 or Si-Pin1 group. 图 6 Pin1经NF-κB/p65通路对CDK2表达的影响 Fig.6 Effect of Pin1 on CDK2 protein expression via NF-κB/p65 pathway |
3 讨论
研究[9-10]表明,中心体功能障碍可能导致癌症,有些癌症是源于中心体功能障碍引起的染色体异常。中心粒分裂出现在G1期晚期,复制始于S期早期,随着中心体在G2期分裂,中心体复制完成,中心体分离延迟和加速都增加了中期纺锤体几何缺陷和有丝分裂错误。在cyclin B2过表达细胞中,中心体分离加速能导致中期异常纺锤体定位,形成双极牵引动粒和染色体滞后,而在cyclin B2过表达大鼠中G2期加速中心体分离是促进肿瘤的关键因素。
Pin1和NF-κB都参与细胞周期的调控,二者可能与中心体异常扩增相关。前期实验[11]发现在喉癌细胞系Hep-2细胞中过表达Pin1加剧了中心体异常扩增,本研究结果表明Pin1可以通过NF-κB/p65通路作用于Hep-2细胞而影响其生物学行为。NF-κB能够被多种基因磷酸化,从而调节NF-κB通路的活性[12]。NF-κB p65/p50二聚体和IκBα关联,在调控p65核转位以及基因转录中发挥至关重要的作用[13]。Pin1特异性结合p65的pThr254-Pro序列并且抑制了p65和IκBα的结合,导致p65在细胞核积累以及p65蛋白稳定增加[14]。此外,Pin1可以和Tax结合,调节Tax介导的NF-κB激活[15]。本研究证实了Pin1在Hep-2细胞中可以促进NF-κB/p65核转位,与以往研究结果一致。另一方面,NF-κB受反馈抑制机制调控,通过NF-κB激活补充稀少的IκB蛋白。IκB可直接作用于NF-κB,新合成IκB(特别是IκBa)进入细胞核结合到NF-κB二聚体上,并且将NF-κB运回细胞质中失活[16]。本研究结果显示在Hep-2细胞Pin1过表达中与NC组比较,Pin1过表达后细胞增殖及凋亡都无明显变化,可能是Pin1过表达使得NF-κB激活,随后通过上述的IκB反馈机制抑制了NF-κB的活性。然而具体的调控机制有待进一步研究。
研究[17-19]显示NF-κB信号传导通路通过CDK2来调控细胞周期。而且CDK2在细胞分化和有丝分裂中起促进作用。CDK2活性增强可促进细胞分裂、增殖和分化。Cyclin E/CDK2是促进G1/S进程的关键激酶复合物。CDK2表达正常时,Cyclin E/CDK2复合物表达水平保持不变并调控细胞周期进程正常进行,但CDK2表达异常时可影响多种细胞生物学行为,包括干扰细胞周期进程、促进细胞增殖和分化等,最终导致癌症的发生[20-23]。本研究结果显示Pin1过表达刺激细胞CDK2表达上调,而NF-κB/p65抑制剂可消除此上调作用。
综上所述,在Hep-2细胞中,Pin1促进NF-κB/p65核转位,上调CDK2的表达。Pin1可能是通过NF-κB通路调节CDK2表达,从而影响肿瘤细胞的中心体异常扩增、克隆形成、细胞迁移、细胞增殖等生物学行为。本研究为揭示喉癌的发生发展机制提供了理论基础。
| [1] |
YILMAZ M, KARATAS OF, YUCETURK B, et al. Alpha-B-crystallin expression in human laryngeal squamous cell carcinoma tissues[J]. Head Neck, 2015, 37(9): 1344-1348. DOI:10.1002/hed.23746 |
| [2] |
PYO JS, SON BK, OH IH. Cytoplasmic Pin1 expression is correlated with poor prognosis in colorectal cancer[J]. Pathol Res Pract, 2018, 214(11): 1848-1853. DOI:10.1016/j.prp.2018.09.018 |
| [3] |
CHEN L, XU X, WEN X, et al. Targeting Pin1 exerts potent antitumor activity in pancreatic ductal carcinoma via inhibiting tumor metastasis[J]. Cancer Sci, 2019, 110(8): 2442-2455. DOI:10.1111/cas.14085 |
| [4] |
LIOU YC, ZHOU XZ, LU KP. Prolyl isomerase Pin1 as a molecular switch to determine the fate of phosphoproteins[J]. Trends Biochem Sci, 2011, 36(10): 501-514. DOI:10.1016/j.tibs.2011.07.001 |
| [5] |
SUIZU F, RYO A, WULF G, et al. Pin1 regulates centrosome duplication, and its overexpression induces centrosome amplification, chromosome instability, and oncogenesis[J]. Mol Cell Biol, 2006, 26(4): 1463-1479. DOI:10.1128/mcb.26.4.1463-1479.2006 |
| [6] |
XIAO G, FU J. NF-κB and cancer: a paradigm of Yin-Yang[J]. Am J Cancer Res, 2011, 1(2): 192-221. |
| [7] |
SHINODA K, KUBOKI S, SHIMIZU H, et al. Pin1 facilitates NF-kappa B activation and promotes tumour progression in human hepatocellular carcinoma[J]. Br J Cancer, 2015, 113(9): 1323-1331. DOI:10.1038/bjc.2015.272 |
| [8] |
LIU JL, MA HP, LU XL, et al. NF-kappa B induces abnormal centrosome amplification by upregulation of CDK2 in laryngeal squamous cell cancer[J]. Int J Oncol, 2011, 39(4): 915-924. DOI:10.3892/ijo.2011.1125 |
| [9] |
NAM HJ, VAN DEURSEN JM. Cyclin B2 and p53 control proper timing of centrosome separation[J]. Nat Cell Biol, 2014, 16(6): 538-549. DOI:10.1038/ncb2952 |
| [10] |
SILKWORTH WT, NARDI IK, PAUL R, et al. Timing of centrosome separation is important for accurate chromosome segregation[J]. Mol Biol Cell, 2012, 23(3): 401-411. DOI:10.1091/mbc.e11-02-0095 |
| [11] |
温行, 李章富, 王辉, 等. miR-200c调控肽基脯氨酰顺反异构酶对喉癌Hep-2细胞生物学行为的影响[J]. 中国医科大学学报, 2019, 48(1): 23-28. DOI:10.12007/j.issn.0258-4646.2019.01.004 |
| [12] |
ZHANG L, SHAO L, CREIGHTON CJ, et al. Function of phosphorylation of NF-kB p65 ser536 in prostate cancer oncogenesis[J]. Oncotarget, 2015, 6(8): 6281-6294. DOI:10.18632/oncotarget.3366 |
| [13] |
REBER L, VERMEULEN L, HAEGEMAN G, et al. Ser276 phosphorylation of NF-κB p65 by MSK1 controls SCF expression in inflammation[J]. PLoS One, 2009, 4(2): e4393. DOI:10.1371/journal.pone.0004393 |
| [14] |
CARL YS, THERESA JB, PARITOSH G, et al. Phosphorylation of RelA/p65 on serine 536 defines an IκBα-independent NF-κB pathway[J]. J Biol Chem, 2005, 280(41): 34538-34574. DOI:10.1074/jbc.M504943200 |
| [15] |
PELOPONESE JM, YASUNAGA J, KINJO T, et al. Peptidylproline cis-trans-isomerase Pin1 interacts with human T-cell leukemia virus type 1 tax and modulates its activation of NF-kappa B[J]. J Virol, 2009, 83(7): 3238-3248. DOI:10.1128/jvi.01824-08 |
| [16] |
SUN SC, GANCHI PA, BALLARD DW, et al. NF-kappa B controls expression of inhibitor I kappa B alpha: evidence for an inducible autoregulatory pathway[J]. Science, 1993, 259(5103): 1912-1915. DOI:10.1126/science.8096091 |
| [17] |
HUO YN, YEH SD, LEE WS. Androgen receptor activation reduces the endothelial cell proliferation through activating the cSrc/AKT/p38/ERK/NFκB-mediated pathway[J]. J Steroid Biochem Mol Biol, 2019, 194: 105459. DOI:10.1016/j.jsbmb.2019.105459 |
| [18] |
ZHOU Y, XU H, YE D, et al. AMPKα1 deletion in fibroblasts promotes tumorigenesis in athymic nude mice by p52-mediated elevation of erythropoietin and CDK2[J]. Oncotarget, 2016, 7(33): 53654-53667. DOI:10.18632/oncotarget.10687 |
| [19] |
CHUANG TD, REHAN A, KHORRAM O. Tranilast induces miR-200c expression through blockade of RelA/p65 activity in leiomyoma smooth muscle cells[J]. Fertil Steril, 2020, 113(6): 1308-1318. DOI:10.1016/j.fertnstert.2019.12.002 |
| [20] |
Ehedego H, Mohs A, JANSEN B, et al. Loss of Cyclin E1 attenuates hepatitis and hepatocarcinogenesis in a mouse model of chronic liver injury[J]. Oncogene, 2018, 37(25): 3329-3339. DOI:10.1038/s41388-018-0181-8 |
| [21] |
JIN X, GE LP, LI DQ, et al. LncRNA TROJAN promotes proliferation and resistance to CDK4/6 inhibitor via CDK2 transcriptional activation in ER+ breast cancer[J]. Mol Cancer, 2020, 19(1): 87. DOI:10.1186/s12943-020-01210-9 |
| [22] |
NIE L, WEI Y, ZHANG F, et al. CDK2-mediated site-specific phosphorylation of EZH2 drives and maintains triple-negative breast cancer[J]. Nat Commun, 2019, 10(1): 5114. DOI:10.1038/s41467-019-13105-5 |
| [23] |
KUMARI S, KUMAR P, KUMAR M, et al. Expression of p27 and p16 and their clinical significance in gastric cancer[J]. Clin Transl Oncol, 2021, 23(4): 856-865. DOI:10.1007/s12094-020-02479-4 |
 2021, Vol. 50
2021, Vol. 50




