文章信息
- 刘会缔, 李彦科, 苗鹏, 邢承忠
- LIU Huidi, LI Yanke, MIAO Peng, XING Chengzhong
- circZEB1通过竞争性结合hsa-miR-656调控胃癌细胞的增殖和凋亡
- circZEB1 regulates the proliferation and apoptosis of gastric cancer cells by sponging hsa-miR-656
- 中国医科大学学报, 2021, 50(6): 516-520, 525
- Journal of China Medical University, 2021, 50(6): 516-520, 525
-
文章历史
- 收稿日期:2020-11-11
- 网络出版时间:2021-05-26 15:53
胃癌是世界范围内第五大常见肿瘤,在癌症相关死亡中排第3位[1]。2015年中国癌症统计数据显示,中国平均每年新增胃癌患者679 000例,因胃癌死亡人数达498 000例,仅次于肺癌[2]。因此,探寻胃癌发生、发展的分子机制及有效的治疗靶点对改善胃癌患者的预后极为迫切。20世纪90年代,人们发现一类新型具有共价闭合环状结构并且无多聚腺苷酸尾结构的非编码RNA,将其命名为环状RNA(circular RNA,circRNA)[3]。研究[4]发现,circRNA的共价闭合环状结构能够耐RNA外切酶和RNAse酶降解,因此与线性mRNA相比,circRNA具有更高的稳定性。此外,越来越多的证据表明circRNA参与癌症的发生、发展过程,并可能成为癌症的新型生物标志物和潜在的治疗靶点。如circPVT1能够通过竞争性结合miR-199a-5p抑制胶质瘤的增殖和转移,有望成为胶质瘤潜在的治疗靶点[5];hsa_circ_0000518通过miR-326/FGFR1轴调控乳腺癌的发展进程,进而成为乳腺癌治疗靶标[6];在肝癌中敲除circHIPK3,能够通过靶向miR-582-3p/DLX2抑制肝癌的致瘤性[7]。本研究鉴定了一个全新的circRNA——hsa-circ_0018084(circZEB1),发现其在多种胃癌细胞系中高表达,并检测circZEB1在多种胃癌细胞和胃黏膜上皮细胞中的表达情况,探查其在胃癌细胞中的定位,并深入探索其在胃癌发展进程中的生物学功能,为胃癌的临床治疗提供了一个新的治疗靶点。
1 材料与方法 1.1 主要试剂和仪器胃癌细胞系HGC-27、SGC-7901、AGS、MGC-823、MKN-45和正常上皮细胞系GES-1购自中国科学院上海生命科学院细胞库;RPMI 1640培养基、胰酶和PBS购自中国Hyclone公司;胎牛血清、青霉素和链霉素混合液购自美国Gibco公司;RNA提取试剂TRIzol和Lipofectamine 2000转染试剂购自日本Invitrogen公司;RNA反转录试剂盒和实时荧光定量PCR试剂盒购自日本TaKaRa公司;CCK-8试剂盒购自日本Dojindo公司。
实时PCR仪(LightCyclerR480Ⅱ)购自瑞士Roche公司);酶标仪(Model 680)购自美国Bio-Rad;流式细胞仪(FACS calibur)购自美国BD Bioscience。
1.2 细胞培养所有细胞均使用含10%胎牛血清的RPMI 1640培养基,在5% CO2、37 ℃、饱和湿度的恒温培养箱内孵育。每2 d更换1次完全培养基,取处于对数生长期的细胞用于后续实验。
1.3 CCK-8增殖实验在MGC-803和HGC-27细胞系中转染si-circZEB1以及阴性对照siRNA,48 h后用1 mL含10%胎牛血清的培养基消化并计数细胞,配制含有8×104个细胞、4 mL的细胞悬液,充分颠倒混匀后,在si-circZEB1组和阴性对照组分别取100 μL细胞悬液接种于96孔板,置于37 ℃、湿度95%、含有5%CO2的孵箱中培养。分别于0、24、48、72和96 h加入10 μL CCK-8试剂,于孵箱中继续培养1 h后利用酶标仪测定si-circZEB1组和阴性对照组450 nm处的光密度值,计算细胞增殖率。
1.4 细胞周期检测在MGC-803和HGC-27细胞系中转染si-circZEB1和阴性对照siRNA,根据细胞周期检测试剂盒说明书进行操作,收集并调整处理后的细胞浓度为1×106/mL,取1 mL细胞悬液,PBS洗涤细胞1次,离心去除上清,在细胞中加入体积分数为70%的冷乙醇500 μL固定过夜,计算所需染色工作液体积,每个样本用500 μL工作液孵育,将RnaseA和碘化丙啶按1:9比例配制成染色工作液。室温避光孵育30~60 min,上机检测。比较si-circZEB1组和阴性对照组处于各个周期的细胞丰度。
1.5 细胞凋亡检测在MGC-803和HGC-27细胞系中转染si-circZEB1和阴性对照siRNA,根据细胞凋亡检测试剂盒说明书,用不含EDTA胰酶消化收集待处理细胞,PBS洗涤细胞2次,收集5×106个细胞。在50 μL的结合缓冲液中加入5 μL 7-AAD染液,混匀。在上述收集的细胞中加入7-AAD染液,混匀;室温避光5~15 min。反应后再加入450 μL结合缓冲液混匀。加入1 μL Annexin V-PE混匀,室温、避光反应5~15 min,在1 h内应用流式细胞仪观察和检测。
1.6 RNA提取及反转录分别检测胃癌细胞系HGC-27、SGC-7901、AGS、MGC-823、MKN-45和正常上皮细胞系GES-1中circZEB1的内源性表达含量。检测转染si-circZEB1后的转染效率。取出待处理细胞,利用TRIzol法提取待处理细胞RNA,根据反转录试剂盒说明书配制反应体系,最终合成cDNA于-20 ℃保存。
1.7 实时荧光定量PCR应用TRIzol试剂盒提取待处理细胞总RNA,使用反转录试剂盒将RNA反转录为cDNA后,设置反应条件为95 ℃ 5 min;95 ℃ 30 s;60 ℃ 30 s,共45个循环。以β-actin作为内参,以2-ΔΔCt值表示目的基因的相对表达量。引物序列:β-actin,正向5’-GAGGCGTACAGGGATAGCAC-3’,反向5’-GTCACCAACTGGGACGACAT-3’;circZEB1,正向5’-TCCTGCACCAAGAAAGATCTGC-3’,反向5’-TACAAAACCTCGCGTTTCGC-3’;ZEB1,正向5’-AGCGAGGTAAAGTTGCGTCT-3’,反向5’-AGGTTTTCTGGGCCATACCG-3’。
1.8 细胞核质分离纯化实验在胃癌细胞系MGC-803中检测内源性circZEB1的核质表达丰度。根据细胞核质分离纯化试剂盒说明书,利用1 mL PBS吹刮下细胞并收集到1.5 mL去酶离心管中,4 ℃、600 g离心5 min收集细胞。加入300 μL细胞核质分离反冲液,吹匀悬液,冰上放置5 min,1 200 g离心5 min,取上清于新管中,4 ℃、500 g离心5 min去除杂质,获得纯化细胞质。沉淀部分加入300 μL冲洗液,4 ℃、1 200 g离心5 min,取上清,重复一遍,加入300 μL细胞核质分离反冲液重悬细胞核,获得纯化细胞核,接下来利用Trizol法提取细胞核质分离纯化的RNA。
1.9 统计学分析采用SPSS 21.0软件对数据进行统计分析。所有实验均独立重复3次以上。数据以x±s表示。2组比较采用独立样本t检验;多组比较采用方差分析,组内两两比较采用LSD-t检验。P < 0.05为差异有统计学意义。
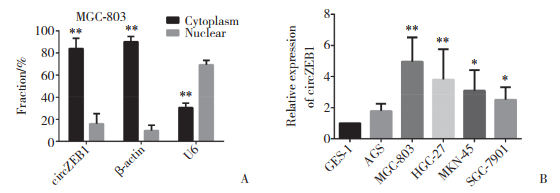
2 结果 2.1 circZEB1的特征circZEB1共有66 132个碱基,由位于10号染色体上的ZEB1基因的内含子反向剪接而成,故将其命名为circZEB1。在MGC-803细胞系中利用细胞核质分离实验检测circZEB1在细胞中的定位情况,发现circZEB1主要表达在细胞质中(图 1A)。在HGC-27、AGS、BGC-823、SGC-7901、MKN-45以及GES-1细胞系中检测circZEB1的表达水平,发现其在胃癌细胞系中显著高表达(图 1B)。
|
| A, nucleocytoplasmic separation assay demonstrating that circZEB1 is mainly expressed in the cytoplasm; B, circZEB1 is highly expressed in various gastric cancer cell lines. * P < 0.05; ** P < 0.01. 图 1 circZEB1在胃癌细胞系中的表达和定位 Fig.1 Expression and localization of circZEB1 in gastric cancer cells |
2.2 沉默circZEB1抑制胃癌细胞增殖
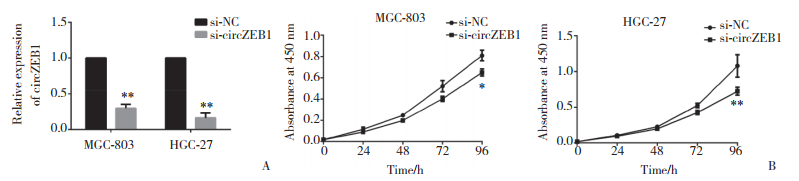
在MGC-803和HGC-27细胞系中转入si-circZEB1,并利用实时PCR检测转染效率,结果显示,2种细胞系均能够显著沉默circZEB1的表达(图 2A)。进一步利用CCK-8实验检测circZEB1对胃癌细胞增殖能力的影响,结果显示,与对照组相比,敲除circZEB1后能够显著抑制胃癌细胞的增殖能力(图 2B)。
|
| A, transfection of gastric cancer cells with si-circZEB1 significantly inhibits circZEB1 expression as determined by real-time PCR; B, silencing circZEB1 expression significantly inhibits the proliferation of gastric cancer cells as shown by CCK-8 assay. * P < 0.05; ** P < 0.01. 图 2 敲除circZEB1抑制胃癌细胞增殖 Fig.2 circZEB1 knockout inhibits the proliferation of gastric cancer cells |
2.3 沉默circZEB1促进胃癌细胞凋亡并诱导细胞周期阻滞
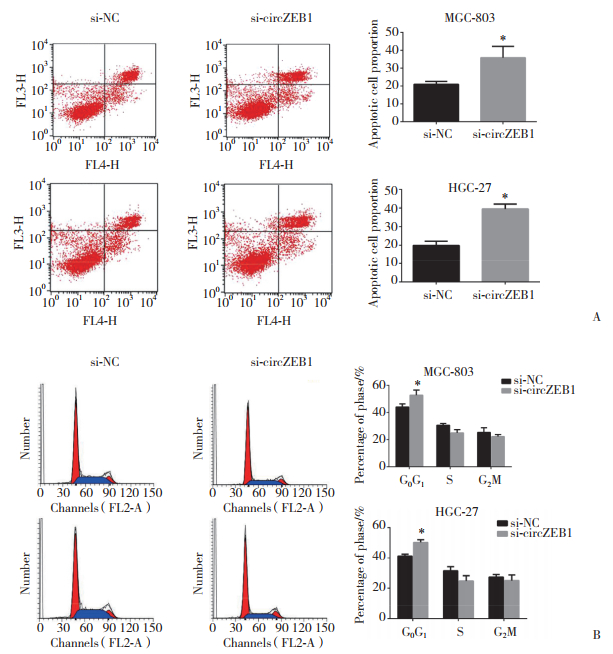
鉴于沉默circZEB1能够抑制胃癌细胞的增殖能力,进一步在MGC-803和HGC-27细胞系中检测circZEB1对胃癌细胞凋亡和细胞周期分布的影响。流式细胞术结果显示,沉默circZEB1能够促进胃癌细胞凋亡并诱导细胞周期阻滞于G0/G1期(图 3)。这在一定程度上解释了敲除circZEB1对胃癌细胞增殖能力的抑制作用。
|
| A, silencing circZEB1 promotes apoptosis in gastric cancer cells; B, circZEB1 knockdown induces cycle arrest in G0/G1 phase in gastric cancer cells. * P < 0.05. 图 3 敲减circZEB1促进胃癌细胞凋亡并诱导细胞周期阻滞 Fig.3 circZEB1 knockdown promotes apoptosis and induces cell cycle arrest in gastric cancer cells |
2.4 circZEB1通过竞争性结合hsa-miR-656调控胃癌细胞增殖和凋亡
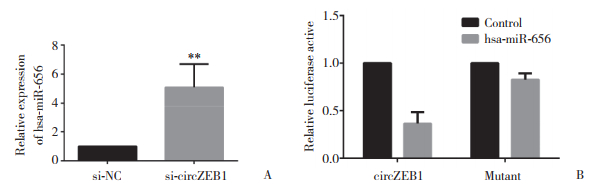
通过circRNA靶miRNA预测网站Circular RNA Interactome(https://circinteractome.irp.nia.nih.gov)发现,circZEB1可能竞争性结合hsa-miR-656。实时PCR进一步发现,沉默circZEB1后hsa-miR-656的表达显著上调(图 4A)。进一步在胃癌MGC-803细胞系中利用荧光素酶基因报告实验验证circZEB1和hsa-miR-656的直接靶向关系(图 4B)。由此提出假设,circZEB1可能通过竞争性结合hsa-miR-656调控胃癌细胞的增殖和凋亡能力。
|
| A, silencing circZEB1 results in upregulation of hsa-miR-656 as revealed by real-time quantitative PCR; B, luciferase reporter assay shows that circZEB1 directly binds to hsa-miR-656. ** P < 0.01. 图 4 实时定量PCR和荧光素酶实验证实circZEB1和hsa_miR-656具有直接靶向关系 Fig.4 Real-time quantitative PCR and luciferase reporter assay confirm the direct physical interaction between circZEB1 and hsamiR-656 |
3 讨论
迄今为止,胃癌在世界范围内的发病率和病死率仍高居不下,尤以我国为重。虽然近年来人们探索胃癌治疗方案的脚步从未停止,但治疗效果始终不甚显著,胃癌患者的5年生存率仍低于30%[8]。因此,进一步深入探索胃癌的发生和发展机制以及寻找新的胃癌预测分子标志物意义重大。circRNA是近年新发现的一类具有共价闭合环状结构的RNA。与传统线性mRNA相比,circRNA没有5’末端帽子和3’末端poly尾巴结构,其独有的共价闭合环状结构使其具有更强的抗消化作用和更高的稳定性。因此,circRNA被认为具有更高的研究潜能。
目前,人们发现circRNA能够参与多种肿瘤的发展进程。如circFNDC3B能够在结直肠癌中竞争性结合miR-937-5p,调控TIMP3的表达,从而抑制结直肠癌的发展进程[9];circ0000144能够通过miR-217/AKT3信号通路,促进甲状腺癌的进展[10];胰腺癌中,hsa_circ_001587能够通过海绵miR-223上调SLC4A4的表达,从而抑制胰腺癌细胞的迁移、侵袭和血管生成,成为胰腺癌治疗的潜在靶点[11];circ0079593在黑色素瘤中高表达,并能够通过miR-516b/GRM3轴促进黑色素瘤的增殖、转移和糖代谢并抑制其凋亡[12]。
本研究鉴定了一个全新的circRNA——circZEB1。hsa_circ-0018084是由位于10号染色体上的ZEB1基因内含子首尾剪接而成,其成熟序列共有66 132个碱基。利用细胞核质分离实验检测其在细胞内的定位情况,发现其主要表达在细胞质中,这暗示其更有可能通过竞争性结合miRNA发挥作用。此外,本研究在多种胃癌细胞系和胃生理上皮细胞系中检测了circZEB1的表达情况,结果表明,与生理细胞系相比,其在胃癌细胞系中表达显著上调,提示circZEB1在胃癌的发展进程中更有可能发挥促癌作用。因此,本研究接下来检测了其对胃癌细胞生物学功能的影响。在MGC-803和HGC-27细胞系中敲除circZEB1后,与对照组相比,敲除circZEB1能显著抑制胃癌细胞的增殖;流式细胞术结果也显示,敲除circZEB1能够促进胃癌细胞的凋亡;并且细胞周期结果表明,沉默circZEB1能够将胃癌细胞周期阻滞于G0/G1,这在一定程度上也解释了circZEB1对胃癌细胞增殖能力的作用。鉴于circZEB1主要表达在细胞质,由此推测该circRNA更有可能通过海绵miRNA发挥功能。利用Circular RNA Interactome在线预测网站,本研究发现circZEB1最有可能竞争性结合hsa-miR-656,进一步利用实时PCR检测,发现敲除circZEB1后hsa-miR-656表达显著上调,并且荧光素酶报告基因实验证实了circZEB1与hsa-miR-656的直接靶向关系。由此做出假设,circZEB1可能通过竞争性结合hsa-miR-656,进而调控胃癌细胞的增殖和凋亡。
综上所述,circZEB1主要表达在胃癌细胞胞质中,在胃癌细胞系中显著上调,并通过竞争性结合hsa-miR-656调控胃癌细胞的增殖、凋亡和周期分布,影响胃癌发展进程。因此,circZEB1有望成为胃癌治疗的潜在治疗靶点。
| [1] |
CHEN W, ZHENG R, BAADE PD, et al. Cancer statistics in China, 2015[J]. CA Cancer J Clin, 2016, 66(2): 115-132. DOI:10.3322/caac.21338 |
| [2] |
SUGANO K. Screening of gastric cancer in Asia[J]. Best Pract Res Clin Gastroenterol, 2015, 29(6): 895-905. DOI:10.1016/j.bpg.2015.09.013 |
| [3] |
BACH DH, LEE SK, SOOD AK. Circular RNAs in cancer[J]. Mol Ther Nucleic Acids, 2019, 16: 118-129. DOI:10.1016/j.omtn.2019.02.005 |
| [4] |
KRISTENSEN LS, ANDERSEN MS, STAGSTED LVW, et al. The biogenesis, biology and characterization of circular RNAs[J]. Nat Rev Genet, 2019, 20(11): 675-691. DOI:10.1038/s41576-019-0158-7 |
| [5] |
CHI G, YANG F, XU D, et al. Silencing hsa_circ_PVT1(circPVT1) suppresses the growth and metastasis of glioblastoma multiforme cells by up-regulation of miR-199a-5p[J]. Artif Cells Nanomed Biotechnol, 2020, 48(1): 188-196. DOI:10.1080/21691401.2019.1699825 |
| [6] |
JIANG J, LIN H, SHI S, et al. Hsa_circRNA_0000518 facilitates breast cancer development via regulation of the miR-326/FGFR1 axis[J]. Thorac Cancer, 2020, 11(11): 3181-3192. DOI:10.1111/1759-7714.13641 |
| [7] |
ZHANG H, DAI Q, ZHENG L, et al. Knockdown of circ_HIPK3 inhibits tumorigenesis of hepatocellular carcinoma via the miR-582-3p/DLX2 axis[J]. Biochem Biophys Res Commun, 2020, 533(3): 501-509. DOI:10.1016/j.bbrc.2020.09.050 |
| [8] |
ALLEMANI C, WEIR HK, CARREIRA H, et al. Global surveillance of cancer survival 1995-2009:analysis of individual data for 25, 676, 887 patients from 279 population-based registries in 67 countries (CONCORD-2)[J]. Lancet, 2015, 385(9972): 977-1010. DOI:10.1016/S0140-6736(14)62038-9 |
| [9] |
ZENG W, LIU Y, LI WT, et al. CircFNDC3B sequestrates miR-937-5p to derepress TIMP3 and inhibit colorectal cancer progression[J]. Mol Oncol, 2020, 14(11): 2960-2984. DOI:10.1002/1878-0261.12796 |
| [10] |
FAN YX, SHI HY, HU YL, et al. Circ_0000144 facilitates the progression of thyroid cancer via the miR-217/AKT3 pathway[J]. J Gene Med, 2020, 22(12): e3269. DOI:10.1002/jgm.3269 |
| [11] |
ZHANG XT, TAN P, ZHUANG Y, et al. hsa_circRNA_001587 upregulates SLC4A4 expression to inhibit migration, invasion, and angiogenesis of pancreatic cancer cells via binding to microRNA-223[J]. Am J Physiol Gastrointest Liver Physiol, 2020, 319(6): G703-G717. DOI:10.1152/ajpgi.00118.2020 |
| [12] |
LU JJ, LI Y. Circ_0079593 facilitates proliferation, metastasis, glucose metabolism and inhibits apoptosis in melanoma by regulating the miR-516b/GRM3 axis[J]. Mol Cell Biochem, 2020, 475(1/2): 227-237. DOI:10.1007/s11010-020-03875-8 |
 2021, Vol. 50
2021, Vol. 50




