文章信息
- 高媛, 周妍, 周新佳, 郑锐
- GAO Yuan, ZHOU Yan, ZHOU Xinjia, ZHENG Rui
- 白细胞介素-9及其受体在非小细胞肺癌组织中的表达及临床意义
- Expression and clinical significance of IL-9 and IL-9 receptors in non-small cell lung cancer
- 中国医科大学学报, 2021, 50(6): 511-515
- Journal of China Medical University, 2021, 50(6): 511-515
-
文章历史
- 收稿日期:2020-07-24
- 网络出版时间:2021-05-27 8:56
2. 中国医科大学附属盛京医院耳鼻咽喉科, 沈阳 110004
2. Department of Otolaryngology, Shengjing Hospital of China Medical University, Shenyang 110004, China
肺癌是全世界最主要的癌症死亡原因之一[1]。肺癌根据组织学分为非小细胞肺癌(non-small cell lung cancer,NSCLC)和小细胞肺癌,肺癌患者中NSCLC约占85%[2]。研究[3]发现,有2/3的NSCLC患者在诊断时已处于Ⅲ/Ⅳ期,并且超过50%的患者在诊断时已经出现转移,转移性晚期NSCLC患者5年生存率低于5%,提高晚期NSCLC患者的生存率需要更多新的治疗策略[4]。免疫微环境在控制肺癌发生、发展和转移中起着至关重要的作用[5]。近年来白细胞介素-9(interleukin-9,IL-9)在肿瘤免疫中的作用得到了越来越多的关注。研究[6]发现在肺癌恶性胸腔积液中辅助性T细胞9(helper T cell 9,Th9)及其分泌的细胞因子IL-9可促进肺癌细胞增殖及迁移,同时促进肺癌细胞与胸膜间皮细胞间黏附,进而促进肺癌恶性胸腔积液进展[6]。但是也有研究[7]发现在不同的肿瘤微环境中IL-9及Th9细胞具有复杂的抗肿瘤及促肿瘤的双重作用。在黑色素瘤中Th9及IL-9促进CD8+T细胞介导的细胞毒性,进而发挥抗肿瘤作用[8]。IL-9通过刺激抗肿瘤M1巨噬细胞抑制黑素瘤的肺转移[9]。
目前,癌症中IL-9促肿瘤和抗肿瘤的作用仍然存在争议。对于IL-9、白细胞介素-9受体(interleukin-9 receptor,IL-9R)表达与NSCLC的临床及病理特征关系的研究鲜有报道。本研究探讨NSCLC组织中IL-9、IL-9R表达水平及其与临床病理特征之间的关系,旨在为NSCLC免疫治疗提供新的治疗思路。
1 材料与方法 1.1 材料收集110例2017年1月至2018年12月中国医科大学附属盛京医院胸外科手术切除并经过病理确诊的NSCLC的癌组织及其癌旁正常肺组织(距肿瘤边缘5 cm以上)石蜡包埋标本。收集其中19例新鲜NSCLC癌组织及其周围正常肺组织,新鲜组织在液氮中保存。110例患者中男80例,女30例;平均年龄(58.9±7.9)岁,其中年龄 < 50岁28例,≥50岁82例;病理分级(分化程度)中高分化80例,低分化30例;肿瘤直径 < 3 cm 42例,肿瘤直径≥3 cm 68例;明确淋巴结转移(N1、N2和N3)54例,无淋巴结转移(N0)56例。根据TNM分期[10]分为:Ⅰ期36例,Ⅱ期28例,Ⅲ期44例,Ⅳ期2例。
1.2 免疫组织化学染色及结果判读石蜡切片进行脱蜡,抗原修复;3%H2O2室温孵育15 min,洗片,5%BSA50 µL滴入进行封闭。在室温下孵育10 min;滴加IL-9(ab203386;1∶200;英国Abcam公司)、IL-9R一抗(ab233757;1∶200;英国Abcam公司)4 ℃孵育过夜。然后加入二抗室温60 min静置,PBS洗片3次;DAB显色5 min,苏木精复染,脱水、透明、封片观察。
染色结果由2位病理科医生综合判定。随机观察10个视野(×200),计数视野内细胞总数及染色阳性细胞数,染色阳性细胞百分比评分:0分,着色细胞≤5%(阴性);1分,着色细胞 > 5%~25%;2分,着色细胞 > 25%~50%;3分,着色细胞 > 50%~75%;4分,着色细胞 > 75%。染色程度评分:0分,基本未染色;1分,弱染色(呈淡黄色);2分,中等强度染色(呈棕黄色);3分,强染色(呈棕褐色)。将染色阳性细胞百分比评分与染色程度评分相加,≥4分为阳性,< 4分为阴性。
1.3 Western blotting检测NSCLC癌组织及癌旁正常组织中IL-9蛋白表达使用RIPA和1%PMSF提取总蛋白,通过BCA法确定样品的蛋白质浓度。将组织裂解液在10%SDS-聚丙烯酰胺凝胶上电泳,转移到硝酸纤维素膜上。在室温下用5%脱脂奶封闭90 min,然后室温下孵育一抗,包括兔抗人IL-9抗体(ab203386,1∶1 000,英国Abcam公司)和β-actin抗体(ab179467,1∶5 000;英国Abcam公司),在4 ℃下过夜。在室温下,将辣根过氧化物酶偶联的二抗IgG抗体应用1 h后检测。印迹结果分析使用Las-4000 Image软件和Multi Gauge Ver 3.0软件(日本富士胶片生命科学公司)。
1.4 统计学分析应用Prism7.0软件进行统计分析,计数资料采用率表示,组间比较采用χ2检验;正态分布的计量资料采用x±s表示,组间比较采用t检验,P < 0.05为差异有统计学意义。
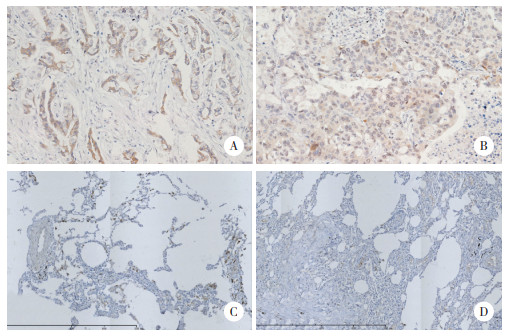
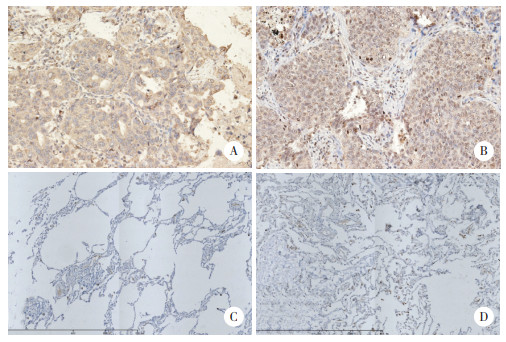
2 结果 2.1 免疫组织化学检测NSCLC癌组织及癌旁组织中IL-9、IL-9R的表达结果显示,NSCLC癌组织中IL-9阳性表达88例(80%),其中男性64例,女性24例;IL-9阴性表达22例(20%),男性16例,女性6例。癌旁正常组织中IL-9阳性表达30例(27.3%),阴性80例(72.7%)。癌组织中IL-9的阳性表达率明显高于癌旁组织,差异有统计学意义(χ2=61.489,P < 0.01),见图 1。NSCLC癌组织中IL-9R阳性表达82例(74.5%),其中,男性60例,女性22例;IL-9R阴性表达28例(25.5%),其中男性20例,女性8例。癌旁组织中IL-9R阳性表达12例(10.9%),阴性表达98例(89.1%)。癌组织中IL-9R阳性表达率明显高于癌旁组织,差异有统计学意义(χ2=91.017,P < 0.01),见图 2。
|
| A, positive for IL-9 in lung adenocarcinoma; B, positive for IL-9 in lung squamous cell carcinoma; C, negative for IL-9 in the adjacent tissues of lung adenocarcinoma; D, negative for IL-9 in the adjacent tissues of lung squamous cell carcinoma. 图 1 免疫组织化学检测NSCLC癌组织及癌旁组织IL-9表达×200 Fig.1 Immunohistochemical detection of IL-9 expression in cancer tissues and adjacent tissues from NSCLC patients ×200 |
|
| A, IL-9R positive in lung adenocarcinoma; B, IL-9R positive in lung squamous cell carcinoma; C, IL-9R negative in adjacent tissues of lung adenocarcinoma; D, IL-9R negative in adjacent tissues of lung squamous cell carcinoma. 图 2 免疫组织化学检测NSCLC癌组织及癌旁组织IL-9R表达 ×200 Fig.2 Immunohistochemical detection of IL-9R protein expression in cancer and adjacent tissues from NSCLC patients ×200 |
2.2 Western blotting检测NSCLC癌组织及癌旁组织IL-9表达
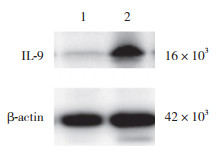
结果显示,IL-9蛋白在癌组织中的表达水平(0.63±0.28)较癌旁组织(0.37±0.15)明显增高(P < 0.05),见图 3。
|
| 1, adjacent normal tissues; 2, cancer tissues. 图 3 Western blotting检测NSCLC患者癌组织及癌旁组织IL-9蛋白表达 Fig.3 IL-9 protein expression in cancer tissues and adjacent tissues from NSCLC patients detected by Western blotting |
2.3 NSCLC癌组织中IL9及IL-9R的表达与临床指标的相关分析
结果显示,NSCLC癌组织中IL-9的表达与患者性别、年龄、肿瘤分化程度均不相关(均P > 0.05),而与肿瘤大小、淋巴结转移及TNM分期相关(均P < 0.05)。NSCLC癌组织中IL-9R的表达与患者性别、年龄、肿瘤分化程度、肿瘤大小均不相关(均P > 0. 05),而与淋巴结转移、TNM分期相关(均P < 0.001),发生淋巴结转移和分期较晚期患者癌组织中IL-9及IL-9R高表达,见表 1。
| Item | IL-9 | IL-9R | |||||||
| Positive | Negative | χ2 | P | Positive | Negative | χ2 | P | ||
| Gender | 0.568 | 0.451 | 0.032 | 0.858 | |||||
| Male | 64 | 16 | 60 | 20 | |||||
| Female | 24 | 6 | 22 | 8 | |||||
| Age | 0.048 | 0.827 | 0.192 | 0.661 | |||||
| < 50 year-old | 22 | 6 | 20 | 8 | |||||
| ≥50 year-old | 66 | 16 | 62 | 20 | |||||
| Tumor size | 5.381 | 0.020 | 3.625 | 0.057 | |||||
| < 3 cm | 32 | 14 | 30 | 16 | |||||
| ≥3 cm | 56 | 8 | 52 | 12 | |||||
| Differentiation | 1.146 | 0.284 | 0.398 | 0.528 | |||||
| Medium/highly differentiated | 62 | 18 | 58 | 22 | |||||
| Poorly differentiated | 26 | 4 | 24 | 6 | |||||
| Lymph node metastasis | 10.511 | 0.001 | 18.211 | < 0.001 | |||||
| Yes | 50 | 4 | 50 | 4 | |||||
| No | 38 | 18 | 32 | 24 | |||||
| TNM | 12.106 | 0.001 | 10.477 | 0.001 | |||||
| Ⅰ-Ⅱ | 44 | 20 | 40 | 24 | |||||
| Ⅲ-Ⅳ | 44 | 2 | 42 | 4 | |||||
3 讨论
IL-9主要由Th9细胞分泌,在支气管哮喘、自身免疫性疾病中发挥关键作用[11-13]。IL-9与IL-9R结合,激活JAK/STAT通路促进炎症及自身免疫反应[14]。近年来,IL-9在肿瘤免疫中的作用备受关注。最初研究[15]认为IL-9是具有潜在致癌活性的T细胞生长因子,IL-9在非实体肿瘤(多数血液系统肿瘤)中驱动肿瘤生长。有研究[16]发现IL-9可促进弥漫性大B细胞淋巴瘤的细胞存活和耐药性,同时可促进大细胞间变性淋巴瘤的发生及发展。实体肿瘤研究[17]显示肝癌组织IL-9、IL-9R表达明显高于癌旁组织,IL-9、IL-9R显著促进肝癌细胞增殖、侵袭,抑制细胞凋亡。然而在肺癌实体瘤组织中关于IL-9、IL-9R的研究目前较少,本研究结果显示,肺癌组织中IL-9的表达明显高于癌旁正常组织(P < 0.05),提示IL-9可能促进NSCLC进展。
IL-9具有复杂的双重功能,在不同的肿瘤微环境中可以促进或抑制肿瘤细胞的生长和迁移[11]。研究[18]发现Th9细胞分泌的IL-9对于黑色素瘤的生长有抑制作用,将肿瘤抗原特异性Th1、Th9和Th17细胞转移到黑色素瘤小鼠体内,可以明显抑制黑色素瘤的生长。然而Th9细胞的抗肿瘤作用并不局限在黑色素瘤模型中,在乳腺癌模型中Th9、IL-9表达的增高可通过增强CD8+T细胞介导的细胞毒性发挥抗肿瘤作用[19]。同时也有研究[20]发现Th9细胞在小鼠结肠腺癌模型、肺腺癌模型中也发挥了重要的抗肿瘤作用。但是也有研究[6]发现肺癌恶性胸腔积液中,Th9具有促进肺癌进展和转移的作用,恶性胸腔积液中存在大量的促炎症细胞因子,可促进Th9细胞的诱导及分化,其分泌的IL-9通过激活STAT3信号通路促进肺癌细胞的增殖和迁移,抑制γ干扰素对肿瘤细胞的杀伤作用。近期研究[21]发现IL-9可通过增强NSCLC的血管生成促进肿瘤发生。本研究结果显示IL-9及IL9R表达在NSCLC癌组织较癌旁组织明显增高,IL-9表达与患者肿瘤大小、淋巴结转移及TNM分期相关,IL-9R表达与患者TNM分期和淋巴结转移相关,IL-9及IL-9R在TNM分期较晚及淋巴结转移患者中高表达,说明IL-9可能通过与IL-9R结合促进NSCLC转移和进展。
综上所述,IL-9及IL9R在NSCLC癌组织中高表达,其表达水平与NSCLC的淋巴结转移以及TNM分期相关。因此推测IL-9/IL-9R在NSCLC免疫微环境中起到促癌作用,IL-9/IL-9R可能成为NSCLC调节免疫微环境进行免疫治疗的新靶点,但仍需更多的研究进一步来验证。
| [1] |
BRAY F, FERLAY J, SOERJOMATARAM I, et al. Global cancer statistics 2018:globocan estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA: Cancer J Clin, 2018, 68(6): 394-424. DOI:10.3322/caac.21492 |
| [2] |
ZAPPA C, MOUSA SA. Non-small cell lung cancer: current treatment and future advances[J]. Transl Lung Cancer Res, 2016, 5(3): 288-300. DOI:10.21037/tlcr.2016.06.07 |
| [3] |
ETTINGER DS, WOOD DE, AKERLEY W, et al. Non-small cell lung cancer, Version 6.2015[J]. J Nat Comprehen Cancer Network, 2015, 13(5): 515-524. DOI:10.6004/jnccn.2015.0071 |
| [4] |
HENSING T, CHAWLA A, BATRA R, et al. A personalized treatment for lung cancer: molecular pathways, targeted therapies, and genomic characterization[J]. Adv Exp Med Biol, 2014, 799: 85-117. DOI:10.1007/978-1-4614-8778-4_5 |
| [5] |
SALAZAR Y, ZHENG X, BRUNN D, et al. Microenvironmental Th9 and Th17 lymphocytes induce metastatic spreading in lung cancer[J]. J Clin Invest, 2020, 130(7): 3560-3575. DOI:10.1172/JCI124037 |
| [6] |
YE ZJ, ZHOU Q, YIN W, et al. Differentiation and immune regulation of IL-9-producing CD4+T cells in malignant pleural effusion[J]. Am J Respir Crit Care Med, 2012, 186(11): 1168-1179. DOI:10.1164/rccm.201207-1307oc |
| [7] |
CHEN T, GUO J, CAI Z, et al. Th9 cell differentiation and its dual effects in tumor development[J]. Front Immunol, 2020, 11: 1026. DOI:10.3389/fimmu.2020.01026 |
| [8] |
CHANDWASKAR R, AWASTHI A. Emerging roles of Th9 cells as an anti-tumor helper T cells[J]. Int Rev Immunol, 2019, 38(5): 204-211. DOI:10.1080/08830185.2019.1648453 |
| [9] |
PARK SM, DO-THI VA, LEE JO, et al. Interleukin-9 inhibits lung metastasis of melanoma through stimulating anti-tumor M1 macrophages[J]. Mol Cells, 2020, 43(5): 479-490. DOI:10.14348/molcells.2020.0047 |
| [10] |
KUTOB L, SCHNEIDER F. Lung cancer staging[J]. Surg Pathol Clin, 2020, 13(1): 57-71. DOI:10.1016/j.path.2019.10.003 |
| [11] |
GERLACH K, WEIGMANN B. The dichotomous function of interleukin-9 in cancer diseases[J]. J Mol Med (Berl), 2019, 97(10): 1377-1383. DOI:10.1007/s00109-019-01826-5 |
| [12] |
CHEN J, GUAN L, TANG L, et al. T Helper 9 cells: a new player in immune-related diseases[J]. DNA Cell Biol, 2019, 38(10): 1040-1047. DOI:10.1089/dna.2019.4729 |
| [13] |
STAUDT V, BOTHUR E, KLEIN M, et al. Interferon-regulatory factor 4 is essential for the developmental program of T helper 9 cells[J]. Immunity, 2010, 33(2): 192-202. DOI:10.1016/j.immuni.2010.07.014 |
| [14] |
NEURATH MF, FINOTTO S. IL-9 signaling as key driver of chronic inflammation in mucosal immunity[J]. Cytokine Growth Factor Rev, 2016, 29: 93-99. DOI:10.1016/j.cytogfr.2016.02.002 |
| [15] |
ZHANG J, WANG WD, GENG QR, et al. Serum levels of interleukin-9 correlate with negative prognostic factors in extranodal NK/T-cell lymphoma[J]. PloS One, 2014, 9(4): e94637. DOI:10.1371/journal.pone.0094637 |
| [16] |
LV X, FENG L, GE X, et al. Interleukin-9 promotes cell survival and drug resistance in diffuse large B-cell lymphoma[J]. J Exp Clin Cancer Res, 2016, 35(1): 106. DOI:10.1186/s13046-016-0374-3 |
| [17] |
LI HJ, SUN QM, LIU LZ, et al. High expression of IL-9R promotes the progression of human hepatocellular carcinoma and indicates a poor clinical outcome[J]. Oncol Report, 2015, 34(2): 795-802. DOI:10.3892/or.2015.4060 |
| [18] |
LU Y, HONG S, LI H, et al. Th9 cells promote antitumor immune responses in vivo[J]. J Clin Invest, 2012, 122(11): 4160-4171. DOI:10.1172/JCI65459 |
| [19] |
YOU FP, ZHANG J, CUI T, et al. Th9 cells promote antitumor immunity via IL-9 and IL-21 and demonstrate atypical cytokine expression in breast cancer[J]. Inter Immunopharmacol, 2017, 52: 163-167. DOI:10.1016/j.intimp.2017.08.031 |
| [20] |
KIM IK, KIM BS, KOH CH, et al. Glucocorticoid-induced tumor necrosis factor receptor-related protein co-stimulation facilitates tumor regression by inducing IL-9-producing helper T cells[J]. Nat Med, 2015, 21(9): 1010-1017. DOI:10.1016/j.intimp.2017 |
| [21] |
HE J, WANG L, ZHANG C, et al. Interleukin-9 promotes tumorigenesis through augmenting angiogenesis in non-small cell lung cancer[J]. Inter Immunopharmacol, 2019, 75: 105766. DOI:10.1016/j.intimp.2019.105766 |
 2021, Vol. 50
2021, Vol. 50




