文章信息
- 李香雨, 于漫, 聂梓陶, 陈彦如, 王嘉会, 韩喜彬, 赵微
- LI Xiangyu, YU Man, NIE Zitao, CHEN Yanru, WANG Jiahui, HAN Xibin, ZHAO Wei
- 酵母双杂交筛选与星状病毒衣壳蛋白ORF2互作的宿主蛋白
- Screening of proteins that interact with astrovirus capsid protein ORF2 using the yeast two-hybrid system
- 中国医科大学学报, 2021, 50(6): 491-495
- Journal of China Medical University, 2021, 50(6): 491-495
-
文章历史
- 收稿日期:2020-10-14
- 网络出版时间:2021-05-26 16:15
星状病毒是引起婴幼儿及免疫缺陷人群腹泻的重要病原体,发病率仅次于轮状病毒,常与其他肠道病毒混合感染,造成患儿严重腹泻甚至死亡[1]。由于星状病毒属于食源性和医院获得性病原体,常呈现群体爆发感染,严重危害公共卫生安全[2-3]。
星状病毒为星状病毒科无囊膜、单股、正链RNA病毒。人星状病毒(human astrovirus,HAstV)具有8个传统的血清型(HAstV 1~8)及3种新的亚型(MLB型、VA型及HMO型)[4]。其中,HAstV-1型在婴幼儿群体中感染最为普遍[5]。HAstV基因组编码非结构蛋白nsP1a(编码3C-like丝氨酸蛋白酶)、非结构蛋白nsP1b(编码RNA依赖性的RNA聚合酶RdRp)和结构蛋白ORF2(编码病毒衣壳蛋白)3种蛋白。ORF2蛋白主要决定了细胞的嗜异性,并能够刺激宿主细胞产生应答,是参与调控细胞基因的转录与表达及参与病毒受体结合的重要成分,在病毒粒子的成熟和包装中起重要作用[6-8],因此,以ORF2为靶基因筛选与之互作的蛋白具有重要意义。
酵母双杂交系统是基于转录因子对细胞内蛋白质相互作用进行筛选与鉴定的系统,已被广泛应用于病毒与宿主的互作研究[9-10]。本研究利用实验室分离到的HAstV-1型1d亚株作为模板,将病毒衣壳蛋白ORF2基因成功克隆到酵母双杂交表达载体pGBKT7中,并以ORF2作为诱饵蛋白,从人结肠癌细胞Caco-2 cDNA文库中初步鉴定与ORF2存在相互作用的宿主蛋白,为进一步研究ORF2的生物学功能及参与病毒致病性等方面奠定基础。
1 材料与方法 1.1 材料HAstV-1d病毒株、人Caco-2 cDNA文库、Caco-2细胞、pMD-18T-ORF2质粒为本实验室保存。Y2H酵母感受态细胞、胶回收试剂盒、Prime STAR HS DNA聚合酶、dNTP、限制性内切酶NdeⅠ、SalⅠ、T4DNA连接酶、DNA Marker、2×蛋白上样缓冲液,均购自大连TaKaRa公司;质粒pGBKT7、pGBKT7-53、pGADT7、pGADT7-T、酵母质粒小提试剂盒和酵母双杂交试剂盒及各种营养缺陷型培养基均购自美国Clontech公司;Lipofectamine3000转染试剂、ECL发光试剂盒购自美国Thermo公司;胎牛血清、DMEM培养基、胰蛋白酶购自美国GIBCO公司。
1.2 方法 1.2.1 构建pGBKT7-ORF2诱饵表达载体以HAstV-1d病毒株衣壳蛋白pMD-18T-ORF2质粒作为模板,设计针对ORF2的PCR引物,ORF-F引物序列为5’-CATATGATGGCTAGCAAGTCCAATAAGCAGGTAACT-3’;ORF-R引物序列为5’-GTCGACCTCGGCGTGGCCGCGGCTTCCAGAAGT-3’。分别用Prime STAR HS DNA聚合酶进行PCR扩增,经1%琼脂糖凝胶检测、回收,用NdeⅠ和SalⅠ对PCR产物和pGBKT7质粒分别进行双酶切、鉴定、回收。再经T4连接酶连接并转化DH5α感受态细胞。用检测引物ORF-F和ORF-R对得到的转化子进行菌落PCR扩增,1%琼脂糖凝胶检测,并将阳性转化子送上海杰李公司进行测序。
1.2.2 诱饵蛋白自激活性鉴定将pGBKT7-ORF2和pGADT7共转化至Y2H Gold中,以pGADT7-T和pGADT7-53作为阳性对照、pGBKT7-Lam和pGADT7-T作为阴性对照。转化菌液于SD/-Leu/-Trp和SD/-Leu/-Trp/-His固体培养基上划线,30 ℃培养3~5 d。观察是否有蓝色克隆菌生长,判断是否有自激活及毒性作用。
1.2.3 酵母双杂交筛选与鉴定酵母双杂交筛选按照说明书进行。将诱饵质粒pGBKT7-ORF2转化至Y2H酵母感受态细胞,并接种到全培养基中,30 ℃培养24 h,OD600值达到1时收集细胞。用5 mL SD/-Trp液体培养基进行重悬,加入1 mL Caco-2 cDNA文库(克隆数 > 2×107)。培养24 h后,取少许菌液在显微镜下观察菌体形态,判断是否融合。将融合的菌液涂布于SD/-Trp/-Leu/-His培养基进行初步筛选,获得的阳性菌落涂布于SD/-Trp/-Leu/-His/-Ade固体培养基上,30 ℃培养3~5 d,进行第二次筛选。挑选二次筛选到的阳性菌落接种到SD/-Trp/-Leu/-His/-Ade/AbA/X-α-gal培养基,30 ℃培养3~5 d,进一步筛选。阳性菌落,经菌液PCR扩增ORF2基因,回收后送上海杰李公司进行序列测定。获得的序列信息在NCBI数据库中进行检索与对比,确定互作蛋白的基因序列信息。
2 结果 2.1 酵母诱饵质粒pGBKT7-ORF2的鉴定用ORF-R与ORF-F引物对已构建好的重组质粒pGBKT7-ORF2进行菌落PCR检测,可扩增出2 364 bp的片段(图 1A),测序结果与HAstV-1d上传GenBank的ORF2基因片段(GenBank:KF211475.1)序列一致,说明pGBKT7-ORF2诱饵质粒构建成功。重组质粒经双酶切鉴定、琼脂糖凝胶电泳检测,出现大小为2 364 bp目的条带(图 1B),与预期相符。

|
| A, ORF2 gene amplification; B, identification of plasmid pGBKT7-ORF by restriction enzyme digestion. M, DNA marker. 图 1 诱饵载体pGBKT7-ORF2的鉴定 Fig.1 Detection of bait plasmid pGBKT7-ORF2 by PCR |
2.2 诱饵质粒自激活和毒性检测
pGBKT7-ORF2和pGADT7、pGADT7-T和pGADT7-53(阳性对照)、pGBKT7-Lam和pGADT7-T(阴性对照)菌落均能在SD/-Leu/-Trp固体培养基上生长,而仅有pGADT7-T和pGADT7-53在SD/-Leu/-Trp/-His固体培养基上生长,其余均无菌落生长(图 2)。说明ORF2蛋白不能激活酵母菌下游基因,不具有自激活性。
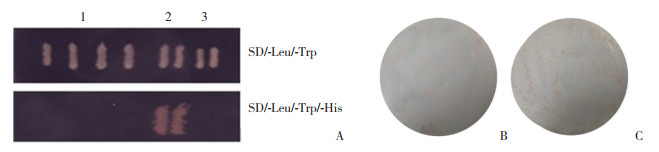
|
| A, the activation test of pGBKT7-ORF21;B, pGBKT7-ORF2 transformed yeast; C, pGBKT7 transformed yeast. 1, pGBKT7-ORF2+pGADT7;2, pGBKT7-53+pGADT7-T, positive control; 3, pGBKT7-Lam+pGADT7-T, negative control. 图 2 诱饵质粒自激活和毒性检测 Fig.2 Toxicity and the activation test of pGBKT7-ORF2 |
将含pGBKT7-ORF2和pGBKT7质粒的Y2H酵母菌涂布于SD/-Leu/-Trp培养基培养3 d,结果显示,pGBKT7-ORF2重组菌与空载体pGBKT7的菌落大小和数量基本一致(图 2B、2C),表明ORF2蛋白对菌体明显无毒性。
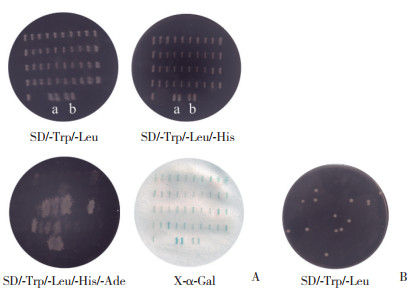
2.3 筛选与ORF2蛋白互作的宿主蛋白将pGBKT7-ORF2转化的Y2H酵母菌和Caco-2 cDNA文库融合得到的菌液涂布于不同报告基因缺失的固体平板进行表型鉴定(图 3A)。经过4轮缺失培养基筛选获得克隆,将Caco-2细胞cDNA文库转化产物104倍稀释后,在SD/-Trp/-Leu培养基平板进行培养,得到了14个阳性克隆菌(图 3B),总筛选克隆数为1.4×105。
|
| A, phenotype identification of positive clones; B, total screened clones. a, pGBKT7-53+pGADT7-T, positive control; b, pGBKT7-Lam+pGADT7-T, negative control. 图 3 以pGBKT7-ORF2为诱饵筛选Caco2细胞cDNA文库 Fig.3 Screening of Caco2 cell cDNA library |
2.4 阳性克隆菌的回转验证及测序分析
对获得的阳性克隆菌行2次回转验证,结果显示,转化的菌株能够在SD/-Trp/-Leu、SD/-Trp/-Leu/-His和SD/-Trp/-Leu/-His/-Ade平板上生长,且在SD/-Trp/-Leu/-His/-Ade/X-α-Gal/Aba平板上菌落呈蓝色,与阳性对照结果一致(图 4)。经测序鉴定得到阳性菌的基因序列,与NCBI数据库中数据进行比对分析,获得15种蛋白,见表 1。

|
| a, pGBKT7-53+pGADT7-T, positive control; b, pGBKT7-Lam+pGADT7-T, negative control; c, pGBKT7-ORF2+pGADT7, self-activation control. 图 4 阳性克隆回转验证 Fig.4 Return test of pGBKT7-ORF2 proreins |
| Sequence name | NCBI number | Gene name | Gene description |
| ORF2-3-8 | NM_002026.2 | FN1 | Homo sapiens fibronectin 1 |
| ORF2-3-7 | NM_152516.2 | COMMD1 | copper metabolism domain containing 1 |
| ORF2-3-6 | NM_170692.2 | RASAL2 | RAS protein activator like 2 |
| ORF2-3-5 | NM_130851.2 | BMP4 | bone morphogenetic protein 4 |
| ORF2-3-3 | NM_001199802.1 | RPL11 | ribosomal protein L11 |
| ORF2-3-2 | NM_005105.4 | RBM8A | RNA binding motif protein 8A |
| ORF2-3-1 | NM_003352.4 | SUMO1 | small ubiquitin like modifier 1 |
| ORF2-3-18 | NM_024949.5 | WWC2 | WW and C2 domain containing 2 |
| ORF2-3-17 | NM_001042635.1 | NGDN | neuroguidin |
| ORF2-3-16 | NM_001011.3 | RPS7 | ribosomal protein S7 |
| ORF2-3-15 | NM_001243259.1 | HINFP | histone H4 transcription factor |
| ORF2-2-8 | NM_006839.2 | IMMT | inner membrane mitochondrial protein |
| ORF2-2-7 | NM_003345.4 | UBE2I | ubiquitin conjugating enzyme E2 I |
| ORF2-2-6 | NM_001402.5 | EEF1A1 | eukaryotic translation elongation factor 1 alpha 1 |
| ORF2-2-5 | NM_000146.3 | FTL | ferritin light chain |
3 讨论
星状病毒ORF2蛋白主要决定了细胞的嗜异性,并能够刺激宿主细胞产生应答,参与病毒粒子的装配、核酸的包装、病毒粒子的成熟[11-12]。目前关于星状病毒衣壳蛋白与宿主相互作用的报道较少,通过对其结构基因的预测表明,ORF2蛋白的C端与某些病毒相关蛋白和受体具有结构上的相似性[13],可能参与病毒与受体的结合。
星状病毒的宿主细胞为Caco-2,该细胞体外培养条件下可自发上皮样分化,形成与小肠上皮细胞相同的微绒毛结构和紧密连接,与小肠柱状上皮细胞很相似。因此,本研究选择Caco-2细胞构建cDNA文库,进行宿主蛋白筛选[14]。以星状病毒的ORF2蛋白作为诱饵蛋白,通过酵母双杂交系统在Caco-2细胞的cDNA文库中筛选出与ORF2蛋白互作的15种蛋白。对15种蛋白进行了初步功能分析和文献检索,其中,纤维连接蛋白1(fibronectin 1,FN)与病毒感染具有相关性[15]。FN1的细胞型是细胞外基质的重要组成部分,在细胞形态形成、迁移、炎症和表面受体内化等方面发挥作用[16-18]。文献[19]报道,FN与EV71病毒颗粒有直接的相互作用,通过促进EV71的入侵促进EV71的感染。而流感病毒H1N1入侵宿主时需要FN的参与[20]。FN能与乙型肝炎病毒(hepatitis B,HBV)的S抗原相互作用,促进其与细胞表面结合[21-22],并且还可能参与HBV的入侵[23]。而FN1与星状病毒互作后对病毒感染有何影响目前尚无报道,有待进一步深入研究。
本研究利用酵母双杂交系统筛选并鉴定出与HAstV-1 ORF2蛋白互作蛋白。后续将进一步对其中感兴趣的蛋白,尤其是FN1与ORF2的互作进行免疫共沉淀检测,并进行基因功能分析,为研究星状病毒与宿主相互作用、ORF2蛋白功能及病毒的致病机制奠定基础。
| [1] |
JOHNSON C, HARGEST V, CORTEZ V, et al. Astrovirus pathogenesis[J]. Viruses, 2017, 9(1): 22. DOI:10.3390/v9010022 |
| [2] |
RUDAN I, CHAN KY, ZHANG JS, et al. Causes of deaths in children younger than 5 years in China in 2008[J]. Lancet, 2010, 375(9720): 1083-1089. DOI:10.1016/s0140-6736(10)60060-8 |
| [3] |
LI CY, LIU N, GUO WD, et al. Outbreak of neonatal gastroenteritis associated with astrovirus serotype 1 at a hospital in Inner Mongolia, China[J]. J Clin Microbiol, 2010, 48(11): 4306-4309. DOI:10.1128/jcm.00797-10 |
| [4] |
CORTEZ V, MELIOPOULOS VA, KARLSSON EA, et al. Astrovirus biology and pathogenesis[J]. Annu Rev Virol, 2017, 4(1): 327-348. DOI:10.1146/annurev-virology-101416-041742 |
| [5] |
HOU ML, LIANG XX, TAN LQ, et al. Outbreak of human astrovirus 1 lineage 1d in a childcare center in China[J]. Virol Sin, 2016, 31(3): 258-261. DOI:10.1007/s12250-015-3701-5 |
| [6] |
BOGDANOFF WA, CAMPOS J, PEREZ EI, et al. Structure of a human astrovirus capsid-antibody complex and mechanistic insights into virus neutralization[J]. J Virol, 2017, 91(2): e01859-16. DOI:10.1128/jvi.01859-16 |
| [7] |
DONG J, DONG L, MENDEZ E, et al. Crystal structure of the human astrovirus capsid spike[J]. PNAS, 2011, 108(31): 12681-12686. DOI:10.1073/pnas.1104834108 |
| [8] |
ARIAS C, DUBOIS R. The astrovirus capsid: a review[J]. Viruses, 2017, 9(1): 15. DOI:10.3390/v9010015 |
| [9] |
PAIANO A, MARGIOTTA A, DE LUCA M, et al. Yeast two-hybrid assay to identify interacting proteins[J]. Curr Protoc Protein Sci, 2019, 95(1): e70. DOI:10.1002/cpps.70 |
| [10] |
MAKUCH L. Yeast two-hybrid screen[J]. Methods enzymol, 2014, 539: 31-51. DOI:10.1016/b978-0-12-420120-0.00003-7 |
| [11] |
YORK RL, YOUSEFI PA, BOGDANOFF W, et al. Structural, mechanistic, and antigenic characterization of the human astrovirus capsid[J]. J Virol, 2015, 90(5): 2254-2263. DOI:10.1128/jvi.02666-15 |
| [12] |
TOH Y, HARPER J, DRYDEN KA, et al. Crystal structure of the human astrovirus capsid protein[J]. J Virol, 2016, 90(20): 9008-9017. DOI:10.1128/jvi.00694-16 |
| [13] |
BOGDANOFF WA, PEREZ EI, LÓPEZ T, et al. Structural basis for escape of human astrovirus from antibody neutralization: broad implications for rational vaccine design[J]. J Virol, 2018, 92(1): e01546-17. DOI:10.1128/jvi.01546-17 |
| [14] |
ZHAO W, LI X, LIU WH, et al. Construction of high-quality Caco-2 three-frame cDNA library and its application to yeast two-hybrid for the human astrovirus protein-protein interaction[J]. J Virol Methods, 2014, 205: 104-109. DOI:10.1016/j.jviromet.2014.05.007 |
| [15] |
BEER C, PEDERSEN L. Matrix fibronectin binds Gammaretrovirus and assists in entry: new light on viral infections[J]. J Virol, 2007, 81(15): 8247-8257. DOI:10.1128/jvi.00312-07 |
| [16] |
HUBMACHER D, SABATIER L, ANNIS DS, et al. Homocysteine modifies structural and functional properties of fibronectin and interferes with the fibronectin-fibrillin-1 interaction[J]. Biochemistry, 2011, 50(23): 5322-5332. DOI:10.1021/bi200183z |
| [17] |
FRAME MD, LIN FB, DEWAR AM, et al. Vasoactive effect of fibronectin-derived epiviosamine-1 and related peptides in quiescent and stress models[J]. Microcirculation, 2017, 24(6): e12369. DOI:10.1111/micc.12369 |
| [18] |
MEZZENGA R, MITSI M. The molecular dance of fibronectin: conformational flexibility leads to functional versatility[J]. Biomacromolecules, 2019, 20(1): 55-72. DOI:10.1021/acs.biomac.8b01258 |
| [19] |
HE QQ, REN S, XIA ZC, et al. Fibronectin facilitates Enterovirus 71 infection by mediating viral entry[J]. J Virol, 2018, 92(9): e02251-17. DOI:10.1128/jvi.02251-17 |
| [20] |
LEUNG HSY, LI OTW, CHAN RWY, et al. Entry of influenza A virus with a 2, 6-linked sialic acid binding preference requires host fibronectin[J]. J Virol, 2012, 86(19): 10704-10713. DOI:10.1128/jvi.01166-12 |
| [21] |
REN S, WANG J, CHEN TL, et al. Hepatitis B virus stimulated fibronectin facilitates viral maintenance and replication through two distinct mechanisms[J]. PLoS One, 2016, 11(3): e0152721. DOI:10.1371/journal.pone.0152721 |
| [22] |
YANG J, WANG F, TIAN L, et al. Fibronectin and asialoglyprotein receptor mediate hepatitis B surface antigen binding to the cell surface[J]. Arch Virol, 2010, 155(6): 881-888. DOI:10.1007/s00705-010-0657-5 |
| [23] |
YAN H, ZHONG G, XU G, et al. Sodium taurocholate cotransporting polypeptide is a functional receptor for human hepatitis B and D virus[J]. Elife, 2012, 1: e00049. DOI:10.7554/elife.00049 |
 2021, Vol. 50
2021, Vol. 50




