文章信息
- 穆盛田, 唐洁, 仲宇, 郑振
- MU Shengtian, TANG Jie, ZHONG Yu, ZHENG Zhen
- 乌司他丁对脂多糖诱导小鼠急性肾损伤的保护作用及其机制
- Protective effect of ulinastatin on lipopolysaccharide-induced acute kidney injury in mice and its mechanism
- 中国医科大学学报, 2021, 50(4): 336-340, 355
- Journal of China Medical University, 2021, 50(4): 336-340, 355
-
文章历史
- 收稿日期:2020-11-03
- 网络出版时间:2021-04-08 10:30
急性肾损伤(acute kidney injury,AKI) 是危重症领域一种常见的临床综合征,在部分重症医学科发病率甚至超过50%,严重威胁患者的生命安全[1]。脓毒症是引起AKI的最常见病因,但确切机制目前尚不清楚[2]。研究[3]显示,过度的氧化应激和炎性因子大量释放在脓毒症导致AKI的过程中发挥重要作用。近期研究[4]发现,核因子E2相关因子2 (nuclear factor erythroid 2-related factor 2,Nrf2) 作为细胞抗氧化应激的关键蛋白,其相关信号通路的激活在氧化应激和炎症反应调节中发挥重要作用。近期还有研究[5-6]发现,Nrf2可参与预防各种肾功能不全的发生发展,因此Nrf2也成为AKI治疗的一个潜在靶点。
乌司他丁是临床危重症领域常用的广谱蛋白酶抑制剂,在急重症胰腺炎、急性循环衰竭、感染性休克以及多器官功能障碍等多种临床综合征的救治中发挥重要的抗炎和抑制氧化应激的作用。前期临床研究[7]发现,乌司他丁可减少心脏手术后AKI的发生,但具体机制尚不清楚。近期有临床研究[8]发现,大剂量(160万U/d) 乌司他丁可预防肝移植术后患者发生迟发性急性肾衰竭。且前期对健康志愿者的研究[9]发现,大剂量乌司他丁并无严重不良反应,这为临床大剂量应用乌司他丁提供了安全保障。本研究的目的是探讨不同剂量的乌司他丁对脂多糖(lipopolysaccharide,LPS) 诱导的小鼠脓毒症AKI的保护作用和可能机制。
1 材料与方法 1.1 动物分组C57BL/6雄性小鼠40只,体质量22~25 g,来自中国医科大学实验动物部。将小鼠随机分为4组: 对照组、LPS组(腹腔注射LPS 10 mg/kg)、LPS+5 000 U/kg乌司他丁组和LPS+50 000 U/kg乌司他丁组。本研究中动物处理方法符合动物伦理学标准。
1.2 试剂和药品LPS (美国Sigma公司);乌司他丁(国药准字H19990134,100 000 U/支,广东天普生化医药股份有限公司);Nrf2抗体(英国Abcam公司);肿瘤坏死因子-α (tumor necrosis factor-α,TNF-α) 和白细胞介素-6 (interleukin-6,IL-6) ELISA检测试剂盒(武汉博士德生物有限公司);丙二醛(malondialdehyde,MDA) 和过氧化物歧化酶(super oxide dismutase,SOD) 检测试剂盒(南京建成生物科技有限公司)。
1.3 血清肌酐(creatinine,Cr) 和尿素氮(blood urea nitrogen,BUN) 检测LPS处理24 h后处死小鼠,通过心腔取血,2 000 r/min下离心20 min后取上清液,应用罗氏自动生化检测仪(瑞士罗氏公司) 检测各组小鼠血清Cr和BUN水平。
1.4 肾脏组织病理学检测取各组小鼠右肾,4%多聚甲醛固定,包埋切片后进行HE染色。用Leica DMi8显微镜(德国徕卡公司) 观察肾组织的形态变化(×400)。对肾脏病理损伤程度进行盲法评分,AKI评分标准分5个等级: 0分,正常肾组织;1分,肾小管受损范围 < 25%;2分,肾小管受损范围25%~ < 50%;3分,肾小管受损范围50%~ < 75%;4分,肾小管受损范围≥75%。
1.5 ELISA法检测血清中TNF-α和IL-6水平LPS处理24 h后处死小鼠,通过心腔取血,2 000 r/min下离心20 min后取上清液,根据试剂盒的操作说明,采用ELISA法检测各组血清中TNF-α和IL-6的水平。
1.6 ELISA法检测肾组织MDA和SOD的浓度取各组小鼠左肾,用RIPA裂解液裂解匀浆,12 000 r/min下离心15 min后取上清液,根据试剂盒的操作说明,采用ELISA法检测各组肾组织中MDA和SOD的浓度。
1.7 免疫组化方法检测Nrf2取各组小鼠右肾,4%多聚甲醛固定,包埋切片后,二甲苯脱蜡,乙醇脱水,清除内源性过氧化物酶,抗原修复后冲洗,封闭,一抗用Nrf2抗体稀释液(1∶150),二抗用生物素化羊抗兔IgG,DAB显色,苏木素复染。Leica DMi8光学显微镜下观察Nrf2在肾组织的表达(×400)。
1.8 Western blotting检测Nrf2取各组小鼠左肾组织,经裂解、匀浆、离心后,提取总蛋白,用BCA法进行蛋白定量,依次进行凝胶电泳,电转膜,室温封闭2 h,加入洗膜缓冲液洗膜,加Nrf2抗体稀释液(1∶1 000),4 ℃孵育过夜,缓冲液冲洗后加入二抗室温下孵育,使用免疫印迹化学发光法显色,最后应用凝胶图像处理系统分析目标条带。
1.9 统计学分析应用Graphpad Prism 6.0统计分析数据。结果以x±s表示,2组间比较采用t检验。P < 0.05为差异有统计学意义。
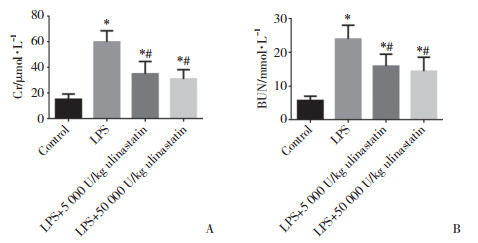
2 结果 2.1 不同剂量的乌司他丁对LPS刺激小鼠肾功能的影响与对照组比较,LPS组小鼠血清Cr和BUN水平明显升高(P < 0.05)。与LPS组比较,LPS+5 000 U/kg乌司他丁组和LPS+50 000 U/kg乌司他丁组小鼠血清Cr和BUN水平明显降低(P < 0.05)。但LPS+5 000 U/kg乌司他丁组与LPS+50 000 U/kg乌司他丁组比较,血清Cr和BUN水平无统计学差异(P > 0.05)。见图 1。
|
| A, Cr in the serum; B, BUN in the serum. Cr, creatinine; BUN, blood urea nitrogen; LPS, lipopolysaccharide. * P < 0.05 vs control group; # P < 0.05 vs LPS group. 图 1 各组小鼠血清中Cr和BUN的水平 Fig.1 Levels of creatinine and blood urea nitrogen in the serum of mice in each group |
2.2 不同剂量的乌司他丁对LPS刺激小鼠AKI肾组织损伤的影响
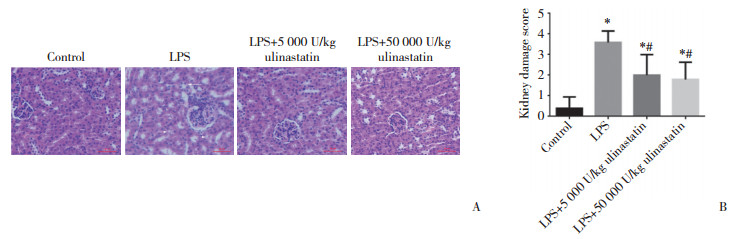
对照组小鼠肾组织结构完整。LPS组小鼠肾小管上皮细胞肿胀或脱落,间质水肿,肾小管明显扩张,肾损伤评分明显增加(P < 0.05)。与LPS组比较,LPS+5 000 U/kg乌司他丁和LPS+50 000 U/kg乌司他丁组肾损伤程度明显改善,肾损伤评分明显降低(P < 0.05)。但LPS+5 000 U/kg乌司他丁组与LPS+50 000 U/kg乌司他丁组比较,肾损伤评分无统计学差异(P > 0.05)。见图 2。
|
| A, hematoxylin-eosin staining (×400). Arrows indicate damaged tubular epithelial cells. B, kidney damage score. LPS, lipopolysaccharide. * P < 0.05 vs control group; # P < 0.05 vs LPS group. 图 2 各组小鼠肾组织HE染色 Fig.2 Hematoxylin-eosin staining of the renal tissues of mice in each group |
2.3 不同剂量的乌司他丁对LPS刺激小鼠血清炎性因子水平的影响
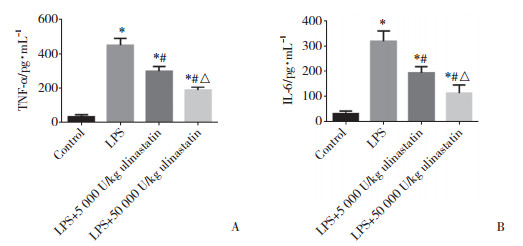
与对照组比较,LPS组小鼠血清TNF-α和IL-6水平明显升高(P < 0.05)。与LPS组比较,LPS+5 000 U/kg乌司他丁和LPS+50 000 U/kg乌司他丁组小鼠血清TNF-α和IL-6水平明显降低(P < 0.05)。且LPS+50 000 U/kg乌司他丁组TNF-α和IL-6水平较LPS+5 000 U/kg乌司他丁组进一步降低(P < 0.05),说明乌司他丁的抗炎作用呈一定剂量依赖性。见图 3。
|
| A, TNF-α in the serum; B, IL-6 in the serum. TNF-α, tumor necrosis factor-α; IL-6, interleukin-6;LPS, lipopolysaccharide. * P < 0.05 vs control group; # P < 0.05 vs LPS group; △ P < 0.05 vs 5 000 U/kg ulinastatin group. 图 3 各组小鼠血清中TNF-α和IL-6的水平 Fig.3 Levels of tumor necrosis factor-α and interleukin-6 in the serum of mice in each group |
2.4 不同剂量的乌司他丁对LPS刺激小鼠肾组织氧化应激损伤的影响
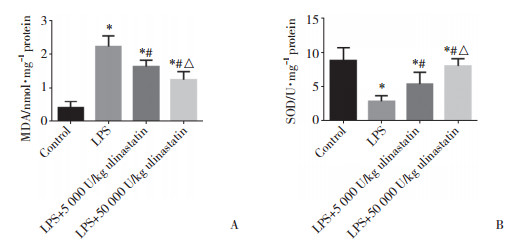
与对照组比较,LPS组小鼠肾组织中MDA浓度明显升高,SOD浓度明显下降(均P < 0.05)。与LPS组比较,LPS+5 000 U/kg乌司他丁组和LPS+50 000 U/kg乌司他丁组肾组织中MDA浓度明显降低,SOD浓度明显升高(均P < 0.05)。且LPS+50 000 U/kg乌司他丁组肾组织中MDA浓度较LPS+5 000 U/kg乌司他丁组进一步降低,SOD浓度进一步升高(均P < 0.05),说明乌司他丁改善AKI时氧化应激损伤的作用呈一定剂量依赖性。见图 4。
|
| A, MDA in the renal tissues; B, SOD in the renal tissues. MDA, malondialdehyde; SOD, superoxide dismutase; LPS, lipopolysaccharide. * P < 0.05 vs control group; # P < 0.05 vs LPS group; △ P < 0.05 vs 5 000 U/kg ulinastatin group. 图 4 各组小鼠肾组织中MDA和SOD的浓度 Fig.4 Concentrations of malondialdehyde and superoxide dismutase in the renal tissues of mice in each group |
2.5 不同剂量的乌司他丁对LPS刺激小鼠AKI肾组织中Nrf2表达水平的影响
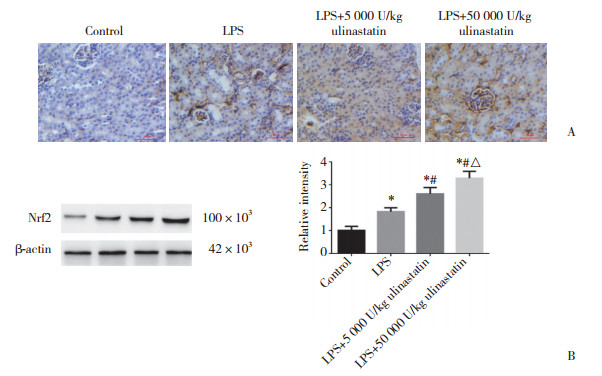
与对照组比较,LPS组小鼠肾组织中Nrf2表达水平升高(P < 0.05)。与LPS组比较,LPS+5 000 U/kg乌司他丁组和LPS+50 000 U/kg乌司他丁组肾组织中Nrf2表达水平明显升高(P < 0.05)。且LPS+50 000 U/kg乌司他丁组较LPS+5000 U/kg乌司他丁组Nrf2表达水平进一步升高(P < 0.05),说明乌司他丁增加AKI时Nrf2的表达水平呈一定剂量依赖性。见图 5。
|
| A, immunohistochemical staining images of Nrf2 (×400);B, Western blotting results. LPS, lipopolysaccharide. * P < 0.05 vs control group; # P < 0.05 vs LPS group; △ P < 0.05 vs 5 000 U/kg ulinastatin group. 图 5 免疫组化染色和Western blotting检测各组小鼠肾组织中Nrf2的表达 Fig.5 Expression of Nrf2 detected by immunohistochemical staining and western blotting in the renal tissues of mice in each group |
3 讨论
目前,脓毒症导致的AKI仍是危重症领域的常见疾病,一旦合并AKI,脓毒症患者的死亡率将增加6~8倍[3]。近年研究[3,10]发现,过度的炎症反应和氧化应激损伤在其病理过程中发挥了重要作用。体外研究[11]已证实,氧化应激和线粒体呼吸链功能异常在脓毒症相关的AKI中发挥至关重要的作用。
近年来,Nrf2相关通路受到广泛关注,其在氧化应激损伤过程中发挥重要作用。Nrf2的激活可诱导其下游多种抗氧化酶的表达,从而参与机体的抗氧化应激反应。Nrf2已被发现在多种与氧化应激有关疾病(如动脉粥样硬化、糖尿病、肿瘤、急性肺损伤、肝脏缺血再灌注损伤) 的发生和进展中发挥重要作用。近期也有研究[12]发现,Nrf2在脓毒症引起的AKI中有保护作用。
乌司他丁作为临床抑制机体内蛋白酶活性的药物,被广泛用于急重型胰腺炎、脓毒症及多器官功能障碍等危重症的救治。近期有研究[13]对106例脓毒症AKI患者进行分析,发现乌司他丁联合持续血液净化治疗可明显降低患者血浆中TNF-α、IL-6等炎性因子水平,降低C反应蛋白和降钙素原,减少氧化应激损伤和改善肾功能。还有研究[7]发现,乌司他丁可减少心脏手术后AKI的发生。体外实验[14]发现,乌司他丁可通过激活Nrf2来减轻LPS引起的小鼠巨噬细胞炎症反应。且动物试验[15]发现,乌司他丁可减少冷缺血再灌注AKI的炎性因子水平和氧化应激产物。所以,本研究探讨了不同剂量的乌司他丁是否可通过Nrf2抑制脓毒症AKI小鼠的炎症反应和氧化应激损伤来发挥保护作用。
通过HE染色和血清Cr、BUN的检测发现,乌司他丁可改善LPS刺激小鼠引起的AKI,不同剂量的乌司他丁并无明显差异。但高剂量乌司他丁对全身炎性因子水平(血清TNF-α和IL-6) 和肾组织中氧化应激损伤相关指标(MDA和SOD) 的改善作用优于低剂量乌司他丁,且高剂量组Nrf2的表达水平也明显高于低剂量组,说明乌司他丁的抗炎和抗氧化应激作用呈一定程度的剂量依赖性,这为临床大剂量应用乌司他丁提供了研究依据。
综上所述,乌司他丁可通过抑制氧化应激损伤和炎症反应来保护LPS刺激引起的AKI,且乌司他丁的抗氧化应激和抗炎作用呈一定程度的剂量依赖性。乌司他丁的保护作用可能与激活Nrf2的表达有关。本研究并未直接证实Nrf2参与其中,需要今后进一步的深入研究。
| [1] |
RONCO C, BELLOMO R, KELLUM JA. Acute kidney injury[J]. Lancet, 2019, 394(10212): 1949-1964. DOI:10.1016/S0140-6736(19)32563-2 |
| [2] |
POSTON JT, KOYNER JL. Sepsis associated acute kidney injury[J]. BMJ, 2019, 364: k4891. DOI:10.1136/bmj.k4891 |
| [3] |
GÓMEZ H, KELLUM JA. Sepsis-induced acute kidney injury[J]. Curr Opin Crit Care, 2016, 22(6): 546-553. DOI:10.1097/MCC.0000000000000356 |
| [4] |
OHL K, FRAGOULIS A, KLEMM P, et al. Nrf2 is a central regulator of metabolic reprogramming of myeloid-derived suppressor cells in steady state and sepsis[J]. Front Immunol, 2018, 9: 1552. DOI:10.3389/fimmu.2018.01552 |
| [5] |
NEZU M, SUZUKI N, YAMAMOTO M. Targeting the KEAP1-NRF2 system to prevent kidney disease progression[J]. Am J Nephrol, 2017, 45(6): 473-483. DOI:10.1159/000475890 |
| [6] |
GUERRERO-HUE M, FARRE-ALINS V, PALOMINO-ANTOLIN A, et al. Targeting Nrf2 in protection against renal disease[J]. Curr Med Chem, 2017, 24(33): 3583-3605. DOI:10.2174/0929867324666170511120814 |
| [7] |
WAN X, XIE X, GENDOO Y, et al. Ulinastatin administration is associated with a lower incidence of acute kidney injury after cardiac surgery: a propensity score matched study[J]. Crit Care, 2016, 20: 42. DOI:10.1186/s13054-016-1207-7 |
| [8] |
LV H, WEI X, YI X, et al. High-dose ulinastatin to prevent late-onset acute renal failure after orthotopic liver transplantation[J]. Ren Fail, 2020, 42(1): 137-145. DOI:10.1080/0886022x.2020.1717530 |
| [9] |
CHEN Q, HU C, LIU Y, et al. Safety and tolerability of high-dose ulinastatin after 2-hour intravenous infusion in adult healthy Chinese volunteers: a randomized, double-blind, placebo-controlled, ascending-dose study[J]. PLoS One, 2017, 12(5): e0177425. DOI:10.1371/journal.pone.0177425 |
| [10] |
UMBRO I, GENTILE G, TINTI F, et al. Recent advances in pathophysiology and biomarkers of sepsis-induced acute kidney injury[J]. J Infect, 2016, 72(2): 131-142. DOI:10.1016/j.jinf.2015.11.008 |
| [11] |
QUOILIN C, MOUITHYS-MICKALAD A, LÉCART S, et al. Evidence of oxidative stress and mitochondrial respiratory chain dysfunction in an in vitro model of sepsis-induced kidney injury[J]. Biochim Biophys Acta, 2014, 1837(10): 1790-1800. DOI:10.1016/j.bbabio.2014.07.005 |
| [12] |
WANG W, ZHANG S, YANG F, et al. Diosmetin alleviates acute kidney injury by promoting the TUG1/Nrf2/HO-1 pathway in sepsis rats[J]. Int Immunopharmacol, 2020, 88: 106965. DOI:10.1016/j.intimp.2020.106965 |
| [13] |
FANG QY, ZHAO XH. Clinical effect of combined ulinastatin and continuous renal replacement therapy on management of severe sepsis with acute kidney injury[J]. Trop J Pharm Res, 2017, 16(4): 925. DOI:10.4314/tjpr.v16i4.26 |
| [14] |
LI ST, DAI Q, ZHANG SX, et al. Ulinastatin attenuates LPS-induced inflammation in mouse macrophage RAW264.7 cells by inhibiting the JNK/NF-κB signaling pathway and activating the PI3K/Akt/Nrf2 pathway[J]. Acta Pharmacol Sin, 2018, 39(8): 1294-1304. DOI:10.1038/aps.2017.143 |
| [15] |
WANG Y, PENG C, ZHANG Z, et al. Intravenous infusion of ulinastatin attenuates acute kidney injury after cold ischemia/reperfusion[J]. Int Urol Nephrol, 2019, 51(10): 1873-1881. DOI:10.1007/s11255-019-02204-3 |
 2021, Vol. 50
2021, Vol. 50




