文章信息
- 刘金霞, 王钰池, 郭卓, 赵江月, 孔珺, 秦宇
- LIU Jinxia, WANG Yuchi, GUO Zhuo, ZHAO Jiangyue, KONG Jun, QIN Yu
- microRNA-125b通过调控Nrf2/Keap1信号通路影响光感受器细胞氧化应激
- Regulatory role of microRNA-125b in oxidative stress of photoreceptor cells via the Nrf2/Keap1 signaling pathway
- 中国医科大学学报, 2021, 50(11): 976-980, 985
- Journal of China Medical University, 2021, 50(11): 976-980, 985
-
文章历史
- 收稿日期:2021-01-27
- 网络出版时间:2021-11-03 18:05
年龄相关性黄斑变性(age-related macular degeneration,AMD)是老年人群不可逆转性盲的主要原因之一[1]。AMD分为干性和湿性2种类型,其中,干性AMD占比较多,目前尚无有效治疗手段[2-3]。干性AMD的病理改变以光感受器细胞变性为主[4]。视网膜氧化损伤已被确定为干性AMD的主要致病因素之一,光感受器细胞受到各种来源的氧化应激刺激,导致视网膜退行性变,严重影响视力[5]。
核因子E2相关因子2(nuclear factor-erythroid 2-related factor 2,Nrf2)是机体发挥抗氧化应激反应的重要转录因子。基础状态下,Kelch样环氧氯丙烷相关蛋白1(Kelch-like ECH-associated protein-1,Keap1)与Nrf2在细胞质中结合,引起Nrf2降解;氧化应激时,Nrf2与Keap1解离,移位入核,与下游基因血红素单加氧酶(heme oxygenase-1,HO-1)结合,发挥抗氧化作用[6-7]。因此,通过激活Nrf2/Keap1信号通路,可增加细胞抗氧化反应能力,减轻细胞氧化损伤[8]。微RNA(microRNA,miRNA)可通过内源性RNA干扰机制抑制多种靶基因的表达,调节各种细胞功能[9]。已有研究[10]证明,多种miRNAs可通过调控Nrf2影响AMD发病,包括miR-144[11]、miR-141[12]、miR-626[13]等。但光感受器细胞中miRNAs对Nrf2的调控机制尚未完全明确。本研究通过细胞实验,研究在干性AMD中miR-125b通过Nrf2/Keap1信号通路对光感受器细胞氧化应激反应的调控作用。
1 材料与方法 1.1 材料小鼠视锥细胞系661W细胞由美国休斯顿大学Muayyad R. AL-UBAIDI教授赠予。DMEM培养液、青链霉素混合液、胰蛋白酶、PBS(中国江苏凯基生物公司),3%过氧化氢(H2O2)溶液、DMSO(美国SIGMA公司),胎牛血清(澳大利亚AusGeneX公司),RNAiso Plus、LipofectamineTM RNAiMAX、OPTI-MEM(美国Invitrogen公司),PrimerScript RT reagent Kit(日本TaKaRa公司)、TB Green premix Ex Taq Ⅱ(日本TaKaRa公司),增强型CCK-8试剂盒(美国Apexbio公司),mRNA引物(中国上海生工生物工程公司),miR-125b与RNU6B的RT引物、PCR引物、miR-125b模拟物、模拟物对照、抑制物、抑制物对照(中国广州锐博公司),SDS-PAGE胶(中国碧云天生物技术有限公司),PCR逆转录仪(美国BIO-RAD公司)。RT-PCR仪(美国AppliedBiosystem公司),荧光显微镜(日本Olympus公司)。
1.2 方法 1.2.1 细胞培养用含5%胎牛血清和1%青链霉素混合液的DMEM培养基,于37 ℃、5% CO2的培养箱中,培养661W细胞。待细胞生长至80%~90%融合后,用0.25%胰蛋白酶进行消化、传代,用于后续实验。
1.2.2 CCK-8试剂盒检测细胞增殖活性取对数生长期661W细胞消化并离心后,用含5%胎牛血清DMEM培养基重悬细胞,制成细胞悬液,以每孔2×104细胞接种于96孔板中。用正常培养细胞组作为对照组,用培养基不含细胞组作为空白对照组。用不同浓度H2O2(400,600,800,1 000 µmol/L)处理细胞6 h后,每孔加入10 µL CCK-8溶液,37 ℃培养箱中孵育1 h,用酶标仪检测450 nm波长处的吸光度值(A)。细胞增殖活性=(A实验组-A空白组)/(A对照组-A空白组)×100%。
1.2.3 细胞转染将661W细胞培养至30%~50%融合。用LipofectamineTM RNAiMAX和无血清Opti-MEM培养基将miR-125b模拟物、模拟物对照(100 nmol/L)和miR-125b抑制物、抑制物对照(30 nmol/L)分别转染至661W细胞,在37 ℃培养箱中继续培养48 h后,进行后续实验。
1.2.4 实时荧光定量PCR(qPCR)检测用TRIzol提取各组细胞的总RNA,用反转录试剂盒Primer Script RT reagent Kit反转录为cDNA,qPCR试剂盒TB Green premix Ex Taq Ⅱ检测miR-125b与Keap1/Nrf2/HO-1 mRNA的表达水平,RNU6B为miR-125b内参对照,GAPDH为Keap1/Nrf2/HO-1内参对照。所有操作均严格遵循说明书。引物序列见表 1。
| Gene | Forward primer sequence | Reverse primer sequence |
| Nrf2 | TAGATGACCATGAGTCGCTTGC | GCCAAACTTGCTCCATGTCC |
| Keap1 | GGAAAGTTTAAACGAGAAGCCTCTGGGCTCTG | GGAAATCTAGACCATCAGGATCTGCGTGTATT |
| HO-1 | TCTATCGTGCTCGCATGAAC | CTGTCTGTGAGGGACTCTGG |
| GAPDH | GTCTCCTCTGACTTCAACAGCG | ACCACCCTGTTGCTGTAGCCAA |
1.2.5 Western blotting检测
利用RIPA细胞裂解液提取各组细胞总蛋白,BCA法测定蛋白浓度。95 ℃水浴10 min变性,蛋白上样行SDS-PAGE凝胶电泳。转移至PVDF膜,5%脱脂奶粉室温封闭1 h。用Keap1抗体(1︰5 000)4 ℃过夜孵育,GAPDH作为内参对照。将孵育过一抗的PVDF膜用TBST洗3次,10 min/次,用山羊抗兔二抗(1︰5 000)室温孵育2 h,TBST洗膜3次,10 min/次。ECL发光显影,采用Image J软件分析条带灰度值。
1.3 统计学分析采用SPSS 25.0软件进行统计学分析,用GraphPad Prism 8作统计图。所有结果均以x±s表示;采用独立样本t检验和单因素方差分析对结果进行显著性比较,检验水准α=0.05。
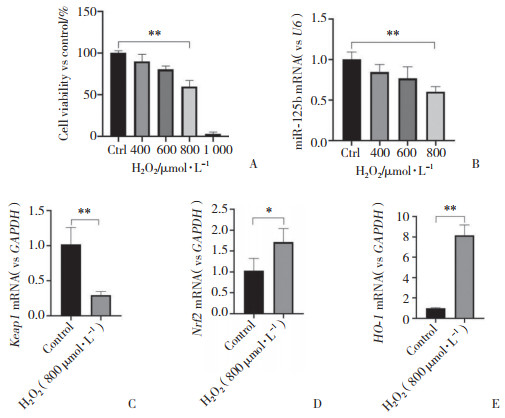
2 结果 2.1 661W细胞氧化应激模型中miR-125b与Keap1/Nrf2/HO-1 mRNA的表达分别利用400、600、800、1 000 µmol/L H2O2处理661W细胞6 h,用CCK-8试剂盒检测细胞活性变化。结果显示,当H2O2浓度为800 µmol/L时,细胞活性降低至50%左右,故后续试验选用800 µmol/L H2O2构建细胞氧化应激模型。qPCR结果显示,与对照组相比,随着H2O2浓度逐渐增加,miR-125b表达逐渐降低。661W细胞氧化应激模型中,Nrf2及其下游基因HO-1 mRNA表达升高,Keap1 mRNA表达降低,差异均有统计学意义(P < 0.05)。见图 1。说明661W细胞受到氧化应激刺激后,miR-125b表达降低,Nrf2及其下游基因HO-1表达水平升高,Keap1表达水平降低。
|
| A,oxidative stress model was established using H2O2;B,miR-125b expression in oxidative stress model of 661W cells;C to E,Keap1/Nrf2/HO-1 mRNA expression in oxidative stress model of 661W cells. *P < 0.05,**P < 0.01. Ctrl,control. 图 1 661W细胞氧化应激模型中miR-125b及Keap1/Nrf2/HO-1 mRNA的表达 Fig.1 Expression of miR-125b and Keap1/Nrf2/HO-1 mRNA in oxidative stress model of 661W cells |
2.2 miR-125b调控661W细胞氧化应激模型中Keap1/Nrf2/HO-1 mRNA的表达
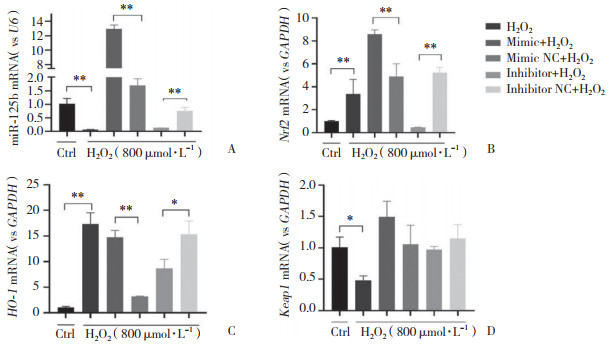
661W细胞氧化应激模型中,转染miR-125b模拟物组miR-125b、Nrf2和HO-1 mRNA的表达显著高于转染模拟物对照组,差异均有统计学意义(P < 0.05);转染miR-125b抑制物组miR-125b、Nrf2和HO-1 mRNA的表达水平显著低于转染抑制物对照组,差异均有统计学意义(P < 0.05);转染miR-125b模拟物组和转染miR-125b抑制物组分别与转染模拟物对照组和转染抑制物对照组比较,Keap1表达在mRNA水平无明显变化,见图 2。说明miR-125b可能通过调控Nrf2及HO-1 mRNA的表达以增强661W细胞抗氧化应激能力,但对Keap1 mRNA的表达无明显影响。
|
| A,expression of miR-125b after transfection of miR-125b mimic or inhibitor in oxidative stress model;B to D,expression of Keap1/Nrf2/HO-1 mRNA after transfection of miR-125b mimic or inhibitor in oxidative stress model. *P < 0.05,**P < 0.01. NC,negative control;Ctrl,control. 图 2 调控miR-125b对661W细胞氧化应激模型中Keap1/Nrf2/HO-1 mRNA表达的影响 Fig.2 Up- or down-regulating miR-125b affects expression of Keap1/Nrf2/HO-1 mRNA |
2.3 miR-125b通过在转录后水平调控Keap1蛋白表达调控Nrf2信号通路
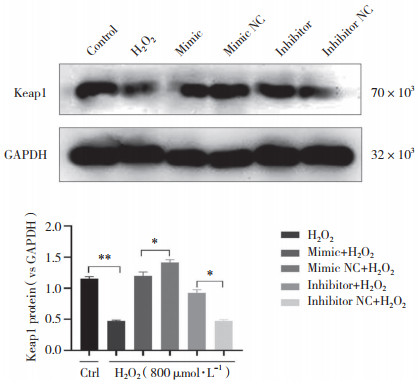
如前所述,661W细胞氧化应激模型中,miR-125b对Keap1 mRNA的表达无明显影响,Western blotting结果显示,转染miR-125b模拟物组Keap1的蛋白表达水平显著低于转染模拟物对照组;转染miR-125b抑制物组Keap1的蛋白表达水平显著高于转染抑制物对照组,差异均有统计学意义(P < 0.05)。见图 3。说明miR-125b可能通过在转录后水平调控Keap1蛋白的表达,调控Nrf2及HO-1的表达,从而促进661W细胞抗氧化应激能力。
|
| *P < 0.05,**P < 0.01. 图 3 调控miR-125b对Keap1蛋白表达水平的影响 Fig.3 Up- or down-regulating miR-125b affects expression of Keap1 protein |
3 讨论
干性AMD早期病变主要表现为玻璃膜疣形成,玻璃膜疣数目和大小的增加显著增加疾病进展的风险;干性AMD的晚期病变地图状萎缩的形成主要由光感受器和视网膜色素上皮(retinal pigment epithelium,RPE)细胞死亡引起[14]。视网膜由RPE和神经视网膜组成,其生理结构和高代谢活性对视觉功能至关重要,尤其容易受到氧化损伤。视网膜氧化损伤是包括AMD在内的视网膜退行性疾病的主要致病因素之一[15]。
Nrf2信号通路是体内主要的抗氧化信号通路之一,关于miRNAs对该通路的调控目前国内外尚未见明确报道。LAI等[16]发现,虾青素能够通过PI3K/Akt/Nrf2通路减少661W细胞中活性氧的产生,并抑制细胞凋亡。CARLOTTA等[17]发现2-乙酰基-5-四羟基丁基咪唑能够通过激活Nrf2/HO-1通路减轻H2O2诱导的661W细胞的氧化应激反应和细胞凋亡。此外,Nrf2激动剂RS9能够减轻光诱导的661W细胞损伤[18]。miR-125b与细胞增殖、迁移、凋亡和分化等密切相关[19]。YANG等[20]发现,miR-125b通过Keap1/Nrf2通路减轻肝损伤,并利用双荧光素酶报告基因系统验证了miR-125b与Keap1之间存在直接的连接位点,提示了miR-125b对Keap1/Nrf2直接的调控作用。
本研究利用H2O2构建光感受器细胞氧化应激模型,研究在干性AMD发病过程中miR-125b对抗氧化信号通路Keap1/Nrf2/HO-1可能的调控机制。结果显示,与对照组相比,miR-125b在光感受器细胞氧化应激模型中表达显著降低,Nrf2及其下游基因HO-1表达增加,Keap1表达降低,表明当光感受器细胞受到氧化刺激以后,Keap1表达减少,对Nrf2的锚定作用降低,因此Nrf2表达增加且移位入核发挥抗氧化作用。转染miR-125b模拟物后,Nrf2/HO-1表达增加,Keap1表达在mRNA水平无明显变化,在蛋白水平显著降低,提示miR-125b可能在转录后水平调控Keap1蛋白的表达,进而促进Nrf2/HO-1的表达,从而增强光感受器细胞的抗氧化能力,转染miR-125b抑制物的结果也证明了这一点。然而,miR-125b与Keap1之间的直接靶向关系还需将来进一步验证。
综上所述,miR-125b可促进光感受器细胞的抗氧化应激能力,该作用可能通过调控Keap1/Nrf2/HO-1信号通路实现。本研究利用细胞转染的方法调控miR-125b在光感受器细胞中的表达,初步论证了miR-125b在干性AMD发病过程中的调控作用,提示miR-125b可能成为干性AMD治疗的新靶点。
| [1] |
LI XH, HE SK, ZHAO MW. An updated review of the epigenetic mechanism underlying the pathogenesis of age-related macular degeneration[J]. Aging Dis, 2020, 11(5): 1219-1234. DOI:10.14336/AD.2019.1126 |
| [2] |
AMBATI J, FOWLER BJ. Mechanisms of age-related macular degeneration[J]. Neuron, 2012, 75(1): 26-39. DOI:10.1016/j.neuron.2012.06.018 |
| [3] |
黄洁, 吴星伟. 干性年龄相关性黄斑变性动物模型研究进展[J]. 中国中医眼科杂志, 2020, 30(7): 515-517. DOI:10.13444/j.cnki.zgzyykzz.2020.07.014 |
| [4] |
LAMBROS ML, PLAFKER SM. Oxidative stress and the Nrf2 anti-oxidant transcription factor in age-related macular degeneration[J]. Adv Exp Med Biol, 2016, 854: 67-72. DOI:10.1007/978-3-319-17121-0_10 |
| [5] |
CHAKRAVARTHY U, PETO T. Current perspective on age-related macular degeneration[J]. JAMA, 2020, 324(8): 794-795. DOI:10.1001/jama.2020.5576 |
| [6] |
KENSLER TW, WAKABAYASHI N, BISWAL S. Cell survival responses to environmental stresses via the Keap1-Nrf2-ARE pathway[J]. Annu Rev Pharmacol Toxicol, 2007, 47: 89-116. DOI:10.1146/annurev.pharmtox.46.120604.141046 |
| [7] |
RUIZ S, PERGOLA PE, ZAGER RA, et al. Targeting the transcription factor Nrf2 to ameliorate oxidative stress and inflammation in chronic kidney disease[J]. Kidney Int, 2013, 83(6): 1029-1041. DOI:10.1038/ki.2012.439 |
| [8] |
NAKAGAMI Y. Nrf2 is an attractive therapeutic target for retinal diseases[J]. Oxid Med Cell Longev, 2016, 2016: 7469326. DOI:10.1155/2016/7469326 |
| [9] |
LIN CW, CHANG YL, CHANG YC, et al. MicroRNA-135b promotes lung cancer metastasis by regulating multiple targets in the Hippo pathway and LZTS1[J]. Nat Commun, 2013, 4: 1877. DOI:10.1038/ncomms2876 |
| [10] |
NATOLI R, FERNANDO N. MicroRNA as therapeutics for age-related macular degeneration[J]. Adv Exp Med Biol, 2018, 1074: 37-43. DOI:10.1007/978-3-319-75402-4_5 |
| [11] |
JADEJA RN, JONES MA, ABDELRAHMAN AA, et al. Inhibiting microRNA-144 potentiates Nrf2-dependent antioxidant signaling in RPE and protects against oxidative stress-induced outer retinal degeneration[J]. Redox Biol, 2020, 28: 101336. DOI:10.1016/j.redox.2019.101336 |
| [12] |
CHENG LB, LI KR, YI N, et al. miRNA-141 attenuates UV-induced oxidative stress via activating Keap1-Nrf2 signaling in human retinal pigment epithelium cells and retinal ganglion cells[J]. Oncotarget, 2017, 8(8): 13186-13194. DOI:10.18632/oncotarget.14489 |
| [13] |
XU XZ, TANG Y, CHENG LB, et al. Targeting Keap1 by miR-626 protects retinal pigment epithelium cells from oxidative injury by activating Nrf2 signaling[J]. Free Radic Biol Med, 2019, 143: 387-396. DOI:10.1016/j.freeradbiomed.2019.08.024 |
| [14] |
GAO ML, WU KC, DENG WL, et al. Toll-like receptor 3 activation initiates photoreceptor cell death in vivo and in vitro[J]. Invest Ophthalmol Vis Sci, 2017, 58(2): 801-811. DOI:10.1167/iovs.16-20692 |
| [15] |
HAN SX, CHEN JJ, HUA JJ, et al. MITF protects against oxidative damage-induced retinal degeneration by regulating the NRF2 pathway in the retinal pigment epithelium[J]. Redox Biol, 2020, 34: 101537. DOI:10.1016/j.redox.2020.101537 |
| [16] |
LAI TT, YANG CM, YANG CH. Astaxanthin protects retinal photoreceptor cells against high glucose-induced oxidative stress by induction of antioxidant enzymes via the PI3K/Akt/Nrf2 pathway[J]. Antioxidants, 2020, 9(8): 729. DOI:10.3390/antiox9080729 |
| [17] |
FABIANI C, ZULUETA A, BONEZZI F, et al. 2-Acetyl-5-tetrahydroxybutyl imidazole (THI) protects 661W cells against oxidative stress[J]. Naunyn Schmiedeberg's Arch Pharmacol, 2017, 390(7): 741-751. DOI:10.1007/s00210-017-1374-3 |
| [18] |
INOUE Y, SHIMAZAWA M, NODA Y, et al. RS9, a novel Nrf2 activator, attenuates light-induced death of cells of photoreceptor cells and Müller Glia cells[J]. J Neurochem, 2017, 141(5): 750-765. DOI:10.1111/jnc.14029 |
| [19] |
ZHAO Y, LI X, ZHU SQ. rs78378222 polymorphism in the 3'-untranslated region of TP53 contributes to development of age-associated cataracts by modifying microRNA-125b-induced apoptosis of lens epithelial cells[J]. Mol Med Rep, 2016, 14(3): 2305-2310. DOI:10.3892/mmr.2016.5465 |
| [20] |
YANG D, YUAN Q, BALAKRISHNAN A, et al. MicroRNA-125b-5p mimic inhibits acute liver failure[J]. Nat Commun, 2016, 7: 11916. DOI:10.1038/ncomms11916 |
 2021, Vol. 50
2021, Vol. 50




