文章信息
- 王静, 陆晓萱, 蔡大利
- 免疫介导获得性因子ⅩⅢ缺乏症2例报道并文献复习
- Autoimmune acquired factor ⅩⅢ deficiency: a report of two cases and literature review
- 中国医科大学学报, 2021, 50(11): 1050-1053
- Journal of China Medical University, 2021, 50(11): 1050-1053
-
文章历史
- 收稿日期:2021-01-12
- 网络出版时间:2021-11-03 18:06
凝血因子ⅩⅢ,也称纤维蛋白稳定因子,参与凝血过程,可使疏松可溶性纤维蛋白多聚体转变为牢固高度机化的不溶性交联结构而促进血凝块稳定。因子ⅩⅢ缺乏症是一种罕见出血性疾病,发生率约为1/200万,占出血性疾病的4.7%[1],分为遗传性和获得性2种类型[2]。获得性因子ⅩⅢ缺乏症多见于老年人,根据发病机制可分为非免疫介导和免疫介导两种,此2种类型患者临床表现、诊断及治疗上差异显著[3]。非免疫介导获得性因子ⅩⅢ缺乏症由于ⅩⅢ因子消耗增加或合成减少导致。消耗增加见于大型手术、弥散性血管内凝血、败血症、血栓形成等;合成减少见于严重肝病、白血病、丙戊酸、托珠单抗等用药史,此种类型患者常见,出血症状较少。免疫介导获得性因子ⅩⅢ缺乏症(autoimmune acquired factor ⅩⅢ/13 deficiency,AAⅩⅢ/13D)罕见,患者常有严重出血而危及生命[3-4]。而临床上常规止凝血检查[血小板计数(blood platelet count,PLT)、血小板功能、凝血五项和血管性假性血友病抗原等]结果均正常,因此容易延误诊治,本研究报道我科室就诊的2例AAⅩⅢ/13D患者的临床特征及诊治经过,并进行相关的文献复习。
1 临床资料病例1,男,59岁。因“反复血尿10个月,左侧躯干皮肤瘀斑、局部肿胀6 d” 2019年9月26日在我院急诊就诊。患者病史包括:2018年12月无明显诱因出现血尿,行全腹CT检查未见明显异常,未经治疗,血尿逐渐减轻。2019年7月出现左下腹疼痛后再次出现肉眼血尿,就诊于中国医科大学附属盛京医院急诊科行双肾输尿管膀胱CT检查结果显示左侧盆壁包块,考虑血肿而采用抗炎治疗,但效果欠佳,2019年8月21日于我院泌尿外科实施右侧输尿管软镜检查术,患者术前PLT、血浆凝血酶原时间(prothrombin time,PT)、活化部分凝血活酶时间(activated partial thromboplastin time,APTT)、凝血酶时间(thrombin time,TT)均正常,术中见右肾盂黏膜出血,置入1枚双J管,术后血尿逐渐好转。2019年9月20日出现左侧肩背部多发肿胀、皮肤瘀斑,进行性加重,3 d后出现左腰部瘀斑、肿胀再次就诊于我院急诊。患者既往腔隙性脑梗死病史5个月,口服阿司匹林治疗;无自幼出血性疾病和家族史;无高血压、糖尿病、冠状动脉粥样硬化性心脏病病史;无重大手术、外伤史。辅助检查:血常规及常规筛查试验结果显示血小板及常规止、凝血功能测定未见异常,见表 1。
| 项目 | 病例1 | 病例2 | 正常值 |
| 血红蛋白(g/L) | 89 | 83 | 130~175 |
| 血小板(×109/L) | 202 | 167 | 125~350 |
| PT(s) | 13.1 | 13.1 | 11.0~13.7 |
| APTT(s) | 41.2 | 33.4 | 31.5~43.5 |
| TT(s) | 33.1 | - | 14.0~21.0 |
| 纤维蛋白原(g/L) | 6.55 | 4.13 | 2.00~4.00 |
| 血管性假性血友病因子抗原测定(%) | 328 | 114 | 50~160 |
| 免疫球蛋白(g/L) | |||
| IgG | 20.06 | 8.56 | 7.00~17.00 |
| IgA | 4.02 | 2.02 | 0.70~3.80 |
| IgM | 0.77 | 0.43 | 0.60~2.50 |
| 凝血因子XⅢ | 阳性 | 33.3% | 75.2%~154.8% |
| 肿瘤标志物 | 正常 | 正常 | |
| 风湿抗体系列 | 均阴性 | 均阴性 | |
| 狼疮抗凝物 | 均阴性 | 均阴性 | |
| 抗心磷脂抗体 | 均阴性 | 均阴性 | |
| 血清蛋白电泳 | 正常 | 正常 |
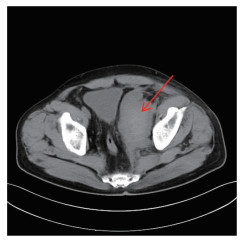
全腹增强CT检查结果显示,左侧盆壁可见约11.3 cm×5.5 cm团片状血性密度影,CT值32~63 Hu,增强扫描未见确切强化。影像学诊断为左侧盆壁血肿可能性大(图 1)。
|
| 图 1 病例1增强CT图像 |
患者血块稳定试验结果显示,纤维蛋白凝块4 h完全溶解,对照组24 h纤维蛋白凝块完全不溶解,临床诊断为因子ⅩⅢ缺乏症。结合临床、家族史和既往史考虑为AAⅩⅢ/13D。患者风湿抗体系列、狼疮抗凝物、抗心磷脂抗体测定、免疫球蛋白、肿瘤标志物、血清蛋白电泳未见异常。
治疗上停用阿司匹林,滤白病毒灭活血浆(400 mL)隔日输注1次,共5次。患者皮下血肿逐渐吸收,贫血明显好转。治疗期间(2019年10月1日)患者再发脑梗死(梗死区域为右侧基底节区、左侧半卵圆区及脑室旁、左侧额叶皮层下、双侧枕叶皮层下),考虑患者存在出血倾向,未采用溶栓、抗凝等治疗,仅给予营养神经治疗。14 d后出院,于当地医院行康复治疗。2019年10月16日患者出现恶心、呕吐,复查头CT提示大面积脑出血,位置与脑梗死位置相同,考虑不除外脑梗死后脑出血,2 d后患者因脑出血死亡。
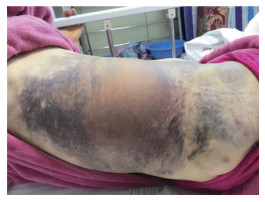
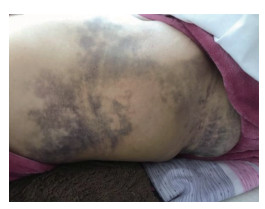
病例2,女,57岁。因“腰部疼痛,右侧腰背部瘀斑”2020年1月18日于我院急诊就诊。患者主诉半个月前无明显诱因出现腰部疼痛,无发热,无恶心、呕吐,无腹泻。10 d前右侧腰背部出现大片瘀斑,无牙龈出血、尿血和便血。查体显示右侧腰背部大片瘀斑(图 2),其他皮肤黏膜未见明显出血。既往病史为皮肤型红斑狼疮10年,目前口服强的松(15 mg)1次/d。无外伤史、自发性出血史及类似家族史。辅助检查结果显示常规止凝血指标未见异常,ⅩⅢ因子活性为33.3%。风湿抗体系列、补体未见明显异常,见表 1。全腹增强CT显示右侧腹壁及腹内血肿。临床诊断为获得性因子ⅩⅢ缺乏症,免疫介导性可能性大。继续口服强的松同时给予血浆输注治疗(400 mL/d,共4 d),患者腰痛、皮肤血肿明显减轻(图 3)。2020年6月随访时患者未再出血。
|
| 图 2 病例2右侧腰背部大片瘀斑 |
|
| 图 3 治疗后右侧腰背部瘀斑减轻 |
2 讨论
研究[5-6]显示,AAⅩⅢ/13D是由于患者体内产生了针对ⅩⅢ因子的自身抗体(抗体类型一般为IgG),常见于以下几种情况:(1)自身免疫性疾病,如系统性红斑狼疮、类风湿性关节炎、干燥综合征等;(2)实体瘤;(3)骨髓增殖性疾病、淋巴增殖性疾病和意义未明的单克隆免疫球蛋白血症;(4)药物,如异烟肼、青霉素、普鲁卡因胺、环丙沙星等;(5)先天性ⅩⅢ因子缺乏接受长期ⅩⅢ因子替代治疗;(6)怀孕等或不明原因。AAⅩⅢ/13D治疗上与非免疫介导性获得性因子ⅩⅢ缺乏症不同,仅仅依靠补充ⅩⅢ因子效果欠佳,需同时进行清除抗体治疗。本研究病例1因受条件限制未能检测自身抗体,完善自身免疫性疾病、肿瘤标志物等检查未能明确具体病因。而病例2既往多年皮肤型红斑狼疮病史,长期口服激素治疗,与既往报道相符。
本研究中,病例1以反复血尿起病,并伴盆壁、皮下、肌肉血肿;病例2亦无明显诱因出现皮下、肌肉血肿起病。MUSZBEK等[7]报道显示,AAⅩⅢ/13D通常表现为自发性或延迟的术后出血,在自发性出血患者中以皮下出血和肌肉出血为首发表现的占70%,颅内出血发生率约为13%~18%。另外,腹膜内、腹膜后出血发生率也较高。因此,AAⅩⅢ/13D是危及生命的严重出血性疾病。病例1在肌肉出血、尿血减轻的情况下,最终发生脑出血临床死亡;另外,患者脑出血部位与脑梗死部位相同,不除外脑梗死后脑出血,可见脑梗死可增加患者脑出血风险。
已有研究[8]表明,对于存在严重出血症状患者应该进行止凝血实验室筛查试验,包括血小板计数、凝血功能测定、血小板功能测定、血管性假性血友病抗原检测等。检测结果正常时,需考虑因子ⅩⅢ缺乏症的可能性,进而进一步行凝血因子活性检测。本研究病例1反复血尿,多次检查显示止凝血指标正常,病程持续数月无法确诊,因此需要血液专业医生增加对AAⅩⅢ/13D的认识。
目前关于ⅩⅢ因子的实验室检查依然存在挑战,具有特异度和灵敏度的ⅩⅢ因子功能测定检测方法并未确定和广泛应用[9]。相关的检查方法包括:(1)ⅩⅢ因子活性定性试验,常用于筛查,多数正常人纤维蛋白凝块溶解时间 > 24 h,< 1 h为阳性。灵敏度不高,若为阳性须做定量分析;(2)定量功能性ⅩⅢ因子活性测定,此方法已建议作为一线筛查试验[10];(3)抗原检测,检测ⅩⅢ-A、ⅩⅢ-B和(或)ⅩⅢ-A2B2抗原浓度来确定缺乏的亚型[10];(4)自身抗体可以在ⅩⅢ因子上具有不同的抗原靶标,包括ⅩⅢ-A、ⅩⅢ-B或2个亚基上的表位;(5)ⅩⅢ因子基因筛查:进行分子遗传缺陷分析。本研究2例患者均未能进行相关抗原、抗体及基因筛查,根据患者病史、临床经过等综合考虑诊断为AAⅩⅢ/13D,因此,临床上需开展相应的检查对患者进行分型诊断,从而使患者得到精准治疗。ICHINOSE等[5]报道因子ⅩⅢ缺乏症患者ⅩⅢ因子活性差异很大,ⅩⅢ因子活性平均为(8.5±8.2)%,中位活性为6%,活性越低越容易并发严重自发性出血,但目前对于可导致严重出血的临界ⅩⅢ因子活性值尚未明确。本研究病例2ⅩⅢ因子活性为33.3%,仅表现为严重皮下、肌肉出血,未发生危及生命的出血(颅内出血等)。
AAⅩⅢ/13D治疗上以控制出血和清除自身抗体为主[5, 7]。控制出血主要通过替代治疗,包括ⅩⅢ因子浓缩物制剂、重组ⅩⅢ因子制剂、冷沉淀、新鲜冰冻血浆等。其中,新鲜冰冻血浆和冷沉淀较易获得,而ⅩⅢ因子浓缩物制剂和重组ⅩⅢ因子制剂虽然不会增加输血相关的病毒感染,且具有较高的ⅩⅢ因子滴度,但一般医疗中心没有药物储备[11]。清除自身抗体主要通过免疫抑制剂治疗,包括环磷酰胺、糖皮质激素、利妥昔单抗、丙种球蛋白、血浆置换及免疫吸附治疗等。对于出血严重的患者,常需要联合治疗方案。本研究2例患者在给予多次血浆输注治疗后,未再新发出血,出血症状逐渐减轻,血红蛋白逐渐上升。但病例1未给予免疫抑制剂治疗,最终并发脑出血,可能与此相关;病例2因长期口服激素治疗,未再给予其他免疫抑制剂联合治疗,疾病控制最终好转出院,随访亦未再有出血。
综上所述,AAⅩⅢ/13D缺乏特征性改变,常规止凝血检查无法发现异常,极易延误诊治而危及生命,因此需要血液专业医生增加对本病的认识,同时临床需开展相应的实验室检查进行精确分型诊断,从而使患者获得精准治疗。
| [1] |
中华医学会血液学分会血栓与止血学组, 中国血友病协作组. 罕见遗传性出血性疾病诊断与治疗中国专家共识(2021年版)[J]. 中华血液学杂志, 2021, 42(2): 89-96. DOI:10.3760/cma.j.issn.0253-2727.2021.02.001 |
| [2] |
GREGORY TF, COOPER B. Case report of an acquired factor ⅩⅢ inhibitor: diagnosis and management[J]. Proc Bayl Univ Med Cent, 2006, 19(3): 221-223. DOI:10.1080/08998280.2006.11928166 |
| [3] |
YAN MTS, RYDZ N, GOODYEAR D, et al. Acquired factor ⅩⅢ deficiency: a review[J]. Transfus Apher Sci, 2018, 57(6): 724-730. DOI:10.1016/j.transci.2018.10.013 |
| [4] |
SCHROEDER V, KOHLER HP. Factor ⅩⅢ deficiency: an update[J]. Semin Thromb Hemost, 2013, 39(6): 632-641. DOI:10.1055/s-0033-1353392 |
| [5] |
ICHINOSE A, JAPANESE COLLABORATIVE RESEARCH GROUP ON AH13. Autoimmune acquired factor ⅩⅢ deficiency due to anti-factor ⅩⅢ/13 antibodies: a summary of 93 patients[J]. Blood Rev, 2017, 31(1): 37-45. DOI:10.1016/j.blre.2016.08.002 |
| [6] |
AHMAD F, SOLYMOSS S, POON MC, et al. Characterization of an acquired IgG inhibitor of coagulation factor ⅩⅢ in a patient with systemic lupus erythematosus[J]. Br J Haematol, 1996, 93(3): 700-703. DOI:10.1046/j.1365-2141.1996.d01-1678.x |
| [7] |
MUSZBEK L, KATONA É. Diagnosis and management of congenital and acquired FⅩⅢ deficiencies[J]. Semin Thromb Hemost, 2016, 42(4): 429-439. DOI:10.1055/s-0036-1572326 |
| [8] |
DORGALALEH A, RASHIDPANAH J. Blood coagulation factor ⅩⅢ and factor ⅩⅢ deficiency[J]. Blood Rev, 2016, 30(6): 461-475. DOI:10.1016/j.blre.2016.06.002 |
| [9] |
SCHROEDER V. Laboratory assessment of coagulation factor ⅩⅢ[J]. Hamostaseologie, 2020, 40(4): 467-471. DOI:10.1055/a-1181-0327 |
| [10] |
KOHLER HP, ICHINOSE A, SEITZ R, et al. Diagnosis and classification of factor ⅩⅢ deficiencies[J]. J Thromb Haemost, 2011, 9(7): 1404-1406. DOI:10.1111/j.1538-7836.2011.04315.x |
| [11] |
ODAME JE, CHAN AK, WU JK, et al. Factor ⅩⅢ deficiency management: a review of the literature[J]. Blood Coagul Fibrinolysis, 2014, 25(3): 199-205. DOI:10.1097/mbc.0000000000000029 |
 2021, Vol. 50
2021, Vol. 50




