文章信息
- 王晶, 李玉宏
- WANG Jing, LI Yuhong
- 三维全自动左心室容积定量技术在评价冠状动脉粥样硬化性心脏病患者左心收缩功能中的应用
- Application of three-dimensional fully automated left ventricular volume quantification technique in evaluating left heart systolic function in patients with coronary heart disease
- 中国医科大学学报, 2021, 50(10): 925-929
- Journal of China Medical University, 2021, 50(10): 925-929
-
文章历史
- 收稿日期:2020-11-24
- 网络出版时间:2021-09-30 10:54
冠状动脉粥样硬化性心脏病(简称冠心病)是全球关注的公共卫生问题,人口老龄化及危险因素的持续作用使其发病率仍然处于较高水平,随病情进展,可导致心力衰竭甚至猝死,造成巨大的精神和经济负担[1]。目前,冠状动脉造影是诊断冠心病的金标准,但该方法不能了解心室重构及缺血对心肌的影响程度。超声心动图是最便捷的检查方式,可以通过评估室壁运动情况、左心室容积及射血分数为临床诊断冠心病提供影像学依据,有助于监测冠心病患者药物治疗或PCI手术前后心功能变化,准确评估患者预后,及时调整治疗方案,减缓冠心病导致的心功能损伤。三维全自动左心室容积定量技术(3D-heart model,HM)是近年来发展的新技术,利用人工智能特点一键式测量左心室容积和射血分数[2-4],本研究旨在探讨HM技术在冠心病患者左心收缩功能的定量分析中的可行性和可重复性,为临床提供一种可快速、准确评估冠心病患者左心收缩功能的方法。
1 材料与方法 1.1 一般资料及分组选取2019年6月至2020年6月于锦州医科大学附属第一医院心内科住院的冠心病患者100例。排除RT-3DE声像图中左心室心肌17节段中3节段以上显示不清者;临床资料不全者;合并心律失常、瓣膜病变、先天性心脏病患者等。纳入标准:临床确诊冠心病患者符合《稳定性冠心病诊断与治疗指南》 [5];冠状动脉造影至少1支血管狭窄≥50%,超声心动图检查图像清晰者。
根据冠状动脉造影检查结果、心电图、病史及心肌酶学水平将患者分为冠心病心梗组(A组,n = 60),其中,男39例,女21例,年龄(58.750±14.498)岁,心率(77.280±12.408)次/min,收缩压为(126.520± 7.108)mmHg,舒张压为(79.580±7.198)mmHg;冠心病非心梗组(B组,n = 40),其中,男25例,女15例,年龄(59.050±11.325)岁,心率(72.880±11.241)次/min,收缩压为(125.200±7.148)mmHg,舒张压为(78.700± 7.304)mmHg。同期选取与病例组相匹配的正常对照组(C组,n = 50),既往均无心脏病史、高血压病史,行常规心电图及超声心动图检查均正常,其中,男30例,女20例,年龄(54.020±16.069)岁,心率(73.260± 9.398)次/min,收缩压为(125.180±6.365)mmHg,舒张压为(77.780±6.028)mmHg。本研究经本院伦理委员会审核通过,所有患者均签署知情同意书。
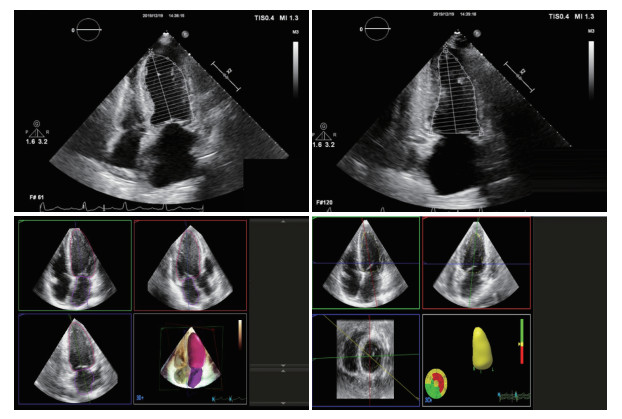
1.2 方法采用Philips EPIQ 7C型彩色多普勒超声诊断仪,探头X5-1,S5-1,频率1~5 MHz,内置3D-HM图像采集模式。嘱患者左侧卧位,连接心电图,必要时嘱患者改变体位并配合屏气,获得清晰内膜图像,分别记录图像采集时间(T1)、分析时间(T2)及总时间(T3)。双平面Simpson’s法:在心尖分别采集并存储4个周期心尖四腔观和两腔观动态图像;分别描绘心尖四腔观和两腔观的左心室舒张末和收缩末心内膜曲线,以Simpson’s法计算出左心室容积和射血分数。HM法:HM边界值设为舒张末60%,收缩末40%[6],心尖四腔观使左心室中心沿着轴线,点击屏幕上的HM ACQ按钮收集图像,启动HM自动分析获得HM结果。RT-3DE法:全容积模式下,存储4个心动周期心尖四腔观的动态图像,采用QLab 10.7软件3DQ Advance插件脱机分析,于舒张末和收缩末分别在心尖长轴四腔、两腔观二尖瓣环水平及左心室心尖部心内膜面标记5个参考点,获得RT-3DE结果。见图 1。
|
| 图 1 双平面Simpson’s法、HM法及RT-3DE法测量图像 Fig.1 Pictures of biplane Simpson's, HM and RT-3DE |
1.3 统计学分析
采用SPSS 23.0软件进行统计学分析。计数资料采用χ2检验。计量资料以x±s表示。多组间比较方差齐时采用单因素方差分析,方差不齐时采用非参数Kruskal-Wallis H检验;相关性分析采用Pearson相关性检验;采用Bland-Altman进行一致性检验,分析散点的分布与一致性界限的位置关系,若一致性界限在临床上可接受,则认为2种方法之间一致性较好。重复性检验采用组内相关系数(intraclass correlation coefficient,ICC),ICC < 0.4为重复性差,0.4~0.75为重复性好,> 0.75为重复性很好。P < 0.05为差异有统计学意义。
2 结果 2.1 3组一般资料比较3组年龄(F = 2.511,P = 0.081)、性别(F = 0.292,P = 0.864)、心率(F = 1.923,P = 0.150)、收缩压(F = 0.670,P = 0.513)、舒张压(F = 0.944,P = 0.392)比较,差异均无统计学意义。
2.2 HM法、Simpson’s法与RT-3DE法测量结果比较如表 1~3所示,HM法测得的左心室舒张末容积(left ventricular end-diastolic volume,LVEDV)、左心室收缩末容积(left ventricular end-systolic volume,LVESV)均高于RT-3DE法测得值,左心室射血分数(left ventricular ejection fraction,LVEF)无统计学差异;A、B组中HM法及RT-3DE法测得的LVEF略低于双平面Simpson’s法,而C组中3种方法测得的LVEF无统计学差异。HM法、Simpson’s法及RT-3DE法A组LVEDV及LVESV均高于B组及C组,LVEF低于B组和C组(均P < 0.05)。
| Method | n | LVEDV(mL) | LVESV(mL) | LVEF(%) |
| Simpson’s | 50 | 88.304±16.000 | 30.205±6.891 | 65.716±3.625 |
| 3D-HM | 50 | 93.500±14.7761) | 33.440±7.3411) | 64.440±3.775 |
| RT-3DE | 50 | 84.424±13.635 | 29.442±6.342 | 65.204±3.830 |
| F | 4.711 | 4.773 | 1.471 | |
| P | 0.010 | 0.010 | 0.233 | |
| 1)compared with RT-3DE,P < 0.05. | ||||
| Method | n | LVEDV(mL) | LVESV(mL) | LVEF(%) |
| Simpson’s | 60 | 146.825±47.7651) | 82.192±32.989 | 45.247±6.601 |
| 3D-HM | 60 | 151.900±44.8751) | 90.917±34.4721) | 41.283±7.1552) |
| RT-3DE | 60 | 125.488±35.230 | 73.453±27.158 | 42.715±6.5432) |
| F | 6.386 | 4.553 | 5.270 | |
| P | 0.002 | 0.012 | 0.006 | |
| 1)compared with RT-3DE,P < 0.05;2)compared with Simpson’s,P < 0.05. | ||||
| Method | n | LVEDV(mL) | LVESV(mL) | LVEF(%) |
| Simpson’s | 40 | 97.540±15.2091) | 36.855±6.606 | 62.088±3.000 |
| 3D-HM | 40 | 104.075±14.5711) | 42.695±7.4891) | 59.125±3.3372) |
| RT-3DE | 40 | 87.488±13.519 | 34.830±6.533 | 60.280±3.3172) |
| F | 13.375 | 14.053 | 8.592 | |
| P | < 0.001 | < 0.001 | < 0.001 | |
| 1)Compared with RT-3DE,P < 0.05;2)compared with Simpson’s,P < 0.05. | ||||
2.3 HM法、Simpson’s法与RT-3DE法测量结果相关性及一致性分析
HM法LVEDV、LVESV、LVEF测得值与RT-3DE法相关性高,一致性均在临床接受范围内,见表 4。
| Group | n | Simpson’s | 3D-HM | |||
| r | bias±LOA | r | bias±LOA | |||
| Group A | ||||||
| LVEDV(mL) | 60 | 0.842 | 21.337±51.501 | 0.842 | 26.412±47.763 | |
| LVESV(mL) | 60 | 0.894 | 8.738±29.300 | 0.904 | 17.463±29.912 | |
| LVEF(%) | 60 | 0.893 | 2.532±8.496 | 0.932 | -1.432±5.094 | |
| Group B | ||||||
| LVEDV(mL) | 40 | 0.848 | 10.053±15.849 | 0.882 | 16.588±13.538 | |
| LVESV(mL) | 40 | 0.891 | 2.025±6.007 | 0.924 | 7.865±5.672 | |
| LVEF(%) | 40 | 0.900 | 1.808±2.838 | 0.930 | -1.155±2.444 | |
| Group C | ||||||
| LVEDV(mL) | 50 | 0.863 | 3.880±15.856 | 0.910 | 9.076±11.986 | |
| LVESV(mL) | 50 | 0.918 | 0.763±5.351 | 0.936 | 3.998±5.155 | |
| LVEF(%) | 50 | 0.928 | 0.512±2.795 | 0.948 | -0.764±2.413 | |
| Group A,myocardial infarction;group B,non-myocardial infarction;group C,healthy control. | ||||||
2.4 3种方法测量时间比较
3D-HM法T1 [(8.127±0.932)s]、T2 [(21.198±3.246)s]及T3 [(29.325±4.136)s]均短于双平面Simpson’s法[(15.197±1.411,73.805±3.431,89.002±4.796)s] 及RT-3DE法[(13.736±1.311,79.547±3.772,93.282± 5.057)s],差异有统计学意义(P < 0.05)。
2.5 重复性检验从纳入的100例患者中随机抽取20例,由2名医师分别以HM法测量LVEDV、LVESV和LVEF,ICC分别为0.987,0.993,0.989;其中1名医师10 min后再次测量,ICC分别为0.996,0.996,0.990。
3 讨论由于冠状动脉发生粥样硬化管腔狭窄,导致冠心病心肌缺血,当斑块破裂或血管完全闭塞时发生心肌坏死,终末期并发心力衰竭。目前,临床上推荐冠心病患者使用双平面Simpson’s法评估左心收缩功能,但受几何假设及局部空间形态影响[7]。本研究中以RT-3DE作为评估的金标准,但是RT-3DE数据后处理需要繁琐的手动调节,主观性强且耗时。HM技术是飞利浦公司开发的一种全自动左心定量分析技术,可以实现在三维图像基础上一键式采集、分析,从而快速、准确测出左心室容积及射血分数,本研究对比分析了HM法的可行性。HM运用一种自适应智能分析算法,通过获取最优的边界识别左心室心内膜面,通过运动分析自动建立左心室3D模型,匹配大数据库中的模型,呈现左心室容积参数和射血分数值[4, 8]。
本研究结果显示,HM法测得的LVEDV及LVESV均高于RT-3DE法,这与BARLETTA等[3]研究结果相似,可能是由于图像分析的原理及对心内膜边界的界定不同,HM检测血流组织与致密心肌间界面,更易识别心内膜小梁,本研究中HM边界值设为舒张末期60%,收缩末期40%,与李萌等[6]研究一致,根据边界设定值识别心内膜区域并自动匹配数据库模型,而RT-3DE在界定界面时由操作者勾画内膜可能未将小梁纳入左心室心腔,导致其三维容积偏小,TAMBORINI等[9]研究也曾报道三维超声心动图测值小于心脏磁共振(cardiac magnetic resonance,CMR)。冠心病心梗组LVEDV及LVESV高于正常组,LVEF低于正常组,这是由于冠状动脉闭塞,心肌缺血坏死,出现左心室重构,代偿失调则会导致射血能力减低、心腔扩大等。本研究表明冠心病患者中HM法及RT-3DE法测得的LVEF略低于双平面Simpson’s法,可能是由于HM是在三维基础上建立的心脏模型,而双平面的二维心腔不能完全表示左心室整体结构,容积差异可导致LVEF的高估[10]。相关性和一致性分析中显示HM法与RT-3DE法存在正相关,且高于双平面Simpson’s法与RT-3DE法的相关性,一致性均在临床可接受范围内。HM法图像采集、分析时间均短于双平面Simpson’s法及RT-3DE法,可能由于后者图像采集时呼吸、体位移动等会造成图像拼接的错位,采集时间延长,后两者分析时均需要操作者主观描记心内膜,耗时较长。本研究还表明HM可重复性高,HM重复分析同一数据集时具有确定性收敛效应。
本研究的局限性在于样本量小;未与CMR金标准对比;未纳入心内膜图像欠清晰者,未研究HM局部编辑功能对于图像欠清晰者的价值。
综上所述,HM是一项重复性好、客观性强且快速、准确的心功能测定方法,对于长期监测冠心病患者左心功能的波动及评估治疗效果具有重要意义。
| [1] |
刘小清. 冠心病流行病学研究进展及疾病负担[J]. 中华心血管病杂志, 2008, 36(6): 573-576. DOI:10.3321/j.issn:0253-3758.2008.06.026 |
| [2] |
SUN L, FENG H, NI L, et al. Realization of fully automated quantification of left ventricular volumes and systolic function using transthoracic 3D echocardiography[J]. Cardiovasc Ultrasound, 2018, 16(1): 2. DOI:10.1186/s12947-017-0121-8 |
| [3] |
BARLETTA V, HINOJAR R, CARBONELL A, et al. Three-dimensional full automated software in the evaluation of the left ventricle function: from theory to clinical practice[J]. Int J Cardiovasc Imaging, 2018, 34(8): 1205-1213. DOI:10.1007/s10554-018-1336-y |
| [4] |
MEDVEDOFSKY D, MOR-AVI V, AMZULESCU M, et al. Three-dimensional echocardiographic quantification of the left-heart Chambers using an automated adaptive analytics algorithm: multicentre validation study[J]. Eur Heart J Cardiovasc Imaging, 2018, 19(1): 47-58. DOI:10.1093/ehjci/jew328 |
| [5] |
王斌, 李毅, 韩雅玲. 稳定性冠心病诊断与治疗指南[J]. 中华心血管病杂志, 2018, 46(9): 680-694. |
| [6] |
李萌, 金炫佚, 马春燕, 等. 三维全自动左心容积定量技术评价左心室容积及射血分数的可行性及影响因素[J]. 中国医学影像技术, 2019, 35(1): 63-68. DOI:10.13929/j.1003-3289.201805119 |
| [7] |
BADANO LP, MIGLIORANZA MH, MIHAILA S, et al. Left atrial volumes and function by three-dimensional echocardiography: reference values, accuracy, reproducibility, and comparison with two-dimensional echocardiographic measurements[J]. Circ Cardiovasc Imaging, 2016, 9(7): e004229-e004229. DOI:10.1161/CIRCIMAGING.115.004229 |
| [8] |
TSANG W, SALGO IS, MEDVEDOFSKY D, et al. Transthoracic 3D echocardiographic left heart chamber quantification using an automated adaptive analytics algorithm[J]. JACC Cardiovasc Imaging, 2016, 9(7): 769-782. DOI:10.1016/j.jcmg.2015.12.020 |
| [9] |
TAMBORINI G, PIAZZESE C, LANG RM, et al. Feasibility and accuracy of automated software for transthoracic three-dimensional left ventricular volume and function analysis: comparisons with two-dimensional echocardiography, three-dimensional transthoracic manual method, and cardiac magnetic resonance imaging[J]. J Am Soc Echocardiogr, 2017, 30(11): 1049-1058. DOI:10.1016/j.echo.2017.06.026 |
| [10] |
RODRIGUEZ-MAÑERO M, AZCÁRATE-AGÜERO P, KREIDIEH B, et al. Quantitative assessment of left ventricular size and function in cardiac transplant recipients: side-by-side comparison of real time two-dimensional echocardiography, contrast-enhanced two-dimensional echocardiography, three-dimensional echocardiography, and contrast-enhanced three-dimensional echocardiography as compared to magnetic resonance imaging[J]. Echocardiography, 2019, 36(2): 306-311. DOI:10.1111/echo.14232 |
 2021, Vol. 50
2021, Vol. 50




