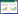文章信息
- 尤放, 王美莲
- YOU Fang, WANG Meilian
- DNA损伤修复通路因子53BP1在骨髓干细胞自我更新和分化发育中的作用
- Role of the DNA damage repair pathway factor, 53BP1, in the self-renewal and differentiation of bone marrow stem cells
- 中国医科大学学报, 2021, 50(1): 19-24
- Journal of China Medical University, 2021, 50(1): 19-24
-
文章历史
- 收稿日期:2020-04-14
- 网络出版时间:2020-12-23 9:49
维持基因组序列信息的完整性对于生物体的存在至关重要,细胞应对各种类型损伤因子所导致的DNA损伤主要是通过激活复杂而精细的DNA损伤应答(DNA damage response,DDR)通路[1]。具有细胞毒性的双链断裂损伤(double strand breaks,DSBs)是最为严重的DNA损伤形式之一,未得到正确处理的DSBs除可增加细胞的致死率外,还会增加癌症的易感性[2]。53BP1 (P53 binding protein 1)是一种蛋白质编码基因,在DSBs损伤相关信号转导通路中扮演极其重要的角色,主要参与并影响DSBs的修复决策[3]。53BP1是脊椎动物芽殖酵母Rad9和裂殖酵母Crb2/Rhp9检查点蛋白的直系同源蛋白。作为进化保守的DNA损伤检查点蛋白家族的一员,53BP1与p53结合可调节细胞周期进程和细胞增殖[4]。DSBs发生后,因损伤周围的染色质性质发生变化,高度磷酸化的53BP1迅速聚集于断裂位点。53BP1通过调控DNA末端处理方式及DSBs的动力学过程来避免产生突变修复的结果[5]。
近年来,对53BP1相关功能的探索一直是国内外科研领域的研究热点,53BP1与诸多体内生理反应间均存在联系,本研究拟探讨53BP1对骨髓干细胞(bone marrow stem cell,BMSC)自我更新及分化的影响,从干性细胞周期检查点入手,着眼于53BP1对BMSC数量和质量的控制,重点研究53BP1与BMSC自我更新及分化过程的内在联系。
1 材料与方法 1.1 动物、细胞及主要试剂C56/7小鼠购自辽宁长生生物技术有限公司,C2C12细胞由本实验室保存,ProCount Progenitor Cell Enumeration Kit (美国BD公司),HRP-labeled Goat Anti-Mouse IgG (H+L) (北京鼎国生物技术有限公司),Anti-53BP1抗体(美国Novus Biologicals公司),Anti-Mouse-CD117 (c-Kit) PE抗体(美国PeproTech公司),Anti-Mouse-Ly6A/E (Sca-1) -Biotin抗体(英国Abcam公司),Lineage Cell Dection Cocktail-Biotin,Mouse组合抗体(德国Miltenyi Biotec公司),FITC anti-mouse CD4和粒系分化抗原-1 (gran-ulocyte differentiation antigen-1,Gr-1)单克隆抗体(美国Lsbio公司)。
1.2 构建53BP1全身敲除小鼠模型以小鼠53BP1的cDNA片段为探针从129小鼠基因组DNA噬菌体文库中分离出53BP1小鼠基因组DNA,克隆至pZErO-2质粒,通过将外显子替换构建靶向载体,线性化后电转入129/Sv小鼠的胚胎干细胞(embryonic stem cells,ESCs)中。利用分子杂交筛选出约200个G418抗性ES克隆。靶向注射获得嵌合体小鼠后同C57/6小鼠杂交,成功杂交鼠将用于获得53BP1-/-小鼠。此外,选取3 d的胚胎独立培养,并严格按照国际标准程序建立胚胎细胞系。
1.3 细胞分选及其表面分子标记检测 1.3.1 小鼠骨髓细胞的分离和计数麻醉后处死小鼠,消毒后分离双侧股骨和左右胫骨,小心剔除软组织,抽取2 mL的缓冲液彻底冲洗骨髓腔,获得骨髓血后,使用滤器及筛网过滤,胰蛋白酶消化30 min,加入2 mL的伊斯科夫改良的杜贝克培养基(Iscove’s modified Dubecco’s medium,IMDM) 1 000 r/min离心5 min,制备单细胞悬液,基于2个胫骨和2个股骨包含小鼠体内所有骨髓细胞25%的假设,通过细胞分析仪进行计数。
1.3.2 细胞分选使用2 mL IMDM冲洗骨髓细胞,加入Gey’s Lysis Buffer,冰上孵育10 min。用预混的抗体混合物于冰上标记30 min,加入1:100稀释的链霉亲和素结合的量子红(streptavidin-conjugated quantum red,SAQR)试剂,免疫染色30 min。流式细胞分选仪进行分选,每个样本取40×106进行染色分选,流速控制为约200/s,分选纯度≥97%。
1.3.3 细胞表面分子标记检测收集待染细胞,进行染色和固定,上机检测,打印本次实验分析报告。
1.4 细胞培养及诱导分化C2C12细胞培养于杜贝克改良培养基(Dulbecco’s modified Eagle’s medium,DMEM),放置于CO2振荡孵箱中培养。诱导分化培养基由添加2%马血清的DMEM组成,当细胞融合率达90%,更换为分化培养基(differentiation medium,DM)。分选获得的KSL细胞培养于IMDM,需向其中添加相应细胞因子混合物。
粒细胞-巨噬细胞集落形成单位(granulocyte-macrophage colony forming unit,CFU-GM)体外检测跟据加拿大STEMCELL Technologies公司的生产商指示说明进行操作。培养5~7 d后,评估菌落形成的数量。
1.5 53BP1表达检测 1.5.1 DAPI荧光染色观察53BP1表达情况细胞预处理,使用预冷的甲醇固定,Triton X-100透膜,PBS清洗,DAPI染色,封片,荧光显微镜下观察并拍照留存。
1.5.2 Western blotting检测53BP1蛋白的表达含量提取细胞总蛋白,并进行蛋白质浓度测定,RIPA稀释后,取样进行SDS-PAGE电泳,转膜,封闭,抗体杂交,ECL化学发光。
1.6 Co-IP检测磷酸化修饰蛋白免疫共沉淀(co-immunoprecipitation,Co-IP):加入750 μL细胞裂解液,用细胞刮刀刮取细胞,转移至EP管中,冰上裂解30 min,每间隔10 min,使用涡旋仪混合5 s,4 ℃,13 000 r/min离心10 min,吸取上清,4 ℃过夜;次日,涡旋磁珠5 min,取30 μL重悬的磁珠,PBS洗涤,于磁力架上进行磁性分离;加入500 μL预先稀释的相应抗体,孵育15 min,每间隔5 min使用涡旋混匀器5 s,磁性分离后收集磁珠,变性洗脱,吸取上清,煮样5 min进行SDS-PAGE电泳。
1.7 统计学分析收集相关数据,分对照组(WT)和实验组(Mut) 2组。采用SPSS 22.0进行统计学分析,计量资料以x±s表示,采用双侧t检验进行比较,Graphpad Prism 8.0制图,P < 0.05为差异有统计学意义。
2 结果 2.1 53BP1对小鼠胚胎形成和细胞分化的影响伴随小鼠胚胎不断发育形成,53BP1表达呈下降趋势,12 d可见WT组53BP1大量表达,Mut组无表达,16 d观察到WT组53BP1表达显著减少,Mut组无表达,18 d 2组均未观察到53BP1表达,见图 1A。伴随ESCs、KSL细胞和C2C12细胞分化发育过程进行,53BP1表达呈上升趋势,表达量均显著增加。24 h见53BP1微量表达,48 h后53BP1表达增加,主要位于细胞质中,72 h观察见53BP1逐渐由胞质向细胞核扩散,最终大量弥散表达于所有ESCs中,见图 1B。伴随KSL细胞分化进行,53BP1表达递增,5 d 2组均未观察到53BP1的表达,10 d可见WT组53BP1在KSL细胞中大量表达,Mut组无表达,见图 1C。就C2C12细胞而言,1 d未观察到53BP1的表达,4 d可见53BP1的表达量显著增加,见图 1D。以上结果表明53BP1主要作用于小鼠胚胎形成早期,伴随ESCs、C2C12细胞及KSL细胞的分化进行,53BP1表达量显著增加,证实了53BP1参与BMSC的分化发育过程。
|
| A, levels of 53BP1 during mouse embryogenesis; B, levels of 53BP1 in embryonic stem cells; C, levels of 53BP1 in KSL cells; D, levels of 53BP1 in C2C12 cells. DAPI, 4', 6-diamidino-2-phenylindole. 图 1 53BP1对小鼠胚胎形成和细胞分化的影响×200 Fig.1 Changes in 53BP1 levels during mouse embryogenesis and cell differentiation ×200 |
2.2 53BP1对KSL细胞总数、细胞周期及表面分子标记的影响
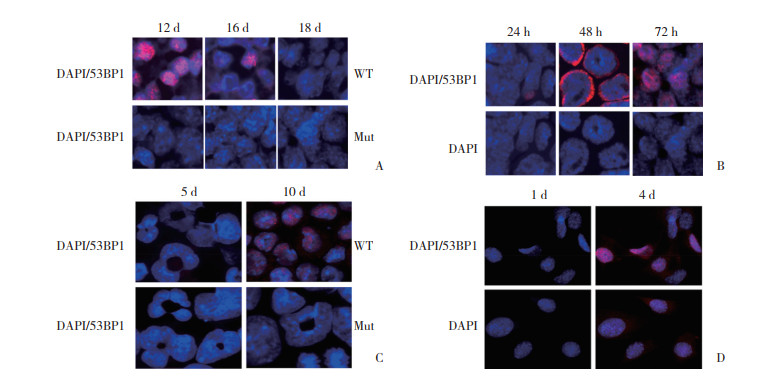
结果显示,53BP1参与并影响KSL细胞的自我更新过程,53BP1基因敲除可影响KSL细胞分化过程中表面分子标记的表达。53BP1基因敲除使得KSL细胞总数较之于WT组显著减少,WT组KSL细胞数量为0.093±0.010,Mut组KSL细胞数量为0.033±0.006,差异有统计学意义(P = 0.003),见图 2A。53BP1基因敲除与否并不显著影响处于细胞周期静息期(G0期)及细胞间期(G1期)的KSL细胞百分含量,G0期WT组KSL细胞百分含量为88.333±5.774,Mut组KSL细胞百分含量为86.667±3.055,差异无统计学意义(P = 0.681);G1期WT组KSL细胞百分含量为11.667±5.774,Mut组KSL细胞百分含量为13.333±3.055,差异无统计学意义(P = 0.681),见图 2B。53BP1基因敲除使得KSL细胞表面干性分子标记CD34+表达较之于WT组显著减少,WT组CD34+KSL细胞数量为0.073±0.014,Mut组CD34+KSL细胞数量为0.013±0.007,差异有统计学意义(P = 0.007),见图 2C。53BP1基因敲除与否并不显著影响KSL细胞表面标记CD34-的表达,WT组CD34-KSL细胞数量为0.021±0.001,Mut组CD34-KSL细胞数量为0.020±0.003,差异无统计学意义(P = 0.789),见图 2D。53BP1基因敲除与否并不显著影响体外培养的KSL细胞的生长速率,差异无统计学意义(P = 0.742),见图 2E。53BP1基因敲除使得体外培养的KSL细胞伴随分化进行,其表面分子标记Mar/Gr-1+百分含量显著增加,WT组Mar/Gr-1+相对百分含量为24.250±5.737,Mut组Mar/Gr-1+相对百分含量为49.250±12.580,差异有统计学意义(P = 0.011),见图 2F;53BP1基因敲除使得KSL细胞表面标记CD45+表达则明显减少,WT组CD45+KSL细胞数量为34.500±4.796,Mut组CD45+KSL细胞数量为15.750±4.349,差异有统计学意义(P = 0.001),见图 2G。
|
| A, total number of KSL cells; B, KSL cells in the G0/G1 phase; C, CD34+ KSL cells; D, CD34-KSL cells; E, growth curves of KSL cells; F, Mar/Gr-1+ cells; G, CD45+ cells.* P < 0.05 vs WT group. WT, wild-type; Mut, mutant. 图 2 53BP1对KSL细胞总数、细胞周期及表面分子标记的影响 Fig.2 Effects of 53BP1 on the number of KSL cells, the cell cycle, and surface molecular markers |
2.3 53BP1对PBL细胞定向分化的影响
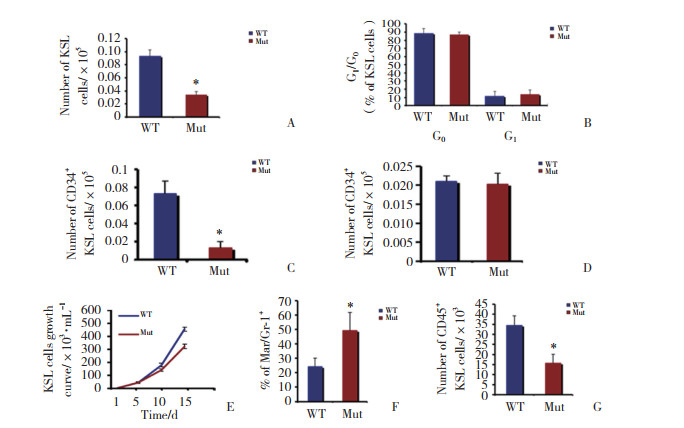
53BP1基因敲除使得外周血淋巴细胞(peripheral blood lymphocytes,PBL)定向分化产生的单核细胞、嗜酸性粒细胞、嗜碱性粒细胞较WT组均显著增加,差异有统计学意义(P分别为 < 0.001、0.004和0.002)。结果显示,53BP1可影响BMSC的分化发育过程,53BP1基因敲除可使定向分化产生的单核细胞、嗜酸性粒细胞和嗜碱性粒细胞细胞显著增加。见图 3。
|
| A, monocytes; B, eosinophils; C, basophils. The horizontal lines indicate the means. * P < 0.05 vs WT group. WT, wild-type; Mut, mutant. 图 3 53BP1对PBL定向分化的影响 Fig.3 Effects of 53BP1 on the directional differentiation of peripheral blood lymphocytes |
2.4 53BP1对磷酸化修饰蛋白表达的影响
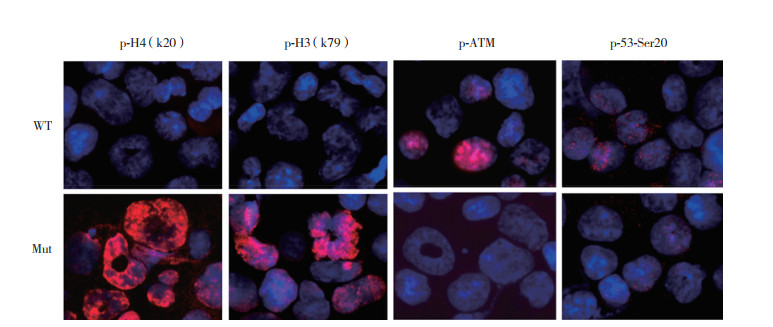
53BP1基因敲除可显著影响磷酸化修饰蛋白p-H4 (k20)、p-H3 (k79)、p-ATM和p-53-Ser20的表达水平。53BP1基因敲除上调了p-H4 (k20)和p-H3 (k79) 2种磷酸化修饰蛋白的表达水平,WT组未观察到上述2种蛋白的表达;此外,53BP1基因敲除导致p-ATM和p-53-Ser20蛋白表达显著减少,见图 4。
|
| 图 4 53BP1对磷酸化修饰蛋白表达的影响×200 Fig.4 Effect of 53BP1 on the expression of phosphorylated proteins ×200 |
3 讨论
ESCs具有较高的同组重组(homologous recom-bination,HR)发生频率,并伴有DSBs修复。延迟ESCs中细胞周期G1/S的转变可形成含有53BP1的核小体,并抑制ssDNA的堆积[6]。C2C12细胞作为经典成体干细胞模型,来源于小鼠成肌细胞株的亚克隆,在体外经诱导分化,可形成富含蛋白质的多核肌管[7]。造血干细胞(hematopoietic stem cells,HSCs)缺乏成熟血细胞标志物的表达,不表达Lin家族蛋白,故被称为Lin-细胞。c-kit的表达是HSCs的主要表型特征,作为受体与其配体干细胞因子(stem cell factor,SCF)的相互作用可触发一系列信号转导事件。小鼠骨髓中的KSL细胞,即表达c-kit和Sca-1的Lin-细胞群,具有极强的多向分化潜能和自我更新能力,可在体外培养条件下进行细胞增殖及分化[8]。伴随ESCs、C2C12细胞和KSL细胞分化的进行,53BP1表达量均显著增加,这证实了本研究关于53BP1可影响BMSC分化发育过程的推测。
CD34+可广泛高水平表达于早期造血干/祖细胞,随着细胞不断成熟,其表达则呈进化性下降,乃至最终消失,可作为多能干细胞向髓系定向分化的标志[9]。经γ射线辐射诱导后CD34+的HSCs相比于成熟淋巴细胞,53BP1蛋白的招募水平提升,DNA修复能力亦随之增强[10]。Gr-1高水平表达于中性粒细胞表面,亦可表达于记忆型T细胞以及树突状细胞的表面。肿瘤浸润的Gr-1+骨髓细胞可拮抗衰老[11]。CD45分子可选择性表达于除红细胞、血小板和浆细胞以外的所有造血细胞表面。髓系细胞的成熟度和分化程度越高,其表达CD45分子量相应也越多[12]。53BP1基因敲除使得KSL细胞表面标记Mar/Gr-1+百分含量显著增加,而CD34+和CD45+分子标记表达则明显减少,提示53BP1参与并影响KSL细胞的自我更新及分化发育过程,53BP1基因敲除可影响KSL细胞表面分子标记的表达。
细胞周期静息期(G0期)细胞随暂时停止分裂活动但仍保存相应潜力,受刺激后亦可继续进行增殖,而细胞间期(G1期)则作为细胞周期调节主要阶段,其阻留决定了细胞周期的进展方向。53BP1基因敲除与否并不显著影响处于细胞周期G0/G1的KSL细胞百分含量。53BP1基因敲除后,发现KSL细胞的生长曲线较之于WT组稍有下降,但并不显著。
p-H4 (k20)可伴随有丝分裂细胞周期的进展显著增加,p-H3 (k79)同信号转导和基因转录密切相关[13]。p-ATM在DNA修复的激活、多种致癌途径以及基因组完整性的维持中起扮演关键角色[14]。p-53-Ser20的存在对细胞生长具有抑制作用[15]。本研究发现53BP1基因敲除后p-H4 (k20)和p-H3 (k79)含量显著增多,但p-ATM和p-53-Ser20显著减少,据此推测53BP1可影响这4种磷酸化蛋白的表达水平,进而影响BMSC的自我更新和分化发育过程。
综上,DNA损伤通路因子53BP1参与并影响BMSC的自我更新及定向分化过程,这一结论将为日后对于53BP1功能更为深入的探索提供新的理论基础与支撑,使其进入更加广阔的研究领域。
| [1] |
WUNDERLICH R, RUEHLE PF, DELOCH L, et al. Interconnection between DNA damage, senescence, inflammation, and cancer[J]. Front Biosci, 2017, 22: 348-369. DOI:10.2741/4488 |
| [2] |
SHERILL-ROFE D, RAHAT D, FINDLAY S, et al. Mapping global and local coevolution across 600 species to identify novel homologous recombination repair genes[J]. Genome Res, 2019, 29(3): 439-448. DOI:10.1101/gr.241414.118 |
| [3] |
EKE I, ZONG DL, ARYANKALAYIL MJ, et al. 53BP1/RIF1 signaling promotes cell survival after multifractionated radiotherapy[J]. Nucleic Acids Res, 2020, 48(3): 1314-1326. DOI:10.1093/nar/gkz1139 |
| [4] |
GUO X, BAI Y, ZHAO M, et al. Acetylation of 53BP1 dictates the DNA double strand break repair pathway[J]. Nucleic Acids Res, 2018, 46(2): 689-703. DOI:10.1093/nar/gkx1208 |
| [5] |
VILLA M, BONETTI D, CARRARO M, et al. Rad9/53BP1 protects stalled replication forks from degradation in Mec1/ATR-defective cells[J]. EMBO Rep, 2018, 19(2): 351-367. DOI:10.15252/embr.201744910 |
| [6] |
ZHOU ZC, WANG LL, GE FX, et al. Pold3 is required for genomic stability and telomere integrity in embryonic stem cells and meiosis[J]. Nucleic Acids Res, 2018, 46(7): 3468-3486. DOI:10.1093/nar/gky098 |
| [7] |
MATSUBARA T, URATA M, NAKAJIMA T, et al. Geranylgeraniol-induced myogenic differentiation of C2C12 cells[J]. In Vivo, 2018, 32(6): 1427-1431. DOI:10.21873/invivo.11395 |
| [8] |
GOLAN K, KUMARI A, KOLLET O, et al. Daily onset of light and darkness differentially controls hematopoietic stem cell differentiation and maintenance[J]. Cell Stem Cell, 2018, 23(4): 572-585.e7. DOI:10.1016/j.stem.2018.08.002 |
| [9] |
VISWANATHAN C, KULKARNI R, BOPARDIKAR A, et al. Significance of CD34 negative hematopoietic stem cells and CD34 positive mesenchymal stem cells - a valuable dimension to the current understanding[J]. Curr Stem Cell Res Ther, 2017, 12(6): 476-483. DOI:10.2174/1574888x12666170502095625 |
| [10] |
JAKL L, MARKOVÁ E, KOLÁRIKOVÁ L, et al. Biodosimetry of low dose ionizing radiation using DNA repair foci in human lymphocytes[J]. Genes, 2020, 11(1): 58. DOI:10.3390/genes11010058 |
| [11] |
WU Q, ZHU YH, XU J, et al. Lactobacillus rhamnosus GR-1 ameliorates Escherichia coli-induced activation of NLRP3 and NLRC4 inflammasomes with differential requirement for ASC[J]. Front Microbiol, 2018, 9: 1661. DOI:10.3389/fmicb.2018.01661 |
| [12] |
AL-AGHBAR MA, CHU YS, CHEN BM, et al. High-affinity ligands can trigger T cell receptor signaling without CD45 segregation[J]. Front Immunol, 2018, 9: 713. DOI:10.3389/fimmu.2018.00713 |
| [13] |
WEI SH, LI CX, YIN ZN, et al. Histone methylation in DNA repair and clinical practice:new findings during the past 5-years[J]. J Cancer, 2018, 9(12): 2072-2081. DOI:10.7150/jca.23427 |
| [14] |
BAKKENIST CJ, CZAMBEL RK, LIN Y, et al. Quantitative analysis of ATM phosphorylation in lymphocytes[J]. DNA Repair, 2019, 80: 1-7. DOI:10.1016/j.dnarep.2019.06.002 |
| [15] |
FU XM, WU SH, LI B, et al. Functions of p53 in pluripotent stem cells[J]. Protein Cell, 2020, 11(1): 71-78. DOI:10.1007/s13238-019-00665-x |
 2021, Vol. 50
2021, Vol. 50