文章信息
- 王雪, 李琳, 张红, 张雪, 王振华
- WANG Xue, LI Lin, ZHANG Hong, ZHANG Xue, WANG Zhenhua
- 长链非编码RNA RUNX1-IT1对口腔鳞状细胞癌增殖、迁移的影响及其作用机制
- Effect of long non-coding RNA RUNX1-IT1 on proliferation and migration of oral squamous cell carcinoma and its actional mechanism
- 中国医科大学学报, 2020, 49(9): 824-828, 834
- Journal of China Medical University, 2020, 49(9): 824-828, 834
-
文章历史
- 收稿日期:2019-09-12
- 网络出版时间:2020-09-11 10:07
2. 中国医科大学 附属口腔医院干诊科, 沈阳 110002
2. VIP Department, School and Hospital of Stomatology, China Medical University, Shenyang 110002, China
口腔鳞状细胞癌(oral squamous cell carcinoma,OSCC)是具有高转移率和高复发率的恶性肿瘤,约占口腔癌的90% [1]。目前手术仍为主要治疗方式,但患者术后易发生转移和复发,5年生存率仅为50%[2]。因此,寻找OSCC的发病和转移机制十分重要。长链非编码RNA(long non-coding RNA,lncRNA)是一种没有编码蛋白能力的RNA。越来越多的证据表明lncRNA在OSCC的进展中发挥调控作用[3-5]。lncRNA RUNX1-IT1位于染色体21q22.12区域,长约1 502个核苷酸,研究[6-7]表明它在结直肠癌和胃癌中发挥调控作用,然而lncRNA RUNX1-IT1在OSCC中的功能和机制尚未明确。本研究通过体外实验探讨lncRNA RUNX1-IT1对OSCC增殖、迁移的影响及其作用机制。
1 材料与方法 1.1 材料 1.1.1 标本来源收集2018年5月至2019年2月期间中国医科大学附属口腔医院颌面外科手术切除的47例OSCC癌组织和癌旁正常组织,OSCC的诊断依据组织病理学确定。标本收集前经中国医科大学附属口腔医院伦理委员会批准,并经患者知情同意。
1.1.2 细胞培养OSCC细胞系CAL27、SCC25均购于美国ATCC细胞库。HaCaT购于中国典型培养物保藏中心细胞库。CAL27、HaCaT以DMEM高糖培养基(含有10%的胎牛血清)培养,SCC25以DMEM/F12培养基培养,培养液中加入10%胎牛血清,400 ng/mL氢化可的松,0.5 mmol/mL丙酮酸钠。细胞于37 ℃,5%CO2培养箱中培养。
1.2 方法 1.2.1 实时qPCR用Trizol法提取组织和细胞RNA。采用PrimeScriptTMRT reagent Kit试剂盒进行反转录。利用SYBR®Premix Ex Taq Ⅱ在LightCycler®480Ⅱ实时PCR仪上进行实时定量PCR反应。引物序列:lncRNA RUNX1-IT1,上游引物5’-GGACACGCAGAGGAAGTCAA-3’,下游引物5’-GTTCTTGAGGTTGGCGGAGA-3’;GAPDH,上游引物5’-CGGATTTGGTCGTATTGGG-3’,下游引物5’-CTGGAAGATGGTGATGGGATT-3’。以2-ΔΔCt法计算结果。
1.2.2 载体构建和细胞转染过表达慢病毒载体购于上海吉玛基因公司,当CAL27细胞密度达到70%~80%时进行转染。取CAL27分为LV5组(对照组)和LV-RUNX1-IT1组(实验组),用1 μg /mL嘌呤霉素构建稳定细胞系。SiRNA购于广州锐博公司,采用lipofectamine 2000进行转染。转染空白载体细胞为si-NC组,转染lncRNA RUNX1-IT1沉默载体细胞为si-RUNX1-IT1组。
1.2.3 细胞增殖细胞增殖能力用CCK8检测。常规胰酶消化细胞后在96孔板内接种100 μL对照组和实验组细胞悬液,含2 000个细胞。在37 ℃孵箱内孵育24、48、72、96 h。每孔加入10 μL CCK8试剂孵育1 h,在450 nm波长处测定吸光度。
1.2.4 细胞周期细胞消化后用PBS洗涤细胞(2 000 r/min,5 min)并收集,加入70%冷乙醇固定4 ℃过夜。根据细胞周期试剂盒说明书加入500 μL PI/RNaseA染色,室温避光30~60 min后流式细胞仪采集数据并分析。
1.2.5 Transwell实验向Transwell小室上方加入含1×105个细胞的200 μL无血清培养基,下室加入600 μL含10%胎牛血清的培养液,37 ℃孵育48 h。弃掉培养基,将上室置于甲醇固定1 min,苏木素染色3 min和伊红染色15~30 s。倒置显微镜随机取图并计数。
1.2.6 Western blotting采用全蛋白试剂盒提取细胞总蛋白,SDS-PAGE凝胶电泳后,常规转膜。加入一抗(E-cadherin、N-cadherin、β-catenin、Vimentin、PCNA、Cyclin D1、MMP2、β-actin)孵育4 ℃过夜,然后加入二抗,孵育1.5 h。利用凝胶成像仪采集图像。
1.3 统计学分析运用SPSS 20.0统计软件进行数据分析。采用非参数检验方法分析lncRNA RUNX1-IT1表达水平和OSCC患者临床病理资料的相关性。计量资料以x±s表示,2组比较采用配对t检验。P < 0.05为差异有统计学意义。
2 结果 2.1 lncRNA RUNX1-IT1在OSCC中的表达利用实时qPCR检测47例OSCC患者lncRNA RUNX1-IT1的表达,结果显示,38例(81%)OSCC癌组织lncRNA RUNX1-IT1表达(6.03±2.73)显著高于癌旁正常组织(7.04±2.75,P < 0.001)。lncRNA RUNX1-IT1在OSCC细胞系CAL27(13.19±0.92)、SCC25(8.55±1.17)表达显著高于正常细胞系HaCaT(1.00±0.00,P < 0.01)。lncRNA RUNX1-IT1相对表达水平和淋巴结转移相关(P < 0.05),见表 1。这些结果说明lncRNA RUNX1-IT1的高表达可能在OSCC转移过程中发挥重要作用。
| Characteristics | n | lncRNA RUNX1-IT1 expression | P |
| Gender | 0.440 | ||
| Male | 34 | 3.517±3.639 | |
| Female | 13 | 3.738±2.988 | |
| Age(year) | 0.138 | ||
| < 60 | 17 | 4.447±3.729 | |
| ≥60 | 30 | 3.285±3.227 | |
| Smoking | 0.991 | ||
| Yes | 27 | 3.656±3.695 | |
| No | 20 | 3.473±3.156 | |
| Drinking | 0.881 | ||
| Yes | 22 | 3.653±3.892 | |
| No | 25 | 3.512±3.071 | |
| Tumor size | 0.313 | ||
| < 4cm | 28 | 2.959±2.698 | |
| ≥4cm | 19 | 4.489±4.226 | |
| Differentiation | 0.190 | ||
| Poor/moderate | 36 | 3.901±3.638 | |
| Well | 11 | 2.521±2.557 | |
| TNM stage | 0.862 | ||
| Ⅰ-Ⅱ | 19 | 3.189±2.536 | |
| Ⅲ-Ⅳ | 28 | 3.842±3.963 | |
| Lymph node metastasis | 0.023 | ||
| Yes | 25 | 4.696±3.955 | |
| No | 22 | 2.307±2.210 |
2.2 lncRNA RUNX1-IT1对CAL27细胞增殖的影响
过表达和沉默lncRNA RUNX1-IT1后实时qPCR检测转染效率。结果显示,与LV5组(1.00±0.00)比较,LV-RUNX1-IT1组(48.44±7.33)中lncRNA RUNX1-IT1表达水平显著增高(P < 0.01);与si-NC组(1.00±0.00)比较,si-RUNX1-IT1组(0.24±0.06)lncRNA RUNX1-IT1表达水平显著降低(P < 0.01)。
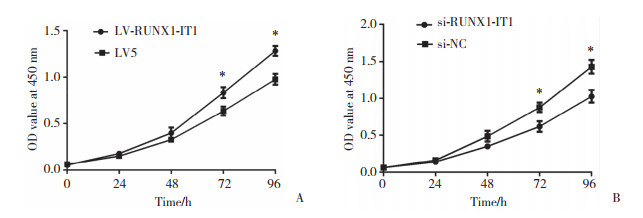
CCK8实验结果显示,与LV5组比较,LV-RUNX1-IT1组在72、96 h OD值明显增高(P < 0.05),细胞增殖活性显著增强(图 1A);lncRNA RUNX1-IT1沉默后,si-RUNX1-IT1组在72、96 h OD值明显降低(P < 0.05),细胞增殖活性显著减弱(图 1B)。
|
| A, CAL27 cells transfected with LV-RUNX1-IT1; B, CAL27 cells transfected with si-RUNX1-IT1. *P < 0.05 vs LV5 group or si-NC group. 图 1 lncRNA RUNX1-IT1对CAL27细胞增殖的影响 Fig.1 Effect of CAL27 cell proliferation on lncRNA RUNX1-IT1 |
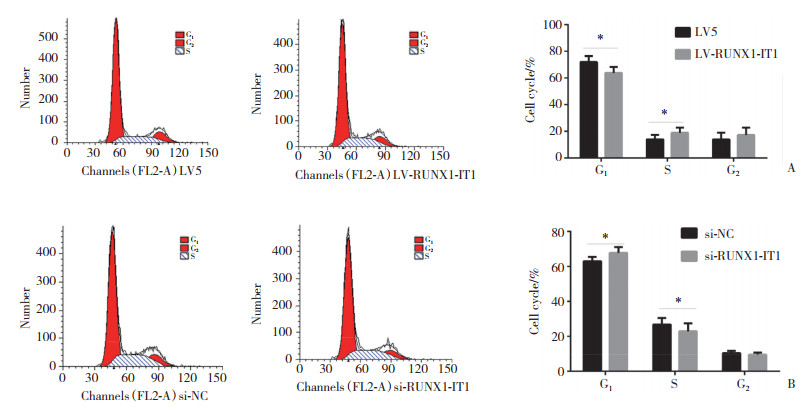
流式细胞术检测结果显示,与LV5组比较,LV-RUNX1-IT1组G1期细胞显著减少,S期细胞显著增加;而沉默lncRNA RUNX1-IT1后细胞阻滞在G1期,G1期细胞显著增加,S期细胞显著减少,见图 2。
|
| A, cell distribution between LV5 and LV-RUNX1-IT1; B, cell distribution between si-NC and si-RUNX1-IT1. *P < 0.05 vs LV5 group or si-NC group. 图 2 流式细胞术细胞周期分析结果 Fig.2 Results of cell cycle analysis by flow cytometry |
2.3 lncRNA RUNX1-IT1对CAL27细胞迁移的影响
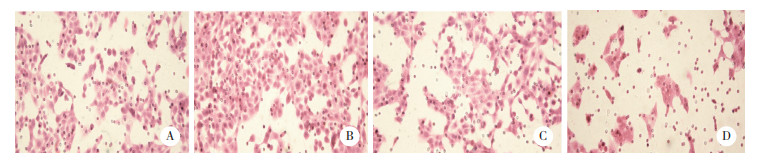
Transwell结果显示,LV5组、LV-RUNX1-IT1组、si-NC组、si-RUNX1-IT1组细胞迁移数量分别为110±14、214±10、109±9、54±5。与LV5组比较,LV-RUNX1-IT1组CAL27细胞迁移数量增多(P < 0.01),提示过表达lncRNA RUNX1-IT1后细胞迁移能力显著增强;与si-NC组比较,si-RUNX1-IT1组CAL27细胞迁移数量显著减少(P < 0.01),提示沉默lncRNA RUNX1-IT1后细胞迁移能力显著减弱,见图 3。
|
| A, LV5 group; B, LV-RUNX1-IT1 group; C, si-NC group; D, si-RUNX1-IT1 group. 图 3 lncRNA RUNX1-IT1对CAL27细胞迁移的影响×200 Fig.3 Effect of CAL27 cell migration on lncRNA RUNX1-IT1 ×200 |
2.4 过表达的lncRNA RUNX1-IT1促进CAL27细胞上皮-间质转化(epithelial-mesenchymal transition,EMT)
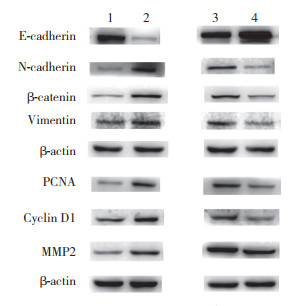
Western blotting检测EMT相关标志物结果显示,过表达lncRNA RUNX1-IT1后,与LV5组比较,LV-RUNX1-IT1组上皮标志物E-cadherin显著减少(P < 0.01),而间充质标志物N-cadherin、β-catenin、Vimentin(均P < 0.05)显著增多,促进了上皮细胞向间质细胞转换;沉默lncRNA RUNX1-IT1后发现结果与之相反,抑制了上皮细胞向间质细胞转化。PCNA、Cyclin D1和MMP2蛋白水平均在lncRNA RUNX1-IT1过表达后显著上调;在lncRNA RUNX1-IT1沉默后显著下调。以上结果表明lncRNA RUNX1-IT1可能通过调控EMT促进CAL27细胞增殖和迁移,见表 2、图 4。
| Item | LV5 group | LV-RUNX1-IT1 group | si-NC group | si-RUNX1-IT1 group |
| E-cadherin | 1.00±0.00 | 0.28±0.051) | 1.00±0.00 | 1.73±0.102) |
| N-cadherin | 1.00±0.00 | 2.26±0.161) | 1.00±0.00 | 0.34±0.072) |
| β-catenin | 1.00±0.00 | 1.78±0.201) | 1.00±0.00 | 0.43±0.062) |
| Vimentin | 1.00±0.00 | 1.41±0.111) | 1.00±0.00 | 0.48±0.062) |
| PCNA | 1.00±0.00 | 1.60±0.101) | 1.00±0.00 | 0.39±0.092) |
| Cyclin D1 | 1.00±0.00 | 1.48±0.051) | 1.00±0.00 | 0.38±0.072) |
| MMP2 | 1.00±0.00 | 1.59±0.081) | 1.00±0.00 | 0.46±0.052) |
| 1)P < 0.05 vs LV5 group;2)P < 0.01 vs si-NC group. | ||||
|
| 1, LV5 group; 2, LV-RUNX1-IT1 group; 3, si-NC group; 4, si-RUNX1-IT1 group. 图 4 各组EMT相关蛋白表达结果 Fig.4 Expression of EMT-related proteins in all groups |
3 讨论
近年来,研究[8-10]表明,lncRNA的异常表达可能与癌症(胃癌、卵巢癌和乳腺癌等)的预后和转移相关。本研究结果显示lncRNA RUNX1-IT1在OSCC组织和细胞中高表达,lncRNA RUNX1-IT1的表达和淋巴结转移显著相关,这说明lncRNA RUNX1-IT1高表达可能参与OSCC的转移过程。
已有研究[11]显示,lncRNA生长特异抑制物5(growth arrest-specific 5,GAS5)过表达通过激活PTEN/AKT轴抑制OSCC细胞的增殖和侵袭。lncRNA母系表达基因3(maternally expressed gene 3,MEG3)吸附miR-548d-3p调节JAK-STAT通路抑制OSCC的迁移并促进凋亡[12]。本研究结果发现过表达lncRNA RUNX1-IT1促进CAL27细胞的增殖和迁移,加快细胞从G1期向S期分化;而沉默lncRNA RUNX1-IT1抑制CAL27细胞的增殖和迁移,使细胞阻滞在G1期。
已有研究[13]认为EMT是细胞骨架重组、上皮细胞逐渐向间质细胞转化的过程,其特点在于细胞形态学的变化。在这个过程中,上皮标志物(E-cadherin)减少而间充质标志物(N-cadherin、Vimentin)增加,使细胞具有更强的迁移和运动能力。转录因子Snail可以诱导EMT的发生,通过降解MMP2和介导靶基因Cyclin D1转录,调节膀胱癌细胞增殖、凋亡、侵袭和迁移[14]。lncRNA肝癌高表达转录本(highly upregulated in liver cancer,HULC)在OSCC中高表达,敲除HULC后抑制了EMT过程,从而影响癌细胞的增殖和侵袭[15]。本研究结果显示过表达lncRNA RUNX1-IT1后E-cadherin显著减少,而N-cadherin、β-catenin、Vimentin显著增多;沉默lncRNA RUNX1-IT1后结果与之相反。PCNA是细胞增殖相关的蛋白。细胞周期从G1期向S期分化时,Cyclin D1的水平发生了改变。MMP2作为MMP家族的一员在细胞发生侵袭和迁移时发挥重要作用。PCNA、Cyclin D1和MMP2的表达水平均在lncRNA RUNX1-IT1过表达后显著上调,在lncRNA RUNX1-IT1沉默后显著下调。以上结果提示lncRNA RUNX1-IT1诱导CAL27细胞EMT的发生。
综上所述,本研究首次发现lncRNA RUNX1-IT1在OSCC组织和CAL27、SCC25细胞中显著高表达,lncRNA RUNX1-IT1高表达可以促进细胞增殖、加快细胞从G1期向S期分化,促进细胞迁移和EMT等恶性生物学行为,这为OSCC的研究提供了新的方向。
| [1] |
HEALY CM, MORAN GP. The microbiome and oral cancer:more questions than answers[J]. Oral Oncol, 2019, 89: 30-33. DOI:10.1016/j.oraloncology.2018.12.003 |
| [2] |
BRANDS MT, BRENNAN PA, VERBEEK ALM, et al. Follow-up after curative treatment for oral squamous cell carcinoma[J]. Eur J Surg Oncol, 2018, 44(5): 559-565. DOI:10.1016/j.ejso.2018.01.004 |
| [3] |
ZHOU X, LIU S, CAI GS, et al. Long non coding RNA MALAT1 promotes tumor growth and metastasis by inducing epithelial-mesenchymal transition in oral squamous cell carcinoma[J]. Sci Rep, 2015, 5: 15972. DOI:10.1038/srep15972 |
| [4] |
WANG Y, ZHANG XJ, WANG Z, et al. lncRNA-p23154 promotes the invasion-metastasis potential of oral squamous cell carcinoma by regulating Glut1-mediated glycolysis[J]. Cancer Lett, 2018, 434: 172-183. DOI:10.1016/j.canlet.2018.07.016 |
| [5] |
SUN CC, ZHANG L, LI G, et al. The lncRNA PDIA3P interacts with miR-185-5p to modulate oral squamous cell carcinoma progression by targeting cyclin D2[J]. Mol Ther Nucleic Acids, 2017, 9: 100-110. DOI:10.1016/j.omtn.2017.08.015 |
| [6] |
SHI JX, ZHONG X, SONG YX, et al. Long non-coding RNA RUNX1-IT1 plays a tumour-suppressive role in colorectal cancer by inhibiting cell proliferation and migration[J]. Cell Biochem Funct, 2019, 37(1): 11-20. DOI:10.1002/cbf.3368 |
| [7] |
YANG ZG, ZHI QM, WANG D, et al. Long noncoding RNA C21 or F96 promotes the migration, invasion and lymph node metastasis in gastric cancer[J]. Anticancer Agents Med Chem, 2016, 16(9): 1101-1108. DOI:10.2174/1871520616666151116122921 |
| [8] |
SONG YX, SUN JX, ZHAO JH, et al. Non-coding RNAs participate in the regulatory network of CLDN4 via Cerna mediated miRNA evasion[J]. Nat Commun, 2017, 8(1): 289. DOI:10.1038/s41467-017-00304-1 |
| [9] |
ZHU LF, GUO QX, LU XX, et al. CTD-2020K17, a novel long non-coding RNA, promotes migration, invasion, and proliferation of serous ovarian cancer cells in vitro[J]. Med Sci Monit, 2018, 24: 1329-1339. DOI:10.12659/msm.908456 |
| [10] |
WANG MZ, WANG MS, WANG ZN, et al. Long non-coding RNA-CTD-2108O9.1 represses breast cancer metastasis by influencing leukemia inhibitory factor receptor[J]. Cancer Sci, 2018, 109(6): 1764-1774. DOI:10.1111/cas.13592 |
| [11] |
ZENG BH, LI Y, JIANG FF, et al. lncRNA GAS5 suppresses proliferation, migration, invasion, and epithelial-mesenchymal transition in oral squamous cell carcinoma by regulating the miR-21/PTEN axis[J]. Exp Cell Res, 2019, 374(2): 365-373. DOI:10.1016/j.yexcr.2018.12.014 |
| [12] |
TAN JW, XIANG LX, XU GC. lncRNA MEG3 suppresses migration and promotes apoptosis by sponging miR-548d-3p to modulate JAK-STAT pathway in oral squamous cell carcinoma[J]. IUBMB Life, 2019, 71(7): 882-890. DOI:10.1002/iub.2012 |
| [13] |
ZHANG Y, WEINBERG RA. Epithelial-to-mesenchymal transition in cancer:complexity and opportunities[J]. Front Med, 2018, 12(4): 361-373. DOI:10.1007/s11684-018-0656-6 |
| [14] |
SHAN YJ, ZHANG LW, BAO YP, et al. Epithelial-mesenchymal transition, a novel target of sulforaphane via COX-2/MMP2, 9/Snail, ZEB1 and miR-200c/ZEB1 pathways in human bladder cancer cells[J]. J Nutr Biochem, 2013, 24(6): 1062-1069. DOI:10.1016/j.jnutbio.2012.08.004 |
| [15] |
SU W, TANG J, WANG YF, et al. Long non-coding RNA highly up-regulated in liver cancer promotes epithelial-to-mesenchymal transition process in oral squamous cell carcinoma[J]. J Cell Mol Med, 2019, 23(4): 2645-2655. DOI:10.1111/jcmm.14160 |
 2020, Vol. 49
2020, Vol. 49




