文章信息
- 田广伟, 李楠, 李光
- TIAN Guangwei, LI Nan, LI Guang
- 基于公共数据库分析PEG3基因在肺腺癌中的表达及预后意义
- The prognostic significance of PEG3 gene expression in lung adenocarcinoma using online public databases
- 中国医科大学学报, 2020, 49(9): 793-797
- Journal of China Medical University, 2020, 49(9): 793-797
-
文章历史
- 收稿日期:2019-07-11
- 网络出版时间:2020-09-11 10:06
近年来, 肺癌的发病率及死亡率均呈逐渐上升趋势, 是癌症死亡的首要原因。非小细胞肺癌(non-small cell lung cancer, NSCLC)约占肺癌的80%左右, 其中腺癌是NSCLC中常见的病理类型, 早期易发生血行转移, 尽管目前针对肺腺癌的治疗手段较多, 但其5年生存率仍不理想[1]。
PEG3基因编码kruppel C2H2型锌指蛋白, 其转录本可编码1572个氨基酸序列[2]。PEG3蛋白参与Wnt[3]、p53[4]、NF-κB[5]等多条信号通路, 调控调亡[4]、自噬[6]等重要生物学过程, 在肿瘤研究中PEG3基因作为抑癌基因, 被证实在子宫颈癌[7]及胶质瘤[3]中能抑制肿瘤的生长。
PEG3作为人类的印迹基因, 位于染色体19q13.43上[2]。由于PEG3基因包含一些非编码区域, 目前有多个研究[8-9]探讨了与PEG3相关的非编码RNA。但PEG3在肺腺癌中是否发挥作用, 及其与肺腺癌发生、发展的关系, 目前尚无相关研究。本研究通过公共数据库分析PEG3基因在肺腺癌中的表达及其对预后的影响, 为进一步研究PEG3在肺腺癌发生发展过程中的作用奠定了基础。
1 材料与方法 1.1 TIMER和人类蛋白质图谱数据库应用TIMER数据库[10] (www.cistrome.shinyapps.io/timer)分析PEG3在TCGA肺腺癌数据库中的mRNA表达情况。人类蛋白质表达图谱(THE HUMAN PROTEIN ATLAS, www.proteinatlas.org)分析PEG3在肺癌TCGA数据库中的预后情况。
1.2 Kaplan-Meier曲线数据库应用Kaplan-Meier曲线(Kaplan-Meier Plotter, www.kmplot.com)数据库网站分析PEG3在肺腺癌数据库中的预后情况。
1.3 LinkedOmics公共网站应用LinkedOmics公共网站[11] (www.linkedomics.org/login.php)中的LinkFinder模块分析PEG3表达与肺腺癌临床病理特征的关系, TCGA中运用HiSeqRNA平台的RNAseq数据, 分析PEG3 mRNA的表达水平与肺腺癌临床病理特征的关系。
1.4 MethHC数据库应用MethHC数据库[12]分析PEG3基因在正常肺组织和肺腺癌组织中的甲基化模式, 并分析甲基化和表达之间的关系。
1.5 TargetScanHuman数据库应用TargetScanHuman数据库[13] (www.targetscan.org) 2018年3月在线的7.2版本在线分析PEG3相关的微小RNA (microRNA, miRNA)。
1.6 STRING数据库采用STRING数据库(www.string-db.org/)对PEG3基因进行蛋白相互作用的网络分析。
1.7 统计学分析肺腺癌与正常肺组织中PEG3基因的表达差异采用t检验。PEG3基因表达与患者预后的关系采用Kaplan-Meier模型进行生存分析。采用在线统计学分析数据, P < 0.05为差异有统计学意义。
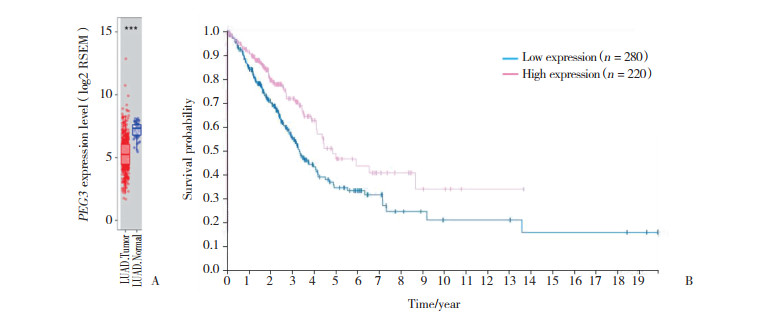
2 结果 2.1 PEG3 mRNA在肺腺癌及正常肺组织中的表达情况通过TCGA数据库分析PEG3 mRNA在肺腺癌的表达情况, 其中包括肺腺癌组织483例, 正常肺组织347例。结果显示, 与正常肺组织相比, PEG3 mRNA在肺腺癌中表达显著降低, 差异有统计学意义(P < 0.001, 图 1A)。
|
| A, the difference in PEG3 expression between normal lung tissue and lung adenocarcinoma based on TCGA database search; B, the overall survival curves of lung adenocarcinoma patients with high and low PEG3 mRNA levels. 图 1 TCGA数据库中肺腺癌PEG3 mRNA表达水平及预后分析 Fig.1 PEG3 mRNA expression and prognosis data of lung adenocarcinoma patients from the TCGA database |
2.2 PEG3 mRNA表达与肺腺癌预后的关系
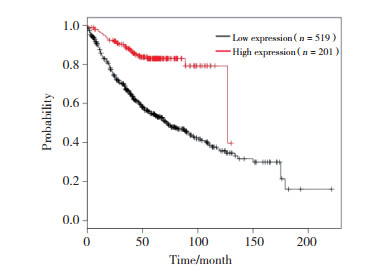
与PEG3 mRNA高表达(n = 220)的肺腺癌相比, PEG3 mRNA低表达(n = 280)的肺腺癌患者总生存率明显提高, 5年生存率分别为49%和35%, 差异有统计学意义(P = 0.002 2, 图 1B)。为进一步验证其预后意义, 通过Kaplan-Meier Plotter在线网站再次分析其在肺腺癌组织中高低表达与肺腺癌患者预后的相关性。结果发现, PEG3 mRNA的表达情况与总生存率明显有关, 高表达组的死亡风险较低表达组有下降趋势(HR=0.3, 95%CI:0.21~0.43, P < 0.001, 图 2)。与TCGA肺腺癌数据库中的结果一致。
|
| 图 2 Kaplan-Meier Plotter肺腺癌PEG3表达的总体生存期曲线 Fig.2 The overall survival curves of lung adenocarcinoma patients with high and low PEG3 mRNA levels generated using Kaplan-Meier Plotter |
2.3 PEG3 mRNA表达与肺腺癌临床病理特征的关系
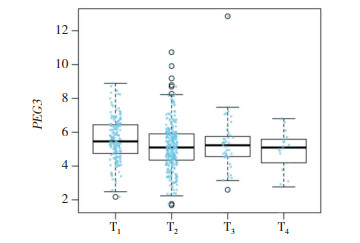
通过LinkedOmics在线分析PEG3 mRNA与肺腺癌临床病理特征的关系, 结果发现, PEG3的表达仅与肿瘤T分期有相关性(P < 0.005, 图 3);与N分期(P = 0.06)、M分期(P = 0.24)、病理分级(P = 0.07)和种族(P = 0.25)不相关。
|
| 图 3 PEG3 mRNA表达与肺腺癌T分期的关系 Fig.3 Correlation between the PEG3 mRNA expression and T staging of lung adenocarcinoma |
2.4 PEG3启动子区DNA甲基化水平分析
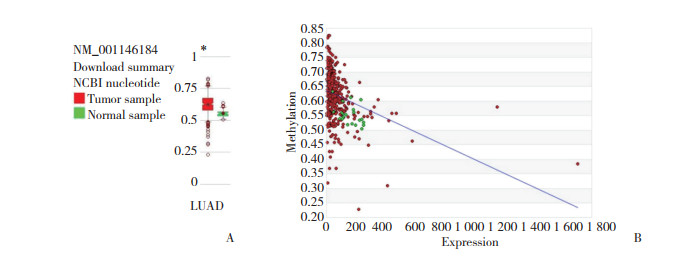
在MethHC数据库中, PEG3有NM_001146184、NM_001146185、NM_001146186、NM_001146187、NM_006210共5个转录模板。其中, NM_001146184、NM_001146185、NM_001146187、NM_006210在肺腺癌中甲基化水平均较正常肺组织高(P < 0.005)。以NM_001146184为例, 肺腺癌中PEG3基因启动子区甲基化水平较正常组织显著升高。见图 4。
|
| A, the boxplot of PEG3 promoter methylation data from TCGA database; B, the scatter plot of PEG3 promoter methylation data from TCGA database.Green represents normal lung tissue and red represents lung adenocarcinoma tissue. *P < 0.05. 图 4 PEG3基因NM_001146184转录本在肺腺癌和正常组织中甲基化情况 Fig.4 The methylation level of PEG3 (NM_001146184) transcript in lung adenocarcinoma and normal lung tissues |
2.5 PEG3基因相关的miRNA预测
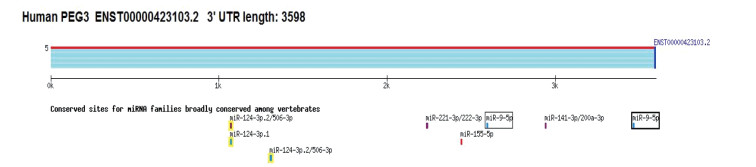
TargetScanHuman数据库预测结果显示, miR-124-3p.2/506-3p、miR-124-3p.1、miR-9-5p、miR-221-3p/222-3p、miR-141-3p/200a-3p和miR-155-5p可能与PEG3相关。见图 5。
|
| 图 5 TargetScanHuman分析PEG3相关的miRNA Fig.5 TargetScanHuman analysis of PEG3-related miRNA |
2.6 PEG3蛋白相互作用网络
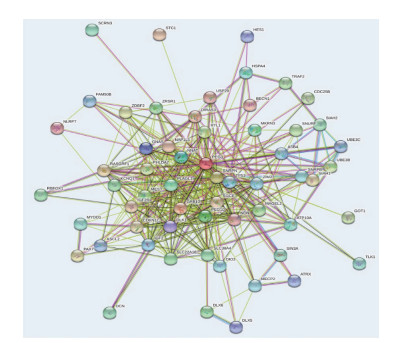
在STRING网站中选择物种为人类, 置信度选择为0.400, 相互作用最大数选择60 (图 6)。PEG3的作用蛋白包括TP53和BECLIN1, 均是影响凋亡及自噬的关键蛋白。GO富集分析发现PEG3主要参与蛋白印记、调控染色质构型、发育进程、细胞周期、甲基化和凋亡等。
|
| 图 6 STRING分析PEG3相互作用的蛋白 Fig.6 STRING analysis of PEG3-related proteins |
3 讨论
肺腺癌是肺癌常见的病理分型之一, 目前对于其治疗方式的研究比较广泛。尽管针对肺腺癌的放化疗和靶向治疗取得了一些成果, 但在早期诊断肺腺癌及预后分子靶标等方面, 还需要进一步的探索。
本文探讨了PEG3在肺腺癌中的表达及对于预后的影响。首先通过对TCGA数据库的分析, 比较了PEG3在肺腺癌和正常肺组织中的表达差异, 发现PEG3在肺腺癌中呈显著低表达。其次, 应用TIMER分析TCGA数据库中PEG3表达高低对肺腺癌预后不同影响, 结果显示PEG3的表达水平越低, 其预后较差。在乳腺癌中, BURASCHI等[14]通过数据分析发现PEG3呈现出低表达的情况。陈展等[15]也在mRNA水平上发现了PEG3在肾透明细胞癌中较正常肾组织显著低表达, 并且其表达水平与肾癌预后呈负相关。但DENIZ等[16]在睾丸生殖细胞肿瘤中却得到了相反的结论, 发现PEG3在该肿瘤中呈现高表达状态。有研究[17]发现PEG3在胚胎系肿瘤中呈现出高表达状态, 而在非胚胎性肿瘤中表达相对较低。
PEG3基因是1996年Kuroiwa等[18]通过母系和父系二体胚胎的研究所发现的印迹基因之一。PEG3基因被鉴定为锌指基因之一, 位于人类染色体19q13.4区域中[2]。随着研究的不断深入, PEG3被发现参与了多条人体重要信号通路, 包括Wnt[3]、p53[4]、NF-κB[5]及自噬[6]等。PEG3可以通过Siah1、Bax从胞浆向线粒体的移位以及对Wnt信号通路的抑制[3], 诱导p53介导的细胞凋亡[4], 提示其具有促凋亡作用。相反, 还有研究[5]发现PEG3还可以通过TRAF2激活NF-κB, 保护细胞免受凋亡影响。PEG3也是内皮细胞自噬过程中转录因子EB的上游调控因子[6]。
有研究[7, 19]发现, PEG3基因通常在肿瘤细胞系和肿瘤中表达减少或者缺失的原因是存在启动子的甲基化以及丢失杂合性。本研究中发现, 相对于正常组织, PEG3在肺腺癌组织中的甲基化水平很高。同样在胶质瘤细胞株[19]、乳腺癌[20]和子宫颈癌[7]中均存在这种因甲基化造成PEG3表达的影响。另外富集分析进一步发现PEG3参与甲基化的过程。当DNA甲基化后虽然核苷酸顺序没有改变, 但是却可能导致染色体的结构发生改变, 也有可能通过关闭抑癌基因, 进而导致肿瘤发生。目前已有多种DNA去甲基化作用的化合物药物被开发, 这些药物可重新激活高甲基化的肿瘤抑制基因, 并陆续进入临床试验[21]。PEG3或许是去甲基化的新靶点。
另外, 非编码RNA也可能进一步影响PEG3的表达, 甚至对其功能造成影响。目前发现PEG3基因区一个214核苷酸长的环状RNA-circPeg3, 提示该环状RNA也可能进一步影响PEG3这一印迹基因的作用及相关调控, 但仍需要进一步的实验探索[8]。在睾丸生殖细胞肿瘤中发现miR-514a-3p通过调控PEG3从而激活NF-κB通路[16]。通过TargetScanHuman在线分析了PEG3相关的miRNA, 发现了miR-506等多个相关miRNA, 也为进一步研究PEG3与非编码RNA的关系, 提供了相应的理论基础。
综上所述, 本研究通过对公共数据库中肺腺癌相关数据的挖掘, 发现PEG3在肺腺癌组织中低表达, PEG3高表达的肺腺癌患者预后好于PEG3低表达的肺癌患者, 研究结果为肺腺癌患者的预后指标的筛选提供了一定的理论基础, 未来仍需更多的基础研究对其具体分子机制进行深入探讨。
| [1] |
SIEGEL RL, MILLER KD, JEMAL A. Cancer statistics, 2017[J]. CA Cancer J Clin, 2017, 67(1): 7-30. DOI:10.3322/caac.21387 |
| [2] |
KIM J, ASHWORTH L, BRANSCOMB E, et al. The human homolog of a mouse-imprinted gene, Peg3, maps to a zinc finger gene-rich region of human chromosome 19q13.4[J]. Genome Res, 1997, 7(5): 532-540. DOI:10.1101/gr.7.5.532 |
| [3] |
JIANG XL, YU Y, YANG HW, et al. The imprinted gene PEG3 inhibits wnt signaling and regulates glioma growth[J]. J Biol Chem, 2010, 285(11): 8472-8480. DOI:10.1074/jbc.M109.069450 |
| [4] |
RELAIX F, WEI XJ, LI W, et al. Pw1/Peg3 is a potential cell death mediator and cooperates with Siah1a in p53-mediated apoptosis[J]. Proc Natl Acad Sci U S A, 2000, 97(5): 2105-2110. DOI:10.1073/pnas.040378897 |
| [5] |
RELAIX F, WEI XJ, WU XW, et al. Peg3/Pw1 is an imprinted gene involved in the TNF-NFΚB signal transduction pathway[J]. Nat Genet, 1998, 18(3): 287-291. DOI:10.1038/ng0398-287 |
| [6] |
NEILL T, SHARPE C, OWENS RT, et al. Decorin-evoked paternally expressed gene 3 (PEG3) is an upstream regulator of the transcription factor EB (TFEB) in endothelial cell autophagy[J]. J Biol Chem, 2017, 292(39): 16211-16220. DOI:10.1074/jbc.M116.769950 |
| [7] |
NYE MD, HOYO C, HUANG ZQ, et al. Associations between methylation of paternally expressed gene 3 (PEG3), cervical intraepithelial neoplasia and invasive cervical cancer[J]. PLoS One, 2013, 8(2): e56325. DOI:10.1371/journal.pone.0056325 |
| [8] |
PERERA BPU, GHIMIRE S, KIM J. Circular RNA identified from Peg3 and Igf2r[J]. PLoS One, 2018, 13(9): e0203850. DOI:10.1371/journal.pone.0203850 |
| [9] |
ZHANG L, CHEN S, WANG BX, et al. An eight-long noncoding RNA expression signature for colorectal cancer patients' prognosis[J]. J Cell Biochem, 2019, 120(4): 5636-5643. DOI:10.1002/jcb.27847 |
| [10] |
LI TW, FAN JY, WANG BB, et al. TIMER:a web server for comprehensive analysis of tumor-infiltrating immune cells[J]. Cancer Res, 2017, 77(21): e108-e110. DOI:10.1158/0008-5472.CAN-17-0307 |
| [11] |
VASAIKAR SV, STRAUB P, WANG J, et al. LinkedOmics:analyzing multi-omics data within and across 32 cancer types[J]. Nucleic Acids Res, 2018, 46(D1): D956-D963. DOI:10.1093/nar/gkx1090 |
| [12] |
HUANG WY, HSU SD, HUANG HY, et al. MethHC:a database of DNA methylation and gene expression in human cancer[J]. Nucleic Acids Res, 2015, 43(D1): D856-D861. DOI:10.1093/nar/gku1151 |
| [13] |
AGARWAL V, BELL GW, NAM JW, et al. Predicting effective microRNA target sites in mammalian mRNAs[J]. eLife, 2015, 4: e05005. DOI:10.7554/eLife.05005 |
| [14] |
BURASCHI S, NEILL T, OWENS RT, et al. Decorin protein core affects the global gene expression profile of the tumor microenvironment in a triple-negative orthotopic breast carcinoma xenograft model[J]. PLoS One, 2012, 7(9): 45559. DOI:10.1371/journal.pone.0045559 |
| [15] |
陈展, 崔强, 齐阎, 等. 基于数据挖掘分析PEG3基因在肾透明细胞癌中的表达及预后意义[J]. 现代肿瘤医学, 2018, 26(4): 548-553. |
| [16] |
ÖZATA DM, LI XD, LEE L, et al. Loss of miR-514a-3p regulation of PEG3 activates the NF-kappa B pathway in human testicular germ cell tumors[J]. Cell Death Dis, 2017, 8(5): e2759. DOI:10.1038/cddis.2016.464 |
| [17] |
REZVANI G, LUI JCK, BARNES KM, et al. A set of imprinted genes required for normal body growth also promotes growth of rhabdomyosarcoma cells[J]. 2012, 71 (1): 32-38. DOI: 10.1038/pr.2011.6.
|
| [18] |
KUROIWA Y, KANEKO-ISHINO T, KAGITANI F, et al. Peg3 imprinted gene on proximal chromosome 7 encodes for a zinc finger protein[J]. Nat Genet, 1996, 12(2): 186-190. DOI:10.1038/ng0296-186 |
| [19] |
OTSUKA S, MAEGAWA S, TAKAMURA A, et al. Aberrant promoter methylation and expression of the imprinted PEG3 gene in glioma[J]. Proc Jpn Acad, Ser B, 2009, 85(4): 157-165. DOI:10.2183/pjab.85.157 |
| [20] |
BARROW TM, BARAULT L, ELLSWORTH RE, et al. Aberrant methylation of imprinted genes is associated with negative hormone receptor status in invasive breast cancer[J]. Int J Cancer, 2015, 137(3): 537-547. DOI:10.1002/ijc.29419 |
| [21] |
XU P, HU G, LUO C, et al. DNA methyltransferase inhibitors:an updated patent review (2012-2015)[J]. Expert Opin Ther Patents, 2016, 26(9): 1017-1030. DOI:10.1080/13543776.2016.1209488 |
 2020, Vol. 49
2020, Vol. 49




