文章信息
- 唐诗, 辛颖
- TANG Shi, XIN Ying
- 宫内发育迟缓大鼠胰腺骨保护素的表达及其对胰腺发育的影响
- Osteoprotegerin expression in the pancreas of intrauterine growth retardation rats and its effect on pancreatic development
- 中国医科大学学报, 2020, 49(8): 716-721, 726
- Journal of China Medical University, 2020, 49(8): 716-721, 726
-
文章历史
- 收稿日期:2019-08-15
- 网络出版时间:2020-07-29 9:30
宫内发育迟缓(intrauterine growth retardation,IUGR)是指胎儿未能达到其遗传基因影响下应有的大小。IUGR可增加成年期发生胰岛素抵抗、2型糖尿病等代谢综合征的风险[1-3],其机制尚不十分清楚。目前普遍被认可的机制是“节俭表型假说”[2],该假说指出胎儿及新生儿早期营养不良会导致胰岛β细胞的发育异常及胰岛功能损伤,这种解剖结构和功能的变化可能导致胰岛素敏感性降低,进而成年后发生2型糖尿病。
骨保护素(osteoprotegerin,OPG)是肿瘤坏死因子受体家族的成员,1997年由SIMONET等[4]发现,因具有保护骨的作用而得名。近年的研究[5-8]发现,OPG在人类及大鼠胰岛中均有表达。RIECK等[5]通过芯片筛查发现OPG在怀孕、肥胖和β细胞损伤动物模型中的表达水平均升高,提示OPG与胰岛β细胞之间存在密切的关系。但OPG对胰岛β细胞的具体影响目前仍存在争议[6-8]。
IUGR与OPG相关性的研究鲜有报道,且均集中于血清中OPG水平与IUGR关系的研究[9-11]。临床研究[9-10]表明,出生后1~4 d,IUGR组和健康组母亲和婴儿血清中OPG水平无差异;而动物研究[11]发现,IUGR幼鼠的血清OPG水平显著低于正常幼鼠。目前,尚无针对IUGR个体生长发育过程中胰腺组织中OPG表达情况的研究。本研究拟检测新生至成年期IUGR大鼠胰腺组织中OPG蛋白及mRNA的表达水平,旨在探讨OPG对IUGR大鼠胰腺发育的影响。
1 材料与方法 1.1 建立IUGR大鼠动物模型将体质量(body weight,BW)250~300 g的健康雌性处女Wistar大鼠(辽宁长生生物技术有限公司)以雌雄比例4:1与Wistar雄性大鼠合笼。将已受孕的大鼠按照喂养饲料不同随机分成2组:孕期全程低蛋白饮食组(蛋白含量8%)和标准饲料饮食组(蛋白含量20%)。低蛋白饮食组母鼠喂养至分娩,得到出生BW低于相应孕周第10百分位数以下的子鼠,即IUGR鼠,作为IUGR组;标准饲料饮食组母鼠喂养至分娩,得到正常子鼠,作为正常对照组(CON组)。
选择生后第1天、第1周、第3周及第12周作为研究时间点。为了排除雌激素的影响,选择雄性大鼠为研究对象。每个时间点、每组大鼠均为10只。
1.2 HE染色观察胰岛形态取大鼠胰腺组织,固定并石蜡包埋,制3 μm厚切片。二甲苯及梯度乙醇脱蜡;苏木素染色5 min,自来水冲洗30 min返蓝;伊红复染1.5 min;梯度乙醇脱水,二甲苯透明,中性树脂封片。光镜下观察胰岛形态。
1.3 Ki-67与insulin免疫荧光双染检测胰岛β细胞增殖情况将石蜡切片依次放入二甲苯及梯度乙醇中脱蜡,Tris-EDTA修复液微波7 min煮沸修复,驴血清室温封闭40 min,加入抗Ki-67抗体(1:200,美国Abcam公司)及抗insulin抗体(1:50,中国武汉博士德生物工程有限公司),4 ℃孵育过夜;次日复温后,驴抗小鼠Alexa Fluor 488(1:400,美国Abcam公司)与驴抗兔Alexa Fluor 594(1:400,美国Abcam公司)室温孵育2.5 h,DAPI染核5 min,甘油封片后在免疫荧光共聚焦显微镜(FV1000S,日本Olympus公司)下观察并拍照。每组选取5只大鼠,计算各组Ki-67+细胞数/总细胞数。
1.4 Western blotting检测胰腺组织OPG蛋白表达水平用RIPA裂解液提取大鼠胰腺组织总蛋白,BCA法检测蛋白浓度,调整蛋白浓度并变性。40 μg蛋白上样,10%SDS-PAGE电泳分离蛋白,恒压电泳湿转电转法将蛋白质转移到PVDF膜上,5%脱脂奶粉溶液室温封闭PVDF膜2 h,分别加入兔抗大鼠OPG抗体(1:1 000,美国Abcam公司)和兔抗大鼠GAPDH抗体(1:6 000,美国Proteintech公司),4 ℃孵育过夜,山羊抗兔二抗(1:5 000,美国Proteintech公司)室温孵育2 h,ECL显色,应用Image J软件进行蛋白灰度分析,以相对灰度值代表蛋白表达量。
1.5 实时PCR检测胰腺组织OPG mRNA表达水平提取总RNA,应用PCR反转录试剂盒(日本TaKaRa公司)逆转录合成cDNA。采用PCR扩增试剂盒(日本TaKaRa公司)进行PCR扩增,反应条件为:95 ℃ 30 s;95 ℃ 5 s,60 ℃ 34 s,40个循环。PCR引物序列如下:OPG,F 5’-AAGTGGCTGTGCTGTGCACTC-3’,R 5’-CGGTTTCTGGGTCATAATGCAA-3’;GAPDH,F 5’-AGACAGCCGCATCTTCTTGT-3’,R 5’- CTTGCCGTGGGTAGAGTCAT-3’。GAPDH作为内参照基因,表达量用2-ΔΔCt计算。
1.6 ELISA法检测血清胰岛素水平按照胰岛素ELISA试剂盒(武汉华美生物有限公司)说明书操作,96孔板中加入标准品和待测样品,37 ℃孵育2 h,弃液体;加入生物素标记抗体工作液,37 ℃孵育1 h,洗涤;加入辣根过氧化物酶标记亲和素工作液,37 ℃孵育1 h,洗涤;加入底物溶液,37 ℃避光显色15~30 min;加入终止溶液终止反应;使用酶标仪在450 nm波长依序测量各孔的光密度值。
1.7 胰岛素抵抗指数(homeostasis model assessment-insulin resistance index,HOMA-IR)计算心脏穿刺取血,用快速生化血糖仪(拜安捷,德国拜耳公司)检测各组大鼠空腹血糖(fasting blood glucose,FPG)。计算HOMA-IR = [空腹胰岛素(fasting insulin,FINS)×FPG] /22.5。
1.8 统计学分析采用SPSS 21.0软件进行统计学分析,计量资料用x±s表示,2组间比较采用独立样本t检验,P < 0.05为差异有统计学意义。
2 结果 2.1 宫内营养不良对IUGR子鼠生长及胰腺发育的影响IUGR组大鼠出生BW明显低于CON组,这种情况一直持续至生后3周,哺乳期后,IUGR组出现生长追赶,至12周时,IUGR组与CON组BW无统计学差异(P = 0.37)。IUGR组大鼠胰腺质量(pancreas weight,PW)及胰腺质量/BW比值(pancreas weight/body weight ratio,PW/BW)在生后1 d及1、3、12周时均低于CON组,差异有统计学意义(P < 0.01,P < 0.01,P < 0.01,P = 0.01)。见表 1。
| Time after birth | BW(g) | PW(g) | PW/BW(‰) |
| 1 day | |||
| CON group | 6.71±0. 49 | 16.15±1.46 | 2.42±0.32 |
| IUGR group | 4.72±0.102) | 10.53±1.3922) | 2.17±0.191) |
| 1 week | |||
| CON group | 15.84±0.88 | 37.16±1.91 | 2.35±0.03 |
| IUGR group | 11.60±0.752) | 25.20±1.862) | 2.17±0.022) |
| 3 weeks | |||
| CON group | 51.18±2.64 | 254.28±8.95 | 4.96±0.16 |
| IUGR group | 44.00±1.752) | 197.76±11.412) | 4.47±0.112) |
| 12 weeks | |||
| CON group | 446.08±14.35 | 2 610.49±106.91 | 5.86±0.38 |
| IUGR group | 455.19±18.84 | 2 321.48±195.671) | 5.09±0.222) |
| 1)P < 0.05 vs CON group;2)P < 0.01 vs CON group. BW,body weight;PW,pancreas weight. | |||
HE染色结果显示,与CON组相比,新生IUGR大鼠胰岛组织松散,胰岛面积明显低于对照组。生后1、3、12周时,IUGR组胰岛细胞团体积亦小于CON组。见图 1。
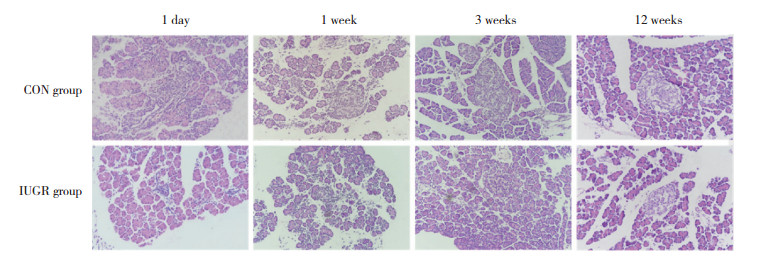
|
| 图 1 CON组和IUGR组胰腺组织HE染色结果×400 Fig.1 HE staining of rats pancreas in CON and IUGR groups ×400 |
进一步通过免疫荧光双染的方法测定子鼠胰岛β细胞增殖情况,其中Ki-67和insulin共表达的部分即提示胰岛β细胞增殖。结果表明,在生后1 d及1、3、12周时,IUGR组胰岛β细胞增殖水平明显低于CON组(P < 0.01)。见图 2。
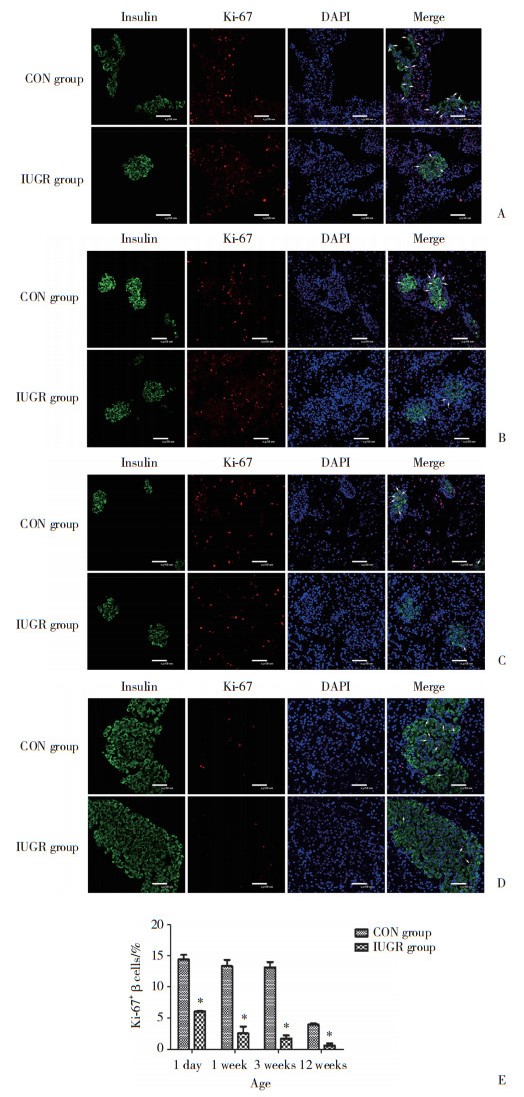
|
| A to D, immunofluorescent staining result of insulin and Ki-67(×400);E, the ratio of proliferative islet cells was calculated as Ki-67+ β-cells/total number of β-cells. A, postnatal 1 day; B, postnatal 1 week; C, postnatal 3 weeks; D, postnatal 12 weeks. *P < 0.01 vs CON group. 图 2 CON组和IUGR组胰腺免疫荧光双染结果(n = 5) Fig.2 Immunofluorescent staining of rats' pancreas in CON and IUGR groups (n = 5) |
2.2 宫内营养不良对IUGR大鼠胰岛功能的影响
不同时间点2组大鼠FPG、FINS及HOMA-IR的结果如表 2所示,出生后1 d、1周、3周时,IUGR组大鼠FPG水平、FINS水平及HOMA-IR与CON组比较无统计学差异。生后12周,IUGR组大鼠FPG水平虽略高于CON组,但无统计学差异;而其FINS水平及HOMA-IR显著高于CON组,差异有统计学意义(P < 0.01)。提示IUGR大鼠在生后12周时存在高胰岛素血症及胰岛素抵抗。
| Time after birth | FPG(mmol/L) | FINS(mIU/L) | HOMA-IR |
| 1 d | |||
| CON group | 4.38±0.17 | 1.47±0.24 | 0.29±0.06 |
| IUGR group | 4.30±0.26 | 1.62±0.09 | 0.31±0.04 |
| 1 week | |||
| CON group | 5.28±0.37 | 3.27±0.53 | 0.76±0.07 |
| IUGR group | 5.18±0.12 | 2.98±0.52 | 0.69±0.13 |
| 3 weeks | |||
| CON group | 5.52±0.26 | 6.11±0.53 | 1.49±0.07 |
| IUGR group | 5.60±0.45 | 6.45±0.54 | 1.60±0.16 |
| 12 weeks | |||
| CON group | 5.68±0.41 | 9.50±0.32 | 2.39±0.25 |
| IUGR group | 6.03±0.42 | 12.72±1.411) | 3.18±0.161) |
| 1)P < 0.01 vs CON group. FPG,fasting blood glucose;FINS,fasting insulin;HOMA-IR,homeostasis model assessment-insulin resistance index. | |||
2.3 IUGR大鼠胰腺中OPG蛋白及mRNA的表达情况
Western blotting和实时PCR结果显示,生后1 d及1、3、12周时,IUGR组OPG蛋白及mRNA的表达水平均低于CON组,其中生后1 d及12周的差异尤为显著(P < 0.01)。见图 3、4。
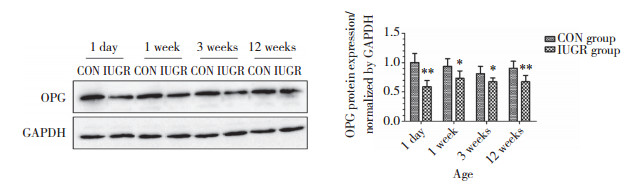
|
| *P < 0.05, **P < 0.01 vs CON group. 图 3 CON组和IUGR组大鼠胰腺组织OPG蛋白表达(n = 6) Fig.3 OPG protein expression in pancreas of rats in CON and IUGR groups(n = 6) |
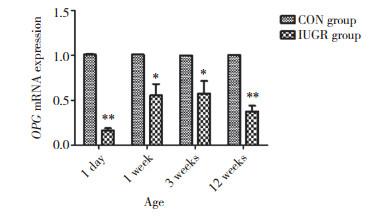
|
| *P < 0.05, **P < 0.01 vs CON group. 图 4 CON组和IUGR组大鼠胰腺组织OPG mRNA表达(n = 5) Fig.4 OPG mRNA expression in pancreas of rats in CON and IUGR groups(n = 5) |
3 讨论
胎盘发育异常、宫内乏氧及宫内营养不良等均会导致胎儿IUGR[12-13]。胎儿期与新生儿早期胰岛β细胞分裂加快、数目增多,这一过程受营养物质的调节,营养物质的数量或质量是保证胰岛β细胞发育的基础。雌性大鼠妊娠期给予低蛋白饮食可使新生大鼠生长发育迟缓,并影响胎鼠胰岛β细胞大小、增殖及功能成熟,造成β细胞缺陷。本研究发现,在生长发育的各个阶段,IUGR大鼠的胰腺发育均较对照组迟缓,表现为胰腺质量低、胰岛细胞团体积减小、胰岛β细胞增殖水平下降。
胰岛β细胞的数量和功能与糖尿病的发生有密切的关系。IUGR个体胰岛β细胞缺陷在2型糖尿病发生中的作用一直受学者关注[14]。临床研究[15-16]也发现,IUGR的患儿在儿童期和成人期会出现胰岛素敏感性下降或胰岛素抵抗。本研究发现,IUGR大鼠在生后12周时出现了高胰岛素血症及胰岛素抵抗。
近年来的研究表明,OPG与糖尿病密切相关。2型糖尿病患者血中OPG水平明显高于对照组[17],但机制尚不清楚,可能与胰岛素抵抗的炎症状态有关[18],也可能与糖尿病血管病变有关[19]。OPG及其配体核因子κB受体活化因子配体(receptor activator of nuclear factor κB ligand,RANKL)在肝脏中均有表达[20]。RANKL可与核因子κB受体活化因子(receptor activator of nuclear factor κB,RANK)结合,激活核因子κB(factor nuclear facto κB,NF-κB)及其下游的炎症信号通路,引起肝脏胰岛素抵抗。而OPG做为RANKL的诱饵受体,竞争性地与RANKL结合,阻止NF-κB及其下游信号通路,进而改善糖代谢。这一结论在临床研究[21]中也得到了证实。
研究[6]表明,在胰腺中,白细胞介素1β(interle-ukin-1β,IL-1β)、肿瘤坏死因子α(tumor necrosis factor-α,TNF-α)可介导OPG的产生,而OPG则通过抑制p38分裂原激活的蛋白激酶(mitogen activated protein kinases,MAPK)的磷酸化,使胰岛β细胞免受损伤,可见OPG具有保护胰岛β细胞的作用。KONDEGOWDA等[7]认为,OPG在催乳素介导的胰岛β细胞再生中起关键的作用,可以促进幼年、老年及糖尿病大鼠胰岛β细胞增殖。而TOFFOLI等[8]则认为OPG可改变胰岛β细胞形态并造成胰岛功能损伤。本研究发现,OPG在正常大鼠及IUGR大鼠胰腺均有表达,但新生儿期(生后1 d)、幼年期(生后1周、3周)及成年期(生后12周)IUGR大鼠胰腺中OPG蛋白及mRNA水平均低于同期正常大鼠。
综上所述,本研究结果表明,IUGR大鼠胰腺中OPG蛋白及mRNA表达水平下降,可能是引起其胰腺发育不良、胰岛β细胞增殖水平下降及成年期胰岛素抵抗的原因之一。
| [1] |
KOPEC G, SHEKHAWAT PS, MHANNA MJ. Prevalence of diabetes and obesity in association with prematurity and growth restriction[J]. Diabetes Metab Syndr Obes, 2017, 10: 285-295. DOI:10.2147/DMSO.S115890 |
| [2] |
HALES CN, BARKER DJ. Type 2(non-insulin-dependent) diabetes mellitus:the thrifty phenotype hypothesis. 1992[J]. Int J Epidemiol, 2013, 42(5): 1215-1222. DOI:10.1093/ije/dyt133 |
| [3] |
MIERZYNSKI R, DLUSKI D, DARMOCHWAL-KOLARZ D, et al. Intra-uterine growth retardation as a risk factor of postnatal metabolic disorders[J]. Curr Pharm Biotechnol, 2016, 17(7): 587-596. DOI:10.2174/1389201017666160301104323 |
| [4] |
SIMONET WS, LACEY DL, DUNSTAN CR, et al. Osteoprotegerin:a novel secreted protein involved in the regulation of bone density[J]. Cell, 1997, 89(2): 309-319. DOI:10.1016/s0092-8674(00)80209-3 |
| [5] |
RIECK S, WHITE P, SCHUG J, et al. The transcriptional response of the islet to pregnancy in mice[J]. Mol Endocrinol, 2009, 23(10): 1702-1712. DOI:10.1210/me.2009-0144 |
| [6] |
SCHRADER J, RENNEKAMP W, NIEBERGALL U, et al. Cytokine-induced osteoprotegerin expression protects pancreatic beta cells through p38 mitogen-activated protein kinase signalling against cell death[J]. Diabetologia, 2007, 50(6): 1243-1247. DOI:10.1007/s00125-007-0672-6 |
| [7] |
KONDEGOWDA NG, FENUTRIA R, POLLACK IR, et al. Osteoprotegerin and denosumab stimulate human beta cell proliferation through inhibition of the receptor activator of NF-κB ligand pathway[J]. Cell Metab, 2015, 22(1): 77-85. DOI:10.1016/j.cmet.2015.05.021 |
| [8] |
TOFFOLI B, BERNARDI S, CANDIDO R, et al. Osteoprotegerin induces morphological and functional alterations in mouse pancreatic islets[J]. Mol Cell Endocrinol, 2011, 331(1): 136-142. DOI:10.1016/j.mce.2010.08.019 |
| [9] |
BRIANA DD, BOUTSIKOU M, BAKA S, et al. Circulating osteoprotegerin and sRANKL concentrations in the perinatal period at term. The impact of intrauterine growth restriction[J]. Neonatology, 2009, 96(2): 132-136. DOI:10.1159/000211666 |
| [10] |
BRIANA DD, BOUTSIKOU M, BOUTSIKOU T, et al. Associations of novel adipocytokines with bone biomarkers in intra uterine growth-restricted fetuses/neonates at term[J]. J Matern Fetal Neonatal Med, 2014, 27(10): 984-988. DOI:10.3109/14767058.2013.852533 |
| [11] |
CHEN JC, CHEN PY, QI HX, et al. Puerarin affects bone biomarkers in the serum of rats with intrauterine growth restriction[J]. J Tradit Chin Med, 2016, 36(2): 211-216. DOI:10.1016/s0254-6272(16)30029-2 |
| [12] |
WIXEY JA, CHAND KK, COLDITZ PB, et al. Review:neuroinflammation in intrauterine growth restriction[J]. Placenta, 2017, 54: 117-124. DOI:10.1016/j.placenta.2016.11.012 |
| [13] |
CHE L, YANG ZG, XU MM, et al. Maternal nutrition modulates fetal development by inducing placental efficiency changes in gilts[J]. BMC Genomics, 2017, 18(1): 213. DOI:10.1186/s12864-017-3601-1 |
| [14] |
UM SH, STICKER-JANTSCHEFF M, CHAU GC, et al. S6K1 controls pancreatic β cell size independently of intrauterine growth restriction[J]. J Clin Invest, 2015, 125(7): 2736-2747. DOI:10.1172/JCI77030 |
| [15] |
MILOVANOVIC I, NJUIEYON F, DEGHMOUN S, et al. SGA children with moderate catch-up growth are showing the impaired insulin secretion at the age of 4[J]. PLoS One, 2014, 9(6): e100337. DOI:10.1371/journal.pone.0100337 |
| [16] |
KAJANTIE E, STRANG-KARLSSON S, HOVI P, et al. Insulin sensitivity and secretory response in adults born preterm:the Helsinki Study of Very Low Birth Weight Adults[J]. J Clin Endocrinol Metab, 2015, 100(1): 244-250. DOI:10.1210/jc.2014-3184 |
| [17] |
AHMED MB, ISMAIL MI, MEKI AR. Relation of osteoprotegerin, visfatin and ghrelin to metabolic syndrome in type 2 diabetic patients[J]. Int J Health Sci (Qassim), 2015, 9(2): 127-139. |
| [18] |
HARITH HH, MORRIS MJ, KAVURMA MM. On the trail of obesity and diabetes[J]. Trends Endocrinol Metab, 2013, 24(11): 578-587. DOI:10.1016/j.tem.2013.07.001 |
| [19] |
丁乐, 汪艳芳, 孙世萌, 等. 骨保护素在糖尿病慢性并发症中的研究进展[J]. 医学综述, 2017, 23(13): 2625-2629. DOI:10.3969/j.issn.1006-2084.2017.13.028 |
| [20] |
KIECHL S, WITTMANN J, GIACCARI A, et al. Blockade of receptor activator of nuclear factor-κB (RANKL) signaling improves hepatic insulin resistance and prevents development of diabetes mellitus[J]. Nat Med, 2013, 19(3): 358-363. DOI:10.1038/nm.3084 |
| [21] |
PASSERI E, BENEDINI S, COSTA E, et al. A single 60 mg dose of denosumab might improve hepatic insulin sensitivity in postmenopausal nondiabetic severe osteoporotic women[J]. Int J Endocrinol, 2015, 2015: 352858. DOI:10.1155/2015/352858 |
 2020, Vol. 49
2020, Vol. 49




