文章信息
- 吴雪艳, 赵依纳, 王小杰, 李美川, 李欣
- WU Xueyan, ZHAO Yina, WANG Xiaojie, LI Meichuan, LI Xin
- 半乳糖凝集素3低表达对肝癌细胞增殖的影响及作用机制
- Effect and mechanism of low expression of galectin 3 on the proliferation of hepatocellular cancer cells
- 中国医科大学学报, 2020, 49(10): 911-914, 920
- Journal of China Medical University, 2020, 49(10): 911-914, 920
-
文章历史
- 收稿日期:2019-11-12
- 网络出版时间:2020-10-07 15:50
2. 河北生殖妇产医院生殖医学科, 石家庄 050000;
3. 承德医学院组织与胚胎学教研室, 河北 承德 067000;
4. 承德医学院基础医学研究所, 河北 承德 067000
2. Department of Reproductive Medicine, Hebei Maternity Hospital, Shijiazhuang 050000, China;
3. Department of Tissue and Embryology, Chengde Medical College, Chengde 067000, China;
4. Institute of Basic Medicine, Chengde Medical College, Chengde 067000, China
肝癌是常见的恶性肿瘤,具有恶性程度高、进展快、术后生存期短、易复发和转移、预后差等特征。探索肝癌的发病机制,寻求有效的分子治疗靶点已成为近年来的研究热点。半乳糖凝集素3 (galectin 3,Gal-3)是半乳糖凝集素家族成员之一,广泛表达于正常细胞和肿瘤细胞,已有研究[1-2]证实,Gal-3在肝癌中表达上调,参与肝癌的发生发展,与预后密切相关。Gal-3是一种新的肿瘤标志物和治疗靶点,具体作用机制尚不明确。本研究通过抑制Gal-3在肝癌HepG2细胞中表达,探讨Gal-3低表达对肝癌HepG2细胞增殖的影响及作用机制,为肝癌发生机制的研究及临床靶向治疗提供一定的实验依据。
1 材料与方法 1.1 细胞、试剂与仪器人肝癌细胞系HepG2 (上海中科院细胞库),细胞培养基DMEM (美国Gibco公司),脂质体lipofectamine2000 (lipo2000)、Trizol试剂和靶向Gal-3 siRNA (美国Invitrogen公司),胎牛血清(FBS) (杭州四季青公司),RIPA裂解液、BCA蛋白定量试剂盒和5×蛋白上样缓冲液(北京索莱宝生物有限公司),Gal-3、磷脂酰肌醇-3激酶(phosphatidylinositol 3-kinase,PI3K)、蛋白激酶(protein kinase B,PKB,Akt)、磷酸化蛋白激酶(phosphorylated protein kinase B,p-Akt)和磷酸化哺乳动物雷帕霉素靶蛋白(phosphorylated mammalian target of rapamycin,p-mTOR)兔抗人单克隆抗体(美国Epitomics公司),β-actin兔抗人单克隆抗体(ABclonal公司),增殖细胞核抗原(proliferating cell nuclear antigen,PCNA)小鼠抗人单克隆抗体(武汉三鹰生物技术有限公司),山羊抗兔二抗、山羊抗小鼠二抗(美国KPL公司),Gal-3和β-actin引物(上海生工有限公司设计并合成),TaKaRa反转录试剂盒(大连宝生物工程有限公司),MTT增殖试剂盒(上海碧云天公司)。主要仪器包括PCR仪(美国MJ公司)、HER Aceu150型CO2培养箱(德国贺利公司)、MK3酶标仪(美国Thermo公司)、Tanon 6100化学发光仪(上海天能公司)。
1.2 方法 1.2.1 细胞分组及转染将HepG2细胞分为siRNA干扰组(转染Gal-3siRNA)、阴性对照组(转染阴性siRNA)及空白对照组(仅加转染试剂)。按5×104/孔在转染前1 d将HepG2种植于6孔板中,使细胞密度24 h内达到60%~70%;将siRNA寡核苷酸(20 pmol/L)与无血清DMEM混合成混悬液(终体积250 μl),将lipo2000与无血清混合成混悬液(终体积250 μl),将2种混悬液在室温下静置5 min后轻柔混匀,室温下静置20 min。然后将混合物均匀加入培养孔,混匀后在37 ℃、5%CO2培养箱中孵育;转染后6 h换成含血清培养基。
1.2.2 Western blotting检测转染后各组细胞Gal-3、PCNA、Akt、p-Akt、p-mTOR蛋白的表达转染48 h后收集各组细胞,PBS洗涤2次,将150 μL RIPA细胞裂解液加至各孔中,冻融裂解,提取总蛋白,用BCA法检测蛋白浓度。将5×上样缓冲液与蛋白混合,煮沸10 min,每孔30 μg,加样,12%SDS-PAGE凝胶电泳80~120 V,2 h;80 V稳压湿转1.5 h;5%脱脂奶粉封闭2 h;Gal-3兔抗人单克隆一抗、PCNA鼠抗人单克隆一抗(1:5 000)、Akt、p-Akt、p-mTOR兔抗人单克隆一抗(1:1 000) 4 ℃孵育过夜;TBST洗膜(15 min、10 min、5 min);羊抗兔、羊抗鼠二抗(1:5 000)室温孵育1.5 h;TBST洗膜(10 min,3次);采用ECL发光法显影,Quantity One 4.62软件进行条带分析。
1.2.3 实时qPCR检测转染后Gal-3 mRNA表达转染后48 h,将1 mL Trizol加入各孔细胞中,提取细胞总RNA,用紫外分光光度计检测RNA纯度,260 nm/280 nm为1.9~2.1 (纯度佳),并取0.2 mL RNA进行1%琼脂糖凝胶电泳检测RNA完整性。符合实验要求后以其为模板用TakaRa反转录试剂盒将RNA反转录成cDNA。β-actin作为内参,Gal-3引物序列:上游5’-TAACCCACGCTTCAATGAGAACAA-3’,下游5’-ACAAGTGAGCATCATTCACTGCAAC-3’;β-actin引物序列:上游5’-TGGCACCCAGCACAATGAA-3’,下游5’-CTAAGTCATAGTCCGCCTAGAAGCA-3’。反应条件:起始模板变性95 ℃ 30 s,1个循环。PCR循环中模板变性95 ℃ 5 s,退火,延伸60 ℃ 20 s,均为40个循环。采用2-ΔΔCt法分析。
1.2.4 MTT法检测细胞增殖每24 h检测1次,转染后胰酶消化细胞,按5×105/mL细胞密度接种于96孔板,各组加入5 mg/mL MTT溶液(20 μL),在5%CO2、37 ℃培养箱孵育4 h,弃培养液加入150 μL二甲基亚砜。酶联免疫检测仪测波长490 nm处各组细胞吸光度(absorbance,A)值。按照A490 nm值大小绘制细胞增殖曲线。
1.3 统计学分析采用SPSS 21.0统计学软件分析数据。计量资料采用x±s表示,多组间两两比较采用LSD-t检验,P < 0.05为差异有统计学意义。
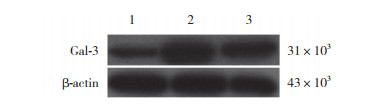
2 结果 2.1 靶向Gal-3 siRNA转染HepG2细胞抑制效率的鉴定结果显示,靶向Gal-3 siRNA转染HepG2细胞抑制效率达70%以上。siRNA干扰组Gal-3蛋白及mRNA表达显著低于阴性对照组和空白对照组(P < 0.05);而阴性对照组与空白对照组Gal-3蛋白及mRNA的表达比较无统计学差异(P > 0.05),见图 1、表 1。
|
| 1, siRNA group; 2, negative control group; 3, blank control group. 图 1 Western blotting法检测各组Gal-3蛋白表达 Fig.1 Expression of Gal-3 protein in siRNA, negative control, and blank control groups by western blotting |
| Group | Gal-3 | |
| Protein | mRNA | |
| si-RNA | 0.04±0.001) | 0.26±0.041) |
| Negative control | 0.12±0.01 | 1.00±0.00 |
| Blank control | 0.13±0.01 | 1.12±0.15 |
| 1) P < 0.05 vs negative control group and blank control group. | ||
2.2 Gal-3低表达对HepG2细胞增殖率的影响
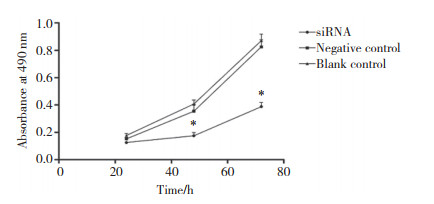
MTT法转染后48 h、72 h检测结果显示,siRNA干扰组细胞增殖速率与阴性对照组和空白对照组比较明显抑制,差异有统计学意义(P < 0.05);而阴性对照组与空白对照组增殖情况比较无统计学差异(P > 0.05),见图 2。
|
| *P < 0.05 compared with negative control and blank control groups. 图 2 Gal-3低表达抑制HepG2细胞增殖 Fig.2 Gal-3 low expression inhibited proliferation of HepG2 cells |
2.3 各组细胞PCNA、Akt、p-Akt、mTOR及p-mTOR蛋白的表达
结果显示,与阴性对照组和空白对照组比较,siRNA干扰组PCNA、p-Akt、p-mTOR的表达明显降低(均P < 0.05),而Akt、mTOR表达差异无统计学意义(P > 0.05)。阴性对照组与空白对照组比较各蛋白表达均无统计学差异(均P > 0.05),见图 3、表 2。

|
| 1, siRNA group; 2, negative control group; 3, blank control group. 图 3 各组PCNA、Akt、p-Akt、mTOR和p-mTOR蛋白的表达 Fig.3 Expression of PCNA, Akt, p-Akt, mTOR, and p-mTOR protein in each group by western blotting |
| Group | PCNA | Akt | p-Akt | mTOR | p-mTOR |
| si-RNA | 0.47±0.051) | 0.12±0.02 | 0.09±0.011) | 0.84±0.11 | 0.10±0.011) |
| Negative control | 0.63±0.01 | 0.12±0.00 | 0.16±0.01 | 0.84±0.02 | 0.17±0.02 |
| Blank control | 0.65±0.04 | 0.13±0.00 | 0.17±0.00 | 0.85±0.05 | 0.17±0.03 |
| 1) P < 0.05 vs negative control and blank control groups. | |||||
3 讨论
Gal-3基因位于14q21-22染色体上,是半乳糖凝集素家族中唯一具有嵌合体结构的成员,在正常细胞、肿瘤细胞的细胞质和细胞膜中广泛存在[3-4],可以与细胞表面分子、细胞外基质蛋白等多种配体结合,影响细胞的黏附、生长和凋亡等生物学过程,调控侵袭、分化和转移[5-7]。研究[8-11]表明,Gal-3在结直肠癌、乳腺癌、甲状腺癌、胃癌等多种肿瘤中显著高表达。敲低Gal-3在胃癌细胞中的表达可抑制细胞增殖[12];QIAO等[13]亦发现抑制食管癌中Gal-3表达后细胞增殖和迁移能力显著降低。本研究MTT结果显示,抑制Gal-3表达后细胞增殖能力明显下降。PCNA是一种表达于细胞核的DNA聚合酶附属蛋白,其合成和表达与细胞增殖密切相关。PCNA是评价细胞增殖状态的指标[14]。本研究发现,siRNA干扰组PCNA表达显著下调,说明Gal-3低表达抑制了PCNA的表达,证实了Gal-3在肝癌发生、发展过程中具有促进细胞增殖的作用。
PI3K/Akt/mTOR信号通路是细胞内重要信号转导通路之一,在细胞的生长、增殖、分化、自噬及肿瘤血管生成等方面发挥重要作用[15]。PI3K是一种胞内磷脂酰肌醇激酶,被G-蛋白耦联受体激活后可使其底物磷酸化,进而活化信号通路[16]。Akt作为PI3K下游的效应分子,可通过磷酸化作用促进细胞生长和抑制细胞凋亡。当Akt位点全部磷酸化后Akt激活,活化的Akt发生转位进入胞质或胞核,通过TSC1/2复合物进一步激活其下游分子mTOR,从而介导细胞生长[16-17]。mTOR是PI3K相关激酶家族中的一员,包括mTORC1和mTORC2两种蛋白复合物,mTORC1通过p-Akt激活Akt,活化的Akt作用于mTORC1,促进肿瘤细胞增殖,增强肿瘤细胞生存力[18-19]。为进一步探究Gal-3表达抑制后HepG2细胞增殖的可能机制,本研究检测了PI3K/Akt/mTOR信号通路相关蛋白酶Akt、p-Akt及mTOR、p-mTOR的表达。结果显示,在抑制Gal-3表达后,p-Akt和p-mTOR表达均显著下调,而Akt、mTOR表达无明显变化,说明Gal-3低表达抑制了p-Akt和p-mTOR的表达。由此推测Gal-3低表达抑制HepG2细胞增殖,可能是通过抑制了PI3K/Akt/mTOR信号通路的磷酸化实现的。
综上所述,肝癌HepG2细胞下调Gal-3蛋白表达后,细胞生长、增殖速度明显抑制,同时PCNA、p-Akt和p-mTOR表达均降低。说明Gal-3在肝癌细胞中发挥着促进细胞增殖作用,细胞增殖作用机制可能与激活PI3K/Akt/mTOR信号通路有关。本研究为肝癌的临床分子靶向治疗提供了潜在靶点,但肿瘤的调控过程非常复杂,Gal-3在肝癌中的具体作用机制今后将进一步论证。
| [1] |
方青青, 倪润洲, 肖明兵, 等. 肝癌组织和血清中半乳糖血凝素-3的表达及其意义[J]. 中华肝脏病杂志, 2011, 19(7): 527-531. DOI:10.3760/cma.j.issn.1007-3418.2011.07.014 |
| [2] |
ZAHRA MK, ATTIA TE, AHMAD AY. Serum galectin-3 levels in patients with hepatocellular carcinoma, liver cirrhosis and chronic viral hepatitis[J]. Egyptian Journal Hospital Medicine, 2018, 70(1): 132-139. DOI:10.12816/0042976 |
| [3] |
CIOCA A, MUNTEAN D, BUNGARDEAN C, et al. Expression and distribution of galectin-3 in chromophobe and papillary carcinomas[J]. Anticancer Res, 2018, 38(1): 259-263. DOI:10.21873/anticanres.12216 |
| [4] |
NANGIA-MAKKER P, HOGAN V, RAZ A. Galectin-3 and cancer stemness[J]. Glycobiology, 2018, 28(4): 172-181. DOI:10.1093/glycob/cwy001 |
| [5] |
AHMED H, ALSADEK DM. Galectin-3 as a potential target to prevent cancer metastasis[J]. Clin Med Insights Oncol, 2015, 9: 113-121. DOI:10.4137/CMO.S29462 |
| [6] |
CHUNG LY, TANG SJ, WU YC, et al. Galectin-3 augments tumor initiating property and tumorigenicity of lung cancer through interaction with β-catenin[J]. Oncotarget, 2015, 6(7): 4936-4952. DOI:10.18632/oncotarget.3210 |
| [7] |
WINTER MP, WIESBAUER F, ALIMOHAMMADI A, et al. Soluble galectin-3 is associated with premature myocardial infarction[J]. Eur J Clin Invest, 2016, 46(5): 386-391. DOI:10.1111/eci.12605 |
| [8] |
PETROVIC S, RADOSAVLJEVIC GD, PANTIC J, et al. Circulating and tissue galectin-1 and galectin-3 in colorectal carcinoma:association with clinicopathological parameters, serum CEA, IL-17 and IL23[J]. J BUON, 2016, 21(4): 941-949. |
| [9] |
SUMANA BS, SHASHIDHAR S, SHIVARUDRAPPA AS. Galectin-3 immunohistochemical expression in thyroid neoplasms[J]. J Clin Diagn Res, 2015, 9(11): EC07-EC11. DOI:10.7860/JCDR/2015/16277.6760 |
| [10] |
GROSSET AA, LABRIE M, VLADOIU MC, et al. Galectin signatures contribute to the heterogeneity of breast cancer and provide new prognostic information and therapeutic targets[J]. Oncotarget, 2016, 7(14): 18183-18203. DOI:10.18632/oncotarget.7784 |
| [11] |
SANTOS SN, JUNQUEIRA MS, FRANCISCO G, et al. O-glycan sialylation alters galectin-3 subcellular localization and decreases chemotherapy sensitivity in gastric cancer[J]. Oncotarget, 2016, 7(50): 83570-83587. DOI:10.18632/oncotarget.13192 |
| [12] |
吴雪艳, 赵依纳, 王小杰, 等. 半乳糖凝集素3低表达对人胃癌MGC-803细胞增殖的影响[J]. 解剖学报, 2018, 50(6): 723-728. DOI:10.16098/j.issn.0529-1356.2018.06.005 |
| [13] |
QIAO LL, LIANG N, XIE J, et al. Gene silencing of galectin-3 changes the biological behavior of Eca109 human esophageal cancer cells[J]. Mol Med Rep, 2016, 13(1): 160-166. DOI:10.3892/mmr.2015.4543 |
| [14] |
ARAZ SERVER E, KALAYCıK ERTUGAY Ç, BAYKAL KOCA S, et al. Predictive role of ki-67 and proliferative-cell nuclear antigen (PCNA) in recurrent cholesteatoma[J]. J Int Adv Otol, 2019, 15(1): 38-42. DOI:10.5152/iao.2018.4976 |
| [15] |
WESTIN JR. Status of PI3K/Akt/mTOR pathway inhibitors in lymphoma[J]. Clin Lymphoma Myeloma Leuk, 2014, 14(5): 335-342. DOI:10.1016/j.clml.2014.01.007 |
| [16] |
FRUMAN DA, CHIU H, HOPKINS BD, et al. The PI3K pathway in human disease[J]. Cell, 2017, 170(4): 605-635. DOI:10.1016/j.cell.2017.07.029 |
| [17] |
CUI HY, WU SF, SHANG YF, et al. Pleurotus nebrodensis polysaccharide (PN50G) evokes A549 cell apoptosis by the ROS/AMPK/PI3K/AKT/mTOR pathway to suppress tumor growth[J]. Food Funct, 2016, 7(3): 1616-1627. DOI:10.1039/c6fo00027d |
| [18] |
CARGNELLO M, TCHERKEZIAN J, ROUX PP. The expanding role of mTOR in cancer cell growth and proliferation[J]. Mutagenesis, 2015, 30(2): 169-176. DOI:10.1093/mutage/geu045 |
| [19] |
SAXTON RA, SABATINI DM. mTOR signaling in growth, metabolism, and disease[J]. Cell, 2017, 168(6): 960-976. DOI:10.1016/j.cell.2017.02.004 |
 2020, Vol. 49
2020, Vol. 49




