文章信息
- 李宁, 张航, 于波
- LI Ning, ZHANG Hang, YU Bo
- 阿托伐他汀通过内质网应激调节乙醇作用下AC16心肌细胞超微结构及脂质合成代谢
- Effects of Atorvastatin on Ultrastructure and Lipid Synthesis of Myocardial AC16 Cells Exposed to Alcohol through Endoplasmic Reticulum Stress
- 中国医科大学学报, 2019, 48(9): 828-832
- Journal of China Medical University, 2019, 48(9): 828-832
-
文章历史
- 收稿日期:2018-08-18
- 网络出版时间:2019-09-09 9:10
酒精性心肌病是长期大量饮酒导致的非缺血性扩张型心肌病,临床表现为心脏扩大、心功能不全和心律失常等[1]。研究[2-3]发现,酒精性心肌病的发病机制涉及多层次、多水平的机制,如乙醇代谢途径的酶代谢及营养失衡、氧化应激、细胞坏死与凋亡以及钙稳态失衡等。近年来,内质网应激(endoplasmic reticulum stress,ERS)在酒精性心肌病发病过程中的作用受到越来越多的重视。国内外学者针对ERS的研究目前多集中在肝脏、肾脏、神经系统、胰腺及部分肿瘤疾病[4-5],较少针对心肌细胞,对酒精性心肌病细胞模型的相关研究更是少之又少。本研究在既往理论研究及实验研究的基础上,探讨阿托伐他汀通过ERS对乙醇作用下心肌细胞超微结构及脂质合成代谢的影响机制,为将来的临床研究提供可靠的依据。
1 材料与方法 1.1 AC16心肌细胞的复苏、培养与分组取出液氮保存的AC16细胞(购自南京科佰生物科技有限公司),立即37 ℃水浴快速解冻,中间过程轻摇冷冻管混匀,加速融化,完全融化后立刻离心。1 000 r/min离心5 min,吸弃上清液。加入1 mL高糖DMEM完全培养基(含10%胎牛血清,1%双抗,购自美国Thermo Fisher Scientific公司)重悬细胞沉淀,轻柔吹打均匀(单细胞悬液)后将细胞转移到10 cm培养皿中,并调整细胞密度约为20%~25%,该密度范围让复苏细胞有足够的培养时间以调整到最佳状态。CO2培养箱中培养(37 ℃,5% CO2),间隔12 h后换液,弃去原有培养基,PBS漂洗2次,加入10 mL新鲜的高糖DMEM完全培养基,在倒置显微镜下观察生长情况。之后2 d换液1次,每次吸弃原有培养基,更换10 mL新鲜的高糖DMEM完全培养基。待复苏细胞生长至80%~90%密度,0.25%胰酶消化,至细胞变圆后吸弃胰酶,加入2~3 mL完全培养基脱离细胞并吹打至单细胞,按照1:3比例传代。传代细胞贴壁12 h后换液,之后2 d换液1次,2~3 d传代1次。按照实验条件添加不同浓度乙醇及阿托伐他汀至培养基中,培养48 h后收集细胞用于后续实验。
实验分组:正常组,未做任何处理,正常培养细胞;乙醇组,200 mmol/L乙醇处理AC16心肌细胞48 h;1、10、100 μmol/L阿托伐他汀组,细胞处理基于乙醇组,分别使用1、10、100 μmol/L阿托伐他汀处理AC16心肌细胞48 h。
1.2 Western blotting提取各组细胞总蛋白,BCA法(试剂盒购自碧云天生物技术公司)测蛋白浓度。根据蛋白分子量选择所需要的SDS-PAGE凝胶浓度,SDS-PAGE电泳。转膜后,加入用封闭液稀释的葡萄糖调节蛋白78(glucose-regulated protein 78,GRP78)、固醇调节原件结合蛋白-1c(sterol regulatory element binding protein-1c,SREBP-1c)和β-actin一抗,室温摇床孵育2 h,并用TBS洗膜3次,每次15 min。再加入用封闭液稀释的相应二抗室温摇床孵育1 h,并用TBS洗膜3次,每次15 min。ECL显色检测。蛋白的相对表达量用待测蛋白与β-actin的灰度值比值计算。
1.3 电镜观察心肌细胞超微结构收集细胞后,倒入2.5%戊二醛固定液,反应4 h。0.1 mol/L PBS清洗3次,30%、50%、70%、85%、95%乙醇梯度脱水各1次,每次20 min。100%乙醇脱水2次,每次20 min,乙酸异戊酯置换2次,每次20 min。将细胞均匀涂布盖玻片上,-70 ℃冷冻12 h,冷冻干燥48 h,将盖玻片样品喷金粉后上样,观察。
1.4 甘油三酯(triglyceride,TG)含量测定收集细胞后,采用TG检测试剂盒(GPO-PAP单试剂微板法,购自北京欣华绿源科技有限公司)检测细胞内TG含量。
1.5 统计学分析采用SPSS 17.0软件进行统计学分析。计量资料用x±s表示,组间两两比较采用独立样本t检验,组内比较采用配对样本t检验,计数资料组间比较采用χ2检验。P < 0.05为差异有统计学意义。
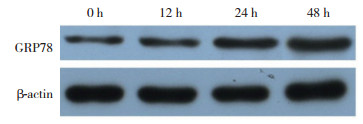
2 结果 2.1 乙醇作用下心肌细胞ERS模型的建立乙醇(200 mmol/L)处理AC16心肌细胞0、12、24、48 h后,Western blotting检测不同时间点GRP78蛋白表达。结果表明,实验组内质网特异性分子伴侣GRP78蛋白相对表达量均显著升高(图 1)。针对Western blotting条带进行灰度值定量分析,GRP78在0 h相对表达值为0.19±0.02,在12、24、48 h相对表达值分别为0.27±0.03、0.39±0.01、0.64±0.02。结果显示,处理12、24、48 h后与0 h比较,GRP78蛋白表达的差异均有统计学意义(均P < 0.05)。表明乙醇作用下AC16心肌细胞ERS模型建立成功,且ERS效应具有时间依赖性。选取乙醇(200 mmol/L)处理AC16心肌细胞48 h,用于后续实验。
|
| 图 1 Western blotting检测200 mmol/L乙醇处理AC16心肌细胞0、12、24、48 h后GRP78蛋白的表达 Fig.1 Expression of GRP78 protein in myocardial AC16 cells treated with 200 mmol/L ethanol for 0, 12, 24, and 48 hours visualized using Western blotting |
2.2 不同浓度阿托伐他汀干预对乙醇作用下心肌细胞ERS状态的影响
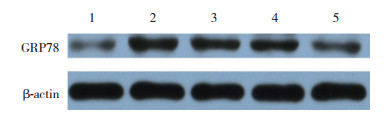
Western blotting检测正常组、乙醇组以及1、10、100 μmol/L阿托伐他汀组的GRP78蛋白的相对表达量,来衡量ERS状态。结果显示,与乙醇组比较,1、10、100 μmol/L阿托伐他汀组GRP78蛋白的表达均显著降低,差异均有统计学意义(均P < 0.05),见图 2、表 1。表明阿托伐他汀可以有效缓解乙醇作用下心肌细胞ERS反应。
|
| 1, normal group; 2, alcohol administered group; 3, 1 μmol/L atorvastatin treated group; 4, 10 μmol/L atorvastatin treated group; 5, 100 μmol/L atorvastatin treated group. 图 2 不同浓度阿托伐他汀干预下心肌细胞GRP78蛋白的相对表达量 Fig.2 Relative expression of GRP78 protein in myocardial cells treated with different concentrations of atorvastatin |
| Group | GRP78 protein | SREBP-1c | Triglyceride |
| Normal group | 0.19±0.02 | 0.25±0.02 | 21.56±1.78 |
| Alcohol administered group | 0.64±0.02 | 0.56±0.03 | 36.35±2.41 |
| 1 μmol/L atorvastatin treated group | 0.50±0.041) | 0.47±0.041) | 31.73±1.591) |
| 10 μmol/L atorvastatin treated group | 0.38±0.031) | 0.39±0.031) | 26.84±1.631) |
| 100 μmol/L atorvastatin treated group | 0.24±0.011) | 0.31±0.021) | 23.11±2.051) |
| 1)P < 0.05 vs alcohol administered group. | |||
2.3 不同浓度阿托伐他汀干预对乙醇作用下心肌细胞超微结构的影响
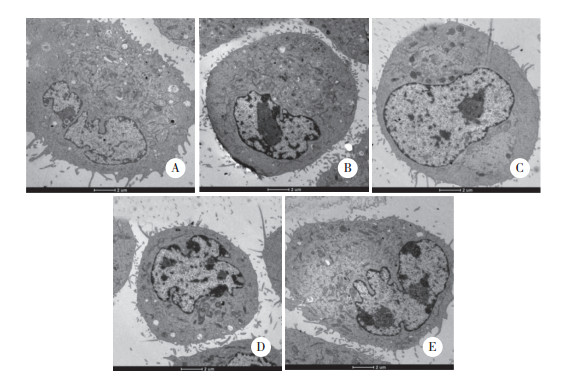
电镜观察结果显示,乙醇组AC16细胞形态异常,细胞内线粒体数量明显减少、线粒体增大、线粒体嵴结构紊乱,时有线粒体嵴结构消失呈空泡样改变。随着阿托伐他汀干预浓度增加,AC16细胞形态及线粒体结构逐渐趋于正常,其中100 μmol/L阿托伐他汀组可见大量线粒体,呈椭圆形,线粒体嵴结构整齐,同正常组(图 3)。表明阿托伐他汀干预可以缓解乙醇作用下心肌细胞超微结构的异常改变。
|
| A, alcohol administered group; B, 1 μmol/L atorvastatin treated group; C, 10 μmol/L atorvastatin treated group; D, 100 μmol/L atorvastatin treated group; E, normal group. 图 3 不同浓度阿托伐他汀干预对乙醇作用下心肌细胞超微结构的影响 ×500 Fig.3 Effects of different concentrations of atorvastatin on ultrastructure of myocardial cells administered with alcohol ×500 |
2.4 不同浓度阿托伐他汀干预对乙醇作用下心肌细胞脂质合成代谢的影响
检测各组脂质合成代谢关键蛋白SREBP-1c及TG含量,结果显示,与乙醇组相比,1、10、100 μmol/L阿托伐他汀组SREBP-1c和TG含量均显著降低,差异均有统计学意义(均P < 0.05),见图 4、表 1。

|
| 1, normal group; 2, alcohol administered group; 3, 1 μmol/L atorvastatin treated group; 4, 10 μmol/L atorvastatin treated group; 5, 100 μmol/L atorvastatin treated group. 图 4 不同浓度阿托伐他汀干预后心肌细胞SREBP-1c蛋白的相对表达量 Fig.4 Relative expression of SREBP-1c protein in myocardial cells upon treatment with different concentrations of atorvastatin |
3 讨论
内质网不只是真核细胞蛋白质合成和折叠、脂质合成以及细胞内储存的亚细胞器,还是调节细胞应激与调亡的亚细胞器,因而对维持心肌细胞功能、蛋白质稳态具有重要作用。ERS是指多种因素导致的使细胞内质网生理功能发生紊乱的一种亚细胞器病理状态。目前国内外研究者一致以内质网特异性分子伴侣GRP78蛋白作为ERS反应激活的标志[6]。早期文献[7-8]报道ERS参与如糖尿病心肌病、冠状动脉粥样硬化性心脏病、缺血再灌注损伤等多种心血管疾病的发生发展,是心血管疾病的重要发病机制。近年来,不断有研究[9]证明ERS在长期乙醇摄入所致的心肌损伤中也发挥着重要作用。
他汀类药物为羟甲基戊二酰辅酶A还原酶抑制剂,具有竞争性抑制细胞内胆固醇的合成早期限速酶的活性,继而上调细胞表面低密度脂蛋白受体,加速血浆低密度脂蛋白分解代谢的作用。近20年来,临床研究[10-11]显示他汀类药物是当前防治高胆固醇血症和动脉粥样硬化性疾病的重要的药物。自从20世纪80年代以来,许多具有里程碑意义的研究证明了他汀类药物在降低血脂方面的积极作用,表明其在心血管方面的许多作用独立于其降低低密度脂蛋白的作用。各类文献频繁以“多效性”来概括其作用,其“多效性”作用包括抗炎、抗血小板聚集、抗氧化、稳定斑块、改善内皮功能、调节免疫、动员内皮祖细胞、抗心律失常及预防碎死等作用。最新文献[12]报道,他汀类药物在ERS过程中具有确切的负性调节作用,可能是其发挥保护作用的多种机制之一,但具体机制尚不清楚。
基于以上研究进展及前期研究结果,为了进一步研究阿托伐他汀通过ERS对酒精性心肌病的影响,本研究首先构建了AC16心肌细胞ERS模型,在用200 mmol/L乙醇处理AC16心肌细胞后检测GRP78蛋白表达,处理心肌细胞12、24、48 h后GRP78含量均较0 h显著增加,表明AC16心肌细胞ERS模型建立成功。并且随着处理时间的增加,GRP78表达量也随之升高,推测在一定作用周期范围内,ERS效应具有时间依赖性。随后,本研究采用不同剂量(1、10、100 μmol/L)阿托伐他汀处理乙醇作用下心肌细胞48 h后,发现随着阿托伐他汀剂量的增加,可以不同程度的降低GRP78蛋白表达水平,100 μmol/L时降低的最多,表明阿托伐他汀可以有效缓解乙醇作用下心肌细胞ERS反应。有关阿托伐他汀与ERS反应的研究,过去大多集中在缺血再灌注发生机制上,如XIA等[13]证实了阿托伐他汀处理具有改善心肌缺血再灌注损伤的保护作用,其机制可能与通过抑制ERS相关细胞凋亡有关;刘忠仁[14]通过观察阿托伐他汀对大鼠心肌缺血再灌注损伤后GRP78和GADD153蛋白表达的影响,证实ERS途径可能是阿托伐他汀对心肌再灌注后损伤发挥保护作用的机制之一。这些结论与上述结果一致,也为探究酒精性心肌病中阿托伐他汀与ERS的关系提供了借鉴。
大量研究表明线粒体功能障碍是多种疾病的病理基础,心肌作为高能量代谢组织,对线粒体功能改变更为敏感。MARÍN-GARCÍA等[15]证实心血管疾病、缺血性心肌病等均存在线粒体功能障碍,TERAGAKI等[16]在酒精性心肌病患者及动物模型中也发现心肌细胞线粒体结构及功能异常。本研究对不同处理组AC16细胞进行电镜观察,结果显示乙醇组AC16细胞形态异常,细胞内线粒体数量明显减少、线粒体增大、线粒体嵴结构紊乱,时有线粒体嵴结构消失呈空泡样改变。随着阿托伐他汀干预浓度增加,AC16细胞形态及线粒体结构逐渐趋于正常,其中100 μmol/L阿托伐他汀组可见大量线粒体,呈椭圆形,线粒体嵴结构整齐,同正常组,表明阿托伐他汀干预可以缓解乙醇作用下心肌细胞超微结构的异常改变,推测乙醇对酒精性心肌病发病的影响可能与其对线粒体生成的影响相关。
SREBP-1c是属于“碱性螺旋-环-螺旋-亮氨酸拉链”锌指结构域家族的转录因子,主要调控TG代谢,其他的亚型分子包括SREBP-1a和SREBP-2,主要调节胆固醇代谢。FANG等[17]研究表明,内质网稳态失衡不只影响蛋白质的合成,还引起脂肪酸和胆固醇的代谢紊乱,在这个过程中SREBP-1c是重要调节机制之一。通过检测脂质合成代谢关键蛋白SREBP-1c和TG含量,检测细胞内脂滴,从而探究阿托伐他汀对心肌细胞脂质合成代谢的影响。本研究检测了SREBP-1c及TG含量,结果表明乙醇引发的ERS会显著提高SREBP-1c及TG含量,而阿托伐他汀干预则可以缓解其异常表达。但是有关阿托伐他汀如何通过激活SREBP-1c促进脂质合成代谢,其机制仍不明确。
综上所述,本研究进一步证实了ERS与脂质沉积的直接关系,并且证明阿托伐他汀可抑制乙醇作用下ERS相关因子GRP78表达,改善酒精性心肌病细胞模型细胞体态、线粒体超微结构及脂代谢情况。本研究在既往理论研究及实验研究的基础上,进一步说明阿托伐他汀通过ERS对乙醇作用下心肌细胞影响的变化规律,为将来的临床研究提供可靠的依据。
| [1] |
PIANO MR, PHILLIPS SA. Alcoholic cardiomyopathy:pathophysiologic insights[J]. Cardiovasc Toxicol, 2014, 14(4): 291-308. DOI:10.1007/s12012-014-9252-4 |
| [2] |
GUZZO-MERELLO G, COBO-MARCOS M, GALLEGO-DELGADO M, et al. Alcoholic cardiomyopathy[J]. World J Cardiol, 2014, 6(8): 771-781. DOI:10.4330/wjc.v6.i8.771 |
| [3] |
GUZZO-MERELLO G, SEGOVIA J, DOMINGUEZ F, et al. Natural history and prognostic factors in alcoholic cardiomyopathy[J]. JACC Heart Fail, 2015, 3(1): 78-86. DOI:10.1016/j.jchf.2014.07.014 |
| [4] |
HONG J, KIM K, KIM JH, et al. The role of endoplasmic reticulum stress in cardiovascular disease and exercise[J]. Int J Vasc Med, 2017, 2017: 2049217. DOI:10.1155/2017/2049217 |
| [5] |
陈娜子, 姜潮, 李校堃. 内质网应激与疾病[J]. 中国生物工程杂志, 2016, 36(1): 76-85. DOI:10.13523/j.cb.20160111 |
| [6] |
ZHOU X, HAN D, YANG X, et al. Glucose regulated protein 78 is potentially an important player in the development of nonalcoholic steatohepatitis[J]. Gene, 2017, 637: 138-144. DOI:10.1016/j.gene.2017.09.051 |
| [7] |
CNOP M, TOIVONEN S, IGOILLO-ESTEVE M, et al. Endoplasmic reticulum stress and eIF2α phosphorylation:the Achilles heel of pancreatic β cells[J]. Mol Metab, 2017, 6(9): 1024-1039. DOI:10.1016/j.molmet.2017.06.001 |
| [8] |
CHRISTEN V, CAMENZIND M, FENT K. Silica nanoparticles induce endoplasmic reticulum stress response, oxidative stress and activatemitogen-activated protein kinase (MAPK) signaling pathway[J]. Toxicol Rep, 2014, 1: 1143-1151. DOI:10.1016/j.toxrep.2014.10.023 |
| [9] |
王晴, 周岩, 韩会, 等. NECA抑制内质网应激抗大鼠心肌缺血再灌注损伤的作用机制[J]. 医学研究生学报, 2017, 30(6): 574-578. DOI:10.16571/j.cnki.1008-8199.2017.06.004 |
| [10] |
徐海燕, 刘冬, 王文刚, 等. 他汀类药物与常见心血管药物相互作用的研究进展[J]. 中国药房, 2016, 27(11): 1582-1584. DOI:10.6039/j.issn.1001-0408.2016.11.47 |
| [11] |
陈曦. 他汀类药物的临床应用评价及效果分析[J]. 中国现代药物应用, 2016, 10(12): 163-164. DOI:10.14164/j.cnki.cn11-5581/r.2016.12.122 |
| [12] |
WU H, TANG Q, YANG J, et al. Atorvastatin ameliorates myocardial ischemia/reperfusion injury through attenuation of endoplasmic reticulum stress-induced apoptosis[J]. Int J Clin Exp Med, 2014, 7(12): 4915-4923. |
| [13] |
XIA JG, XU FF, QU Y, et al. Atorvastatin post-conditioning attenuates myocardial ischemia reperfusion injury via inhibiting endoplasmic reticulum stress-related apoptosis[J]. Shock, 2014, 42(4): 365-371. DOI:10.1097/SHK.0000000000000224 |
| [14] |
刘忠仁. 阿托伐他汀对大鼠心肌缺血再灌注损伤心肌保护的内质网应激途径研究[J]. 右江民族医学院学报, 2010, 32(4): 474-477. DOI:10.3969/j.issn.1001-5817.2010.04.003 |
| [15] |
MAR N-GARC A J, AKHMEDOV AT. Mitochondrial dynamics and cell death in heart failure[J]. Heart Fail Rev, 2016, 21(2): 123-136. DOI:10.1007/s10741-016-9530-2 |
| [16] |
TERAGAKI M, TAKEUCHI K, TODA I, et al. Point mutations in mitochondrial DNA of patients with alcoholic cardiomyopathy[J]. Heart Vessels, 2000, 15(4): 172-175. DOI:10.1007/PL00007268 |
| [17] |
FANG DL, WAN Y, SHEN W, et al. Endoplasmic reticulum stress leads to lipid accumulation through upregulation of SREBP-1c in normal hepatic and hepatoma cells[J]. Mol Cell Biochem, 2013, 381(1/2): 127-137. DOI:10.1007/s11010-013-1694-7 |
 2019, Vol. 48
2019, Vol. 48




