文章信息
- 赵君爽, 李龙, 张天鼎, 陈炼, 周锦鹏, 景治涛
- ZHAO Junshuang, LI Long, ZHANG Tianding, CHEN Lian, ZHOU Jinpeng, JING Zhitao
- 多模态神经导航系统在岩骨-斜坡区肿瘤切除术中的临床应用
- Clinical Application of Multimodal Neuronavigation System in Petroclival Tumor Resection
- 中国医科大学学报, 2019, 48(9): 774-777
- Journal of China Medical University, 2019, 48(9): 774-777
-
文章历史
- 收稿日期:2019-03-08
- 网络出版时间:2019-09-09 9:03
岩骨-斜坡区是指由蝶骨、颞骨及枕骨所围成的区域,是构成中颅窝和后颅窝的重要组成结构,通常简称岩斜区[1]。发生于岩斜区的肿瘤往往位置较深且体积巨大,肿瘤周围的解剖关系复杂,血管和颅神经密集分布,因此手术切除难度大,全切除率低,术后并发症、致残率和死亡率较高[2]。随着神经影像学的不断进步和发展,多模态神经导航系统作为一种可靠的、精准的术中实时引导系统在神经外科日常临床应用中得到了广泛认可[3]。多模态神经导航系统通过结合多种成像方式,提供实时图像以呈现术中颅内解剖结构,用于定位被包裹和移位的血管以及破坏性骨标志物,同时也提供了在手术空间进行三维重建的便利条件[4-5]。
多模态神经导航系统通过多图像融合和三维重建原理,联合多普勒超声和神经电生理监测实时引导指示术中病变与邻近神经血管结构的空间关系,提高了岩斜区肿瘤手术切除的准确性、可靠性和成功率。这些先进的术中技术可以提高神经外科手术的精度,降低岩斜区肿瘤手术操作难度,提高手术切除的安全性和有效性。本文详细阐述了中国医科大学附属第一医院神经外科近6年利用多模态神经导航系统手术治疗岩斜区肿瘤的经验。
1 材料与方法 1.1 研究对象收集2013年1月至2019年1月于中国医科大学附属第一医院行岩斜区肿瘤手术切除的病例87例。其中,在多模态神经导航系统辅助下手术切除者(多模态组)35例,在无术中实时影像学指导下手术切除者(对照组)52例。男30例(34.5%),女57例(65.5%),男女比例为1︰1.9,年龄38~72岁,平均年龄53.6岁。收集患者的临床病史、影像学检查、术前术后神经功能状态、肿瘤手术切除情况及术后并发症等资料,定期随访患者,记录神经功能状态、生活质量等。排除标准:颅内有金属植入物;有脑血管病、心肺疾病以及血液系统疾病,以上因素都可能干扰或影响头部核磁共振成像,故需要排除在外。本研究获得中国医科大学附属第一医院伦理委员会批准。
1.2 临床表现患者的临床表现因肿瘤所在的位置、大小、生长速度及其与周围重要组织结构的关系而异。头痛为主要主诉症状者29例,但大多数患者起初只有轻微的头痛,未引起足够重视而及时就诊。随后,由于颅内组织结构破坏,颅神经压迫症状明显,13例患者出现耳鸣及听觉障碍,11例出现视物模糊,9例出现步态不稳,8例出现三叉神经痛,7例动眼神经瘫痪出现斜视,5例出现面部麻痹,3例出现饮水呛咳,2例无明显症状,在日常体检中发现。肿瘤所引起的症状持续1~24个月(平均6个月)。
1.3 术前相关辅助检查87例患者术前均行CT、MRI平扫与增强扫描检查。CT平扫上显示大多数岩斜区肿瘤为均一高密度或等密度,与颅底连接紧密,增强后肿瘤呈明显均一强化。MRI可以清楚地显示肿瘤的大小、位置、肿瘤侵犯的方向以及肿瘤周围是否存在水肿。尤其T2加权像可以指示岩斜区肿瘤周围的蛛网膜层是否存在,有无脑干水肿及脑干软膜侵犯。术前选择性行脑血管造影能明确肿瘤的供血动脉及基底动脉与肿瘤的关系。
1.4 手术87例患者在全身麻醉下行显微外科手术切除肿瘤,均为颞下经小脑幕入路。多模态组采用多模态神经导航系统辅助切除肿瘤,对照组手术切除肿瘤时则无术中实时影像学指导。多模态组术前将影像数据转移到多模态神经导航系统,通过影像融合和三维重建指导制定手术计划,术中精确定位引导显微手术(图 1)。对照组则根据术者的经验、体表解剖结构、手工测量等方法对肿瘤进行定位,并评估周边结构,其他显微手术操作原则和方法同多模态组。
|
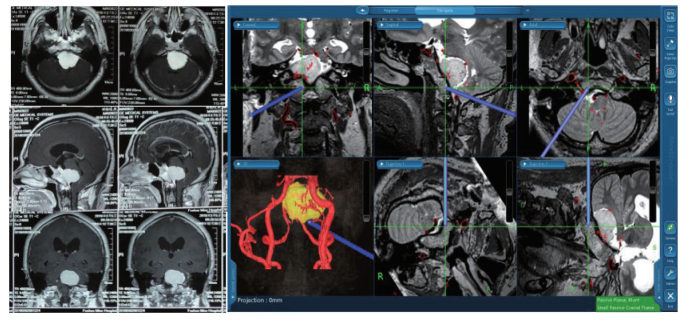
| 图 1 根据患者术前MRI影像资料进行多模态神经导航系统图像融合及三维重建模型,指示病变及其与周围重要组织结构间的空间关系,术中实时引导显微手术 Fig.1 Image fusion and 3D reconstruction model of multimodal neuronavigation system based on preoperative MRI image data of patients, indicatived lesion and its spatial relationship with the surrounding important tissue structure, real-time guided microsurgery during operation |
1.5 统计学分析
采用SPSS 22.0软件进行统计分析。计量资料用x±s表示,计数资料用百分比表示,2组间比较采用χ2检验。P < 0.05为差异有统计学意义。
2 结果 2.1 术中情况多模态组术中经神经导航系统确认基底动脉33例,其中32例与多普勒超声检查定位结果一致,1例由于动脉粥样硬化斑块多普勒超声未检出,但导航指示基底动脉。另有2例因肿瘤生长致脑组织漂移,导航并未给出明确指示。
2.2 术后1周内MRI复查结果多模态组肿瘤完全切除30例(85.7%),次全切除5例(14.3%);对照组完全切除33例(63.5%),次全切除19例(36.5%)。多模态组全切率明显高于对照组,2组比较差异有统计学意义(χ2=5.19,P < 0.05)。
2.3 术后并发症情况多模态组出现术后并发症8例,其中,出血1例,脑脊液漏2例,皮下积液3例,肺部感染1例,展神经功能异常1例。经对症处理后症状缓解,展神经功能异常患者于出院时能够自行眼球运动,仅有轻微视力模糊,随访期间恢复良好。对照组出现术后并发症17例,其中,出血1例,周围性面瘫1例,失语1例,动眼神经功能障碍2例,颅内感染1例,肢体肌力下降2例,肺部感染2例,脑脊液漏2例,皮下积液5例。经对症处理后症状缓解,神经功能障碍患者中,随访期间只有失语患者恢复欠佳,其余均可正常生活。对照组术后并发症发生率高于多模态组,但2组比较差异无统计学意义(P>0.05)。
术后1、3、6个月、1年及之后每年,对手术没有达到肿瘤全切的患者进行临床复查随诊、预后评估。术后随访期内,对照组有3例(5.8%)患者复发,多模态组无复发病例。
3 讨论岩斜区是蝶骨、颞骨及枕骨结合的区域,包含众多解剖结构,且彼此间关系复杂。该区紧邻许多重要神经血管结构,主要包括脑干、面神经、听神经、三叉神经、外展神经、迷走神经、舌咽神经和颈内动脉、后交通动脉、大脑后动脉、基底动脉等[6]。由于岩斜区肿瘤位置深在,且常常存在肿瘤累及重要神经功能区的情况,所以手术完全切除难度大,术后并发症发生率高。岩斜区肿瘤大多数为良性肿瘤,为了使患者获得良好的预后,期望能够完全切除肿瘤,同时术中尽可能地保护神经功能和重要供血血管。如何根据肿瘤的位置及血供关系选择合适的手术入路,尽量达到完全切除肿瘤,尽可能地保证患者术后神经功能恢复,减少术中操作难度及术后并发症发生率至关重要[7]。因此,术中实时影像指导识别、鉴定这些重要的颅内结构对实现岩斜区肿瘤的安全切除十分必要。
神经导航作为一种新型的图像导航工具,在现代神经外科手术中被广泛应用。它可以为颅内重要结构提供精确的术中定位,界定肿瘤边缘,对颅底病损的手术切除具有重要的指导意义[8]。通过影像融合和三维重建技术,多模态神经导航系统能够将脑功能影像资料与CT、MRI解剖成像等融合在一起,直观地展现岩斜区病变与重要神经传导束及血管之间的空间关系,并在术前帮助神经外科医师制定手术计划,还可以将影像坐标系统与手术视野内的位置动态链接起来,提供了术中实时持续定位的便利条件。多模态神经导航系统还可以与手术显微镜整合在一起,实现显微镜下实时导航,使术者能够在显微镜下直观地看到导航的指示[9-10]。岩斜区肿瘤常侵袭周围神经血管,结合磁共振血管造影、多普勒超声和神经导航技术对血管结构进行识别定位,多模态神经导航系统的图像融合和三维重建可以清楚地显示肿瘤与重要血管的关系,多普勒超声对血管回声的测定也可以准确定位血管位置和结构走行[11-12]。本研究中利用二者结合共同辅助岩斜区肿瘤的手术切除。术中神经电生理监测在颅底肿瘤切除术中可以早期预警并发症,避免损伤重要神经[13],在岩斜区肿瘤切除手术中能早期识别三叉神经、外展神经、面神经、听神经、舌咽神经、迷走神经等神经的损伤。
随着神经影像学的不断发展和进步,微创神经外科理念越来越成熟并得到推广,为了减少手术导致的创伤、加快术后神经功能的恢复以及提升患者术后的生活质量,目前,不再单纯追求肿瘤的完全切除以及强调“影像学治愈”的治疗理念已经成为神经外科发展的趋势,手术入路选择也更加倾向于简单化、小型化和实用化[7]。多模态神经导航系统在术中可以实时显示肿瘤的具体位置和其他重要的解剖标志,并将数据标记、存储,然后进行三维重建,其多图像融合和三维重建技术对术前规划和术中指导都有极大的意义[14-15]。三维重建用不同的颜色和图例展示了骨质、血管和病变的空间关系,在三维重建模型的基础上,结合神经外科医生的经验,可获取最佳的手术入路。
本研究中,多模态神经导航系统辅助下岩斜区肿瘤切除的患者肿瘤全切率和术后并发症的发生率均优于无术中实时影像学指导的患者。多模态神经导航系统通过多种影像融合和三维重建技术为岩斜区肿瘤切除提供实时影像学指导,显著提高了岩斜区肿瘤切除的安全性和有效性。然而,脑组织移位和定位错误的潜在可能性会降低神经导航系统的整体准确性,甚至成为并发症发生的危险因素,因此,本研究采用了多普勒超声和神经电生理监测技术,以弥补神经导航系统的不足。虽然多模态神经导航系统的敏感度和特异度仍需要进一步评估,然而不可否认的是,多模态神经导航系统是现代神经外科手术中实时引导的重要工具。
| [1] |
SAFAVI-ABBASI S, DE OLIVEIRA JG, DESHMUKH P, et al. The craniocaudal extension of posterolateral approaches and their combination:a quantitative anatomic and clinical analysis[J]. Oper Neurosurg (Hagerstown), 2010, 66(suppl_1): 54-64. DOI:10.1227/01.NEU.0000354366.48105.FE |
| [2] |
王忠诚. 神经外科学[M]. 武汉: 湖北科学技术出版社, 2015: 597-599.
|
| [3] |
ENCHEV Y. Neuronavigation:geneology, reality, and prospects[J]. Neurosurg Focus, 2009, 27(3): E11. DOI:10.3171/2009.6.FOCUS09109 |
| [4] |
MERT A, MICKO A, DONAT M, et al. An advanced navigation protocol for endoscopic transsphenoidal surgery[J]. World Neurosurg, 2014, 82(6Suppl): S95-S105. DOI:10.1016/j.wneu.2014.07.032 |
| [5] |
赵岩, 孙健, 杨学军. 多模态影像融合技术在神经外科的应用及进展[J]. 中国现代神经疾病杂志, 2012, 12(6): 645-650. DOI:10.3969/j.issn.1672-6731.2012.06.004 |
| [6] |
刘锋, 肖三潮, 千超, 等. 3种不同术式对岩斜区脑膜瘤患者疗效的比较[J]. 神经损伤与功能重建, 2018, 13(4): 208-210. DOI:10.16780/j.cnki.sjssgncj.2018.04.016 |
| [7] |
杨军. 颅底岩斜区脑膜瘤手术新的入路:经颞下-小脑幕入路切除岩斜区脑膜瘤特点的分析[J]. 中华临床医师杂志, 2013, 7(14): 6236-6238. DOI:10.3969/cma.j.issn.1674-0785.2013.14.007 |
| [8] |
STIEGLITZ LH. How reliable is neuronavigation?[J]. Praxis (Bern 1994), 2016, 105(4): 213-220. DOI:10.1024/1661-8157/a002259 |
| [9] |
FEIGL GC, KRISCHEK B, RITZ R, et al. Evaluation of a 3-dimensional voxel-based neuronavigation system with perspective image rendering for keyhole approaches to the skull base:an anatomical study[J]. World Neurosurg, 2014, 81(3/4): 609-616. DOI:10.1016/j.wneu.2013.10.039 |
| [10] |
ORRINGER DA, GOLBY A, JOLESZ F. Neuronavigation in the surgical management of brain tumors:current and future trends[J]. Expert Rev Med Devices, 2012, 9(5): 491-500. DOI:10.1586/erd.12.42 |
| [11] |
辻本文雄.腹部超声精细讲解[M].王建华, 李美兰, 译.北京: 科学出版社, 2018: 208-220.
|
| [12] |
RYGH OM, NAGELHUS HERNES TA, LINDSETH F, et al. Intraoperative navigated 3-dimensional ultrasound angiography in tumor surgery[J]. Surg Neurol, 2006, 66(6): 581-592. DOI:10.1016/j.surneu.2006.05.060 |
| [13] |
KRIEG SM, SHIBAN E, DROESE D, et al. Predictive value and safety of intraoperative neurophysiological monitoring with motor evoked potentials in glioma surgery[J]. Neurosurgery, 2012, 70(5): 1060-1070. DOI:10.1227/NEU.0b013e31823f5ade |
| [14] |
DOLATI P, GOKOGLU A, EICHBERG D, et al. Multimodal navigated skull base tumor resection using image-based vascular and cranial nerve segmentation:a prospective pilot study[J]. Surg Neurol Int, 2015, 6: 172. DOI:10.4103/2152-7806.170023 |
| [15] |
ZHANG F, HONG W, GUO Y, et al. Multimodal neuronavigation in microsurgery resection of brainstem tumors[J]. J Craniofac Surg, 2016, 27(8): e769-e772. DOI:10.1097/SCS.0000000000003123 |
 2019, Vol. 48
2019, Vol. 48




