文章信息
- 陈小斌, 李媛媛, 黄岭, 乔宠
- CHEN Xiaobin, LI Yuanyuan, HUANG Ling, QIAO Chong
- 重度子痫前期胎盘组织中Staufen1的表达及其意义
- Expression and Significance of Staufen1 in the Placenta in Severe Preeclampsia
- 中国医科大学学报, 2019, 48(9): 769-773
- Journal of China Medical University, 2019, 48(9): 769-773
-
文章历史
- 收稿日期:2018-10-10
- 网络出版时间:2019-09-09 9:04
子痫前期(preeclampsia,PE)是孕妇在妊娠期特有的疾病,严重威胁母胎健康。重度子痫前期(severe preeclampsia,SPE)及其并发症,如胎盘早剥、脑出血、胎儿生长受限等,是导致孕产妇和围产儿病死率升高的主要原因之一[1]。以孕34周为界,发病孕周 < 34周为早发型重度子痫前期(early-onset severe preeclampsia,ESPE),34周后为晚发型重度子痫前期(late-onset severe preeclampsia,LSPE)[2]。SPE病因至今尚不清楚,有学者[3]认为ESPE与滋养层细胞浸润不足和子宫螺旋小动脉重铸障碍有关;而LSPE与母体血管系统对妊娠的高敏感性和胎盘动脉硬化有关。MOL等[1]的研究表明,病理性妊娠时胎盘中某些相关蛋白出现异常表达,引起滋养细胞生物学行为失常,导致SPE发生。
Staufen蛋白是JOHNSTON在果蝇中发现的含有126个氨基酸的蛋白质,在果蝇胚胎发育过程中,参与细胞中mRNA的转运和翻译,属于双链RNA结合蛋白(double-stranded RNA binding protein,DRBP)家族。哺乳动物细胞中,Staufen蛋白有2个同源蛋白,即Staufen1(STAU1)和Staufen2,其中Staufen2蛋白只在神经元细胞中表达,而STAU1蛋白在机体各组织中都有表达[4]。研究[4-6]表明,STAU1蛋白可以与细胞中mRNA的3’-非翻译区(3’-UTR)结合,诱导mRNA降解,在细胞的发育、分化和凋亡中发挥着重要作用。研究[7]表明,STAU1蛋白还参与了胃癌的发生。胎盘滋养细胞的生物学行为与肿瘤细胞行为存在类似性,因此推测STAU1可能也参与了胎盘组织生物学行为的调节,并参与了SPE发生的调控。本研究拟通过检测STAU1在SPE胎盘组织中的表达情况,探讨其在PE发病中的作用,为临床早期诊断和治疗PE提供依据。
1 材料与方法 1.1 研究对象和分组选取2016年5月至2018年4月在中国医科大学附属盛京医院住院剖宫产分娩的SPE孕妇30例作为SPE组,并将其进一步分为ESPE组(15例)和LSPE组(15例);另选同期剖宫产分娩的正常妊娠孕妇30例作为对照组(N组),其中,孕周与ESPE组相对应者(EN组)10例,孕周与LSPE组相对应者(LN组)20例。SPE组和N组孕妇均为单胎、剖宫产分娩,排除生殖器官畸形、多胎及其他妊娠相关合并症(如妊娠期糖尿病、原发性高血压、慢性肾炎等),其中,EN组常由宫颈机能不全、胎膜早破、前置胎盘、孕妇合并严重先天性疾病等病因而终止妊娠。
SPE的诊断标准依据《妇产科学》第8版[2]。本研究经中国医科大学附属盛京医院伦理委员会批准(伦理批号:2017PS230K),符合医学伦理学规定,所有参加研究的孕妇及家属均知情同意。
1.2 方法 1.2.1 标本收集取剖宫产分娩后的无菌胎盘组织(在胎盘母体面距离脐带附着处2~3 cm范围取材,避开机化灶、钙化灶、出血灶等),用无菌生理盐水反复冲洗,分割成1 cm×1 cm×1 cm组织块,保存于液氮,用于提取RNA和蛋白质。另取1 cm×1 cm×1 cm组织块,4%多聚甲醛保存,行石蜡包埋、切片,用于免疫组织化学检测。
1.2.2 实时荧光定量PCR(real-time PCR,RT-PCR)取约50 mg胎盘组织,采用RNA iso试剂盒(日本TaKaRa公司)提取总RNA,检测RNA浓度,采用5X-ALL-In-One RT MasterMix试剂盒(加拿大abm公司)逆转录生成cDNA。行PCR,95 ℃ 10 min;95 ℃ 15 s,60 ℃ 1 min;95 ℃ 30 s,60 ℃ 15 s,40个循环,分析溶解曲线及循环阈值(cycle threshold,Ct),每个样本重复3次,取平均值。采用2-△△Ct法计算STAU1 mRNA经内参18S RNA标化后的相对表达水平。引物序列见表 1。
| Gene | Primer sequences(5’-3’) |
| STAU1 | |
| Forward | ATGGTATCGGCAAGGATGTG |
| Reverse | AGACATTGGTCCGTTTCCTG |
| 18SRNA | |
| Forward | ATCCTCAGTGAGTTCTCCCG |
| Reverse | CTTTGCCATCACTGCCATTA |
1.2.3 Western blotting
取约50 mg胎盘组织,提取蛋白质,BCA法检测蛋白浓度,变性后保存于-20 ℃。行凝胶电泳,转膜60 min,5%脱脂奶粉封闭2 h后,加入兔抗人STAU1多克隆抗体(1︰500稀释,美国Signalway公司)和兔抗人GAPDH多克隆抗体(1︰1 000稀释,杭州贤至生物科技有限公司),4 ℃过夜。复温30 min后,加入辣根过氧化物酶标记的山羊抗兔抗体(1︰5 000稀释,北京中杉金桥生物技术有限公司)孵育2 h。ECL显色,应用Biosystems azure C300成像系统采集图像并分析。
1.2.4 免疫组织化学检测取4%多聚甲醛固定后的胎盘组织,石蜡包埋48 h后,制石蜡切片,厚3~4 μm。采用免疫组织化学检测试剂盒(中国福州迈新生物技术开发有限公司)行免疫组化染色。石蜡切片经脱蜡、封闭内源性过氧化物酶30 min,柠檬酸缓冲液抗原修复7 min,封闭非特异性抗原/电荷45 min,加入一抗(STAU1 1︰200稀释),4 ℃孵育10~12 h,二抗(生物素标记的羊抗兔/鼠IgG)孵育30 min,DAB显色,苏木素复染核3~5 min,棕黄色为阳性。应用NIS-Elements软件(日本Nikon公司)对图像进行采集分析。
1.3 统计学分析采用SPSS 22.0统计软件进行统计分析,计量资料用x±s表示,采用t检验或非参数检验(如Mann-Whitney U检验)行组间比较。P<0.05为差异有统计学意义。
2 结果 2.1 基本资料ESPE组和EN组及LSPE组和LN组患者的年龄、孕周间均无统计学差异(P>0.05),而ESPE组和LSPE组的收缩压、舒张压及24 h尿蛋白定量均显著高于同期妊娠对照组,差异有统计学意义(P < 0.001)。见表 2。
| Group | n | Age(year) | Gestational week (week) |
Systolic pressure (mmHg) |
Diastolic pressure (mmHg) |
24-hour urinary protein quantity(g) |
| SPE group | 30 | |||||
| ESPE group | 15 | 32.1±15.6 | 31.2±1.9 | 166.9±11.3 | 103.0±7.2 | 9.4±8.6 |
| LSPE group | 15 | 32.1±5.5 | 36.7±1.2 | 164.9±1.2 | 106.2±9.5 | 4.5±5.1 |
| N group | 30 | |||||
| EN group | 10 | 30.3±5.0 | 32.1±1.2 | 112.8±11.2 | 67.2±7.0 | N/A |
| LN group | 20 | 32.4±15.1 | 37.4±1.3 | 112.8±7.1 | 73.0±6.6 | N/A |
| P1 | 0.333 | 0.191 | < 0.001 | < 0.001 | < 0.001 | |
| P2 | 0.948 | 0.098 | < 0.001 | < 0.001 | < 0.001 | |
| The P1 value represents the probability of comparison between the ESPE group and the EN group;the P2 value represents the probability of comparison between the LSPE group and the LN group;N/A represents the examination was not performed after admission. | ||||||
2.2 胎盘组织中STAU1 mRNA的表达情况
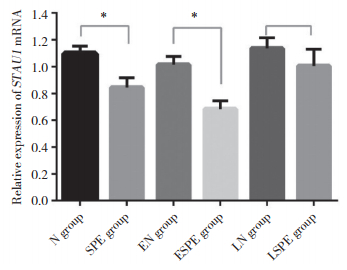
SPE组胎盘组织中STAU1 mRNA的表达水平(0.844±0.074)显著低于N组(1.096±0.057),差异有统计学意义(P < 0.01);其中,ESPE组胎盘组织中STAU1 mRNA的表达水平(0.683±0.061)显著低于EN组(1.015±0.060),差异有统计学意义(P < 0.01),而LSPE组胎盘组织STAU1 mRNA表达水平(1.005±0.124)与LN组(1.136±0.080)比较无统计学差异(P>0.05),见图 1。
|
| *P < 0.01. 图 1 胎盘组织中STAU1 mRNA表达水平 Fig.1 STAU1 mRNA expression levels in different placental tissues |
2.3 胎盘组织中STAU1蛋白的表达情况
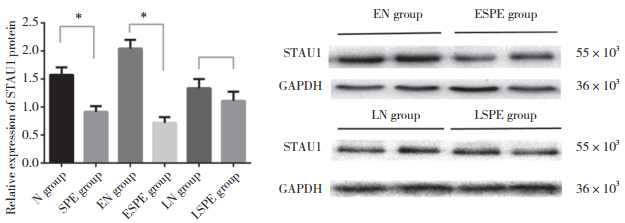
SPE组胎盘组织中STAU1蛋白的表达水平(0.916±0.102)显著低于N组(1.573±0.135),差异有统计学意义(P < 0.001);其中,ESPE组胎盘组织中STAU1蛋白表达水平(0.719±0.101)显著低于EN组(2.025±0.155),差异有统计学意义(P < 0.001),而LSPE组胎盘组织STAU1蛋白表达水平(1.112±0.165)与LN组(1.337±0.165)比较无统计学差异(P>0.05),见图 2。
|
| * P < 0.001. 图 2 胎盘组织中STAU1蛋白表达水平 Fig.2 STAU1 protein expression levels in different placental tissues |
2.4 胎盘组织中STAU1蛋白的表达定位情况
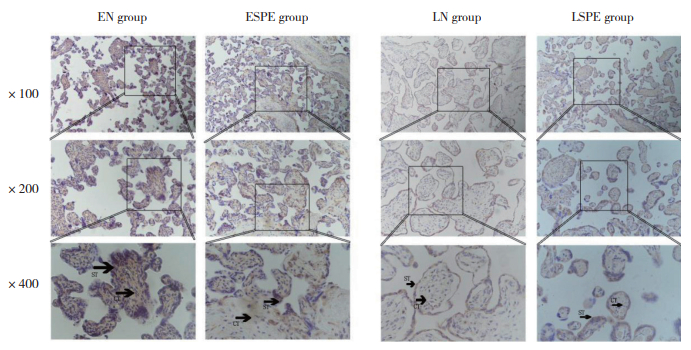
4组胎盘组织的细胞滋养细胞和合体滋养细胞细胞中均有STAU1蛋白的表达,且主要在合体滋养细胞的细胞质中表达,其中ESPE组STAU1蛋白表达水平显著低于EN组(0.014±0.008 vs 0.019±0.002,P < 0.001),LSPE组与LN组则无统计学差异(0.011±0.001 vs 0.012±0.003,P>0.05),见图 3。
|
| ST, syncytiotrophoblasts; CT, cytotrophoblasts. 图 3 胎盘组织中STAU1蛋白的表达定位 Fig.3 Localization of STAU1 protein in different placental tissues |
3 讨论
PE是指妊娠20周后孕妇出现高血压并存在多器官及系统受累,严重影响孕产妇及围产儿健康,尤其SPE及其严重的并发症是导致母婴死亡的重要原因。研究[1]发现PE存在多因素、多机制、多通路发病机制,但具体的发病机制仍不明确。在妊娠早期,细胞滋养细胞促使子宫螺旋动脉发生重构,拟合并替代胎盘组织中的血管内皮细胞和部分血管平滑肌,使子宫螺旋小动脉从高排低阻状态变成低排高阻状态,建立有效的母体和胎儿之间的营养物质交换,维持母体正常妊娠及胎儿的正常发育。同时,滋养细胞浸润行为受到时间和空间的严格调控,滋养细胞浸润过浅可能会导致PE的发生[8]。目前,研究[3, 9]发现多种基因参与滋养细胞浸润能力的调控,如TINP-1、KIR2DL1、MMPs等。
STAU1蛋白是一种含有多个双链RNA的RNA结合蛋白[10]。SUGIMOTO等[11]研究发现,STAU1蛋白具有mRNA和长非编码RNA的结合区域,能分别与其3’-UTR和5’-UTR端结合,参与mRNA的转运、局部翻译和RNA代谢、加工等生物学功能[12]。BONNET-MAGNAVAL等[13]研究发现,STAU1还是一种应激反应基因,正常生理情况下,STAU1 mRNA可以与内部核糖体进入位点(internal ribosome entry sites,IRES)相结合,启动编码细胞内质网中抗氧化蛋白mRNA的翻译,使细胞具有抗氧化应激的保护作用。KRETZ等[6]研究发现,STAU1可与LncRNA相结合,并在人表皮细胞分化过程中发挥着重要的作用。SAKURAI等[14]研究发现,敲低STAU1能够恢复ADAR1敲低引起的应激细胞凋亡,在胃癌细胞中,STAU1可与CDKN2B mRNA的3’-UTR结合,降解CDKN2B,促进胃癌细胞增殖[7]。提示STAU1在正常细胞及肿瘤细胞中发挥着重要的作用,而目前尚无关于STAU1在胎盘滋养细胞中的表达情况及其对SPE影响的研究。
本研究发现,STAU1 mRNA和蛋白在胎盘合体滋养细胞和细胞滋养细胞中均有表达,其中以合体滋养细胞为主;通过比较发现,SPE组(ESPE组和LSPE组)STAU1 mRNA和蛋白的表达均低于N组,表明STAU1很有可能参与了SPE的发病机制,其中STAU1 mRNA和蛋白在ESPE组的表达低于EN组,提示STAU1可能与子宫螺旋小动脉重铸障碍有关,导致滋养层细胞浸润能力不足,从而参与PE的发病;而LSPE组STAU1 mRNA和蛋白的表达与LN组无统计学差异,可能是由于LSPE的发生主要与内皮细胞损伤及胎盘动脉硬化、全身系统性免疫炎症反应有关[15],进一步说明STAU1蛋白可能在滋养细胞浸润行为中发挥着重要的作用。
综上所述,本研究结果表明,STAU1的表达水平可能与SPE的发病有关,尤其与ESPE的发生相关。
| [1] |
MOL BWJ, ROBERTS CT, THANGARATINAM S, et al. Pre-eclampsia[J]. Lancet, 2016, 387(10022): 999-1011. DOI:10.1016/s0140-6736(15)00070-7 |
| [2] |
谢幸, 苟文丽. 妇产科学[M]. 第8版. 北京: 人民卫生出版社, 2013: 66-67.
|
| [3] |
HUHN O, CHAZARA O, IVARSSON MA, et al. High-resolution genetic and phenotypic analysis of kir2dl1 alleles and their association with pre-eclampsia[J]. J Immunol, 2018, 201(9): 2593-2601. DOI:10.4049/jimmunol.1800860 |
| [4] |
GONG C, MAQUAT LE. lncRNAs transactivate STAU1-mediated mRNA decay by duplexing with 3'UTRs via Alu elements[J]. Nature, 2011, 470(7333): 284-288. DOI:10.1038/nature09701 |
| [5] |
KIM MY, PARK J, LEE JJ, et al. Staufen1-mediated mRNA decay induces Requiem mRNA decay through binding of Staufen1 to the Requiem 3'UTR[J]. Nucleic Acids Res, 2014, 42(11): 6999-7011. DOI:10.1093/nar/gku388 |
| [6] |
KRETZ M, SIPRASHVILI Z, CHU C, et al. Control of somatic tissue differentiation by the long non-coding RNA TINCR[J]. Nature, 2013, 493(7431): 231-235. DOI:10.1038/nature11661 |
| [7] |
XU TP, WANG YF, XIONG WL, et al. E2F1 induces TINCR transcriptional activity and accelerates gastric cancer progression via activation of TINCR/STAU1/CDKN2B signaling axis[J]. Cell Death Dis, 2017, 8(6): e2837. DOI:10.1038/cddis.2017.205 |
| [8] |
陈小斌, 陈国庆, 乔宠. 转录因子在滋养细胞浸润行为调控中的作用[J]. 中国现代医学杂志, 2018, 28(3): 46-50. DOI:10.3969/j.issn.1005-8982.2018.03.009 |
| [9] |
LASKOWSKA M. Altered maternal serum matrix metalloproteinases MMP-2, MMP-3, MMP-9, and MMP-13 in severe early-and late-onset preeclampsia[J]. Biomed Res Int, 2017, 2017: 6432426. DOI:10.1155/2017/6432426 |
| [10] |
PAUL S, DANSITHONG W, FIGUEROA KP, et al. Staufen1 links RNA stress granules and autophagy in a model of neurodegeneration[J]. Nat Commun, 2018, 9(1): 3648. DOI:10.1038/s41467-018-06041-3 |
| [11] |
SUGIMOTO Y, VIGILANTE A, DARBO E, et al. hiCLIP reveals the in vivo atlas of mRNA secondary structures recognized by Staufen 1[J]. Nature, 2015, 519(7544): 491-494. DOI:10.1038/nature14280 |
| [12] |
PEREDO J, VILLACÉ P, ORTÍN J, et al. Human Staufen1 associates to miRNAs involved in neuronal cell differentiation and is required for correct dendritic formation[J]. PLoS One, 2014, 9(11): e113704. DOI:10.1371/journal.pone.0113704 |
| [13] |
BONNET-MAGNAVAL F, PHILIPPE C, VAN DEN BERGHE L, et al. Hypoxia and ER stress promote Staufen1 expression through an alternative translation mechanism[J]. Biochem Biophys Res Commun, 2016, 479(2): 365-371. DOI:10.1016/j.bbrc.2016.09.082 |
| [14] |
SAKURAI M, SHIROMOTO Y, OTA H, et al. ADAR1 controls apoptosis of stressed cells by inhibiting Staufen1-mediated mRNA decay[J]. Nat Struct Mol Biol, 2017, 24(6): 534-543. DOI:10.1038/nsmb.3403 |
| [15] |
SARWEEN N, DRAYSON MT, HODSON J, et al. Humoral immunity in late-onset Pre-eclampsia and linkage with angiogenic and inflammatory markers[J]. Am J Reprod Immunol, 2018, 80(5): e13041. DOI:10.1111/aji.13041 |
 2019, Vol. 48
2019, Vol. 48




