文章信息
- 胡明, 张淑红, 陈跟林, 凌存宝, 樊伟平, 孙海燕, 刘爽, 张虎
- HU Ming, ZHANG Shuhong, CHEN Genlin, LING Cunbao, FAN Weiping, SUN Haiyan, LIU Shuang, ZHANG Hu
- 泛癌症分析DEAH盒解旋酶16的表达及其预后意义
- Pan-Cancer Analysis of DEAH-Box Helicase 16 Expression and Prognostic Significance
- 中国医科大学学报, 2019, 48(3): 201-204
- Journal of China Medical University, 2019, 48(3): 201-204
-
文章历史
- 收稿日期:2018-04-28
- 网络出版时间:2019-02-28 14:05
2. 佳木斯大学基础医学院生物学教研室, 黑龙江 佳木斯 154007;
3. 江苏医药职业学院基础医学部生物化学教研室, 江苏 盐城 224005;
4. 江苏医药职业学院护理学院内科护理学教研室, 江苏 盐城 224005
2. Department of Biology, Basic Medical College, Jiamusi University, Jiamusi 154007, China;
3. Department of Biochemistry, Basic Medical College, Jiangsu Vocational College of Medicine, Yancheng 224005, China;
4. Department of Internal Medicine Nursing, College of Nursing, Jiangsu Vocational College of Medicine, Yancheng 224005, China
癌症和肿瘤基因图谱(the cancer genome atlas,TCGA)组织于2012年发起泛癌症研究计划。泛癌症研究将多种肿瘤类型整合,从表观基因组、基因组、转录组和蛋白质组等多组学高通量数据角度出发,揭示不同肿瘤之间的差异性和相似性,进而指导肿瘤诊断、预后以及治疗方案的制定[1]。从广义上讲,任何比较肿瘤间的差异性和相似性的研究均可以称作泛癌症研究。DEAH盒解旋酶16(DEAH-box helicase 16,DHX16)是一种包含天冬氨酸-谷氨酸-丙氨酸-天冬氨酸保守基序的蛋白,参与人类前体RNA的剪接过程[2-3],但是在肿瘤研究中鲜有报道。本研究拟泛癌症分析DHX16在各种肿瘤中的表达、预后意义和可能作用机制。
1 材料与方法 1.1 数据来源TCGA门户网站UALCAN(http://ualcan.path.uab.edu)[4]可深入分析TCGA基因表达谱数据。UALCAN访问TCGA的31种癌症类型的3级RNA测序和临床数据,可以执行以下分析:(1)肿瘤和正常组织间查询基因的差异表达,基于肿瘤分期、分级、患者种族、体质量及其他各种临床病理特征划分的肿瘤亚组间查询基因的差异表达;(2)评估基因表达水平和临床病理特征对患者生存的影响;(3)鉴定个体癌症类型中表达上调和下调基因。该门户网站可以作为平台验证靶基因的表达,并识别肿瘤亚组特异性候选生物标志物。
DHX16相互作用蛋白来自InBio MapTM(https://www.intomics.com/inbio/map/#home),该平台主要研究和可视化蛋白间相互作用,具有高覆盖、高质量、便捷和透明的特点。DAVID Bioinformatics Resources 6.8(https://david.ncifcrf.gov/)作为生物信息学分析工具。
1.2 分析方法登录UALCAN首页,点击“Analysis”,新页面下方点击“Scan my genes”,输入待查询基因名称“DHX16”,查询。分别点击红色显示的癌症简称,下载基因差异表达和生存曲线结果。
DHX16相互作用蛋白基因本体(GO)和KEGG信号通路分析,通过InBio MapTM平台查询并下载DHX16相互作用的蛋白质谱,利用DAVID 6.8进行数据GO和KEGG分析,下载结果并作图。
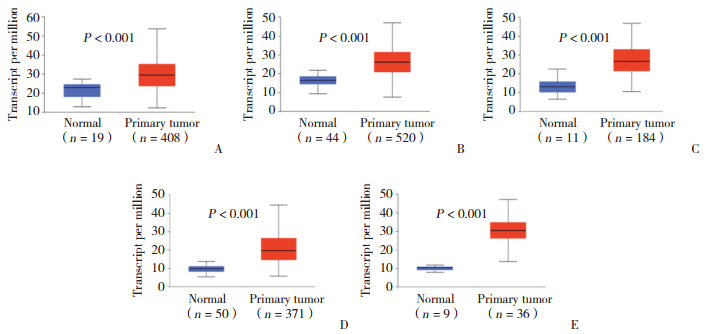
2 结果 2.1 泛肿瘤分析DHX16的差异表达结果显示,膀胱尿路上皮癌、头颈部鳞状细胞癌、食管癌、肝脏肝细胞癌和胆管癌中DHX16基因表达较各自正常组织显著上调(均P < 0.001),见图 1。
|
| A, bladder urothelial carcinoma; B, head and neck squamous cell carcinoma; C, esophageal carcinoma; D, liver hepatocellular carcinoma; E, cholangiocarcinoma. 图 1 DHX16在膀胱尿路上皮癌、头颈部鳞状细胞癌、食管癌、肝脏肝细胞癌和胆管癌及其癌旁组织中的表达 Fig.1 Expression of DHX16 in bladder urothelial carcinoma, head and neck squamous cell carcinoma, esophageal carcinoma, liver hepatocellular carcinoma, and cholangiocarcinoma |
2.2 泛肿瘤分析DHX16的表达与预后关系
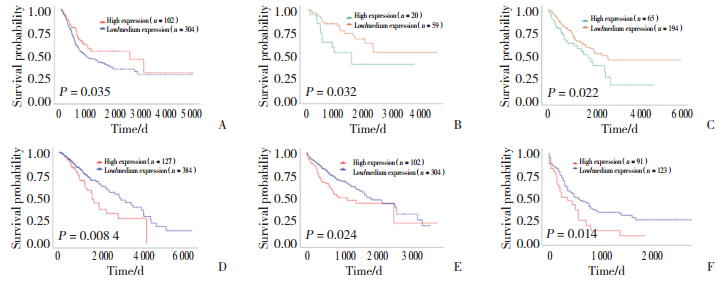
结果显示,与DHX16低表达比较,DHX16高表达利于膀胱尿路上皮癌预后(P < 0.05),见图 2A;DHX16高表达不利于肾上腺皮质癌、脑低级别胶质瘤、肝脏肝细胞癌和急性髓样白血病的预后(均P < 0.05),见图 2B~2F。
|
| A, bladder urothelial carcinoma; B, adrenocortical carcinoma; C, sarcoma; D, brain lower grade glioma; E, liver hepatocellular carcinoma; F, acute myeloid leukemia. 图 2 DHX16高表达与膀胱尿路上皮癌、肾上腺皮质癌、肉瘤、脑低级别胶质瘤、肝脏肝细胞癌和急性髓样白血病预后的关系 Fig.2 Relationship between DHX16 expression and prognosis of bladder urothelial carcinoma, adrenocortical carcinoma, sarcoma, brain lower grade glioma, liver hepatocellular carcinoma, and acute myeloid leukemia |
2.3 DHX16相互作用蛋白基因本体(GO)和KEGG信号通路分析
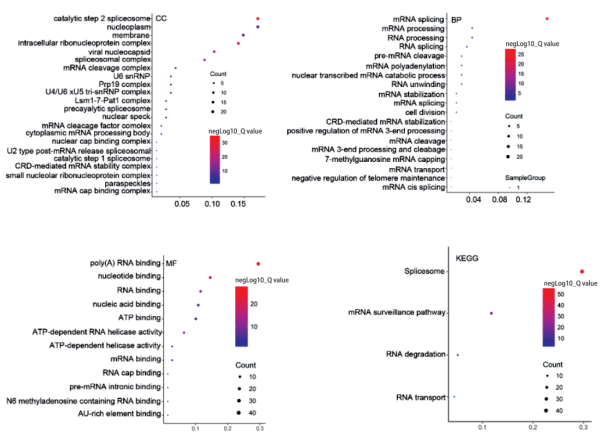
细胞定位分析结果显示DHX16相互作用蛋白主要定位于剪接体、细胞核、质膜、胞内核糖核蛋白复合体等;生物学过程分析结果显示这些蛋白主要参与mRNA剪接、加工等过程;分子功能分析结果显示这些蛋白主要结合多聚腺苷酸(poly A)RNA、核苷酸、核酸、mRNA内含子等,具有RNA解旋酶活性等功能;KEGG信号通路分析结果显示DHX16相互作用蛋白主要参与剪接体、mRNA监测通路、RNA降解和RNA转运过程。见图 3。
|
| 图 3 DHX16相互作用蛋白的基因本体和KEGG信号通路分析 Fig.3 GO and KEGG analyses of proteins interaction with DHX16 |
3 讨论
目前,肿瘤仍是全球范围内重要的公共健康安全问题[5],肿瘤异质性极大制约着肿瘤治疗。肿瘤异质性内在体现为分子表达谱的差异,外在表现为患者预后、复发等区别[6]。肿瘤的精准治疗需要解决异质性问题,根据患者个体化信息合理治疗,减少药物不良反应[7]。而不同类型肿瘤间的相似性是研究肿瘤的共同特点,不同来源肿瘤的分子水平相似度可能比同种肿瘤之间的相似度更高[8]。与肿瘤的异质性一样,肿瘤相似性也能够加深认识肿瘤的发生发展机制,并且可以推动临床治疗方案优化和筛选药物。泛癌症分析旨在通过揭示肿瘤间的差异性和相似性指导肿瘤诊断、治疗和预后[1]。
本研究通过泛癌症分析,发现DHX16在膀胱尿路上皮癌、头颈部鳞状细胞癌、食管癌、肝脏肝细胞癌和胆管癌中均高表达,提示DHX16参与多种肿瘤的发生和发展过程。DEAD盒蛋白是一类包含DEAD的RNA解旋酶。该类蛋白参与RNA二级结构改变的多种细胞过程,包括翻译起始、细胞核和线粒体中的RNA剪接以及核糖体和剪接体的组装。基于此类蛋白的分布特征,一些家族成员参与胚胎发生、精子生成以及细胞生长和分裂[9]。DEAD盒蛋白功能类似于酵母分裂Prp8蛋白,参与细胞周期进展。DEAD盒蛋白编码基因位于染色体6p21.3,即主要组织相容性复合体编码区,此区域与多种恶性、遗传性自身免疫性疾病相关[10]。DHX16是DEAD盒蛋白家族成员之一,具有ATP结合RNA解旋酶活性,参与前体-mRNA(pre-mRNA)剪接过程[2, 11]。重要的是,突变DHX16可导致未剪接前体-mRNA滞留细胞核内[12],不能进行正常的转运和表达,并且mRNA剪接相关基因DHX16单核苷酸多态性位点rs115420460与肺癌风险相关[13]。DHX16的高表达可能通过增加促癌基因前体-mRNA的剪接、转运出核并表达,参与癌症的发生和进展。
本研究还发现DHX16高表达除了利于膀胱尿路上皮癌的预后之外,不利于肾上腺皮质癌、肉瘤、脑低级别胶质瘤、肝脏肝细胞癌和急性髓样白血病的预后。因此推测,膀胱尿路上皮癌中DHX16高表达后的作用机制不同于其他5种肿瘤,可以理解为同一分子在不通癌症中作用机制不同,甚至有可能相反。鉴于DHX16高表达均不利于上述5种肿瘤的预后,推测DHX16发挥相似功能。
本研究通过蛋白质相互作用平台InBio MapTM获得与DHX16相互作用的蛋白质谱,进行了GO和KEGG生物信息学分析,结果显示DHX16主要定位于剪接复合体和核糖核蛋白体,结合RNA,具有RNA解旋酶活性,介导剪接体、mRNA监测通路、RNA降解和RNA转运过程。
总之,泛癌症研究服务于精准医疗,探寻不同类型肿瘤之间的相似性可以开发相同药物,减少不良反应,增加适用人群;发现共同的诊断和预后标志物,为临床制定合理治疗方案提供保障。本研究提供了一个适应5种肿瘤预后的潜在标志物,后续工作需要通过临床数据验证DHX16作为预后标志物的可能性,并研究DHX16在癌症中共同的作用机制,为干预癌症发病和进展提供潜在靶点。
| [1] |
张坤, 王红. 肿瘤基因组图谱泛癌分析计划[J]. 中国肺癌杂志, 2015, 18(4): 219-223. DOI:10.3779/j.issn.1009-3419.2015.04.02 |
| [2] |
GENCHEVA M, KATO M, NEWO AN, et al. Contribution of DEAH-box protein DHX16 in human pre-mRNA splicing[J]. Biochem J, 2010, 429(1): 25-32. DOI:10.1042/BJ20100266 |
| [3] |
RAPPSILBER J, RYDER U, LAMOND AI, et al. Large-scale proteomic analysis of the human spliceosome[J]. Genome Res, 2002, 12(8): 1231-1245. DOI:10.1101/gr.473902 |
| [4] |
CHANDRASHEKAR DS, BASHEL B, BALASUBRAMANYA SAH, et al. UALCAN:a portal for facilitating tumor subgroup gene expression and survival analyses[J]. Neoplasia, 2017, 19(8): 649-658. DOI:10.1016/j.neo.2017.05.002 |
| [5] |
SIEGEL RL, MILLER KD, JEMAL A. Cancer statistics, 2017[J]. CA Cancer J Clin, 2017, 67(1): 7-30. DOI:10.3322/caac.21387 |
| [6] |
MARUSYK A, POLYAK K. Tumor heterogeneity:causes and consequences[J]. Biochimica Biophysica Acta, 2010, 1805(1): 105-117. DOI:10.1038/nature20805 |
| [7] |
COLLINS FS, VARMUS H. A new initiative on precision medicine[J]. NEJM, 2015, 372(9): 793-795. DOI:10.1056/NEJMp1500523 |
| [8] |
CANCER GENOME ATLAS RESEARCH NETWORK, ANALYSIS WORKING GROUP. Integrated genomic characterization of oesophageal carcinoma[J]. Nature, 2017, 541(7636): 169-175. DOI:10.1038/nature20805 |
| [9] |
PUTIRI E, PELEGRI F. The zebrafish maternal-effect gene mission impossible encodes the DEAH-box helicase Dhx16 and is essential for the expression of downstream endodermal genes[J]. Dev Biol, 2011, 353(2): 275-289. DOI:10.1016/j.ydbio.2011.03.001 |
| [10] |
CORDIN O, BANROQUES J, TANNER NK, et al. The DEAD-box protein family of RNA helicases[J]. Gene, 2006, 15(367): 17-37. |
| [11] |
BESSONOV S, ANOKHINA M, WILL CL, et al. Isolation of an active step Ⅰ spliceosome and composition of its RNP core[J]. Nature, 2008, 452(7189): 846-848. DOI:10.1038/nature06842 |
| [12] |
GENCHEVA M, LIN TY, WU X, et al. Nuclear retention of unspliced pre-mRNAs by mutant DHX16/hPRP2, a spliceosomal DEAH-box protein[J]. J Biol Chem, 2010, 285(46): 35624-35632. DOI:10.1074/jbc.M110.122309 |
| [13] |
PAN Y, LIU H, WANG Y, et al. Associations between genetic variants in mRNA splicing-related genes and risk of lung cancer:a pathway-based analysis from published GWASs[J]. Sci Rep, 2017, 17(7): 44634. DOI:10.1038/srep44634 |
 2019, Vol. 48
2019, Vol. 48