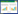文章信息
- 张越, 马涛, 杜静, 刘志
- ZHANG Yue, MA Tao, DU Jing, LIU Zhi
- 胃肠道间质瘤患者行急诊手术的临床及预后分析
- Clinical and Prognostic Analysis of Emergency Operation in Patients with Gastrointestinal Stromal Tumor
- 中国医科大学学报, 2019, 48(12): 1127-1131
- Journal of China Medical University, 2019, 48(12): 1127-1131
-
文章历史
- 收稿日期:2018-10-09
- 网络出版时间:2019-12-06 10:32
胃肠间质瘤(gastrointestinal stromal tumor,GIST)由MAZUR和CLARK [1]于1983年首次提出,是一种起源于Cajal间质细胞(又称胃肠道起搏细胞)或来源于更原始的、具有多分化潜能的中胚层间质干细胞的胃肠道恶性肿瘤[2]。消化道出血、肿瘤破裂、腹痛是急诊GIST患者主要的临床表现,其中伴有消化道出血的患者常因消化道活动性出血或失血性休克需急诊手术治疗。目前鲜有关于GIST急诊手术的相关研究及指南,对于需行急诊手术的GIST患者的术后治疗尚存争议。因此,本研究拟对我院近年收治的、经病理证实的184例GIST患者的临床病理及预后资料进行分析,探讨行急诊手术对患者预后的影响,以期指导GIST治疗。
1 材料与方法 1.1 研究对象收集2010年9月至2018年3月于中国医科大学附属第一医院手术治疗且病理诊断为GIST的病例共195例,回顾性分析其临床资料。随访截止至2018年6月31日,11例患者因未能随访到预后情况,排除出本研究,最终共纳入184例。将184例患者分为急诊手术组(30例)与非急诊手术组(154例)。
纳入标准:收入院后行手术治疗,术后病理诊断为原发性GIST;临床资料完整;肿瘤最大直径 > 2 cm;无其他消化道出血病史或消化系统肿瘤。排除标准:妊娠和哺乳期妇女;罹患其他恶性肿瘤;术后因基础状态差入重症监护病房者。
1.2 研究方法收集临床资料,包括性别、年龄、是否行急诊手术;术后是否进行靶向治疗;术前中性粒细胞计数、淋巴细胞计数、是否合并出血;术中诊断原发肿瘤部位、肿瘤大小、是否完全切除肿瘤;术后病理诊断结果(免疫组化CD34、CD117、DOG1,每50倍高倍镜视野核分裂像数)。将2组数据的临床资料、术后治疗、复发与生存情况进行比较与分析。
1.3 统计学分析采用SPSS 22.0统计软件进行分析,计数资料、等级资料采用Pearson χ2检验,计量资料采用独立样本t检验。预后分析在Kaplan-Meier生存分析单因素分析基础上,对有统计学意义的数据用Cox回归模型进行多因素分析。P < 0.05为差异有统计学意义。
2 结果184例GIST患者中,男92例,女92例;平均年龄57.7岁;109例患者肿瘤原发部位为胃,其余75例为非胃来源;173例患者行肿瘤完全(removed complete,R0)切除,135例患者未行术后辅助治疗。2组患者在术前是否合并出血、中性粒细胞计数、淋巴细胞计数、原发肿瘤部位方面,有统计学差异(P < 0.05)。急诊手术组的复发时间及生存时间均小于非急诊手术组,差异有统计学意义(P < 0.05)。2组性别、年龄、肿瘤大小、是否行完全切除、术后是否接受靶向治疗、核分裂像、术后免疫组化结果(CD34、CD117、DOG1)方面,均无统计学差异(P > 0.05)。见表 1。
| Item | Emergency group(n =30) | Non-emergency group(n =154) | P |
| Gender(male/female) | 17/13 | 75/79 | 0.146 |
| Age(year) | 58.36±11.07 | 57.51±10.71 | 0.814 |
| Primary site of tumor(gastric/non-gastric) | 9/21 | 100/54 | 0.001 |
| Tumor size(cm) | 8.13±5.09 | 6.53±4.99 | 0.678 |
| Complete excision(R0/R1) | 27/3 | 146/8 | 0.402 |
| Targeted therapy(yes/no) | 11/19 | 38/116 | 0.364 |
| Mitotic image(≤5/50 HPF/>5/50 HPF) | 9/21 | 46/154 | 0.989 |
| CD34(+/-) | 28/2 | 136/18 | 0.349 |
| CD117(+/-) | 28/2 | 135/19 | 0.294 |
| DOG1(+/-) | 27/3 | 135/19 | 0.687 |
| Bleeding(yes/no) | 21/9 | 31/123 | <0.001 |
| Neutrophil(×109/L) | 8.06±3.96 | 4.08±2.15 | <0.001 |
| Lymphocyte(×109/L) | 1.31±0.69 | 1.86±0.69 | <0.001 |
| HPF, high power field. | |||
单因素及多因素Cox回归分析影响患者术后生存情况的相关因素,结果发现,可能影响患者术后生存的因素包括肿瘤直径 > 5 cm、核分裂像 > 5/高倍镜视野、原发肿瘤为非胃来源、行急诊手术,其他因素(性别、年龄、是否行完全切除、术后是否接受化疗、术后CD34、CD117、DOG1免疫组化结果)差异均无统计学意义。且急诊手术可能是GIST患者预后不良的独立危险因素。见表 2。
| Factor | Death | Survival | χ2 | P |
| Gender | 0.002 | 0.961 | ||
| Male | 11 | 81 | ||
| Female | 11 | 81 | ||
| Tumor size | 7.565 | 0.006 | ||
| ≤5 cm | 7 | 95 | ||
| >5 cm | 15 | 67 | ||
| Age(year) | 0.314 | 0.575 | ||
| ≤60 | 12 | 98 | ||
| >60 | 10 | 64 | ||
| Primary site | 3.906 | 0.048 | ||
| Gastric | 9 | 100 | ||
| Non-gastric | 13 | 62 | ||
| Mitotic image | 6.32 | 0.012 | ||
| ≤5/50 HPF | 11 | 117 | ||
| >5/50 HPF | 11 | 45 | ||
| Complete excision | 1.375 | 0.241 | ||
| R0 | 20 | 152 | ||
| R1 | 2 | 10 | ||
| Emergency operation | 9.661 | 0.002 | ||
| Yes | 8 | 22 | ||
| No | 14 | 140 | ||
| CD34 | 0.154 | 0.695 | ||
| + | 4 | 16 | ||
| - | 18 | 146 | ||
| CD117 | 0.118 | 0.731 | ||
| + | 4 | 19 | ||
| - | 18 | 143 | ||
| DOG1 | 0.829 | 0.363 | ||
| + | 4 | 22 | ||
| - | 18 | 140 | ||
| Targeted therapy | 1.867 | 0.172 | ||
| Yes | 8 | 40 | ||
| No | 14 | 122 |
2组共有39例患者术后复发,其中,急诊手术组11例,非急诊手术组28例;共有22例患者死亡,其中,急诊手术组8例,非急诊手术组14例;急诊手术组复发率为36.7%,死亡率为26.7%,均高于非急诊手术组的复发率及死亡率(分别为18.3%、9.2%)。绘制Kaplan-Meier生存分析曲线可得出非急诊手术组无论是无瘤生存期还是总生存期均优于急诊手术组,见图 1。
|
| A, survivorship curve; B, recurrence curve. 图 1 急诊手术组与非急诊手术组的生存曲线与复发曲线 Fig.1 Survival curve and recurrence curve of emergency operation group and non-emergency operation group |
3 讨论
GIST约占间叶源性肿瘤的80%,起源于固有肌层和肌间神经丛的Cajal间质细胞[3],约占胃肠道恶性肿瘤的1%[4]。大多数GIST发生于胃(60%~70%)或小肠(25%~35%),结肠、直肠、阑尾(合计5%)和食管(2%~3%)是比较罕见的发生部位[5-7]。功能获得性的基因突变所致的Ⅲ型酪氨酸激酶或血小板源性生长因子受体酪氨酸激酶的改变是大多数GIST发病的关键因素[8],另外,也有一些罕见的野生基因分型[9]。这些突变导致酪氨酸激酶的持续激活状态,这是酪氨酸激酶抑制剂(tyrosine kinase inhibitor,TKI),如甲磺酸伊马替尼应用的研究基础。
GIST起病隐匿,无特异性临床症状,其症状及预后与肿瘤的大小、部位、位置及肿瘤核分裂象有关。GIST的常见症状为腹痛(20%~50%)、腹部肿块、消化道出血(30%~40%)及胃肠道梗阻(10%~30%),无症状的GIST约占20% [8, 10-12],很多患者因消化道出血或外伤导致肿瘤破裂急诊就诊时才发现此病。由于多种因素的干扰及研究样本的局限,GIST的恶性潜能分级和术后的管理仍然存在争议[13]。目前认为治疗GIST的最佳手段是手术切除。术后根据危险度分层使用TKI类药物。GIST在术后若干年后仍有复发的风险[14-15],GIST复发危险度分层与预后息息相关,目前根据美国国立综合癌症网络[16]、美国临床肿瘤协会年会指南及GIST的复发危险度分级相关研究,认为肿瘤的位置、大小、核分裂象、肿瘤是否破裂是评估间质瘤复发最重要的4个因素[5, 17]。本研究结果表明,原发肿瘤为非胃来源、肿瘤直径 > 5 cm、核分裂像 > 5/高倍视野为GIST患者术后发生死亡的危险因素,与其他研究结果一致。本研究还发现,若GIST患者需行急诊手术,可能预后不佳。故GIST患者若行急诊手术治疗,术后需提高其危险分层,酌情使用TKI类药物,降低复发概率,延长无瘤生存期及总生存期,使患者最大程度上从靶向治疗中获益。
本研究发现,急诊手术组患者比非急诊手术组术前中性粒细胞增高,淋巴细胞降低,且更易合并消化道出血,原发位置多为小肠,这些均可能是导致行急诊手术患者预后差的原因。已有研究[18-19]表明,消化道出血是GIST预后不良的独立危险因素。GIST引起的消化道出血是肿瘤破裂的另一种表现形式,破裂使肿瘤在消化道内播散,导致肿瘤细胞种植,增加了GIST复发的可能性。原发肿瘤为非胃来源的患者,绝大部分病灶位于小肠。小肠GIST多呈腔内生长,生长空间受限,多种消化液及肠管的运动均可导致肿瘤的不稳定性,有研究[20]表明GIST在小肠中出血的比例远大于胃,术中可见肿瘤破溃或包膜不完整[21],这也解释了原发肿瘤为非胃来源的患者行急诊手术比例高,易合并出血,且较胃来源的患者预后差的原因。机体对肿瘤的免疫作用主要通过淋巴细胞实现,恶性肿瘤患者外周血肿瘤浸润淋巴细胞能改善患者的生存率,急诊手术患者淋巴细胞数量减少,导致T细胞活性下降,减弱了淋巴细胞介导的抗肿瘤作用,利于肿瘤增殖和播散,这也可能是导致急诊手术患者术后复发风险增高的因素。RUTKOWSKI等[22]研究了232例GIST患者,发现外周血中高水平的中性粒细胞计数(> 5.0×109/L)是影响患者短期无进展生存率的一项显著的负性因素,与本研究结果一致;KUSUMANTO等[23]发现中性粒细胞能分泌血管内皮细胞生长因子,诱导肿瘤血管生成,利于肿瘤生长和增殖。外周血中性粒细胞计数水平的相关研究[24]虽然已证实了其独立的预后作用,并且强调了中性粒细胞在肿瘤生物学中日益增长的重要性,然而中性粒细胞的详细作用机制仍需进一步研究。
本研究中,Kaplan-Meier生存曲线显示,急诊手术组GIST患者无瘤生存期和总生存期均较非急诊手术组短。行急诊手术是GIST患者复发和预后的独立危险因素,可能为预后不良的重要评判指标之一。鉴于本研究结果也受到样本量的限制及其他因素的影响,故仍有待于进一步进行多中心大样本量的研究。
| [1] |
MAZUR MT, CLARK HB. Gastric stromal tumors. reappraisal of histogenesis[J]. Am J Surg Pathol, 1983, 7(6): 507-519. DOI:10.1097/00000478-198309000-00001 |
| [2] |
JOENSUU H, VEHTARI A, RIIHIMÄKI KI J, et al. Risk of recurrence of gastrointestinal stromal tumour after surgery:an analysis of pooled population-based cohorts[J]. Lancet Oncol, 2012, 13(3): 265-274. DOI:10.1016/S1470-2045(11)70299-6 |
| [3] |
SIRCAR K, HEWLETT BR, HUIZINGA JD, et al. Interstitial cells of Cajal as precursors of gastrointestinal stromal tumors[J]. Am J Surg Pathol, 1999, 23(4): 377-389. DOI:10.1097/00000478-199904000-00002 |
| [4] |
ROGGIN KK, POSNER MC. Modern treatment of gastric gastrointestinal stromal tumors[J]. World J Gastroenterol, 2012, 18(46): 6720-6728. DOI:10.3748/wjg.v18.i46.6720 |
| [5] |
MIETTINEN M, LASOTA J. Gastrointestinal stromal tumors:pathology and prognosis at different sites[J]. Semin Diagn Pathol, 2006, 23(2): 70-83. DOI:10.1053/j.semdp.2006.09.001 |
| [6] |
LANKE G, LEE JH. How best to manage gastrointestinal stromal tumor[J]. World J Clin Oncol, 2017, 8(2): 135-144. DOI:10.5306/wjco.v8.i2.135 |
| [7] |
MIETTINEN M, MAJIDI M, LASOTA J. Pathology and diagnostic criteria of gastrointestinal stromal tumors (GISTs):a review[J]. Eur J Cancer, 2002, 38(Suppl 5): S39-S51. DOI:10.1016/s0959-8049(02)80602-5 |
| [8] |
RAMMOHAN A, SATHYANESAN J, RAJENDRAN K, et al. A gist of gastrointestinal stromal tumors:a review[J]. World J Gastrointest Oncol, 2013, 5(6): 102-112. DOI:10.4251/wjgo.v5.i6.102 |
| [9] |
LIU Q, KONG FM, ZHOU JP, et al. Management of hemorrhage in gastrointestinal stromal tumors:a review[J]. Cancer Manag Res, 2018, 10: 735-743. DOI:10.2147/CMAR.S159689 |
| [10] |
NILSSON B, BÜMMING P, MEIS-KINDBLOM JM, et al. Gastrointestinal stromal tumors:the incidence, prevalence, clinical course, and prognostication in the preimatinib mesylate era:a population-based study in western Sweden[J]. Cancer, 2005, 103(4): 821-829. DOI:10.1002/cncr.20862 |
| [11] |
SLEIJFER S, SEYNAEVE C, WIEMER E, et al. Practical aspects of managing gastrointestinal stromal tumors[J]. Clin Colorectal Cancer, 2006, 6(Suppl 1): S18-S23. |
| [12] |
SOROUR MA, KASSEM MI, GHAZAL AEL-H, et al. Gastrointestinal stromal tumors (GIST) related emergencies[J]. Int J Surg, 2014, 12(4): 269-280. DOI:10.1016/j.ijsu.2014.02.004 |
| [13] |
STILES ZE, RIST TM, DICKSON PV, et al. Impact of body mass index on the short-term outcomes of resected gastrointestinal stromal tumors[J]. J Surg Res, 2017, 217: 123-130. DOI:10.1016/j.jss.2017.05.010 |
| [14] |
JOENSUU H, ERIKSSON M, SUNDBY HALL K, et al. Adjuvant imatinib for high-risk GI stromal tumor:analysis of a randomized trial[J]. J Clin Oncol, 2016, 34(3): 244-250. DOI:10.1200/JCO.2015.62.9170 |
| [15] |
FORD SJ, GRONCHI A. Indications for surgery in advanced/metastatic GIST[J]. Eur J Cancer, 2016, 63: 154-167. DOI:10.1016/j.ejca.2016.05.019 |
| [16] |
VON MEHREN M, RANDALL RL, BENJAMIN RS, et al. Soft tissue sarcoma, version 2.2016, NCCN clinical practice guidelines in oncology[J]. J Natl Compr Canc Netw, 2016, 14(6): 758-786. DOI:10.6004/jnccn.2016.0078 |
| [17] |
RUBIN BP, BLANKE CD, DEMETRI GD, et al. Protocol for the examination of specimens from patients with gastrointestinal stromal tumor[J]. Arch Pathol Lab Med, 2010, 134(2): 165-170. DOI:10.1043/1543-2165-134.2.165 |
| [18] |
LV A, LI ZW, TIAN XY, et al. SKP2 high expression, KIT exon 11 deletions, and gastrointestinal bleeding as predictors of poor prognosis in primary gastrointestinal stromal tumors[J]. PLoS One, 2013, 8(5): e62951. DOI:10.1371/journal.pone.0062951 |
| [19] |
YIN ZJ, GAO JB, LIU WZ, et al. Clinicopathological and prognostic analysis of primary gastrointestinal stromal tumor presenting with gastrointestinal bleeding:a 10-year retrospective study[J]. J Gastrointest Surg, 2017, 21(5): 792-800. DOI:10.1007/s11605-017-3385-2 |
| [20] |
LIU Q, LI YJ, DONG M, et al. Gastrointestinal bleeding is an independent risk factor for poor prognosis in GIST patients[J]. Biomed Res Int, 2017, 2017: 7152406. DOI:10.1155/2017/7152406 |
| [21] |
MIETTINEN M, LASOTA J. Gastrointestinal stromal tumors:review on morphology, molecular pathology, prognosis, and differential diagnosis[J]. Arch Pathol Lab Med, 2006, 130(10): 1466-1478. DOI:10.1043/1543-2165(2006)130[1466:GSTROM]2.0.CO;2 |
| [22] |
RUTKOWSKI P, NOWECKI ZI, DEBIEC-RYCHTER M, et al. Predictive factors for long-term effects of imatinib therapy in patients with inoperable/metastatic CD117(+) gastrointestinal stromal tumors (GISTs)[J]. J Cancer Res Clin Oncol, 2007, 133(9): 589-597. DOI:10.1007/s00432-007-0202-4 |
| [23] |
KUSUMANTO YH, DAM WA, HOSPERS GA, et al. Platelets and granulocytes, in particular the neutrophils, form important compartments for circulating vascular endothelial growth factor[J]. Angiogenesis, 2003, 6(4): 283-287. DOI:10.1023/B:AGEN.0000029415.62384.ba |
| [24] |
ZENG DQ, YU YF, OU QY, et al. Prognostic and predictive value of tumor-infiltrating lymphocytes for clinical therapeutic research in patients with non-small cell lung cancer[J]. Oncotarget, 2016, 7(12): 13765-13781. DOI:10.18632/oncotarget.7282 |
 2019, Vol. 48
2019, Vol. 48