文章信息
- 胥丹妮, 靳赢, 王越, 宋利明, 林晓萍
- XU Danni, JIN Ying, WANG Yue, SONG Liming, LIN Xiaoping
- 肥胖伴牙周炎患者龈沟液及血清中脂联素与内脂素的表达
- Expression of Adiponectin and Visfatin in the Gingival Crevicular Fluid and Serum of Patients with Obesity and Chronic Periodontitis
- 中国医科大学学报, 2017, 46(12): 1129-1132, 1137
- Journal of China Medical University, 2017, 46(12): 1129-1132, 1137
-
文章历史
- 收稿日期:2017-06-02
- 网络出版时间:2017-11-30 18:14
牙周炎是由多种因素引起的牙周组织的慢性炎症反应,它主要侵犯牙龈和牙槽骨等牙周支持组织,是牙齿缺失的重要原因之一[1]。肥胖作为全球范围内的流行病,与某些系统性疾病密切相关[2]。近年来,大量的研究[3]表明,肥胖和牙周炎具有相关性。脂联素是所有脂肪因子中唯一呈负性调节的激素,具有抗炎、促进葡萄糖的吸收、增加胰岛素的敏感性等作用。内脂素具有促炎、调节胰岛素的敏感性等作用[4],但有关脂联素和内脂素对牙周炎的影响报道较少。本研究通过检测脂联素与内脂素在患者龈沟液及血清中的表达,探讨肥胖作为危险因素对牙周炎的影响,进而为牙周炎的防治提供更多的客观理论依据。
1 材料与方法 1.1 研究对象选取2016年1月至12月就诊于中国医科大学附属盛京医院口腔科的患者80例,将其分为4组。对照组20例(H组,即未患牙周及肥胖疾病且符合纳入及排除标准者),其中男8例,女12例,年龄(44.50±7.8)岁;牙周炎组20例(CP组),其中男10例,女10例,年龄(49.25±10.59)岁;肥胖组20例(OB组,即未患牙周疾病且符合纳入及排除标准的肥胖患者),其中男13例,女7例,年龄(47.75±9.01)岁,肥胖伴牙周炎组20例(OB+CP组),其中男11例,女9例,年龄(49.50±8.57)岁。纳入标准:年龄18~60周岁有能力理解并签订知情同意书的成年人;每位患者口腔内牙齿≥15颗,每个象限至少有2颗磨牙牙周探诊深度(probing depth,PD)≥4 mm,临床附着丧失(clinical attachment loss,CAL)≥2 mm;正常体质量指数(body mass index,BMI)为 > 18.5 ~ < 23.9 kg/m2,肥胖者BMI≥ 28 kg/ m2。排除标准:怀孕及哺乳期妇女,配戴正畸矫治器的患者;近半年内接受过牙周治疗及降脂治疗者,近3个月内应用免疫抑制剂、非激素类抗炎药物、抗生素者;心脏病患者、甲状腺功能亢进及减退患者和糖尿病患者。
1.2 牙周临床指标的检测牙周检查6颗指数牙(16、11、26、36、31、46),指数牙检查6个位点(近颊、正中颊、远颊、近舌、正中舌、远舌)的PD、CAL、牙龈指数(gingival index,GI)和龈沟出血指数(sulcular bleeding indx,SBI)。
1.3 龈沟液及血清样本的收集 1.3.1 龈沟液收集选择1、2象限第一磨牙颊舌正中2个位点(个别第一磨牙不符合纳入标准者用相邻的第二磨牙或第二前磨牙代替)。去除受试牙的大块龈上牙石,用尖探针侧面刮除龈上菌斑,受试牙以棉卷隔湿,气枪吹干,将25号吸潮纸尖轻轻插入牙周袋底,遇阻力即止,停留1 min取出,如被血或唾液污染,则弃除。将所取纸尖放入EP管中,加入300 μL PBS缓冲液,放置于-80 ℃冰箱保存备用。
1.3.2 血清收集采集2 mL外周血,充分凝血后,2 000 r/min离心20 min、收集上清,-80 ℃保存待检。
1.4 脂联素与内脂素的检测将待测样本于室温下解冻20 min,4 ℃、3 000 r /min离心10 min,离心后取上清液待查,采用人脂联素、内脂素ELISA试剂盒,检测血清及龈沟液中脂联素与内脂素的水平,严格按照试剂盒说明书检测,测定吸光度值,并根据标准曲线计算出脂联素与内脂素的浓度。
1.5 统计学分析采用SPSS 17.0进行统计学分析,数据用x±s表示,若每组资料完全符合正态分布且方差齐,采用单因素方差分析(One-way ANOVA);不符合则采用秩和检验,检测水准为双侧α=0.05;组间采用LSD检验,P < 0.05为差异有统计学意义。
2 结果 2.1 研究对象一般资料的比较各组患者在年龄、性别方面差异无统计学意义(P > 0.05),见表 1。
| Item | H group | CP group | OB group | OB+CP group |
| Age(year) | 44.50±7.80 | 49.25±10.59 | 47.75±9.01 | 49.50±8.57 |
| Sex [n(%)] | ||||
| Male | 8(40) | 10(50) | 13(65) | 11(55) |
| Female | 12(60) | 10(50) | 7(35) | 9(45) |
2.2 研究对象的临床指标
本研究中CP组患者与OB+CP组患者PD、CAL、GI、SBI均显著高于H组及OB组(P < 0.05),OB+CP组患者牙周临床指数高于CP组患者(P < 0.05),OB+CP组及OB组BMI高于CP组及H组(P < 0.05),OB组与H组患者牙周临床指数差异无统计学意义(P > 0.05),OB+CP组与OB组患者BMI差异无统计学意义(P > 0.05),CP组与H组患者BMI差异无统计学意义(P > 0.05),见表 2。
| Group | PD(mm) | CAL(mm) | GI(0-3) | SBI(0-5) | BMI(kg/m2) |
| H | 1.09±0.591) | 0.33±0.191) | 0.24±0.211) | 0.70±0.481) | 21.51±1.77 |
| CP | 3.37±0.25 | 1.58±0.15 | 1.92±0.38 | 2.20±0.42 | 22.08±1.85 |
| OB | 1.26±0.331) | 0.53±0.191) | 0.28±0.161) | 0.40±0.521) | 29.84±2.501),2) |
| OB+CP | 4.05±0.251) | 2.28±0.361) | 2.53±0.291) | 3.00±0.671) | 28.94±0.851),2) |
| P | < 0.001 | < 0.001 | < 0.001 | < 0.001 | < 0.001 |
| 1)compared with CP group,P < 0.05;2)compared with H group,P < 0.05. | |||||
2.3 脂联素和内脂素在血清及龈沟液中的表达水平
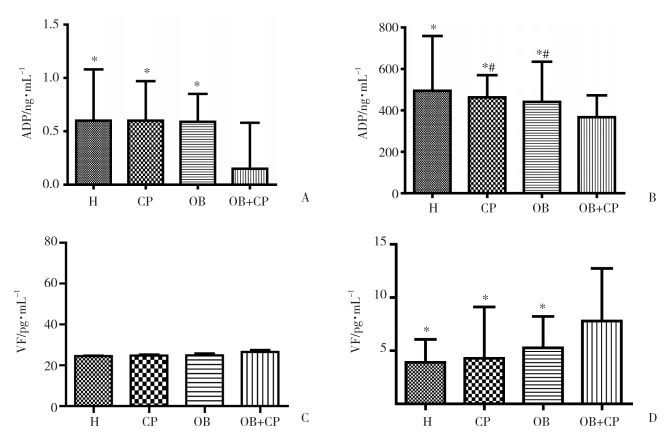
CP组、OB组及H组龈沟液中脂联素的浓度高于OB+CP组(P < 0.05)。CP组、OB组及OB+CP组血清中脂联素的浓度低于健康对照组(P < 0.05),OB+CP组血清中脂联素的浓度低于CP组及OB组(P < 0.05)。CP组、OB组及H组龈沟液中内脂素的浓度低于OB+CP组,组间比较差异无统计学意义(P > 0.05)。CP组、OB组及H组血清中内脂素的浓度低于OB+CP组(P < 0.05)。H组血清中内脂素的浓度低于CP组及OB组,3组间比较差异无统计学意义(P > 0.05)。
|
| A, the expression of adiponectin in the GCF; B, the expression of adiponectin in the serum; C, the expression of visfatin in the GCF; D, the expression of visfatin in the serum.* P < 0.05 compared with OB+CP group; # P < 0.05 compared with H group. 图 1 脂联素和内脂素在龈沟液及血清中的表达 Fig.1 The expression of adiponectin and visfatin in the GCF and serum |
3 讨论
牙周炎不仅仅是口腔的局部炎症,同时也与全身的疾病和健康状况相关。肥胖作为牙周炎的危险因素,主要通过促进氧化应激的发生和炎性细胞因子的分泌来破坏牙周组织的健康[5-6]。脂联素是由脂肪细胞特异性分泌的一种蛋白质,在肥胖患者体内含量较低[7]。同时脂联素作为一种保护性因子,在促进抗炎介质排放的同时也能抑制促炎细胞因子的刺激[8]。有研究[9-10]发现,脂联素在促进白细胞介素(interleukin,IL)10分泌的同时能够抑制活性氧的表达,从而对牙周组织起到一定的保护作用。
内脂素是由内脏脂肪细胞分泌的蛋白质细胞因子,是某些炎症相关疾病的重要介质[11]。近年来,有学者[12]发现,内脂素在牙周组织中有较高的表达,并且在牙周炎的发病机制中发挥重要的作用。体外实验的研究[13-16]表明,内脂素能够促进炎症细胞分泌肿瘤坏死因子α(tumor necrosis factor α,TNF-α)、IL-6、IL-1β,反之,TNF-α、IL-6、IL-1β也能上调内脂素的表达。肥胖和牙周炎均与某些炎性细胞因子的分泌有关,故二者的相关性可能通过中间的炎症机制联系起来。
本研究结果显示,OB+CP组血清中脂联素的降低幅度最大。提示脂联素作为抑炎性细胞因子,在肥胖伴牙周炎患者体内的表达水平呈降低趋势,与龈沟液中脂联素的表达水平具有一致性。因此,推测肥胖和牙周炎对患者龈沟液及血清中脂联素的降低具有协同效应,肥胖可能通过抑制某些抑炎性因子的分泌而影响牙周炎的发生发展。SUPANEE等[17]研究发现肥胖以及重度牙周炎患者血浆中脂联素的浓度低于体质量正常以及轻、中度牙周炎者,而C反应蛋白、瘦素以及细胞间黏附分子等促炎因子的含量较高。伴放线放线杆菌是牙周炎的主要致病菌之一,能产生多种毒力因子,脂联素能够抑制伴放线放线杆菌的活性,本研究中肥胖伴牙周炎患者血清中脂联素浓度的降低,可能改变了机体对伴放线放线杆菌的免疫应答,同时也降低了免疫球蛋白抗体对牙周组织的保护性作用,使肥胖患者更容易罹患牙周炎。脂联素在OB+CP组的表达低于OB组及CP组患者,OB组脂联素的浓度与CP组相比,无统计学差异,提示肥胖与牙周炎虽分别为全身和口腔局部的炎症性疾病,但局部炎症反应与全身炎症反应相互促进,从而造成OB+CP组患者脂联素的表达水平最低,使肥胖作为危险因素加快了牙周炎的发展进程。
TABARI等[18]研究发现牙周炎患者唾液中内脂素的浓度高于牙周健康者,且唾液中内脂素的浓度与患者CAL的水平呈正相关。本研究检测内脂素其在肥胖及牙周炎患者血清及龈沟液中的表达,发现内脂素在H组、OB组、CP组、OB+CP组患者龈沟液中浓度较小,而在各组患者的血清中含量较高。结果显示,OB+CP组患者血清中内脂素的浓度较OB组、CP组以及H组高,OB组与CP组血清中内脂素的表达水平较H组有所升高,但无统计学差异。提示影响因素的叠加,使肥胖伴牙周炎患者的固有免疫机制受到影响,从而使全身对炎症的反应水平升高。OB组、CP组较H组血清中内脂素的含量高,这可能是由于牙周袋内牙周致病菌及其毒性产物刺激牙周组织产生高浓度的促炎因子,这些促炎因子可通过牙周袋内上皮进入血液循环,从而上调血清中内脂素的表达。肥胖患者的脂肪组织除产生内脂素、TNF-α、IL-6外,还产生瘦素、抵抗素、C反应蛋白等促炎因子,这些促炎因子与内脂素相互作用,使相应的炎症反应增强,这可能是肥胖患者易患牙周炎的另一因素。此结论仍需其他方面的研究进一步证实,增强研究结果的可靠性。
| [1] |
GENCO RJ, BORGNAKKE WS. Risk factors for periodontal disease[J]. Periodontol 2000, 2013, 62(1): 59-94. DOI:10.1111/j.1600-0757.2012.00457.x |
| [2] |
SURESH S, MAHENDRA J, SUDHAKAR U, et al. Evaluation of plasma reactive oxygen metabolites levels in obese subjects with periodontal disease[J]. Indian J Dent Res, 2016, 27(2): 155-159. DOI:10.4103/0970-9290.183117 |
| [3] |
AMAR S, LEEMAN S. Periodontal innate immune mechanisms relevant to obesity[J]. Mol Oral Microbiol, 2013, 28(5): 331-341. DOI:10.1111/omi.12035 |
| [4] |
ZCAN E, SAYGUN NI, ILIKI R, et al. Increased visfatin expression is associated with nuclear factor-kappa B and phosphatidylinositol 3-kinase in periodontal inflammation[J]. Clin Oral Investig, 2017, 21(4): 1113-1121. DOI:10.1007/s00784-016-1871-7 |
| [5] |
DURSUN E, AKALIN FA, GENC T, et al. Oxidative stress and periodontal disease in obesity[J]. Medicine, 2012, 95(12): e3136. DOI:10.1902/jop.2013.130388 |
| [6] |
GONCALVES TED, ZIMMERMANN GS, FIGUEIREDO LC, et al. Local and serum levels ofadipokines in patients with obesity after periodontal therapy:one-year follow-up[J]. J Clin Periodontol, 2015, 42(5): 431-439. DOI:10.1111/jcpe.12396 |
| [7] |
AGGELOUSSI S, THEODOROU AA, PASCHALIS V, et al. Adipocytokine levels in children:effects of fatness and training[J]. Pediatr Exerc Sci, 2012, 24(3): 461-471. DOI:10.1123/pes.24.3.461 |
| [8] |
CARBONE F, LA RC, MATARESE G. Immunological functions of leptin and adiponectin[J]. Biochimie, 2012, 94(10): 2082-2088. DOI:10.1016/j.biochi.2012.05.018 |
| [9] |
FANTUZZI G. Adiponectin in inflammatory and immune-mediated diseases[J]. Cytokine, 2013, 64(1): 1-10. DOI:10.1016/j.cyto.2013.06.317 |
| [10] |
NIGRO E, SCUDIERO O, MONACO ML, et al. New insight into adiponectin role in obesity and obesity-related diseases[J]. Biomed Res Int, 2014, 2014(10): 1153-1166. DOI:10.1155/2014/658913 |
| [11] |
ROBERTS KJ, CROSS A, VASIEVRA O, et al. Inhibition of pre-Bcell colony-enhancing factor (PBEF/Nampt/visfatin) decreases the ability of human neutrophils to generate reactive oxidants but not impair bacterial killing[J]. J Leukoc Biol, 2013, 94(3): 481-492. DOI:10.1189/jlb.1012527 |
| [12] |
GHALLAB NA, AMR EM, SHAKER OG. Expression of leptin and visfatin in gingival tissues of chronic periodontitis with and without type 2 diabetes mellitus:a study using enzyme linked immunosorbent assay and real-time polymerase chain reaction[J]. J Periodontol, 2015, 86(7): 882-889. DOI:10.1902/jop.2015.140434 |
| [13] |
XIAO K, ZOU WH, YANG Z, et al. The role of visfatin on the regulation of inflammation and apoptosis in the spleen of LPS-treated rats[J]. Cell Tissue Res, 2015, 359(2): 605-618. DOI:10.1007/s00441-014-1997-3 |
| [14] |
AKHISA M, LANG YW, ASHA J, et al. FK 866, a visfatin inhibitor, protects against acute lung injury after intestinal ischemia-reperfusion in mice via NF-(kappa) B pathway[J]. Ann Surg, 2014, 259(5): 1007-1017. DOI:10.1097/SLA.0000000000000329 |
| [15] |
NOKHBEHSAIM M, EICK S, NOGUEIRA AVB, et al. Stimulation of MMP-1 and CCL2 by NAMPT in PDL cells[J]. Mediat Inflamm, 2013, 2013(4): 437123. DOI:10.1155/2013/437123 |
| [16] |
DAMANAKI A, NOKHBEHSAIM M, EICK S, et al. Regulation of NAMPT in human gingival fibroblasts and biopsies[J]. Mediat Inflamm, 2014, 2014(4): 85-87. DOI:10.1155/2014/912821 |
| [17] |
THANAKUN S, IZUMI Y. Effect of periodontitis on adiponectin, c-reactive protein, and immunoglobulin G against porphyromonas gingivalis in thai people with overweight or obese status[J]. J Periodontol, 2016, 87(5): 566-576. DOI:10.1902/jop.2015.150583 |
| [18] |
TABARI ZA, AZADMEHR A, NOHEKHAN A, et al. Salivary visfatin concentrations in patients with chronic periodontitis[J]. J Periodontol, 2014, 85(8): 1081-1085. DOI:10.1902/jop.2013.130388 |
 2017, Vol. 46
2017, Vol. 46