2. 复旦大学公共卫生学院, 上海 200032
牛奶蛋白过敏(cow’s milk allergy,CMA)是涉及全世界婴幼儿健康的重要公共卫生问题。全球约有2.5%~3.0% 的婴幼儿患有CMA [1-2],我国大城市0~3岁婴幼儿CMA的发病率为0.83% ~ 3.5%,甚至可达7.7%[3]。随着我国经济发展和城镇化水平的不断提高,CMA发病率还在逐步上升[4]。CMA在母乳喂养、配方粉喂养和混合喂养的婴幼儿中均可能发生,大多数患儿在1岁前确诊,4~6月龄为高发年龄段[4]。患儿多表现为特应性皮炎、拒奶、腹泻和便血等皮肤和胃肠道症状,病情严重者可发生严重过敏反应。CMA不但极大地损害婴幼儿的身心健康,且影响其生长发育,同时也给患儿家庭日常生活带来困扰。
对于CMA患儿,国内外指南都推荐使用氨基酸配方(amino acid formula,AAF)或深度水解配方(extensively hydrolyzed formula,eHF)替代喂养[5-6]。临床研究[7-8]显示,AAF和eHF替代喂养均可有效缓解过敏症状,提高患儿舒适度,并促进其对牛奶蛋白产生耐受性。意大利的1项研究[9]发现,使用eHF的患儿中43.6%在12个月观察期内能建立牛奶蛋白耐受,而单独AAF喂养的患儿只有18.2%能建立牛奶蛋白耐受。而土耳其的一项研究[10]显示,在患儿2岁前起始使用AAF喂养建立牛奶蛋白耐受率可达83.7%,但eHF只有48.7%。这些差异可能与目前欧洲指南推荐轻中度CMA患儿使用eHF、重度CMA患儿使用AAF治疗相关。不同国家对优先选择哪一种配方目前尚无定论。由于AAF是无敏配方,我国指南推荐起始使用AAF配方2~6周,尽快帮助CMA的诊断,确诊后的CMA患儿可继续使用AAF或eHF替代喂养,直至逐步引入牛奶蛋白制品[11-12]。在最新国际指南中,AAF也是CMA的诊断推荐配方[13-14]。与AAF相比,仍有29.0%~40.0%的患儿无法耐受eHF配方。虽然AAF在CMA诊断和临床管理方面呈现出明显的优越性,但鉴于AAF在欧美国家的价格是eHF的6~8倍[15],eHF仍然是一些欧美国家临床医生推荐使用的一线替代配方,AAF的使用局限于严重或复杂的CMA病例。
为全面评估AAF和eHF的价值,有研究[16-19]比较了两类配方粉的经济性。英国、西班牙、意大利和波兰的经济学评价结果显示,起始使用eHF性价比优于AAF,在促进患儿口服耐受性产生的同时,可节省国家医疗保险基金和患儿家庭的治疗成本。但澳大利亚和土耳其的模型研究[10, 20]预测结果却表明,起始使用AAF治疗当地CMA患儿具有绝对的经济优势。由此可见,药物经济学评估证据的异质性很高,各类配方粉在不同医疗系统和不同目标人群中的经济学特性差异很大。
与欧美国家相比,我国AAF和eHF的市场价格差别较小。医疗环境、诊疗流程、基础治疗等各方面也和欧美国家存在较大差异。因此,根据我国国情对AAF和eHF两类配方粉开展药物经济学评估具有重要的现实意义。本研究基于患者视角评估AAF和eHF的相对经济性,优选治疗CMA性价比高的配方粉。研究所提供的药物经济学评价证据可供临床医生参考,改善临床决策,合理分配有限的卫生资源,从而减轻患儿家庭的疾病负担,提高CMA治疗的可持续性。
1 对象与方法 1.1 研究对象鉴于国内CMA的流行病学资料,大多数患儿发病年龄在4~6个月,2岁后诊断CMA的人数锐减[22]。所以,本研究以中国大陆2岁以下确诊CMA的儿童为研究对象。
1.2 研究方法 1.2.1 模型构建使用决策树模型来模拟疾病进程。模拟时限从患儿确诊CMA至建立牛奶蛋白耐受,或者到年满2岁,以两者中较短的时间为模拟终点。模拟时限内CMA治疗的总成本包括配方粉(AAF或eHF)、诊断、治疗以及家庭护理的费用。结果指标为模拟时限内建立牛奶蛋白耐受所需的时间。如果患儿最终没有建立耐受,则建立耐受所需时间最少至2岁。
模型的主要假设:①所有患儿从CMA确诊之日起即使用配方粉治疗。②患儿每日配方粉量严格按照产品标签推荐的用量,依从度为100.0%。③患儿在某一配方粉治疗期间没有混合使用其他种类的配方粉。④患儿一旦建立牛奶蛋白耐受,将立刻停止使用配方粉。⑤如果患儿还没有建立牛奶蛋白耐受,则将使用配方粉至2岁。⑥在患儿治疗期间,无论使用AAF还是eHF,其他诊断、治疗、家庭护理手段等情况一致。模型使用Treeage 2021构建。
1.2.2 基线分析和亚组人群分析决策树模型首先估算总体目标人群在模拟时限内建立牛奶蛋白耐受所需的总成本和时间,从而对比3种配方粉的成本和临床效果来评估不同配方粉的经济性。同时根据发病机制和病情严重程度将总体人群区分为亚组人群,分别衡量不同亚组的成本效果。
1.2.3 敏感性分析模型使用单因素和概率敏感性分析衡量参数的不确定性对模型结果的影响。单因素敏感性分析显示了每一参数从最小值到最大值的变化过程中各配方粉成本效果的相应变化。而概率敏感性分析是为了体现参数的随机不确定性对模型结果的影响,在随机不确定因素之下各配方粉的成本效果属性。概率敏感性分析使用蒙特卡洛模拟对每个参数的概率分布进行1 000次抽样。
1.3 数据来源该模型的主要数据来自对一线临床医生的调研。为获得真实世界中患者的就医经历和转归历程,对上海市21家医疗机构的60名医生开展问卷调查。抽样科室来自三级甲等、三级乙等综合医院,儿童专科医院,妇幼保健院,民营医院的10个科室(儿童保健科、儿科、过敏免疫科、皮肤科、普内科、消化科、小儿消化营养科、新生儿科、血液科、中医科)。60名回答问卷的医生中有29名主治医师、20名副主任医师和11名主任医师。
2 结果 2.1 研究对象的基本情况研究对象的流行病学特征见表 1。
| 表 1 研究对象的流行病学特征 |
|
|
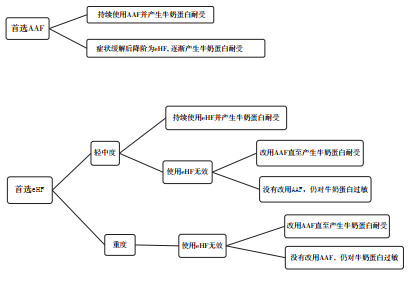
本研究是基于模型的成本效果分析。该模型模拟了我国CMA患儿确诊CMA后的治疗路径。根据指南和临床医生调研[14, 21-23],我国患儿使用AAF和eHF后的治疗和转归路径如图 1所示。从支付方(患儿家庭)的视角, 测算目标人群从首次使用配方粉起直到2岁所产生的直接成本(配方粉、医疗服务和家庭护理等)和患儿建立牛奶耐受所需时间,结合成本和效果评估AAF和eHF的经济性。模型结果参照CHEERS标准报告。
|
注:AAF为氨基酸配方(amino acid formula);eHF为深度水解配方(extensively hydrolyzed formula)。 图 1 首选AAF和eHF的牛奶蛋白过敏患儿治疗和转归路径 |
根据临床实践中各类配方粉的使用广泛度及临床医生反馈,模型选择了相应代表AAF和eHF两类配方粉。代表eHF的配方粉包括含乳糖和无乳糖配方2种。3种配方粉各年龄段标准推荐用量(根据产品说明书)见表 2。
| 表 2 不同年龄段儿童每日配方粉标准推荐用量 |
|
|
课题组自行设计调研问卷,针对患儿在CMA治疗过程中配方粉使用、专业医疗服务和家庭护理消费、配方效果等方面共包括140个问题。受调查者须具备2年及以上CMA的诊疗经验。对数据的客观性、科学性、是否符合临床实际进行验证,核对无误后形成模型参数。对问卷没有涉及的参数,检索国内外文献予以补充。多源数据采取荟萃分析整合成单一参数和对应的置信区间。见表 3。
| 表 3 首选不同种类配方粉的成本核算及临床效果参数 |
|
|
CMA患儿的临床诊疗成本[24]见表 4。与轻中度CMA患儿相比,重度CMA患儿消费了更多的医疗服务,产生了更多的直接医疗成本。
| 表 4 单项临床检验价格以及不同病情程度CMA患儿的医疗和家庭服务成本 |
|
|
根据基线分析(表 5),我国CMA患儿起始使用AAF配方替代喂养平均7.15个月可获得牛奶蛋白耐受,而起始使用eHF则平均需要10.50个月。在接受配方粉治疗过程中,使用AAF的患儿2岁前配方粉、诊疗及家庭护理等总成本平均为23 455元,远低于使用eHF的患儿的成本(无乳糖和含乳糖的eHF总成本分别为30 592和31 337元)。可见,起始使用AAF配方治疗CMA相比eHF配方既节约成本且效果好,是经济性评价中的优势方案。亚组分析中,重度CMA患儿使用AAF的获益更大,在节约总费用的基础上,比使用eHF提前了4.01个月获得牛奶蛋白耐受,轻度CMA患儿使用AAF则比eHF提前3.18个月获得牛奶蛋白耐受。在IgE介导、非IgE介导和混合型CMA患儿中,AAF仍然保持绝对的经济学优势。
| 表 5 3种配方粉在目标人群总体和各亚组人群的成本效果 |
|
|
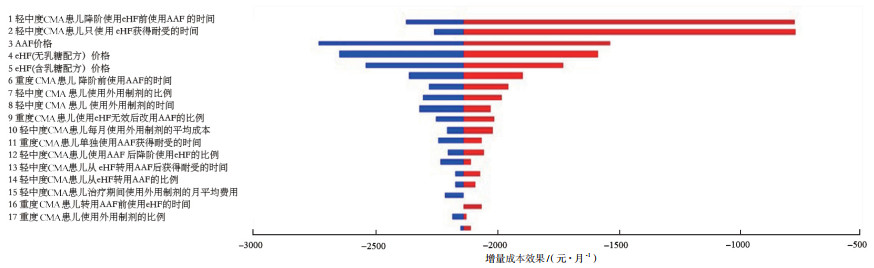
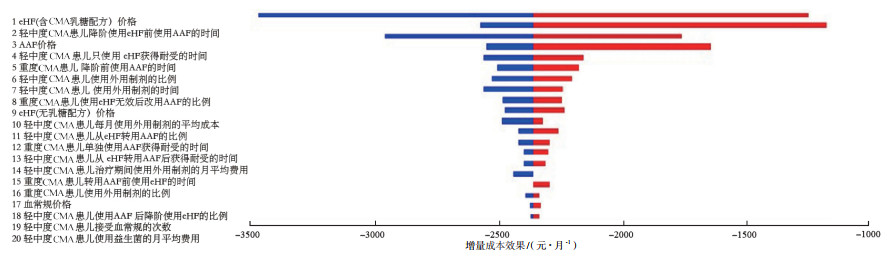
虽然临床、配方粉价格、医疗习惯等因素会影响AAF的成本效果,但与2种eHF对比,AAF的绝对经济学优势并没有变化。相比于含乳糖配方还是无乳糖配方eHF,对AAF成本效果影响最大的前3个因素为轻中度CMA患儿降阶使用eHF前使用AAF的时间,轻中度CMA患儿只使用eHF获得牛奶蛋白耐受的时间和AAF价格。见图 2、图 3。与无乳糖配方eHF相比,对AAF性价比影响最大的因素为轻中度CMA患儿降阶使用eHF前使用AAF的时间(图 2)。如果此时间段不超过12个月,AAF使用时间越长,其经济性越好;如果AAF使用超过12个月,使用时间越长反而会降低AAF的经济学优势。而相对于含乳糖配方eHF,对AAF成本效果影响最大的为eHF价格(图 3)。从药品价格因素分析,显而易见,AAF价格越高或者eHF价格越低,AAF的性价比就会降低。同样,患儿在降阶使用含乳糖配方eHF前使用AAF的时间超过12个月,延长使用AAF时间会对其性价比产生负面影响。临床因素中,重度CMA患儿使用eHF无效后改用AAF的比例越高,或者轻中度CMA患儿单独使用eHF建立牛奶蛋白耐受的时间越长,越能体现起始使用AAF的经济学优势。另外,轻中度CMA患儿使用外用制剂的比例越高、时间越长或者外用制剂的使用成本增高,AAF相比于eHF的成本效果越好。
|
注:AAF为氨基酸配方(amino acid formula);eHF为深度水解配方(extensively hydrolyzed formula);CMA为牛奶蛋白过敏(cow, s milk allergy)。线段长度为AAF成本效果随着参数从最小值到最大值所产生的变化,长度越长说明参数对模型结果的影响越大。红蓝区域的分隔线为当模型所有参数都取最佳值时,AAF成本效果的总体期望值。在蓝色区域,AAF的成本效果低于总体期望值,说明AAF的经济性越好;红色则相反。 图 2 影响AAF和eHF(无乳糖配方)相对经济性的单因素敏感性分析 |
|
注:AAF为氨基酸配方(amino acid formula);eHF为深度水解配方(extensively hydrolyzed formula);CMA为牛奶蛋白过敏(cow, s milk allergy)。线段长度为AAF成本效果随着参数从最小值到最大值所产生的变化,长度越长说明参数对模型结果的影响越大。红蓝区域的分隔线为当模型所有参数都取最佳值时,AAF成本效果的总体期望值。在蓝色区域,AAF的成本效果低于总体期望值,说明AAF的经济性越好;红色则相反。 图 3 影响AAF和eHF(含乳糖配方)相对经济性的单因素敏感性分析 |
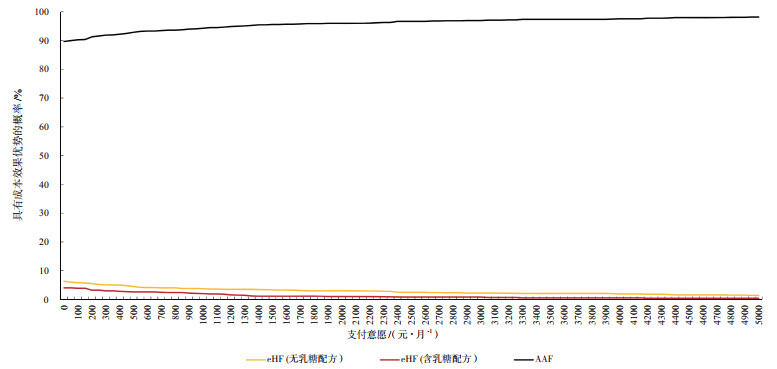
如果患者不愿意为提前实现牛奶蛋白耐受承担额外成本的话,即便考虑到模型参数具有各种随机不确定性,首选AAF成为经济性最佳选项的概率仍然高达90.0%,而无乳糖配方eHF和含乳糖配方eHF成为经济性最佳选项的概率只有6.0%和4.0%(图 4)。随着患者支付意愿金额的提高,AAF成为经济性最佳选项的可能性也随之增大,最高概率可达98.2%。
|
注:AAF为氨基酸配方(amino acid formula);eHF为深度水解配方(extensively hydrolyzed formula)。 图 4 3种配方粉的成本效果接受概率曲线 |
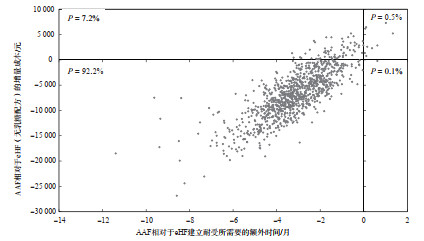
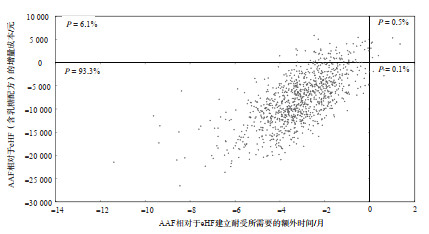
分别对比AAF和2种eHF:即便考虑模型参数的随机不确定性,AAF相对于无乳糖配方eHF成为性价比高的选项的概率为92.2%(图 5)。另外,使用AAF的患儿提前实现牛奶蛋白耐受的概率为7.2%,但需要承担更多的成本。AAF相对于含乳糖配方eHF成为性价比高的选项的概率为93.3%。使用AAF的患儿提前实现牛奶蛋白耐受的概率为6.1%,但需要承担更多的成本(图 6)。
|
注:AAF为氨基酸配方(amino acid formula);eHF为深度水解配方(extensively hydrolyzed formula)。 图 5 AAF相对于eHF(无乳糖配方)的成本效果概率分布 |
|
注:AAF为氨基酸配方(amino acid formula);eHF为深度水解配方(extensively hydrolyzed formula)。 图 6 AAF相对于eHF(含乳糖配方)的成本效果概率分布 |
一方面,国内外指南均推荐使用回避过敏原的饮食替代喂养作为CMA治疗的主要手段,而AAF和eHF是各类指南主要推荐的饮食替代配方。另一方面,配方粉的长期使用会对家庭和社会带来一定的经济负担,所以选择性价比高的配方粉是临床实践必须考虑的问题。目前使用AAF和eHF替代喂养作为缓解患儿过敏症状并最终获得牛奶蛋白耐受的主要临床手段,其经济性在国外已有深入探讨[17, 19, 25-28]。但是由于医疗服务流程、配方粉价格、医疗保障体系国内外差异性很大,不能完全照搬国外研究成果指导我国的临床实践。同时,国内尚无研究证实哪类配方粉更具有经济性,所以患儿家属和临床医生都面临选择困境。本研究选择并对比了AAF和eHF治疗我国婴幼儿CMA的成本效果,结果可供临床医生和患儿家属选择时参考。研究结果显示,与eHF相比,起始使用AAF在治疗我国CMA患儿具有绝对的经济学优势,能够以较低的成本提前帮助患儿实现牛奶蛋白耐受。即使考虑其他因素造成的不确定性,AAF仍然是性价比高的配方粉选择。这种经济学优势在不同病情程度和不同类型的患儿中共同存在,而且重度CMA患儿获益更大。本研究数据显示,24.7%的轻中度、56.6%的重度CMA患儿由于起始使用eHF诊疗4~6周后无效需转AAF治疗(表 3),这可能是因为不同过敏个体对其产生反应的特定蛋白质和表位有很大的异质性,更复杂的是,对牛奶蛋白产生的过敏反应可能由多种免疫机制驱动[29]。仅通过症状来评估疾病的严重性其实是一个非常主观的判断,有些症状或病损可产生较强的视觉冲击(如皮疹、面部肿胀)却不涉及呼吸或心血管等重要脏器,而一些临床表现(如认知受损、意识波动和心排血量轻微异常)可能危及生命,但非专业人员可能对此认识不足。事实上,过敏性疾病临床症状没有明显的特异性,涉及消化、呼吸、皮肤、心血管和神经系统等多个生理系统,非专科医生在门诊环境中缺乏对过敏性疾病症状多样性的认知,可能高估或低估CMA患儿过敏反应的严重程度[30]。基于CMA的复杂性也进一步说明起始使用AAF具有快速确诊CMA、缩短疾病诊疗时间、降低疾病管理费用的优势,为广大患者和医生提供了较有价值的经济学证据。
借鉴国外同类研究的经验[17, 19, 26, 31],同时为了解真实世界中我国患儿的医疗服务情况,本研究主要数据来源为专家调研。根据调研结果,我国患儿确诊CMA的平均年龄为4.23个月,与文献[32]报道的平均确诊年龄4.50个月一致。依据调研专家多年的CMA诊疗经验得出,总体而言我国85.19%的患儿将建立牛奶蛋白耐受,这比文献[33]报道的77.30%高7.89个百分点。但文献报道的数据是基于患儿确诊后12个月之内的耐受率,比本研究2年的调研期要短,因此耐受率理论上会偏低。综上所述,本研究模型数据的真实性和客观性较高,因而结果的可信度也较高。
虽然AAF具备致敏性低的优点,但在欧洲国家eHF仍被推荐为疑似轻中度CMA患儿疾病管理的初始配方。我国最新指南已推荐使用AAF作为CMA的初始诊断配方,同类推荐意见也被越来越多国家基于临床证据、当地医疗费用以及配方粉价格而采用。巴西[28]、土耳其[15]、澳大利亚[31]的研究发现,AAF具有更好的经济性,与同时期eHF替代方案相比,可以节约成本和降低医疗资源消耗;而美国[26]、英国[25]、意大利[27]、波兰[19]的研究发现,eHF总体上经济性要优于AAF。两类配方粉在不同国家的经济性差异主要是由两者的价格差异造成的,国外AAF的价格远高于eHF[34],前者甚至比后者的价格高6~8倍[15]。但两者价格在我国市场差距不大。调查结果显示,我国患儿在首选AAF症状取得缓解之后,74.6%的轻中度CMA患儿和79.5%的重度CMA患儿会降阶使用eHF,获得比较好的CMA疾病管理效应。结合研究模型显示,3类配方粉的价格是影响其经济性的关键因素,研究结论是与国外相比,AAF在我国更具备价格优势。
本研究尚存在一定的局限性。AAF和eHF疗效比较在国外经过多中心前瞻性研究[9]的验证,但在我国尚没有这类研究,所以模型中AAF和eHF疗效只能通过专家调研来获取。另外,调研对象只包括上海市的专家,代表性有一定的局限,模型分析结果在其他地区的适用性有限,后续可以进一步在国内扩大区域进行更多样本的数据分析。
·作者声明本文无实际或潜在的利益冲突
| [1] |
VENTER C, ARSHAD S H. Epidemiology of food allergy[J]. Pediatr Clin North Am, 2011, 58(2): 327-349. DOI:10.1016/j.pcl.2011.02.011 |
| [2] |
FIOCCHI A, BROZEK J, SCHUNEMANN H, et al. World Allergy Organization (WAO) Diagnosis and Rationale for Action against Cow's Milk Allergy (DRACMA) Guidelines[J]. Pediatr Allergy Immunol, 2010, 21(Suppl 21): 1-125. |
| [3] |
陈静, 廖艳. 3城市2岁以下儿童食物过敏现状调查[J]. 中华儿科杂志, 2012, 50(1): 5-9. |
| [4] |
HU Y, CHEN J, LI H Q. Comparison of food allergy prevalence among Chinese infants in Chongqing, 2009 versus 1999[J]. Pediatr Int, 2010, 52(5): 820-824. DOI:10.1111/j.1442-200X.2010.03166.x |
| [5] |
VENTER C, BROWN T, MEYER R, et al. Better recognition, diagnosis and management of non-IgE-mediated cow's milk allergy in infancy: iMAP-an international interpretation of the MAP (Milk Allergy in Primary Care) guideline[J]. Clin Transl Allergy, 2017, 7: 26. DOI:10.1186/s13601-017-0162-y |
| [6] |
陈同辛, 洪莉, 王华, 等. 中国婴儿轻中度非IgE介导的牛奶蛋白过敏诊断和营养干预指南[J]. 中华实用儿科临床杂志, 2022, 37(4): 241-250. DOI:10.3760/cma.j.cn101070-20220106-00016 |
| [7] |
马琳, 申昆玲, 夏晓玲, 等. 肠内营养粉剂治疗食物蛋白过敏婴儿有效性及安全性多中心临床研究[J]. 中国实用儿科杂志, 2012, 27(10): 766-769. |
| [8] |
NIGGEMANN B, BINDER C, DUPONT C, et al. Prospective, controlled, multi-center study on the effect of an amino-acid-based formula in infants with cow's milk allergy/intolerance and atopic dermatitis[J]. Pediatr Allergy Immunol, 2001, 12(2): 78-82. DOI:10.1034/j.1399-3038.2001.012002078.x |
| [9] |
CANANI R B, NOCERINO R, TERRIN G, et al. Formula selection for management of children with cow's milk allergy influences the rate of acquisition of tolerance: a prospective multicenter study[J]. J Pediatr, 2013, 163(3): 771-777. DOI:10.1016/j.jpeds.2013.03.008 |
| [10] |
BERKTAS M, KIRBIYIK F, ARIBAL E, et al. Treatment options for cow's milk protein allergy: a modeling analysis[J]. Clinicoecon Outcomes Res, 2020, 12: 307-315. DOI:10.2147/CEOR.S242021 |
| [11] |
中华医学会儿科学分会消化学组. 食物过敏相关消化道疾病诊断与管理专家共识[J]. 中华儿科杂志, 2017, 55(7): 487-492. DOI:10.3760/cma.j.issn.0578-1310.2017.07.003 |
| [12] |
中国医师协会皮肤科医师分会儿童皮肤病专业委员会, 中华医学会皮肤性病学分会儿童学组, 中华医学会儿科学分会皮肤性病学组. 儿童特应性皮炎相关食物过敏诊断与管理专家共识[J]. 中华皮肤科杂志, 2019, 52(10): 711-716. |
| [13] |
MEYER R, GROETCH M, VENTER C. When should infants with cow's milk protein allergy use an amino acid formula? A practical guide[J]. J Allergy Clin Immunol Pract, 2018, 6(2): 383-399. DOI:10.1016/j.jaip.2017.09.003 |
| [14] |
VANDENPLAS Y, BROUGH H A, FIOCCHI A, et al. Current guidelines and future strategies for the management of cow's milk allergy[J]. J Asthma Allergy, 2021, 14: 1243-1256. DOI:10.2147/JAA.S276992 |
| [15] |
GULER N, COKUGRAS F C, SAPAN N, et al. Diagnosis and management of cow's milk protein allergy in Turkey: region-specific recommendations by an expert-panel[J]. Allergol Immunopathol (Madr), 2020, 48(2): 202-210. DOI:10.1016/j.aller.2019.05.004 |
| [16] |
PETRUS N C M, HULSHOF L, RUTJES N W P, et al. Response to: cost-effectiveness of using an extensively hydrolysed formula compared to an amino acid formula as first-line treatment for cow milk allergy in the UK[J]. Pediatr Allergy Immunol, 2012, 23(7): 686-686. DOI:10.1111/j.1399-3038.2012.01311.x |
| [17] |
GUEST J F, WEIDLICH D, MASCUNAN DIAZ J I, et al. Relative cost-effectiveness of using an extensively hydrolyzed casein formula containing the probiotic Lactobacillus rhamnosus GG in managing infants with cow's milk allergy in Spain[J]. Clinicoecon Outcomes Res, 2015, 7: 583-591. DOI:10.2147/CEOR.S89347 |
| [18] |
OVCINNIKOVA O, PANCA M, GUEST J F. Cost-effectiveness of using an extensively hydrolyzed casein formula plus the probiotic Lactobacillus rhamnosus GG compared to an extensively hydrolyzed formula alone or an amino acid formula as first-line dietary management for cow's milk allergy in the US[J]. Clinicoecon Outcomes Res, 2015, 7: 145-152. DOI:10.2147/CEOR.S75071 |
| [19] |
GUEST J F, WEIDLICH D, KACZMARSKI M, et al. Relative cost-effectiveness of using an extensively hydrolyzed casein formula containing the probiotic Lactobacillus rhamnosus GG in managing infants with cow's milk allergy in Poland[J]. Clinicoecon Outcomes Res, 2016, 8: 307-316. DOI:10.2147/CEOR.S105748 |
| [20] |
GUEST J F, NAGY E. Modelling the resource implications and budget impact of managing cow milk allergy in Australia[J]. Curr Med Res Opin, 2009, 25(2): 339-349. DOI:10.1185/03007990802594685 |
| [21] |
中华医学会儿科学分会免疫学组, 中华医学会儿科学分会消化学组, 中华儿科杂志编辑委员会. 中国婴幼儿牛奶蛋白过敏诊治循证建议[J]. 中华儿科杂志, 2013, 51(3): 183-186. |
| [22] |
陈同辛, 洪莉, 王华, 等. 中国婴儿轻中度非IgE介导的牛奶蛋白过敏诊断和营养干预指南[J]. 中华实用儿科临床杂志, 2022, 37(4): 241-250. |
| [23] |
梁敏, 张立文, 朱美华, 等. 血清IgE测定对牛奶过敏婴儿的临床意义[J]. 中国当代儿科杂志, 2015, 17(6): 618-622. |
| [24] |
上海市物价局, 上海市卫生和计划生育委员会, 上海市医保办. 上海市医疗机构医疗服务项目和价格汇编[EB/OL]. [2023-04-01]. https://wsjkw.sh.gov.cn/ylsfbz/index.html.
|
| [25] |
TAYLOR R R, SLADKEVICIUS E, PANCA M, et al. Cost-effectiveness of using an extensively hydrolysed formula compared to an amino acid formula as first-line treatment for cow milk allergy in the UK[J]. Pediatr Allergy Immunol, 2012, 23(3): 240-249. |
| [26] |
GUEST J F, KOBAYASHI R H, MEHTA V, et al. Cost-effectiveness of using an extensively hydrolyzed casein formula containing Lactobacillus rhamnosus GG in managing infants with cow's milk allergy in the US[J]. Curr Med Res Opin, 2018, 34(9): 1539-1548. |
| [27] |
GUEST J F, PANCA M, OVCINNIKOVA O, et al. Relative cost-effectiveness of an extensively hydrolyzed casein formula containing the probiotic Lactobacillus rhamnosus GG in managing infants with cow's milk allergy in Italy[J]. Clinicoecon Outcomes Res, 2015, 7: 325-336. DOI:10.2147/CEOR.S80130 |
| [28] |
GUEST J F, YANG A C, OBA J, et al. Relative cost-effectiveness of using an extensively hydrolyzed casein formula in managing infants with cow's milk allergy in Brazil[J]. Clinicoecon Outcomes Res, 2016, 8: 629-639. DOI:10.2147/CEOR.S113448 |
| [29] |
CRITTENDEN R G, BENNETT L E. Cow's milk allergy: a complex disorder[J]. J Am Coll Nutr, 2005, 24(6 Suppl): 582S-591S. |
| [30] |
DUBOIS A E J, TURNER P J, HOURIHANE J, et al. How does dose impact on the severity of food-induced allergic reactions, and can this improve risk assessment for allergenic foods? Report from an ILSI Europe Food Allergy Task Force Expert Group and Workshop[J]. Allergy, 2018, 73(7): 1383-1392. |
| [31] |
GUEST J F, NAGY E. Modelling the resource implications and budget impact of managing cow milk allergy in Australia[J]. Curr Med Res Opin, 2009, 25(2): 339-349. |
| [32] |
周少明, 代东伶, 杨郑. 以胃肠道症状为主要表现的婴儿牛奶蛋白过敏280例临床分析[J]. 中国当代儿科杂志, 2019, 21(3): 271-276. |
| [33] |
YANG M, TAN M, WU J, et al. Prevalence, characteristics, and outcome of cow's milk protein allergy in Chinese infants: a population-based survey[J]. Jpen J Parenter Enteral Nutr, 2019, 43(6): 803-808. |
| [34] |
MEYER R, GROETCH M, VENTER C. When should infants with cow's milk protein allergy use an amino acid formula? A practical guide[J]. J Allergy Clin Immunol Pract, 2018, 6(2): 383-399. |
 2023, Vol. 26
2023, Vol. 26


