文章信息
- 何炜, 潘俊敏.
- HE Wei, PAN Jun-min.
- CrPP2C蛋白影响衣藻细胞鞭毛过渡区结构
- Protein Phosphatase 2CInvolved in the Flagellar Transition Zone Structure of Chlamydomonas reinhardtii
- 中国生物工程杂志, 2016, 36(5): 68-73
- China Biotechnology, 2016, 36(5): 68-73
- http://dx.doi.org/DOI:10.13523/j.cb.20160510
-
文章历史
- 收稿日期: 2016-02-19
- 修回日期: 2016-04-05
纤毛是一种高度保守的细胞器,广泛存在于真核生物细胞表面,起对外界信号识别传递的作用,调控生物的生理、发育等功能[1]。纤毛的组装由膜泡在母中心粒的附着起始,轴丝微管从中心粒开始组装,伸展出纤毛突出到胞外空间。轴丝的伸展需要IFT(intraflagellar transport),一个活跃的基于微管-马达过程的运输蛋白复合物,运载微管蛋白和其他的组装成分[2]。纤毛基部存在扩散屏障,称为过渡区(transition zone),Y形结构(Y-link)为过渡区的标志结构,Y形蛋白结构连接着轴丝微管和纤毛膜[3]。过渡区限制纤毛膜和细胞膜之间的蛋白质运输,被认为是对膜结合蛋白定位的必要机制[4]。过渡区的破坏导致很多疾病,如美格氏综合征(Meckel syndrome,MKS)、朱伯特综合征(Joubert syndromes,JBTS)等[5],然而对其分子组分、形成机制和屏障调节了解的还很少。
蛋白质磷酸化与去磷酸化调控纤毛的信号转导,影响纤毛的运动、长度和组装等,在真核细胞纤毛中有调控作用。在衣藻细胞鞭毛中已鉴定出258个磷酸化蛋白,726个磷酸化位点[6]。蛋白丝氨酸、苏氨酸磷酸酶(protein serine/threonine phosphatase,PSP)特异性控制成千上万蛋白磷酸酶的去磷酸化,PSP家族包括PPP(phosphoproteinphatase)、PPM(metal-dependent protein phosphatase)、FCP/SCP(TFII-associating component of RNA polymerase II CTD phosphatases/small CTD phosphatase)。PPM家族没有调节亚基,但包含额外的结构域和具有保守性的模体来决定底物特异性[7]。PP2C是PPM家族的一员,PP2C类蛋白在人类中约有15个、在线虫中8个、在果蝇中10个、酵母中7个、在拟南芥中75个;PP2C蛋白在不同物种中分子质量差别很大,如拟南芥中此蛋白质大小约为48kDa,在草履虫中约为33kDa,在酵母中大约31kDa,其种类和分子质量的多样性表明功能的多样性[8]。
PP2C类蛋白催化核心区PP2C结构域约有272个氨基酸,CrPP2C蛋白具有磷酸蛋白酶催化亚基,含14个磷酸化位点,其中11个丝氨酸磷酸化位点、3个苏氨酸磷酸化位点,参与细胞蛋白修饰过程[6]。PtPP2C(Parameciumtetraurelia type 2C protein phosphatase)调节纤毛动力蛋白,对胞内货物运输和纤毛运动起重要作用[8]。PcPP2C在cAMP依赖的纤毛运动调节中起重要作用[9]。
莱茵衣藻(Chlamydomonas reinharrdtii)是一种单细胞真核生物,具有两根鞭毛,常用于研究鞭毛组装和解聚机制[1]。本文通过插入基因片段的方法筛选出鞭毛运动异常的突变体。分析表明PP2C基因的缺陷导致鞭毛组装缺陷,不组装鞭毛或组装短鞭毛,鞭毛内过渡区Y形结构(Y-link)不完整,揭示PP2C蛋白影响Y-link结构,进而在鞭毛组装过程中发挥重要作用。
1 材料与方法 1.1 材 料 1.1.1 藻株及其培养莱茵衣藻野生型藻株21gr(CC-1690,mt+):购自美国明尼苏达大学衣藻中心。
液体培养:在温度为23℃,光周期(光/暗:14h/10h)下吹气培养。用R液体培养基培养4~5天后,用M液体培养基传代培养[10]。
同步化培养:CO2(5%)吹气条件下在培养箱中光周期培养,在R液体培养基进行3~4天培养后,接入M液体培养基2~3天培养至细胞浓度约为1x106cells/ml。
1.1.2 菌株、质粒及引物本实验所用菌株、质粒及引物见表 1,引物由生工生物合成。
| Strains,plasmids and primers | Phenotype and characters | Source |
| Strains | ||
| Trans1-T1 | 用于分子克隆 | 全式金公司 |
| Plasmids | ||
| pSI103 | 含有aphVIII片段,具有巴龙霉素抗性 | 本室保存 |
| pEXP1 | 含有潮霉素抗性 | 本室保存 |
| pJP-HA | 具有 HSP70/RBCS2 启动子,3xHA tag,RBCS2 的终止子 | 本室保存 |
| pMD19-T | 用于克隆和测序 | TaKaRa |
| Primers | Sequences | |
| PP2C-S | TCTAGACCATGCACACCACCTGTCGCTA(下划线为Xbal酶切位点) | |
| PP2C-AS | AGATCTGCAGCAGCCTACTGTCCGGT(下划线为BglII酶切位点) |
1.1.3 主要试剂
DNA限制性内切核酸酶购于NEB公司;FAST PFU DNA聚合酶购于全式金公司;T4连接酶购于TaKaRa公司;质粒提取试剂盒、胶回收试剂盒购于生工生物公司。
一抗HA(Rat,1∶5 000)购于Roche公司;α-tubulin(Mouse,1∶2 500)购于Sigma-Aldrich公司。二抗HRP标记Goat anti-Rat(1∶5 000)购于Jackson 公司;Goat anti-Mouse(1∶5 000)购于Bio-Rad公司。
1.2 方 法 1.2.1 pp2c突变体的构建及鉴定将连续光照培养的衣藻细胞调整浓度至2.5×105cells/ml,冰上放置10min制成感受态细胞,在每250μl体系中加入0.1~1μg线性化含有巴龙霉素的aphVIII片段,使用电击仪电击之后过夜恢复,涂布于加有巴龙霉素筛选抗性的TAP平板上培养。
待藻落长出后挑至液体培养基,显微镜下观察其运动状态及鞭毛长度,将异常藻株扩大培养,提取基因组,使用限制性酶定点扩增(restriction enzyme site-directed amplification PCR,RESDA-PCR)技术鉴定外源基因在突变衣藻中的插入位置。
1.2.2 衣藻细胞显微成像及鞭毛长度的测量使用5%的戊二醛固定细胞,使用微分相差干涉显微镜(differential interference microscope,DIC)进行拍照,单个细胞的成像使用 100×油镜,量取鞭毛长度用40×物镜。
使用ImageJ软件打开图像并调整清晰度,使用分段线段工具测量鞭毛基部至顶端长度,所得测量数值乘以系数0.387 6即为鞭毛长度,每组样品测量50~100个细胞。
1.2.3 衣藻细胞鞭毛再生与解聚酸处理(pH shock)法诱导鞭毛脱落:用盐酸调节pH至4.0~4.5刺激30s,再用KOH中和 pH为7.0后,更换新鲜培养基,使鞭毛再生。使用焦磷酸钠(NaPPi)诱导鞭毛解聚:以M培养基配制NaPPi母液,加入衣藻细胞悬液中使终浓度为20mmol/L。处理之后在相应的时间点取200μl 细胞加入50μl 5%戊二醛固定细胞用于拍照。
1.2.4 衣藻细胞电镜样品制备收集3x108衣藻细胞,使用10%戊二醛固定液使细胞终浓度为1%,初步固定15min;pH7.2的砷酸盐固定液终浓度为100mmol/L,戊二醛固定液终浓度为1%,再次固定2h;使用100mmol/L的砷酸盐洗涤固定后的细胞3次;将细胞包埋于低温琼脂之中,切片后用透射电镜(transmission electron microscopy,TEM)观察。
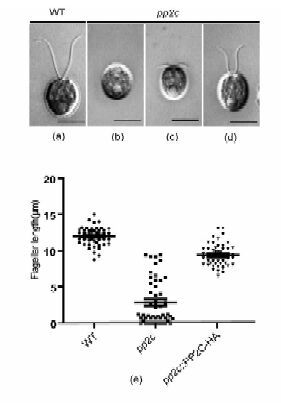
2 结 果 2.1 鞭毛组装突变体筛选野生型21gr细胞有两根等长约为12μm的鞭毛。如图 1(a)所示,细胞分散可活跃游动。通过电转法筛选插入突变体,在普通光学显微镜下挑选出运动异常的衣藻细胞,在微分相差干涉显微镜下进一步观察鞭毛并进行测量,最终得到鞭毛异常突变体。突变体细胞表现为多数细胞没有鞭毛或有极短鞭毛(鞭毛长度小于1μm),约占全部细胞的50%;也存在少数细胞鞭毛长度接近10μm,如图 1(b)~(d)所示。对全部个体均进行统计,无鞭毛细胞鞭毛长度记为0,得出鞭毛平均长度为2.7μm,如图 1(e)所示。有鞭毛的个体可原地转动。
|
| 图 1 突变体及野生型衣藻细胞微分相差干涉显微照片及鞭毛长度分布 Figure 1 DIC images of pp2c and wild type cells,and flagellar length distribution (a)Wild type(21gr)cell,bar 5μm (b)~(d)pp2ccells,bar 5μm (e)Flagellarlength distribution of pp2c,wild type and rescued cells(pp2c::PP2C-HA) |
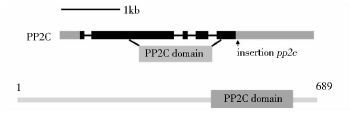
通过限制性酶定点扩增(RESDA-PCR)的方法,找寻外源基因在突变体基因组中的插入位置。通过两轮PCR扩增出约800bp的DNA片段,通过测序并在Chlamy Center网站(http://www.chlamy.org)比对,发现外源基因aphVIII反向插入在藻株CrPP2C基因3′UTR中,距离终止子80bp,如图 2所示,因此将突变体命名为pp2c突变体。
衣藻2C型蛋白磷酸酶基因(CrPP2C)全长2 656bp,包含5个外显子和4个内含子,表达689个氨基酸,其保守的磷酸蛋白酶催化亚基为272个氨基酸。将其序列在Blast软件中比对,PP2C蛋白在多种生物及多种蛋白质中普遍存在。
|
| 图 2 突变体插入位点及相关基因信息 Figure 2 Insertion site of pp2c and the information of PP2C gene |
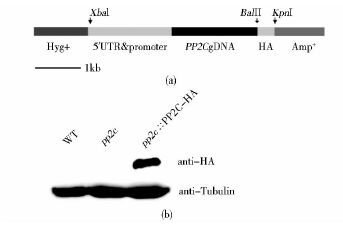
从野生型衣藻细胞的基因组中克隆出完整PP2C基因片段(包含5′UTR及前1.5kb启动序列,不包含终止子)和含有终止子的3xHA(Haemagglutinin)蛋白标签,连接入含有潮霉素抗性基因的表达载体中,如图 3(a)所示。将其通过电转法导入pp2c突变体之中,筛得性状回复藻株,其鞭毛长度回复到9.58μm,如图 1(e)所示。互补藻株虽未完全回复到野生型长度,但较突变体藻株已有显著性状回复。
|
| 图 3 突变互补载体构建及互补藻株蛋白表达检测 Figure 3 PP2C gene rescued plasmid and protein expression detection of rescued strain (a)Schematic diagram of PP2C gene rescued plasmid (b)Rescued strain tested by the western blot with anti-HA |
用Western Blot方法检测藻株PP2C-HA蛋白表达情况,使用HA抗体检测到在74kDa处有蛋白表达,在突变体及野生型细胞中均检测不到,如图 3(b)。此实验进一步证明突变性状是由于PP2C基因突变造成鞭毛缺陷。
2.4 突变体鞭毛组装过程受到阻碍使用酸处理细胞使鞭毛脱落,去除刺激后鞭毛会再次生长。使用NaPPi进行处理,衣藻鞭毛会逐渐解聚直至消失。实验中使用此方法观察突变体的组装和解聚过程。
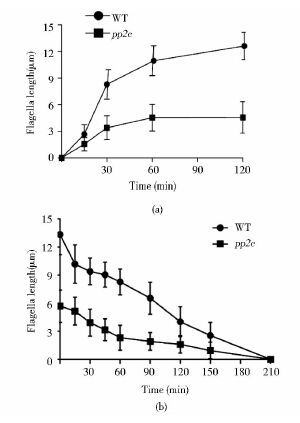
再生实验发现pp2c突变体不能再生至野生型长度,如图 4(a)所示;而使用NaPPi药物处理使鞭毛解聚,突变体鞭毛能够完全解聚,如图 4(b)所示。在此实验中因为需要统计鞭毛缩短趋势,所以将最初无鞭毛的细胞(包括鞭毛长度小于1μm,无法精确测量的细胞)按照50%的比例排除在统计之外,因此初始平均长度为5.68μm。此实验结果说明pp2c突变体鞭毛异常是组装过程受到阻碍。
|
| 图 4 鞭毛再生及解聚过程鞭毛长度曲线 Figure 4 Curve graphs of flagellar length in regeneration and disassembly (a)Curve graph of flagellar length during the period of regeneration (b)Curve graph of flagellar length during the period of disassembly |
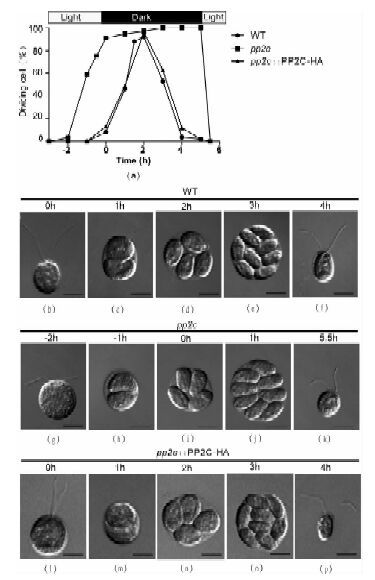
通过以上实验已知突变体鞭毛组装异常。鞭毛会随着细胞周期发生组装和解聚,因此我们想深入了解突变体的细胞周期情况。使用CO2同步法对衣藻细胞进行同步化培养,观察其细胞周期及分裂情况,发现pp2c突变体的分裂周期较野生型的提前,在光照前开始发生分裂,而野生型细胞在光照之后约2h才开始分裂,如图 5(a)所示。野生型细胞在暗周期前细胞体积变大,直至黑暗一直处于此状态,进入黑暗周期后开始发生分裂,细胞呈现二细胞、四细胞、八细胞状态,之后子细胞从母代细胞壁中释放出来,分散为单个细胞,如图 5(b)~(f)所示。pp2c突变体在分裂前同样会体积变大,进入黑暗周期之前2h就开始分裂,会出现二细胞、四细胞、八细胞状态,之后子细胞不能从母代细胞壁中释放出来,一直持续至黑暗周期结束,如图 5(g)~(k)所示。实验中在黑暗5h之后给与光照,0.5h后子代细胞完全从母代细胞壁中释放,子细胞中有少部分鞭毛能达到10μm,如图 5(k)所示。实验中将二细胞、四细胞、八细胞都记为分裂状态。互补细胞的分裂性状恢复为与野生型相同,如图(l)~(p)所示。
此实验证实突变体细胞分裂周期异常,较野生型细胞分裂提前,且子细胞不能及时从母细胞中游离出来,分散成为单个子细胞。
|
| 图 5 衣藻细胞分裂曲线和微分相差干涉显微照片 Figure 5 Curve graph and DIC images of cell division (a)Cell division curve graph of WT and pp2c (b)~(p)Cell division DIC images of WT and pp2c,pp2c::PP2C-HA,bar 5μm |
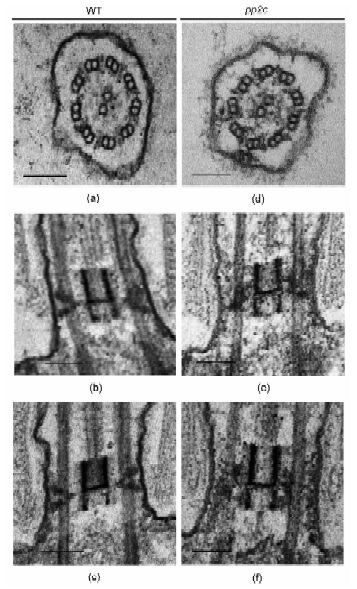
为了进一步了解突变体藻株鞭毛是否存在结构缺陷,使用透射电镜技术观察衣藻鞭毛的显微结构。野生型和突变体细胞鞭毛横切面均为9(2)+2结构,并无异常,如图 6(a)、(d)所示。野生型纵切面在鞭毛过渡区可以明显观察到“H”形结构和“Y”形连接结构,如图 6(b)、(c)所示;突变体pp2c的鞭毛过渡区有明显结构缺失,“Y”形连接区异常,不能形成完整的Y形结构,如图 6(e)、(f)所示。
通过对鞭毛显微结构的观察发现突变体的鞭毛过渡区结构缺陷,表明PP2C基因的破坏影响Y形结构的完整。
|
| 图 6 野生型及突变体鞭毛显微结构 Figure 6 The ultrastructure of wild type and pp2c flagella (a)The cross sections of wild type flagella (b),(c)The longitudinal sections of wild type flagella (d) The cross sections of pp2c flagella (e),(f)The longitudinal sectionsof pp2c flagella,Bar 100nm |
通过筛选大量衣藻插入突变体,得到PP2C基因破坏的衣藻藻株,其鞭毛长度异常,部分细胞没有鞭毛,部分有短鞭毛。在鞭毛再生实验中,突变体细胞不能生长至野生型长度,因此推测PP2C基因的破坏导致鞭毛组装过程受到阻碍。
野生型莱茵衣藻细胞鞭毛伴随着细胞分裂发生周期性的组装和解聚。进入细胞周期之前,鞭毛解聚的进程会影响细胞周期的进行[11-12]。因此探究pp2c突变体的细胞周期,发现突变体细胞分裂较野生型提前,并且分裂的细胞团无法及时释放出子细胞。猜想突变体细胞周期提前是由于细胞在非分裂期无鞭毛或短鞭毛,细胞分裂准备期大大缩短,从而使细胞周期紊乱,细胞分裂提前。而子细胞无鞭毛或短鞭毛,导致子细胞不能及时从细胞团游离开[13]。
野生型衣藻细胞退出细胞周期后,中心体分化成的鞭毛基体通过过渡纤维锚定在细胞质膜上,逐渐将α-tublin和β-tubulin异源二聚体组装到轴丝微管上,从而使鞭毛微管逐渐延长[14-15]。电镜实验显示pp2c突变体鞭毛显微结构过渡区的Y形结构不完整。猜想过渡区结构的缺失影响鞭毛基体锚定在细胞质膜上,影响鞭毛组装,导致鞭毛组装缺陷,不组装鞭毛或组装短鞭毛。
本文对PP2C基因突变藻株进行初步研究,证明PP2C基因破坏会导致鞭毛过渡区Y形结构的缺失,从而影响鞭毛的组装,为之后阐明衣藻细胞鞭毛组装过程的分子机制提供了有效的材料。
| [1] | Muqing C, Junmin P. Cilia and ciliopathies. Chinese Journal of Cell Biology,2012, 34 (9) : 849 –856. |
| [2] | Chih B, Liu P, Chinn Y, et al. A ciliopathy complex at the transition zone protects the cilia as a privileged membrane domain. Nature Cell Biology,2012, 14 (1) : 61 –72. |
| [3] | Czarnecki P G, Shah J V. The ciliary transition zone: from morphology and molecules to medicine. Trends in Cell Biology,2012, 22 (4) : 201 –210. |
| [4] | Garcia-Gonzalo F R, Corbit K C, Sirerol-Piquer M S, et al. A transition zone complex regulates mammalian ciliogenesis and ciliary membrane composition. Nature Genetics,2011, 43 (8) : 776 –784. |
| [5] | Lambacher N J, Bruel A L, van Dam T J P, et al. TMEM107 recruits ciliopathy proteins to subdomains of the ciliary transition zone and causes Joubert syndrome. Nature Cell Biology,2016, 18 (1) : 122 –131. |
| [6] | Wang H, Gau B, Slade W O, et al. The global phosphoproteome of Chlamydomonasreinhardtii reveals complex organellar phosphorylation in the flagella and thylakoid membrane. Molecular & Cellular Proteomics,2014, 13 (9) : 2337 –2353. |
| [7] | Shi Y. Serine/threonine phosphatases: mechanism through structure. Cell,2009, 139 (3) : 468 –484. |
| [8] | Grothe K, Hanke C, Momayezi M, et al. Functional characterization and localization of protein phosphatase type 2C from Paramecium. Journal of Biological Chemistry,1998, 273 (30) : 19167 –19172. |
| [9] | Noguchi M, Sasaki J Y, Kamachi H, et al. Protein phosphatase 2C is involved in the cAMP‐dependent ciliary control in Paramecium caudatum. Cell Motility and the Cytoskeleton,2003, 54 (2) : 95 –104. |
| [10] | Sager R, Granick S. Nutritional studies with Chlamydomonasreinhardi. Annals of the New York Academy of Sciences,1953, 56 (5) : 831 –838. |
| [11] | Kim S, Tsiokas L. Cilia and cell cycle re-entry: more than a coincidence. Cell Cycle,2011, 10 (16) : 2683 –2690. |
| [12] | Sung C H, Li A. Ciliary resorption modulates G1 length and cell cycle progression. Cell Cycle,2011, 10 (17) : 2825 –2826. |
| [13] | Hilton L K, Gunawardane K, Kim J W, et al. The kinases LF4 and CNK2 control ciliary length by feedback regulation of assembly and disassembly rates. Current Biology,2013, 23 (22) : 2208 –2214. |
| [14] | Avidor-Reiss T, Gopalakrishnan J. Cell cycle regulation of the centrosome and cilium. Drug Discovery Today: Disease Mechanisms,2013, 10 (3) : e119 –e124. |
| [15] | Parker J D K, Hilton L K, Diener D R, et al. Centrioles are freed from cilia by severing prior to mitosis. Cytoskeleton,2010, 67 (7) : 425 –430. |
 2016, Vol. 36
2016, Vol. 36




