文章信息
- 殷爽, 冯翠, 张纯, 王祺, 王健, 余蓉, 刘永东, 苏志国
- YIN Shuang, FENG Cui, ZHANG Chun, WANG Qi, WANG Jian, YU Rong, LIU Yong-dong, SU Zhi-guo
- 转铁蛋白-PEG-睫状神经营养因子的制备及其生物活性评价
- Preparation of Transferrin Conjugated Ciliary Neurotrophic Factor and Evaluation of Biological Activity
- 中国生物工程杂志, 2016, 36(4): 43-49
- China Biotechnology, 2016, 36(4): 43-49
- http://dx.doi.org/10.13523/j.cb.20160407
-
文章历史
- 收稿日期: 2015-10-12
- 修回日期: 2015-11-06
2. 中国科学院过程工程研究所生化工程国家重点实验室 北京 100190;
3. 北京生物制品研究所 北京 100024
2. State Key Laboratory of Biochemical Engineering, Institute of Process Engineering, Chinese Academy of Sciences, Beijing 100190, China;
3. National Vaccine and Serum Institute, Beijing 100024, China
睫状神经营养因子(ciliary neuronotrophic factor,CNTF)是上世纪80年代由Barbin等[1]从鸡胚的睫状神经节中提取的一种多功能细胞因子。早期的研究认为它是一种可促进睫状神经元和脊髓中运动神经元存活的营养因子,但在随后的临床研究出乎意料地发现其具减轻个体体重的活性。后续研究发现CNTF与瘦蛋白的作用机理类似,均作用于分布在控制食欲的下丘脑区域的受体[2],通过瘦蛋白样(leptin-like)机制促使机体减轻体重,但其机理又不尽相同。CNTF与Leptin都能够促进基因缺陷所致肥胖型小鼠脂肪含量的减少,然而对于具有Leptin抗性的饮食诱导肥胖型(Diet-induced obesity,DIO)小鼠,仅CNTF表现出强大的减轻体重能力[3]。DIO型肥胖与人类绝大多数肥胖患者发病机理更为贴近。研究发现CNTF作用于下丘脑区域受体,在不引发饥饿感的情况下减少机体对食物的摄取量。更为重要的是其不会引起机体发热、胃肠道不适等副作用,停药后体重不会快速反弹。因此CNTF作为人类肥胖药物表现出了较好的应用前景。
天然CNTF含200个氨基酸,分子量20kDa,一级序列中仅在第17位有一个游离的半胱氨酸,分子内无二硫键、无N-糖基化位点和信号肽[4, 5, 6],其空间结构如图 1a。天然人CNTF在体内半衰期极短,约2.9分钟[7]。另外,文献报道一种生理活性更高的序列截短突变型重组人CNTF,将CNTF C末端15个氨基酸截掉,并且把63位谷氨酰胺突变为精氨酸。研究结果显示每天对小鼠给予一定剂量的改良型CNTF持续一周后,小鼠体重得到显著减轻。改良型CNTF在血液中的半衰期有所提升(约半小时),但仍然需要每天注射给药才能维持药效,过于频繁的注射限制了其临床上的应用[8]。所以,体内半衰期短是限制CNTF用于肥胖疾病治疗的主要因素。

|
| 图 1 CNTF蛋白结构(a)与转铁蛋白结构(b) Fig. 1 Crystal structure of CNTF and transferrin |
转铁蛋白(transferrin ,Tf)在体内主要起着运输金属离子的功能,分子量约为80 kDa,拥有两个独立功能的结构域(N-lobe和C-lobe,图 1b),分别能够与转铁蛋白受体结合。蛋白受体在血脑屏障细胞表面高表达,因为其在大脑物质运输过程中起着不可替代的作用。也正是因为如此,转铁蛋白受体通常被用作脑部靶向药物的媒介[9]。转铁蛋白在人体血液内含量仅次于血清白蛋白,约占血浆总蛋白的4%~6%,来源极为丰富。同时,其在人体血液循环系统中的更新周期长(约10天)[10]。其自身半衰期长的特性源于其抗血液蛋白酶水解的能力(序列特异性以及糖基化修饰)以及分子量较大极少被肾脏滤除,因此转铁蛋白也可应用于长效递药。
在前期研究中,我们已经成功制备了结构正确、且具备高活性的重组人CNTF蛋白[11]。在本研究中,我们拟使用NHS-PEG5k-MAL试剂将转铁蛋白和重组CNTF的C17位点进行定点偶联,反应机理如图 2。再结合重组人CNTF自身的结构性质和偶联后分子体积上的差异分离获得单个转铁蛋白上连接重组人CNTF数量较为均一的Tf-PEG5k-CNTF耦合物。并初步评价了Tf-PEG5k-CNTF的生物活性以及在大鼠体内的代谢半衰期和降低小鼠体重的效力。
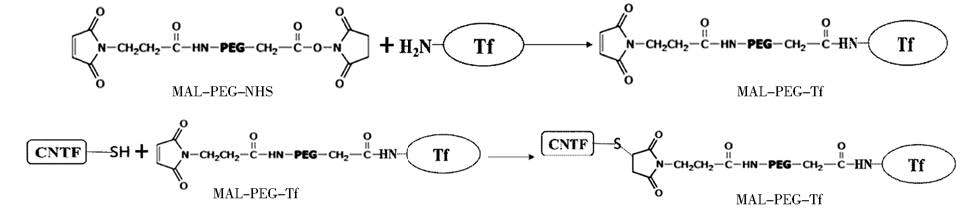
|
| 图 2 NHS-PEG-MAL 偶联Tf与CNTF反应机理 Fig. 2 Mechanism of conjugation of Tf and CNTF by NHS-PEG-MAL |
重组rhCNTF工程菌由北京生物制品研究所提供。
1.1.2 化学试剂层析介质DEAE-Sepharose FF、Ni-Sepharose FF、制备型Superdex200介质购自GE Healthcare公司(美国),NHS-PEG5k-MAL购自北京键凯科技有限公司,其他试剂均为国产分析纯。
1.1.3 设备ÄKTA purifier层析系统(GE Healthcare,美国);Agilent 1100高效液相系统(Agilent,美国)。反相色谱柱C4(4.6 mm×250 mm)(资生堂,日本) SuperdexTM 200 高效凝胶过滤柱(GE Healthcare,美国)。Nano ZSP动态光散射仪(Malvern,英国)。
1.2 方 法 1.2.1 重组CNTF的纯化制备重组CNTF的纯化制备参考我们之前的工作基础[11],简言之,大肠杆菌可溶性表达的重组CNTF破碎上清液经疏水层析、阴离子交换层析和Ni-亲和介质层析纯化而得,纯度用12%SDS-PAGE检测。
1.2.2 转铁蛋白与CNTF的偶联(1) Tf-PEG5k-MAL的制备。取转铁蛋白200 mg,溶于50 ml 20 mmol/L 4-羟乙基哌嗪乙磺酸(HEPES),10mmol/L马来酸,pH7.5的缓冲液中,将终浓度为约4.0 mg/ml蛋白溶液放置在4℃下预冷0.5h后,按转铁蛋白/修饰试剂摩尔比1/3加入NHS-PEG5k-MAL修饰试剂(约40 mg),溶解后缓慢搅拌反应1 h,缓冲液A(20mmol/L HEPES 10mmol/L 马来酸,pH7.5)稀释5倍,将稀释液载入经缓冲液A预先平衡好的装有30 ml DEAE-Sepharose FF介质的层析柱中,流速为5 ml/min。上样完后缓冲液淋洗至基线平稳,使用20%的缓冲液B(缓冲液A+1.0mol/L NaCl)阶跃洗脱下蛋白,留适量洗脱峰样品12%SDS-PAGE分析。
(2) Tf-PEG5k-CNTF的制备。将上述阶跃洗脱下的Tf-PEG5k-MAL加入到20 ml 2.5 mg/ml(20mmol/L HEPES 10mmol/L马来酸,pH7.5)的CNTF溶液中,混匀后,静置于4℃冰箱中反应16h。待反应结束后,将反应液稀释至蛋白浓度约1.0 mg/ml,将稀释液载入经缓冲液C(50mmol/L Tris-HCl pH8.0 0.5mol/L NaCl)装有10 ml Ni-Sepharose FF介质的层析柱中,上样结束后使用2%缓冲液D(缓冲液C+0.5mol/L咪唑)约10mmol/L咪唑淋洗至基线平稳,然后20%缓冲液D阶跃洗脱下蛋白。将洗脱下的蛋白液,再经Superdex200凝胶层析,流动相使用50mmol/L磷酸盐0.15mol/L Na2SO4 pH7.0缓冲液,收集各阶段的流出峰,留适量洗脱峰样品12%SDS-PAGE分析。
1.2.3 蛋白质浓度测定测定方法参照Lowry法[12]。
1.2.4 高效凝胶过滤色谱分析凝胶过滤使用ÄKTA purifier层析系统和SuperdexTM 200(10/300 GL)分析柱,缓冲液为50mmol/L磷酸盐0.15mol/L Na2SO4 pH7.0缓冲液,流速0.6 ml/min ,上样量500 μl,检测波长为280 nm。
1.2.5 反相液相色谱分析采用资生堂proteonavi C4分析柱(4.6×250 mm),检测波长为280 nm,Tf,CNTF和Tf-PEG5k-CNTF进样量都为100 μl,流动相A为超纯水+0.1%三氟乙酸,流动相B为乙腈+0.1%三氟乙酸,洗脱梯度为20%~100%,流速设置为0.5ml/min,时间30 min。
1.2.6 动态光散射(DLS)测定蛋白粒径大小使用Nano ZSP动态光散射仪测定蛋白粒径,将蛋白样品浓度使用50 mmol/L Tris-HCl pH8.0缓冲液稀释并调节浓度至0.5 mg/ml。吸取1.5 ml放入1.0 cm光径的比色杯中,设置3次扫描重复。
1.2.7 生物活性的考察Tf1细胞(人红白血病细胞)测定rhCNTF生物活性[13, 14]。
1.2.8 大鼠体内代谢动力学试验体重为250 g左右雄性SD大鼠13只,随机分为3组,其中生理盐水对照组3只,两组实验为5只,将生理盐水或蛋白从大鼠尾静脉注入后,在既定的时间点通过大鼠眼眶静脉取血0.5 ml,室温放置30min后,高速离心获得血清,保存于-70℃至使用前。所有血清采取结束后,使用hCNTF ELISA试剂盒测得血清中样品的含量。
1.2.9 小鼠体重减轻试验体重约20 g雄性C57BL/6型小黑鼠18只,随机均分为3组。将生理盐水,CNTF和Tf-PEG5k-CNTF按1.0 mg/kg的剂量皮下注射,每周两次,食物和饮水保证绝对充足,自由饮食。每天称取小鼠体重,观察体重变化。
2 结果与分析 2.1 转铁蛋白与CNTF的偶联考虑到CNTF蛋白的一级序列中自带有一个游离半胱氨酸(Cys17)而转铁蛋白中没有游离的半胱氨酸,因此我们选择使用了双末端异功能化的偶联试剂NHS-PEG5k-MAL进行CNTF蛋白和转铁蛋白偶联。偶联试剂NHS活化酯端首先与转铁蛋白上的氨基随机连接,控制偶联试剂与转铁蛋白的使用比例(3∶1或6∶1)以及反应条件(时间,温度和pH值),可获得转铁蛋白连接1或2分子偶联剂的修饰产物。结合转铁蛋白的纯化方法(图 3),通过离子交换柱层析(DEAE-Sepharose)去除未能与转铁蛋白连接的偶联试剂,获得转铁蛋白和Tf-PEG5k-MAL为主的混合物。混合物中Tf-PEG5k-MAL的马来酰亚胺端再与CNTF中的游离半胱氨酸连接。无His-tag亲和标签的CNTF同样对Ni-Sepharose显示出较高的亲和力,在我们前期的工作中已经将这种性质用于CNTF原蛋白的纯化制备。因此,CNTF与Tf-PEG5k-MAL反应结束后,通过CNTF的亲和力,可去除混合物中的转铁蛋白和未反应的Tf-PEG5k-MAL。最后再根据Tf-PEG5k-CNTF与CNTF分子体积上的显著差异,采用凝胶柱去除多余的未偶联的CNTF,获得Tf-PEG5k-CNTF耦合物。偶联反应原蛋白及偶联后层析目标洗脱峰电泳结果如图 4。
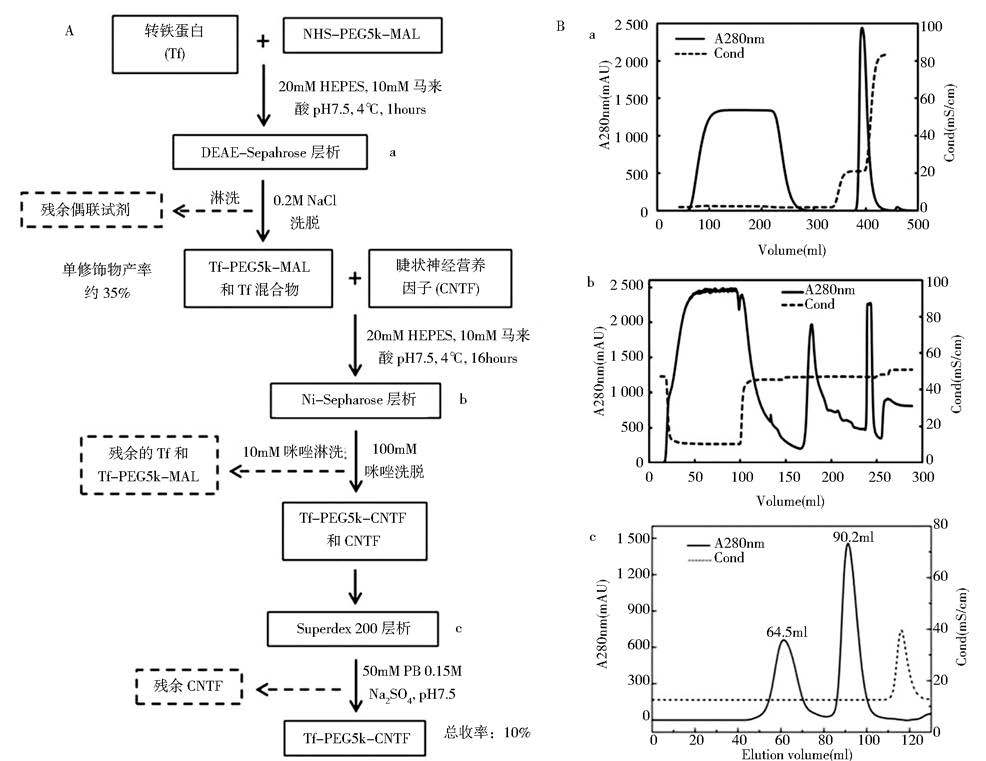
|
| 图 3 转铁蛋白与CNTF耦合物的制备路线图(A)和分离纯化层析图(B) a:DEAE离子交换树脂层析图;b:Ni-亲和层析图;c:Superdex 200凝胶过滤层析图 Fig. 3 Route for preparation of the Tf-PEG5k-CNTF conjugates (A) and its chromatograms (B) |
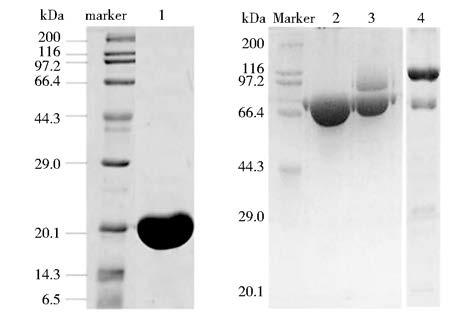
|
| 图 4 层析洗脱峰电泳图 Fig. 4 SDS-PAGE analysis of eluted peaks 1: Purified CNTF; 2: Transferrin; 3: Tf-PEG5k-MAL; 4: Superdex200 eluted peak (elution volume: 64.5ml) |
为了分析耦合物的纯度,我们使用了反相-高效液相色谱分析。分析检测结果表明所制备得到的Tf-PEG5k-CNTF的纯度高于90%(图 5)。
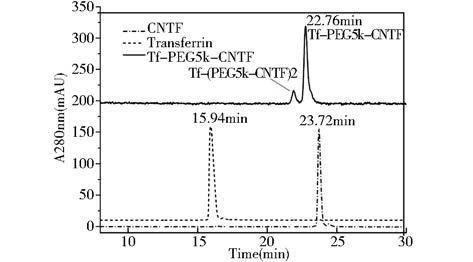
|
| 图 5 高效液相色谱分析蛋白纯度 Fig. 5 RP-HPLC analysis of the protein purity |
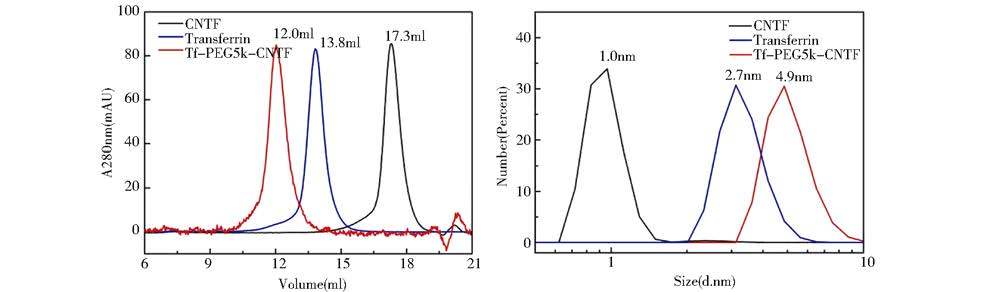
为了考察耦合物与CNTF的表观分子体积,我们使用了高效凝胶过滤色谱分析,结果显示较之CNTF,耦合物的表观分子体积显著增加。同时DLS测定耦合物与CNTF在水溶液中的粒径,结果显示CNTF原本的分子粒径约1.0 nm,而CNTF与转铁蛋白通过NHS-PEG5k-MAL偶联后,分子粒径增加至4.9 nm。高效凝胶过滤分析与DLS分析结果相吻合(图 6)。
|
| 图 6 高效凝胶过滤色谱和动态光散射分析耦合物 Fig. 6 HP-SEC and DLS analysis of the protein conjugates |
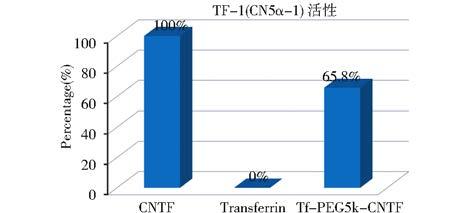
TF-1(CN5α-1)细胞膜表面能够表达CNTF受体,CNTF能够短暂维持其细胞的生长。基于此,细胞活性试验中,细胞的存活率直接反应出蛋白的CNTF活性。与CNTF比较,Tf-PEG5k-CNTF的活性下降至原蛋白活性的65.8%(图 7)。
|
| 图 7 TF-1(CN5α-1)细胞活性测定 Fig. 7 Measurement of the TF-1(CN5α-1) cell survival activity |
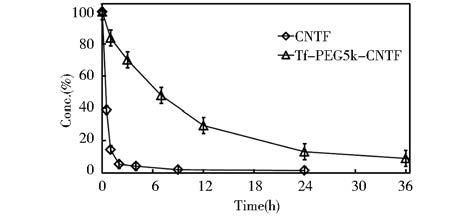
使用Sandwich ELISA法测定CNTF和Tf-PEG5k-CNTF在大鼠血液中的代谢半衰期,结果如图 8。CNTF原蛋白在大鼠中的半衰期约0.5h,注射8h后,血液中几乎检测不出CNTF,与文献所报道相近。Tf-PEG5k-CNTF在大鼠中的代谢半衰期约为8.2h,相对于CNTF原蛋白,半衰期延长了约17倍(图 8)。mPEG5k修饰CNTF的半衰期约1h(数据未给出),这表明转铁蛋白对延长Tf-PEG5k-CNTF在体内的保留半衰期起着决定性作用。
|
| 图 8 雄性SD大鼠体内药代动力学 Fig. 8 Pharmacokinetics of the conjugates in SD male rats |
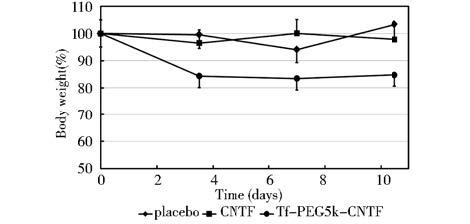
考虑到DIO型肥胖仅与食物摄取相关,而在遗传学上与正常个体并无差异,以及DIO型小鼠模型不易获得的因素,我们选择了正常小鼠进行体重减轻实验。C57小鼠经每周2次皮下给药(1.0 mg/kg)后在10天内的体重变化如图 9和表 1,对照组(生理盐水)在近10天的实验中,体重略有增加,CNTF蛋白组与对照组之间的比较有统计学意义,而与开始试验前自身体重比较无统计学差异。Tf-PEG5k-CNTF组较生理盐水组和CNTF原蛋白组在近10天实验中,均有显著差异,并且在第二次给药后体重得到了较好的维持(起始重量的85%,图 9)。食物的摄入量统计结果显示,小鼠体重的降低与小鼠食物摄入量有一定的相关性(表 1)。
|
| 图 9 耦合物与CNTF对雄性C57小鼠体重的影响比较 Fig. 9 Pharmacodynamics of CNTF and Tf-PEG5k-CNTF in C57 male mouse |
| Phase | 1~3.5天(g) | 3.5~7天(g) | 7~10.5天(g) | 总计(g) |
| 生理盐水对照组 | 78.2 (100%) | 79.78 (100%) | 78.01 (100%) | 236.0 (100%) |
| CNTF | 53.48 (68.4%) | 59.12 (74.5%) | 47.09 (60.4%) | 159.7 (67.7%) |
| Tf-PEG5k-CNTF | 23.61 (31.1%) | 41.49 (52.0%) | 43.58 (55.9%) | 108.7 (46.1%) |
蛋白与蛋白偶联是当今生物技术药物研究的一个重要方向。偶联试剂的不稳定性,偶联反应的低选择性和耦合物的低收率是目前蛋白间偶联仍亟待解决的技术问题[15]。此外,耦合物的分离纯化也是耦合物制备过程中的关键技术。本研究通过合理设计、筛选,成功制备了Tf-PEG5k-CNTF耦合物。利用CNTF中唯一的游离半胱氨酸实现CNTF定点偶联。通过优化反应条件可实现转铁蛋白上连接CNTF蛋白数目的可控,结合蛋白自身的性质,实现耦合物的分离纯化。
转铁蛋白拥有两个独立结构域,随机在转铁蛋白上连接一分子蛋白对转铁蛋白与其受体作用的影响有限。为防止连接试剂中马来酰亚胺官能团在前期制备中过快水解失效,缓冲体系中加入一定量的马来酰亚胺水解物结构类似物在一定程度上能够延缓其快速水解。CNTF与转铁蛋白偶联后,细胞活性与原蛋白相比有所下降,转铁蛋白所带来的空间位阻以及偶联试剂连接CNTF的位点可能是其活性下降的原因。
大鼠药代动力学试验显示转铁蛋白能够显著提升CNTF在大鼠体内的清除半衰期,一方面是偶联的转铁蛋白赋予了CNTF更大的分子体积,高效凝胶过滤色谱分析和DLS分析也证实了这一点,更大的分子体积能够减少被肾脏过滤清除的概率;另一方面是转铁蛋白能够帮助CNTF在一定程度上逃逸体内的蛋白酶以及吞噬细胞的清除。与CNTF原蛋白作比较,小鼠动物试验显示在每周两次的给药频率,每次1.0 mg/kg的剂量下,Tf-PEG5k-CNTF更为显著地影响小鼠的食物摄入量。提示Tf-PEG5k-CNTF能够穿透血脑屏障到达下丘脑区域发生药效作用。其可能的机理为转铁蛋白延长了CNTF在体内的作用时间,且转铁蛋白在CNTF脑部转运中起到了一定作用。综上所述,虽然偶联转铁蛋白对CNTF的生物活性有影响,但是耦合物在动物体内的表现仍然优于原蛋白,转铁蛋白偶联技术可用于作用于脑部的蛋白药物的长效递送。
致谢 感谢教育部博士点基金(NO. 120120181110036),生化工程国家重点实验室开放基金(NO. 2014KF-05)和国家自然科学基金(NO. 21576267)对本研究的支持。
| [1] | Barbin G, Manthorpe M, Varon S. Purification of the chick eye ciliary neuronotrophic factor. Journal of Neurochemistry, 1984,43(5): 1468-1478. |
| [2] | Lambert P D, Anderson K D, Sleeman M W, et al. Ciliary neurotrophic factor activates leptin-like pathways and reduces body fat, without cachexia or rebound weight gain, even in leptin-resistant obesity. Proceedings of the National Academy of Sciences, USA, 2001, 98:4652-4657. |
| [3] | Joseph F K, Carol F E, Charlotte E L. Ciliary neurotrophic factor and leptin induce distinct patterns of immediate early gene expression in the brain. Diabetes, 2004, 53:911-920. |
| [4] | McDonald N Q, Panayotatos N, Hendrickson W A.Crystal structure of dimeric human ciliary neurotrophic factor determined by MAD phasing. The EMBO Journal, 1995, 14 ( 12 ) : 2689-2699. |
| [5] | 杨光,李祎,项光亚. 重组人睫状神经营养因子肽图分析.生物技术通报,2010,11: 162-165. Yang G, Li W, Xiang G Y. Peptide mapping analysis of recombinant human ciliary neurotrophic factor. Biotechnology Bulletin, 2010,11: 162-165. |
| [6] | Lam A, Fuller F, Miller J, et al. Sequence and structural organization of the human gene encoding ciliary neurotrophic factor. Gene, 1991, 102(2):271-276. |
| [7] | Dittrich F, Thoenen H, Sendtner M. Ciliary neurotrophic factor: pharmacokinetics and acute-phase response in rat. Annals of Neurology, 1994, 35:151-163. |
| [8] | Shannon M, Maria B. Ciliary neurotrophic factor variants. US Patent, A1, 20050064555, 2005. |
| [9] | Hopkins C R, Trowbridge I S. Internalization and processing of transferrin and the transferrin receptor in human carcinoma A431 cells. The Journal of Cell Biology, 1983, 97:508-521. |
| [10] | Gomme P T, McCann K B, Bertolini J. Transferrin: structure, function and potential therapeutic actions. Drug Discovery Today, 2005, 10:267-273. |
| [11] | 冯翠,赵大伟 ,张纯,等. 一种重组人睫状神经营养因子突变体的分离纯化及结构鉴定.中国生物工程杂志, 2013,33(10):21-27. Feng C, Zhao D W, Zhang C, et al. Purification and characterization of a new recombinant ciliary neurotrophic factor mutant expressed in soluble form by E.coli. China Biotechnology, 2013, 33(10):21-27. |
| [12] | Lowry O H, Rosebrough N J, Farr A L, et al. Protein measurement with the folin phenol reagent. The Journal of Biological Chemistry, 1951, 193 (1): 265-275. |
| [13] | 周虎,汪怡,朱俊铭.定量测定重组人睫状神经营养因子活性的新方法.中国生物工程杂志,2008,28( 2) : 86-89. Zhou H, Wang Y, Zhu M J. A new quantitative determination method for the biological activity of recombinant human ciliary neurotrophic factor. China Biotechnology, 2008, 28(2):86-89. |
| [14] | 毕华,袁力勇,史新昌,等.睫状神经营养因子突变体蛋白的活性研究.中国生物工程杂志,2007,27( 1) : 1-5. Bi H, Yuan L Y, Shi X C, et al. Activity study of ciliary neurotrophic factor (CNTF) mutant. China Biotechnology, 2007, 27(1):1-5. |
| [15] | Kluger R, Alagic A. Chemical cross-linking and protein-protein interactions-a review with illustrative protocols. Bioorganic Chemistry, 2004, 32:451-472. |
| [16] | 冯翠,王祺,张纯,等.PEG 定点修饰重组人睫状神经营养因子及其生物活性评价.中国生物工程杂志,2015,35(5):15-21. Feng C, Wang Q, Zhang C, et al. Preparation of mPEG-MAL-modified recombinant human ciliary neurotrophic factor and evaluation of biological activity. China Biotechnology, 2015, 35(5):15-21. |
 2016, Vol. 36
2016, Vol. 36




