文章信息
- 董娟, 李佛生, 罗枫雪, 夏芳, 朱淑华, 唐琳
- DONG Juan, LI Fo-sheng, LUO Feng-Xue, XIA Fang, ZHU Shu-hua, TANG Lin
- 水稻miRNA3026启动子及硫氧还蛋白基因OsTxnDC9的克隆与分析
- Cloning and Expression Analysis of Rice miRNA3026 Promoter and Thioredoxin OsTxnDC9
- 中国生物工程杂志, 2016, 36(1): 29-37
- China Biotechnology, 2016, 36(1): 29-37
- http://dx.doi.org/10.13523/j.cb.20160105
-
文章历史
- 收稿日期: 2015-10-19
- 修回日期: 2015-11-18
水稻(Oryza sativa L.)是世界重要粮食作物之一,也是植物发育生物学和分子生物学研究的理想模式植物。水稻基因组测序工作的完成促进了对水稻功能基因的研究。目前,科学家已分析并克隆了大量的水稻功能基因,如控制水稻抽穗期的基因RIDI[1]、与茎强度有关的基因FCI[2]、促进水稻分蘖芽生长的基因MOCI[3]、与水稻抗旱性有关的基因SKCI[4]、Xa26[5]抗水稻白叶枯病的基因Xa26,与水稻穗形态有关的基因GEPE[6]等 。
硫氧还蛋白(thioredoxin,Trx) 是一种低分子质量、热稳定的多功能酸性蛋白质,广泛存在于植物、细菌、酵母和动物体中[7]。Trx 最初发现于大肠杆菌 (Escherichia coli)中作为核苷酸还原酶的氢供体[8],之后人们对其在生物体中的功能做了多方面的研究。按照氨基酸排列顺序的不同将Trx分成两大家族,即家族Ⅰ和家族Ⅱ。根据最初的不同结构,Trx家族Ⅰ又被分为6类:k、f、m、o、x和y[9]。硫氧还原蛋白在多种反应中通过可逆的双硫键和硫醇变化起氧化还原载体的作用,是非常重要的酶活性调节蛋白[10]。
MicroRNA(miRNA)是广泛存在于真核生物的一类长度为21~25nt[11]的内源性非编码单链小分子RNA,在植物中,miRNA调控大量基因的表达,包括控制生长发育的基因[12]和与胁迫反应相关的基因[13, 14]。许多实验表明,miRNA能够调节转录因子,敲除miRNA引发不正常的表型。
通过内含子miRNA数据库(http://inmirna.org/main)查询,可得硫氧还原蛋白基因OsTxnDC9是水稻miRNA3026的宿主基因。本实验利用生物信息学的方法分析水稻miRNA3026启动子和硫氧还蛋白基因OsTxnDC9的序列,并克隆了启动子miRNA3026和OsTxnDC9基因的序列,构建了miRNA3026启动子的缺失片段,瞬时表达表明其是个弱启动子。荧光定量PCR分析OsTxnDC9基因发现,在水稻的根、茎、叶,以及花粉的一核、二核、三核中都有表达且在一核中的表达量最高。亚细胞定位实验发现,OsTxnDC9基因主要在细胞质中表达。这些都为深入研究miRNA3026启动子与其宿主基因OsTxnDC9打下了基础。
1 材料与方法 1.1 材 料 1.1.1 实验材料供试水稻材料为普通籼稻桂朝二号,种植于四川省成都市四川大学实验基地,按常规方法进行田间管理。
1.1.2 质粒、菌株和试剂大肠杆菌Top10、pBI221表达载体由本实验室保存。pMD 19-T购自TaKaRa宝生物工程(大连)有限公司。植物总RNA提取试剂盒、DNA提取试剂盒和DNA柱式胶回收试剂盒购自北京天根生物有限公司。试剂、酶等药品均购自TaKaRa宝生物工程(大连)有限公司。
酶解液:20mmol/L MES(pH 5.7)、1.5%(wt/vol)纤维素酶R10、0.4% (wt/vol)离析酶R10、0.4mol/L甘露醇、20 mmol/L KCl,55℃温育10min,冷却至室温(22~25℃)后加入10mmol/L CaCl2,1~5mmol/L β-巯基乙醇(选加)和0.1% BSA,最后的酶解液呈澄清的浅棕色,0.45μm 过滤灭菌10ml到培养皿(100×25mm2)。 WI溶液:4mmol/L MES(pH 5.7)、0.5mol/L甘露醇、20mmol/L KCl,室温(22~25℃)保存。 W5溶液:2mmol/L MES(pH 5.7)、154mmol/L NaCl、125mmol/L CaCl2、5mmol/L KCl,室温(22~25℃)保存。 MMG溶液:4mmol/L MES(pH 5.7)、0.4mol/L甘露醇、15mmol/L MgCl2,室温(22~25℃)保存。PEG-Ca2+ 转化溶液:20~40%(m/V)PEG4000、0.2mol/L 甘露醇、100mmol/L CaCl2。 荧光素双乙酸酯(FDA):丙酮溶解,2mg/ml,-20℃保存。使用时用MMG或WI 溶液稀释1倍。
1.2 方 法 1.2.1 水稻miRNA3026启动子和硫氧还蛋白基因OsTxnDC9的生物信息学分析从NCBI数据库(http://www.ncbi.nlm.nih.gov/)中下载水稻硫氧还蛋白基因OsTxnDC9的序列(LOC_0s08g15204.1)和miRNA3026启动子的序列。利用PlantCARE(http://bioinformatics.psb.ugent.be/webtools/plantcare/html/)进行启动子序列分析,用PredictProtein、TargetP亚细胞定位及WoLFPSORT等软件预测硫氧还原蛋白质亚细胞定位,MEGA 4.0软件构建系统进化树,DNAMAN软件进行氨基酸序列对比。
1.2.2 水稻RNA,DNA的提取及cDNA合成采用Ttizol总RNA提取试剂盒进行总RNA提取。分别通过测定其OD260/280比值和1%琼脂糖凝胶电泳比值,分析所提取总RNA的纯度、检测其完整性。按照试剂盒操作说明书提取基因组DNA,利用反转录试剂盒对水稻RNA进行反转录获得cDNA。
1.2.3 水稻miRNA3026启动子和硫氧还原蛋白基因OsTxnDC9的克隆根据搜索到的基因序列,设计水稻miRNA3026启动子和OsTxnDC9基因序列的特异引物(表 1),进行PCR扩增。PCR产物进行1%琼脂糖凝胶电泳检测,切下目的条带经琼脂糖凝胶回收试剂盒回收后送华大基因科技服务有限公司进行测序。命名为miRNA3026启动子全长克隆为miR3026PRF。
| Primer | Sequence(5′→3′) |
| BamH3026PR | CGCGGATCCGGATCCAACCTGCCACCCAGTTCTTG |
| Hind3026PF | CCCAAGCTTAAGCTTCTCGTCTGCCACTTCTACCG |
| Hind3026PF1 | CCCAAGCTTATTCGTTGATGCGGAGCG |
| Hind3026PF2 | CCCAAGCTTGGTCGTGCATGTCCATACCG |
| Hind3026PF3 | CCCAAGCTTCTCCATCCAGGCAGTATCTACC |
| Hind3026PF4 | CCCAAGCTTACGATTGGTCCACCTCTAAAAG |
| BamH OsTxnDC9R | CGCGGATCCCAACCATAAACGATGCCGACC |
| Hind OsTxnDC9F | CCCAAGCTT CAGCCTTGCGACCATACTCCC |
| BamH-LUCF | CGCGGATCCATGGAAGACGCCAAAAACATAAAG |
| Sac-LUCR | CCCGAGCTCTTACACGGCGATCTTTCCGC |
| Notes:Straight lines: restriction enzyme cutting site.Small letters:protective bases | |
根据水稻in-miR3026所在基因的序列设计5′序列缺失引物(表 1)。以水稻花粉DNA为模板作PCR扩增,扩增结果经1%琼脂糖电泳分别得到特异性扩增带,将这些不同长度的独立启动子片段纯化回收后,连接到pBI221克隆载体,得到重组质粒,转化大肠杆菌Top10,菌液经PCR鉴定后进行测序。测序结果表明PCR扩增出来的片段序列均正确,将获得的启动子片段依次命名为miR3026PRF1、miR3026PRF2、miR3026PRF3、miR3026PRF4,可用于构建水稻miRNA3026启动子瞬时表达载体。大量质粒DNA的提取纯化、拟南芥叶肉细胞原生质体的制备与转化参照Yoo[15]等的方法。
1.2.5 水稻硫氧还原蛋白基因OsTxnDC9组织表达分析采用Trizol总RNA提取试剂盒分别提取水稻花粉一核、二核、三核,以及根、茎、叶中的总RNA。在Bio-Rad iCycler MyiQ Real-Time PCR Systems平台上对OsTxnDC9基因进行定量表达分析。
1.2.6 水稻硫氧还原蛋白基因OsTxnDC9的亚细胞定位扩增出OsTxnDC9基因正确的ORF,经过SalI和 BamHI进行双酶切连接上GFP,得到OsTxnDC9-GFP荧光定量表达载体,亚细胞定位参照Yoo和Cho[15]的方法。
2 结果分析 2.1 MicroRNA3026启动子的生物信息学分析MicroRNA3026启动子全长1 477bp,经初步分析显示该序列富含AT碱基,比率为55.99%,T含量最高达30.63%,这与启动子高AT含量的特性相符合[14]。利用启动子顺式作用元件预测网站 PLACECARE对miR3026P序列进行启动子的原件分析(表 2),miR3026P序列的正负链上包含54个TATA盒和24个CAAT盒 ,都与启动子增强转录效率有关。另外,在转录起始位点上游约50bp处存在A/T富集区域,并且包括多个TATA盒序列。除此之外,该序列还包含与ABA应答调控有关的ABRE 元件,G-box、TCT-motif及GAG-motif 元件与光反应相关,TGACG-motif元件与茉莉酸甲酯应答相关,P-box元件与赤霉素应答相关,CAT-box元件和CCGTCC-box元件与分生组织的表达相关,GCN4_motif 元件与胚乳表达相关。真核生物mRNA的3′端都有一段多聚A尾巴,这种尾巴不由基因编码,而是在转录后加到mRNA上的。加尾过程被终止密码3′端的加尾信号序列所控制。对in-miRNA3026的3′下游序列进行搜索,发现了两个加尾信号AATAA(图 1)。这意味着in-miRNA3026可能存在自身的转录单元。pre-miRNA3026共有100个核苷酸(图 1阴影部分),成熟的in-miRNA3026有23个核苷酸(图 1红色部分)。
| Site name | Core sequence | Function | Number |
| CAAT-box | TACGTG | common cis-acting element in promoter and enhancer regions | 24 |
| CAT-box | TACGTG | cis-acting regulatory element related to meristem expression | 2 |
| CCGTCC-box | TACGTG | cis-acting regulatory element related to meristem specific activation | 1 |
| CGTCA-motif | TACGTG | cis-acting regulatory element involved in the MeJA-responsiveness | 2 |
| MBS | TACGTG | MYB binding site involved in drought-inducibility | 2 |
| TATA-box | TACGTGATA | core promoter element around -30 of transcription start | 54 |
| TGACG-motif | TACGTG | cis-acting regulatory element involved in the MeJA-responsiveness | 2 |
| TCT-motif | TACGTG | part of a light responsive element | 1 |
| GAG-motif | TACGTG | part of a light responsive element | 1 |
| G-box | TACGTG | cis-acting regulatory element involved in light responsiveness | 9 |
| GCN4_motif | CAAGCCA | cis-regulatory element involved in endosperm expression | 1 |
 |
| 图 1 水稻in-miRNA3026及其近邻上下游序列 Fig. 1 Nucleotide sequences of intronic miR3026 and its upstream and downstream -931~+533bp is the sequence of miR3026P cloned; Single underline: Part of cis elements predicted by PLACE; Box: TATA box predicted by PLACE; The blue word: Predicted transcription start site; The shaded part: pre-miR3026;The red word: Mature miR3026; Wavy lines: Add tail signal |
生物信息学分析表明,水稻硫氧还原蛋白基因OsTxnDC9总长度为8 937bp,包括三个外显子(长度分别为147bp、157bp和176bp)和两个内含子(长度分别为8 376bp和81bp),cDNA长度为480bp,利用基因结构作图网站(http://gsds.cbi.pku.edu.cn/)做出基因的结构图(图 2)。
 |
| 图 2 水稻硫氧还原蛋白OsTxnDC9基因的结构 Fig. 2 Gene structure of OsTxnDC9 |
应用PredictProtein和WoLFPSORT软件预测蛋白质亚细胞定位,PredictProtein软件预测OsTxnDC9基因转录翻译形成的蛋白质定位在液泡膜上;WoLFPSORT(http://wolfpsort.org)软件分析OsTxnDC9基因转录翻译形成的蛋白质定位于质膜、叶绿体、高尔基体或内质网上。综合结果表明,OsTxnDC9基因转录翻译形成的蛋白质可能位于细胞质中。
2.2.3 氨基酸序列比对和进化树分析将水稻OsTxnDC9基因cDNA 序列翻译成氨基酸序列,之后进行氨基酸同源性比对(图 3)。同源性分析结果表明,水稻OsTxnDC9基因编码的氨基酸序列与拟南芥(NP_179489.1)、芜菁(XP_009114388.1)、蓖麻 (XP_002518645.1)、大豆(XP_003536596.1)、甜橙(XP_006486959.1)、胡杨(XP_011001515.1)、茸毛烟草(XP_009599692.1)、马铃薯(XP_006352322.1)的硫氧还原蛋白氨基酸序列的同源性分别为65.07%、63.63%、70.81%、67.49%、70.33%、69.85%、68.35%、67.46%。利用 mega 软件,对 NCBI 数据库中所下载的序列进行进化树分析。结果表明,in-miRNA3026宿主基因编码的氨基酸序列与二穗短柄草基因编码的氨基酸(XP_003573612.1)的同源性最高(图 4),说明水稻和二穗短柄草的亲缘关系最近。
 |
| 图 3 水稻硫氧还原蛋白基因OsTxnDC9氨基酸序列比对 Fig. 3 Alignment of OsTxnDC9 NP_179489.1:Arabidopsis thaliana;XP_009114388.1:Brassica rapa;XP_002518645.1:Ricinus communis; XP_003536596.1:Glycine max; XP_006486959.1:Citrus sinensis;XP_011001515.1:Populus euphratica;XP_009599692.1: Nicotiana tomentosiformis;XP_006352322.1:Solanum tuberosum;LOC_0s08g15204.1:OsTxnDC9 |
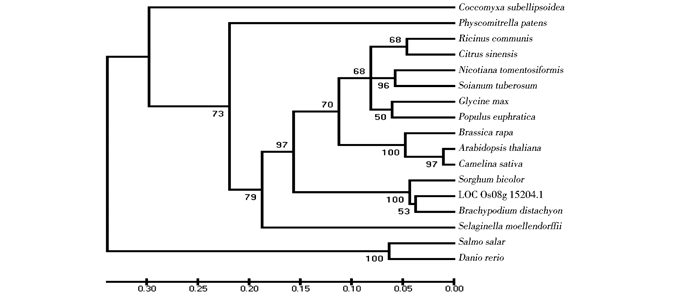 |
| 图 4 水稻硫氧还原蛋白基因OsTxnDC9编码氨基酸序列系统进化树分析 Fig. 4 Phylogenetic analysis of OsTxnDC9 Arabidopsis thaliana:NP_179489.1;Camelia sativa:XP_010489450.1;Brassica rapa:XP_009;Ricinus communis:XP_002518645.1;Glycine max:XP_003536596.1 ;Citrus sinensis:XP_006486959.1;Populus euphratica:XP_011001515.1;Nicotiana tomentosiformis:XP_009599692.1;Solanum tuberosum:XP_006352322.1;Brachypodium distachyon:XP_003573612.1;Sorghum bicolor:XP_002445295.1;Salmo salar:ACI68798.1 |
采用特异引物PCR扩增出OsTxnDC9的开放读码区,结果大约为500bp(图 5),将此条带进行回收、克隆和测序。根据已知的in-miRNA3026的序列设计并合成引物(表 1),以水稻基因组DNA为模板进行扩增,PCR循环为:94℃ 5min,35循环( 98℃ 30s,55℃ 30s,72℃ 90s),72℃ 5 min,得到全长启动子miR3026PRF,结果大约为1 500bp(图 5)。
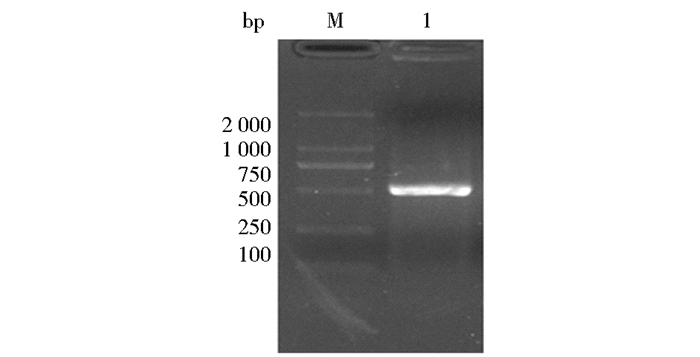 |
| 图 5 PCR扩增水稻硫氧还原蛋白OsTxnDC9基因cDNA序列及全长启动子电泳图 Fig. 5 PCR amplification of OsTxnDC9 and promoter M:DL2000 DNA marker;1: OsTxnDC9;2:miR3026PRF |
本实验回收了水稻花粉中一核、二核、三核中的花粉,采用荧光定量PCR技术分析了根、茎、叶,以及水稻花粉中一核、二核、三核中OsTxnDC9的表达,其中在根、茎、叶中叶片中OsTxnDC9的表达量最高,在花粉中一核OsTxnDC9的表达量最多(图 6)。
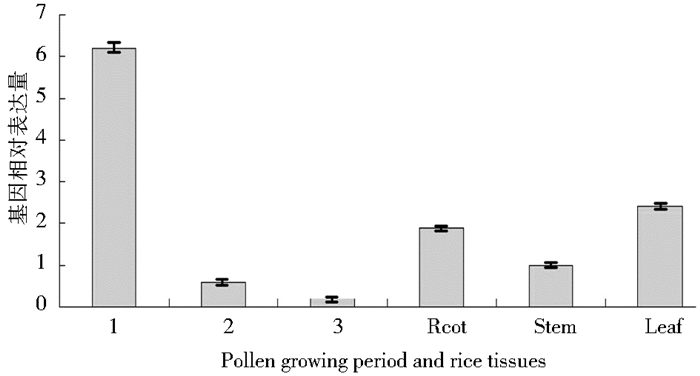 |
| 图 6 水稻硫氧还原蛋白OsTxnDC9基因表达分析 Fig. 6 Expression analysis of OsTxnDC9 1,2,3: Represented uninucleate microspore,bicellular pollen,tricellular pollen |
为了验证OsTxnDC9亚细胞定位的预测结果,构建可瞬时表达OsTxnDC9-GFP的载体,进行亚细胞定位。与对照相比,OsTxnDC9-GFP主要分布在细胞质中,细胞核中并没有检测到较为明显的信号(图 7)。
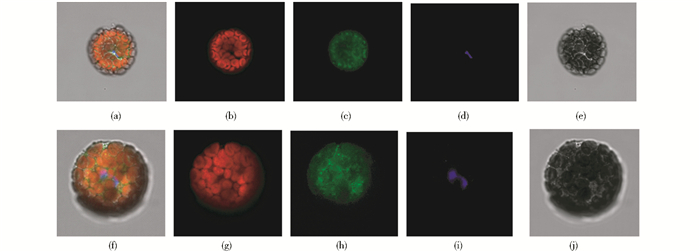 |
| 图 7 OsTxnDC9蛋白的亚细胞定位 Fig. 7 Subcellular localization of OsTxnDC9 protein (a),(b),(c),(d),(e):OsTxnDC9-GFP transient expression;(f),(g),(h),(i),(j):Transient expression of the empty vector |
以水稻花粉DNA为模板作PCR扩增(图 8),将构建好的含有启动子不同缺失片段及全长启动子的植物表达载体转入制备好的原生质体中,培养12~16h后分别检测LUC报告基因活性和GUS报告基因活性。以LUC报告基因活性/GUS报告基因的相对活性代表启动子不同缺失片段的启动活性(图 9),全长的启动子活性大约只有35S启动子活性的1/600,因此,in-miR3026邻近上游序列为弱启动子序列。
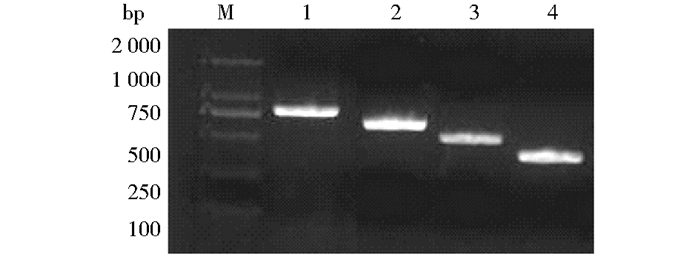 |
| 图 8 PCR扩增不同长度的独立启动子片段的电泳图 Fig. 8 Electropherogram of different PCR products from independent promoters M:DL2000 DNA marker;1:miR3026PRF1;2:miR3026PRF2;3:miR3026PRF3;4:miR3026PRF4 |
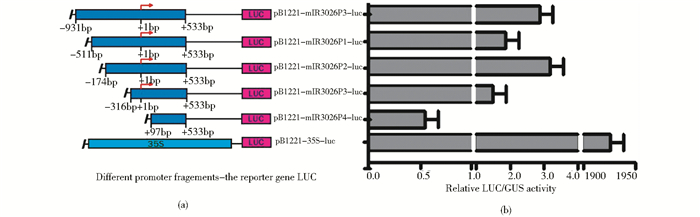 |
| 图 9 含有启动子不同长度片段驱动报告基因luc的植物瞬时表达载体图(a)和不同缺失片段启动子的LUC/GUS相对活性(b) Fig. 9 Diagram of plant expression vectors containing the different promoter segments drived the report gene of luc a) and relative LUC/GUS activity of different promoter segments (b) |
In-miRNA的生物学功能研究得到了迅速的发展,但自身表达调控方面的研究却很少。本实验室在研究miRNA在水稻雄配子体发育过程中的调控作用时,对花粉表达谱芯片和miRNA高通量测序的实验数据进行生物信息学分析,鉴定了93个新的in-miRNA可能存在转录单元。根据in-miRNA3026的序列,克隆其上游序列,生物信息学分析其具有启动子的特性,瞬时表达实验表明该启动子为弱启动子。in-miRNA3026启动子宿主基因为硫氧还原蛋白基因OsTxnDC9,硫氧还原蛋白作为生命体非常重要的蛋白质,广泛存在于植物、动物、微生物中,这类蛋白质拥有许多目的蛋白,也表明了它们有各种各样的功能。在植物中,Trx最初是在叶绿体中发现的,被认为是光合作用中关键酶的活化调节蛋白,之后又在细胞质和线粒体中发现了结构和功能有差异的硫氧还原蛋白[16]。Trx不仅在生物体中的各种各样的反应中起着氧化还原载体[17]的作用,还与植物体的抗性有着密不可分的关系。在麦子中转入外源Trxs基因,不仅能提高大麦的抗氧化酶活性,清除多余的活性氧,还能提高麦子幼苗的耐盐能力[18]。叶绿体中的硫氧还原蛋白参与并调节植物的光合作用[19],在线粒体中,Trx对维持细胞活性和细胞凋亡信号的转导具有重要的调控作用[20]。硫氧还原蛋白在生物工程中具有重要的价值,由于Trx具有催化蛋白质二硫键还原的功能,所以可以帮助蛋白质正确折叠。例如,将hTRX基因扩增连入PkpL24载体中转化大肠杆菌并得到纯化的蛋白质,该蛋白质对鼠内毒素血症有明显的保护作用[21]。Trx能保护内皮细胞和肾脏的缺血再灌注损伤[22]。Trx还具有选择性地激活某些转录因子与DNA的结合,进而激活细胞凋亡的信号[23]。因此研究Trx基因,了解它的种类、功能、特性,为我们更好的利用它解决问题奠定基础。
水稻硫氧还原蛋白基因OsTxnDC9是miRNA3026的宿主基因,本实验表明MiRNA3026启动子为弱启动子。宿主基因硫氧还原蛋白可能参与并且调节水稻的光合作用,并作为氧化还原的载体,与水稻的抗性密不可分。本文为进一步研究水稻MiRNA3026启动子及与宿主基因水稻硫氧还原蛋白基因OsTxnDC9的关系奠定了坚实的基础。
| [1] | Wu C, You C, Li C, et al . RID 1,encoding a Cys2/His2-type zinc finger transcription factor, acts as a master switch from vegetative to floral development in rice. Proc Natl Acad Sci USA,2008,1059(2): 12915-12920. |
| [2] | Li X, Yang Y, Yao J, et al . FLEX IBLE CULM 1 encoding a cinnamyl-alcohol dehydrogenase controlsculm mechanical strength in rice.Plant Mol Biol,2009,69(6): 685-697. |
| [3] | Li X, Qian Q, Fu Z, et al . Control of tillering in rice. Nature, 2003, 422(9): 618-621. |
| [4] | Ren Z, Gao J, Li L, et al . A rice quantitative trait locus for salt to lerance encodes a sodium transporter. Nat Genet, 2005, 37(5): 1141-1146. |
| [5] | Sun X, Cao Y, Yang Z, et al. Xa26,a gene conferring resistance to X anthom on as Oryzae pv. Plant,2004, 37(4): 517-527. |
| [6] | Huang X, Qian Q, Liu Z, et al . Natural variation at the DEP1 locus enhances grain yield in rice. Nat Genet, 2009, 41(7): 494-497. |
| [7] | Heide H, Kalisz H M, Follmann H .The oxygen evolving enhancer protein 1 (OEE) of photosystem Ⅱ in green algae exhibits thioredoxin activity.Plant Physiol,2006,161(2): 139-149. |
| [8] | Laurent T C,Moore E C,Reichard P.Enzymatic synthesis of deoxyribonucleotides .Journal of Biological Chemistry,1964,239(10):3436-3444. |
| [9] | Gelhaye E, Rouhier N,Navrot N,et al.The plant thioredoxin system.Cell Mol,2005,62(1):24-35. |
| [10] | Nishiyama A,Masutani H,Nakamura H,et al.Redox regulation by thioredoxin and thioredoxin binding proteins. Cell Mol,2004, 52 (1): 29-33. |
| [11] | Radfar M H, Wong W, Morris Q. Computational prediction of intronic microRNA targets using host gene expression reveals novel regulatory mechanisms. PLoS One, 2011, 6(6): 193-202. |
| [12] | Laufs P, Peaucelle A, Morin H, et al. MicroRNA regulation of the CUC genes is required for boundary size control in Arabidopsis meristems. Development, 2004, 131(17): 4311-4322. |
| [13] | Jones-Rhoades M W, Bartel D P. Computational identification of plant microRNAs and their targets, including a stress-induced miRNA. Molecular Cell, 2004, 14(6): 787-799. |
| [14] | Sunkar R, Zhu J. Novel and stress-regulated microRNAs and other small RNAs from Arabidopsis. The Plant Cell Online, 2004, 16(8): 2001-2019. |
| [15] | Yoo S D, Cho Y H.Arabidopsis mesophyll protoplasts:a versatile cell system for transient gene expression analysis.Protocol,2007,7(2):1565-1572. |
| [16] | Langhner B J,Sehnke P C,Ferl R J.A novel nuclear member of the thioredoxin superfamily .Plant Physiology,1998,118(9):987-996. |
| [17] | Wong J H,Cai N,Balmer Y,et al.Thioredoxin targets of developing wheat seeds identified by complementary proteomic approaches.Phytochemistry,2004,65(6):1629-1640. |
| [18] | 李巧云,牛洪斌,任江萍,等.转外源Trxs基因大麦耐盐性有关生理生化特性分析.作物,2009,118(5):7-10. Li Q Y,Niu H B,Ren J P,et al.Effects of exogenous Trxs on physiological and biochemical characteristics of salt tolerance in transgenic barley seedlings.Crops,2009,118(5):7-10. |
| [19] | 王玉成, 杨传平, 刘桂丰, 等.紫杆柽柳cDNA文库构建与硫氧还蛋白基因的克隆.分子植物育种,2004, 2(5): 667-673. Wang Y C,Yang C P,Liu G F,et al.Construction of Tamarix androssowii cDNA library and cloning of thioredoxin gene.Molecular Plant Breeding,2004,2(5):667-673. |
| [20] | Tanaka T, Hosoi F, Yamaguchi-Iwai Y, et al. Thioredoxin-2 (TRX-2) is an essential gene regulating mitochondria-dependent apoptosis. Plant Physiology, 2002,21(7): 1695-1703. |
| [21] | 曹丽,黄大无,范慧,等.人硫氧还蛋白在大肠杆茵中的高效表达、 纯化反对内毒素血症小鼠的保护作用.中国生物化学与分子生物学报,2002,18(6):733- 736. Cao L,Huang D W,Fan H,et al.The Expression and purification of human thioredoxin from E.coli and Its protective effects in a mutine model of endotoxemia.Chinese Journal of Biochemistry and Molecular Biology,2002,18(6):733-736. |
| [22] | Shibuki H, Katai N, Kuroiwa S, et al.Protective effect of adult T-cell leukemi-a-derived factor on retinal ischemia-reperfusion injury in the rat. Molecular Cell, 1998,39(8):1470-1477. |
| [23] | Hirota K, Murata M, Sachi Y, et al. Distinct roles of thioredoxin in the cytoplasm and in the nucleus: a two-step mechanism of re-dox regulation of transcription factor NF-κB .Protocol,1999,2(5): 27891-27897. |
 2016, Vol. 36
2016, Vol. 36




