文章信息
- 阮景军, 杨毅, 唐自钟, 陈惠
- RUAN Jing-jun, YANG Yi, TANG Zi-zhong, CHEN Hui
- 基于定点突变技术对苦荞麦胰蛋白酶抑制剂活性位点的研究
- Study on Tartary Buckwheat Trypsin Inhibitor Activity Sites by Using Site-directed Mutagenesis
- 中国生物工程杂志, 2015, 35(12): 30-36
- China Biotechnology, 2015, 35(12): 30-36
- http://dx.doi.org/10.13523/j.cb.20151205
-
文章历史
- 收稿日期: 2015-07-20
- 修回日期: 2015-08-12
2. 武汉生物工程学院 生物科学与技术学院 武汉 430415
2. College of Biological Science and Technology, Wuhan Institute of Biological Engineering, Wuhan 430415, China
目前苦荞在我国西南云贵川红土高原和北方黄土高原等一些高寒、边远、干旱的山区和少数民族聚居地广泛种植,是当地的主要粮食作物和经济作物。四川省凉山彝族自治州拥有最大面积、最集中分布的苦荞麦栽种区域,并且也是苦荞麦的发源地之一[1]。胰蛋白酶抑制(Trypsin inhibitor,TI)在很多种动植物及微生物中都有存在[2]。其中,豆科和乔本科植物在胰蛋白酶抑制剂的研究中充当了重要角色,丝氨酸、半胱氨酸、天冬氨酸、金属蛋白酶抑制剂是组成蛋白酶抑制剂的4大类,其中,胰蛋白酶抑制剂是丝氨酸蛋白酶抑制剂类型(serine proteinase inhibitor,Serpin)[3]。
苦荞麦中含有丰富的胰蛋白酶抑制剂(TI),属于丝氨酸蛋白酶抑制剂类,研究显示,苦荞麦胰蛋白酶抑制剂对于临床新药开发和抗虫转基因作物研究有着实际意义[2]。胰蛋白酶抑制剂在苦荞麦中含量较丰富,如何对其充分利用,以开发抑制肿瘤等新药物或提高药物的功效,提高对苦荞麦蛋白质的利用率非常重要。但是目前对苦荞麦胰蛋白酶抑制剂的研究集中在分离纯化和基因克隆表达方面,对苦荞麦胰蛋白酶抑制剂活性位点的研究极为少见。为探索荞麦胰蛋白酶抑制剂结构与功能之间的关系,找出苦荞麦胰蛋白酶抑制剂的活性关键部位。本实验在前期对苦荞麦胰蛋白酶抑制剂基因的克隆与表达的研究基础上,利用生物信息学软件分析预测苦荞麦胰蛋白酶抑制剂FtTI活性部位所在区域,采用定点突变技术,在区域内选取两个目的突变位点,将该苦荞麦胰蛋白酶抑制剂(FtTI)活性部位的精氨酸和天冬氨酸进行替换,确定其活性部位。为揭示胰蛋白酶抑制剂结构与功能的关系、抗病虫害转基因植物的研究以及抗肿瘤药物的研制奠定基础。
1 材料与方法 1.1 材 料采用当年在四川省凉山州大凉山收获的野生苦荞麦(Fagopyrum tataricum Geonm)种子,在实验室种植后提取的DNA样品作为实验材料。菌株E.coli DH5α,E.coli BL21 (DE3) 和pET-32α (+)载体购自Life Technologies公司,克隆载体pMD19-T Simple(TaKaRa公司)Not I、EcoRI限制性内切酶,定点突变试剂盒TaKaRa MutanBEST Kit,Prime STAR高保真聚合酶(大连TaKaRa公司),引物(上海英潍捷基生物有限公司),质粒抽提纯化试剂盒,PCR产物纯化试剂盒(上海Omega公司),2-氨基-4,5-二甲氧基苯甲酸(L-BApNA) 和N-苯甲酰基-L-精氨酸乙酯盐酸盐(BAEE)(Sigma公司)。
1.2 方 法 1.2.1 PCR扩增FtTI基因取生长15 d的苦荞麦叶片,利用CTAB方法[4]获得基因组DNA,将DNA浓度稀释至50 ng。NCBI上查找FtTI在GenBank注册的登陆号为:KC417045。用苦荞麦基因组DNA作为模板,采用合成全长FtTI基因的带有酶切位点的上游引物R1和下游引物R2扩增FtTI基因,引物如下:
R1:5′-CCGGAATTCCATGTTAATTTACGCTAAAGTT-3′
R2:5′-GAATGCGGCCGCTCAACCGACGGTTGG-3′
取5 μl PCR产物,用1.5%琼脂糖凝胶进行电泳,观察到目的条带大小正确后,采用PCR产物胶回收试剂盒纯化,连接到pMD19-T质粒载体上。
1.2.2 转化大肠杆菌DH5α将连接液(10 μl)加到100 μL DH5α感受态细胞中,冰浴30 min,然后在42℃的水浴中热激90 s,再冰浴5 min。取890 μl的液体LB培养基到上述离心管,放进摇床37℃培养60 min。在Amp抗性的LB平板上培养12 h,观察到有单菌落出现,筛选和鉴定阳性克隆。
1.2.3 提取阳性菌株质粒获得定点突变的模板接种含有FtTI基因质粒的大肠杆菌DH5α于10 ml LB(含100μl/ml Amp抗生素)液体培养基中37 ℃培养12 h~16 h,根据OMEGA公司质粒提取试剂盒操作说明书提取质粒,将提取的质粒溶液储存于-20 ℃冰箱中备用。
1.2.4 苦荞麦胰蛋白酶抑制剂基因的定点突变将FtTI氨基酸序列在UniProtKB/Swiss-Prot和Algorithm blastp (protein-protein BLAST)数据库的17种来源的蛋白酶抑制剂序列进行同源性比对,结果显示,FtTI分子中具有典型的土豆蛋白酶抑制剂Ⅰ保守序列 EWPELVG和CDRVW。据这一家族序列同源性推测 Arg65~Asp67氨基酸残基为FtTI的抑制活性位点[5]。将FtTI分子中第65位Arg和第67位Asp突变为Leu和Val。以含有FtTI基因全序列的克隆载体pMD19-T-FtTI为模板,采用试剂盒定点突变PCR技术对来源于苦荞麦的胰蛋白酶抑制剂FtTI基因进行定点突变。根据FtTI氨基酸序列和目的突变位点,设计3对突变引物(表 1)。采用大连TaKaRa公司的突变试剂盒(TaKaRa MutanBEST Kit),在设计PCR引物时导入突变点,并对PCR产物采取末端平滑化和5′磷酸化,之后采用高效连接试剂自身连接,然后转化、提取突变体DNA,送往上海英潍捷基生物公司测定序列。
| 名称 | 序列信息 |
| aFtTI-R65L | CTTTCTTTGTGACCGGGTGCGTGTTTCGAAAGTGCGGCAGGTGGCTAGAG |
| aFtTI-D67V | CGTTGTGTCCGGGTGCGTGTTTTAAAAAGTGCGGCAGGTGGCTAGAGTGG |
| aFtTI-R65L/ D67V | CTTTCTTTGTGTCCGGGTGCGTGTTTCGAAAGTGCGGCAGGTGGCTAGAG |
测序正确的突变转化子和含有pET-32a (+) 质粒的大肠杆菌DH5α菌株挑取到10 ml的液体LB+Amp液体培养基中,37 ℃,180r/min培养12 h后,提取质粒。将提取的pET-32a(+)和aFtTI的PCR纯化产物分别用EcoR I和Not I限制性内切酶进行双酶切,16℃连接5h后,将连接产物全部加入到DH5α感受态中进行转化,提取质粒进行酶切和测序鉴定。挑取突变后pET-32a(+)-aFtTI/BL21(DE3)和突变前pET-32a(+)-FtTI/BL21(DE3)以及空载体pET-32a(+)/BL21(DE3)的单菌落接种到10 ml的LB+Amp液体培养基中,37 ℃,160 r/min培养12 h。然后转接培养液1 ml到液体 LB+Amp(100μg/ml)的50 ml培养基中,在37 ℃,180 r/min培养到OD600nm=0.8~1.0。加IPTG到终浓度为1 mmol/L,再37℃诱导培养4 h。低温离心收集沉淀菌体,向沉淀中加入磷酸盐缓冲液,洗涤2次,然后重悬于5 ml磷酸盐缓冲液中,用细胞破碎仪进行破碎,随后破碎液以8 000 r/min低温离心20 min。收集上清液进行12 % SDS-PAGE分析,检测表达情况,同时进行镍柱纯化。
1.2.6 表达产物的分离纯化将上清液1 ml置于平衡缓冲液 (pH 7.5,20 mmol/L Tris-HCl,10 mmol/L 咪唑,500 mmol/L NaCl) 充分平衡过的 Ni2+ 亲和层析柱。利用咪唑浓度梯度缓冲液(pH 7.5,20 mmol/L Tris-HCl,50 mmol/L咪唑,100 mmol/L 咪唑,500 mmol/L NaCl)阶段清洗,除去杂蛋白,最后使用洗脱缓冲液(pH 7.5,20 mmol/L Tris-HCl,500 mmol/L NaCl,300mmol/L咪唑) 洗脱目标蛋白。所得蛋白质样品通过考马氏亮蓝法测定其浓度。
1.2.7 胰蛋白酶抑制活性测定以BAEE 3 ml+10 mmol/L HCI 200 μl+待测抑制剂溶液100 μl作空白,取BAEE溶液3 ml与待测液100 μl混匀后,加入胰蛋白酶溶液200 μl,立即计时,迅速混匀后在A253nm,25℃±0.5℃条件下测定吸光值,测定加入抑制剂之后的胰蛋白酶活性。用相同的方法测出没有加胰蛋白酶抑制剂的胰蛋白酶活性A1和加了胰蛋白酶抑制剂的酶活性A2。将A1-A2就可以得到胰蛋白酶抑制剂的抑制活性[6]。
1.2.8 抑制动力学分析配制4.2 mmol/L的BApNA底物溶液 (对0.32 μmol/L的胰蛋白酶足够过量),分别测定各浓度在不同aFtTI浓度 (0,2,4,6,8,10,12 mmol/L)下的剩余胰蛋白酶活性,以抑制摩尔比率为横坐标,以剩余胰蛋白酶活性的百分率为纵坐标作图,曲线的斜率与横坐标的交叉点即为aFtTI的抑制摩尔比率[7]。以BApNA为底物,采用Dixon作图法确定aFtTI的抑制常数。通过添加不同浓度的胰蛋白酶抑制剂(分别为0,1.6,3.3和5.0 nmol/L),两个底物浓度分别为[S1]10.0 mmol/L和[S2]5.0 mmol/L,胰蛋白酶的浓度为0.32 μmol/L。速率的倒数(1/v)对抑制剂浓度[I]作图。两条直线的交点就是aFtTI的抑制常数[8]。每个实验重复3次,各个测定值的差异<5%。每个实验重复3次,各个测定值的差异<5%。
1.2.9 抑制剂稳定性研究pH对抑制剂活性的影响:对aFtTI在pH(2~12)的稳定性进行了检测,样品aFtTI(1 mg/ml)分别在100 ml甘氨酸-盐酸(pH值2~3)、100 ml醋酸钠(pH值4~5)、100 ml磷酸钠(pH值6~7)、100 ml的Tris-盐酸(pH值8~9)和100 ml甘氨酸-氢氧化钠(pH值10~12)缓冲溶液中37℃温浴30 min,在最适反应条件下测定抑制剂的剩余抑制活性[9],以BAEE为底物对样品胰蛋白酶的抑制活性进行测定。
温度对抑制剂活性的影响:对aFtTI热稳定性进行了测试,溶解在缓冲液中的纯化蛋白(1 mg/ml),在不同温度下(10~100℃)温浴30 min。温浴后所有样品均保存在冰上15 min,然后离心,取上清液测定其对胰蛋白酶的抑制活性[10](以BAEE为底物)。
1.2.10 胰蛋白酶抑制剂的三维结构预测分析采用蛋白质三维预测在线网站SWISS-MODEL (http://swissmodel.expasy.org/),并结合swiss-pdbviewer4.10软件对苦荞麦胰蛋白酶抑制剂及其三种突变体进行三级结构预测分析。
1.2.11 统计学处理所有数据均用3次各自独立实验的平均值表示(x±s);组内采用方差进行分析,组间采用t检验。
2 结果与分析 2.1 突变体的基因表达及纯化将原始大肠杆菌表达菌株pET-32a(+)-aFtTI,以及含有突变基因的大肠杆菌表达菌株pET-32a(+)-aFtTI1、pET-32a(+)-aFtTI2、pET-32a(+)-aFtTI3,以及含有pET-32a 空质粒的大肠杆菌表达菌株,在含1 mmol/L IPTG的液体LB中,37 ℃诱导5 h后收集菌液,经过超声波破碎,得到粗酶液。纯化后产物经SDS-PAGE电泳检测为单一条带,其分子质量约为9.5kDa。
苦荞麦FtTI基因的分子有87个氨基酸残基,近似分子量约为9.5kDa。如图 1所示,实验得到的产物与理论相符。

|
| 图 1 纯化的aFtTI SDS-PAGE电泳 Fig. 1 SDS-PAGE of purified aFtTI 1:aFtTI-R65L;2:aFtTI-D67V;3:aFtTI-R65L/ D67V;4:FtTI |
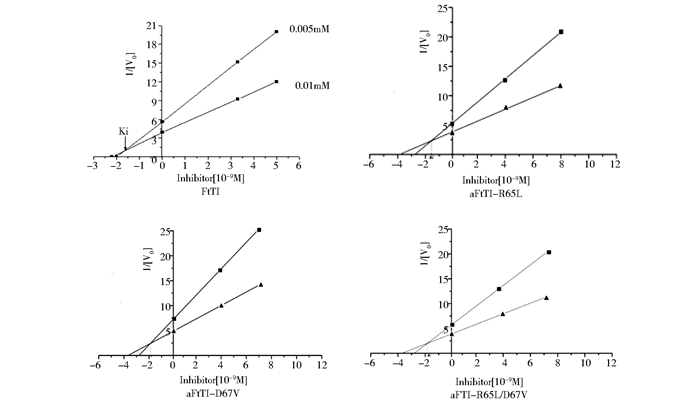
按迪克森作图法,以BApNA为底物,在胰蛋白酶的反应初速度范围内进行FtTI的抑制动力学实验。确定aFtTI和FtTI的特征一致,也是竞争性抑制剂。根据Dixon作图法作图,计算出FtTI及其实变体aFtTI的抑制常数,确定aFtTI和FtTI的特征一致,也是竞争性抑制剂(图 2)。
|
| 图 2 FtTI的抑制活性动力学分析 Fig. 2 Kinetic analysis of trypsin inhibitory activity of FtTI Dixon plot for the determination of the dissociation constant (Ki) value of FtTI at two different concentration of BApNA. Final concentrations of substrate were 0.01 mol/L (■) and 0.005 mol/L (▲).The reciprocals of velocity were plotted against different concentrations of FtTI |
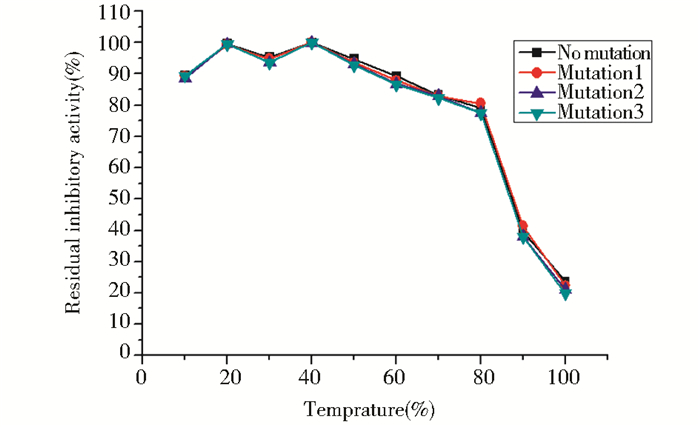
测定不同温度下aFtTI对胰蛋白酶的抑制作用,结果如图 3所示,在10~80 ℃保温30 min后,aFtTI对胰蛋白酶的抑制活性仍保留80 %以上,在90 ℃保温30 min,aFtTI的抑制活性开始显著下降,只保留其抑制活性的39 %左右。因此,aFtTI的耐热性比较高。表明突变后的胰蛋白酶抑制剂,仍然保留了耐热性较高的优点,这对于该抑制剂的应用和继续深入研究有着积极的意义。
|
| 图 3 FtTI的温度 Fig. 3 Temperature of FtTI |
|
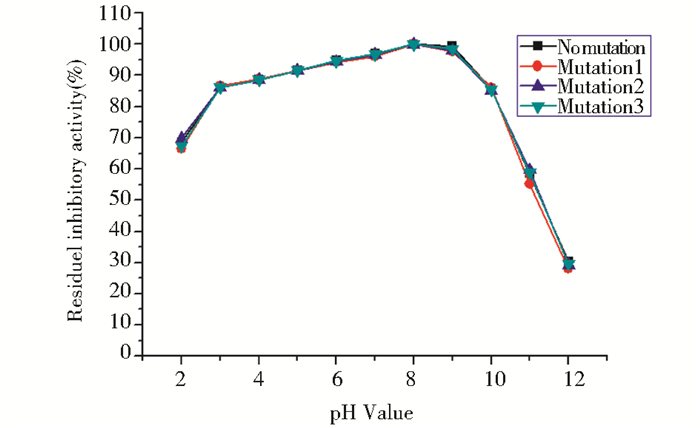
| 图 4 FtTI的pH稳定性 Fig. 4 The pH stability of FtTI |
当aFtTI在pH 3.0~10.0的不同缓冲溶液中放置30 min后,其抑制活性可保留90 %以上;在pH 2.0条件下,aFtTI抑制活性丧失约31 %;在pH 11.0条件下,aFtTI抑制活性丧失约43 %;在pH 12.0条件下,aFtTI抑制活性丧失约70 %。表明aFtTI对强酸和强碱都相对稳定。在pH 8.0左右,aFtTI抑制活性最大,表明苦荞麦蛋白酶抑制剂很可能是一种偏碱性的蛋白酶抑制剂。
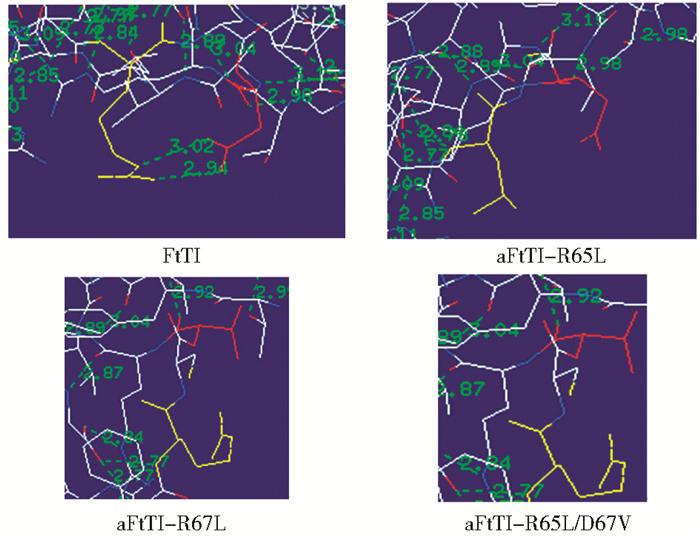
2.4 胰蛋白酶抑制剂三维结构分析三种突变菌株表达的胰蛋白酶抑制剂三维结构与原始结构总体上一致。三个突变蛋白虽然改变了基因中的个别氨基酸组成,但其结果并没有改变蛋白构象形成的中心骨架。以下是局部三维结构分析图:(白色表示C原子,红色表示O原子,蓝色表示N原子) 由图 5可知,突变前位于65位的精氨酸和67位的天冬氨酸之间有两个氢键相互连接。如图 5所示,突变前,位于65位的精氨酸和67位的天冬氨酸之间有两个氢键相互连接;在突变后的65位氨基酸和67位氨基酸之间侧链裸露,没有氢键相互连接,导致该活性区域的稳定性降低,而使得该抑制剂与底物竞争酶分子上的结合位点时竞争性减弱,因而抑制活性降低。
|
| 图 5 FtTI、aFtTI-R65L、aFtTI-D67V和 aFtTI-R65L/ D67V的三维结构图 Fig. 5 Three-dimensional structure of FtTI, aFtTI-R65L, aFtTI-D67V and aFtTI-R65L/ D67V Yellow marked structure is the location of the 65th amino acids and red marked structure is the location of the 67th amino acids |
体外定点突变技术是通过聚合酶链式反应(PCR)等方法对某个已知基因的特定碱基进行定点改变、缺失或者插入(通常是朝着有利方向的变化)。它是研究蛋白质结构与功能之间复杂关系的有力工具,也是实验中改造和优化基因的常用手段[11]。对某个已知基因的特定碱基进行定点突变,可以改变其对应的氨基酸序列和蛋白质的高级结构,对突变基因的表达产物进行研究,对于人们了解蛋白质结构与功能的关系,深入研究和探讨蛋白质相互作用的可能位点、酶的活性或动力学特性等方面具有重要意义[12]。为了使苦荞麦胰蛋白酶抑制剂基因与pET-32α (+)表达载体能够顺利连接,在设计引物时分别在上游引物和下游引物中引入了EcoR I和Not I这两个酶切位点。将酶切得到的载体片段与FtTI和aFtTI基因片段连接,构建了大肠杆菌表达质粒:pET-32a(+)-aFtTI、pET-32a(+)-aFtTI1、pET-32a(+)-aFtTI2和pET-32a(+)-aFtTI3。本实验选取大肠杆菌原核表达系统pET系列载体中的pET-32a (+)作为实验载体,它无论是在操作方面还是在遗传背景方面,都比真核表达载体的相对要简单;同时,该系统只有6个氨基酸大小的6×His标签,这对于目的蛋白的结构与功能的影响比较小[13]。本研究根据同源性比较和理论预测确定 Arg65和Asp67可能为FtTI 的活性位点,采用定点突变技术对其中的一个或两个氨基酸残基进行替换,分别得到 aFtTI-R65L、aFtTI-R67L 和 aFt-TI-R65L/ D67V 3种突变体。
按迪克森作图法,以BApNA为底物,在胰蛋白酶的反应初速度范围内进行FtTI的抑制动力学实验,确定aFtTI和FtTI的特征一致,也是竞争性抑制剂。胰蛋白酶抑制剂在突变后的抑制活性较突变前有所降低,证明了Arg残基和Asp残基是FtTI的活性位点,在FtTI发挥胰蛋白酶抑制作用时起关键作用。
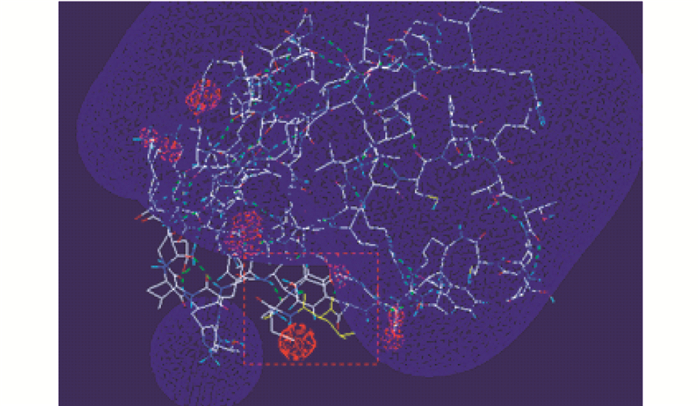
利用在线网站NCBI和SWISS-MODEL (http://swissmodel.expasy.org/),以及swiss-pdbviewer 4.10软件分析推测苦荞麦胰蛋白酶抑制剂FtTI活性部位,三维结构预测如图 6所示(图中用红色虚线方框标示区域,其中用黄色标示出选择突变的位点所在部位):苦荞麦胰蛋白酶抑制剂空间结构形成一个凹陷区,推测此区域为抑制剂的活性部位,在胰蛋白酶催化胰蛋白水解的反应中,该活性部位与胰蛋白酶的催化区域结合点靠近,与底物竞争酶的活性中心,而使底物无法与酶的催化活性部位靠近并结合,减少了底物被催化水解的机会,导致反应速度降低,催化反应受到抑制[14]。
|
| 图 6 FtTI三维结构图 Fig. 6 Three-dimensional structure of FtTI Red indicates the electrostatic potential energy is negative, and blue indicates the electrostatic potential energy is positive, forming depressions |
将极性氨基酸精氨酸和天冬氨酸突变成非极性氨基酸亮氨酸和缬氨酸之后,电荷发生变化,对抑制剂的等电点以及空间位阻产生一定影响,同时抑制剂总的带电荷量减少引起氨基酸之间相互作用改变,当抑制剂与酶靠近时亲和力减弱,表现出苦荞麦胰蛋白酶抑制剂的抑制活性降低[15]。实验预测苦荞麦胰蛋白酶抑制剂的活性部位在此区域,突变此部位的氨基酸位点后,抑制剂活性较突变之前降低,表明此部位在抑制作用中是反应的关键部位,实验预测在此得到了验证。
| [1] | Zhang Y, Chen S, Xu M, et al. Characterization of Thermobifida fusca cutinase-carbohydrate-binding module fusion proteins and their potential application in bioscouring. Appl Environ Microb, 2010, 76(20):6870-6876. |
| [2] | Ruan J, Yan J, Hou S, et al. Expression and purification of the trypsin inhibitor from tartary buckwheat in Pichia pastoris and its novel toxic effect on Mamestra brassicae larvae. Mol Biol Rep, 2015, 42:209-216. |
| [4] | Zeng X C, Liu Y, Shi W, et al. Genome-wide search and comparative genomic analysis of the trypsin inhibitor-like cysteine-rich domain-containing peptides. Peptides, 2014, 53:106-114. |
| [5] | Ruan J J, Chen H, Shao J R, et al. An antifungal peptide from Fagopyrum tataricum seeds. Peptides, 2011, 32(6):1151-1158. |
| [6] | Oddepally R, Sriram G, Guruprasad L. Purification and characterization of a stable Kunitz trypsin inhibitor from Trigonella foenum-graecum (fenugreek) seeds. Phytochemistry, 2013, 96:26-36. |
| [7] | Mukherjee A K, Mackessy S P, Dutta S. Characterization of a Kunitz-type protease inhibitor peptide (Rusvikunin) purified from Daboia russelii russelii venom. Int J Biol Macromol, 2014, 67:154-162. |
| [8] | Cruz A C, Massena F S, Migliolo L, et al. Bioinsecticidal activity of a novel Kunitz trypsin inhibitor from Catanduva (Piptadenia moniliformis) seeds. Plant Physiol Bioch, 2013, 70:61-68. |
| [9] | Guimarães L C, de Oliveira C F R, Marangoni S, et al. Purification and characterization of a Kunitz inhibitor from Poincianella pyramidalis with insecticide activity against the Mediterranean flour moth. Pestic Biochem Phys, 2015, 118:1-9. |
| [10] | Jamal F, Pandey P K, Singh D, et al. A Kunitz-type serine protease inhibitor from Butea monosperma seed and its influence on developmental physiology of Helicoverpa armigera. Process Biochem, 2015, 50:311-316. |
| [11] | Xie Z W, Luo M J, Xu W F, et al. Two reactive site locations and structure-function study of the arrowhead proteinase inhibitors, A and B, using mutagenesis. Biochemistry, 1997, 36(19):5846-5852. |
| [12] | Qi R F, Song Z W, Chi C W. Structural features and molecular evolution of bowman-birk protease inhibitors and their potential application. Acta Bioch Bioph Sin, 2005, 37(5):283-292. |
| [13] | 张继明,杨春,何永林,等.结核分枝杆菌Zmp1基因原核表达载体的构建及表达鉴定.细胞与分子免疫学杂志,2014, 6:573-575. Zhang J M, Yang C, He Y L, et al. Construction and identification of a prokaryotic expression vector for Zmpl gene from Mycobacterium tuberculosis. Chin J Cell Mol Immuno1, 2014, 6:573-575. |
| [14] | Orašem P, Štajner N, Bohanec B. Effect of X-ray irradiation on olive shoot culture evaluated by morphological measurements, nuclear DNA content and SSR and AFLP markers. Trees, 2013, 27(6):1587-1595. |
| [15] | 田欣,李晨,李玉英,等.野生型和突变型荞麦蛋白酶抑制剂的活性比较及抗肿瘤功能分析.生物化学与生物物理进展,2010, 6:654-661. Tian X, Li C, Li Y Y, et al. Analysis of inhibitory activity and antineoplastic effect of wild type rBTI and its mutants. Prog Biochem Biophys, 2010, 6:654-661. |
 2015, Vol. 35
2015, Vol. 35




