文章信息
- 申冬玲, 尚淑梅, 李卫娜, 严金平, 伊日布斯
- SHEN Dong-ling, SHANG Shu-mei, LI Wei-na, YAN Jin-ping, HANGAN Ir-bis
- ack基因敲除对Thermoanaerobacterium calidifontis Rx1发酵代谢的影响
- Characterization of the Disrupted ack Genes on Fermentation by Thermoanaerobacterium calidifontis Rx1
- 中国生物工程杂志, 2015, 35(7): 37-44
- China Biotechnology, 2015, 35(7): 37-44
- http://dx.doi.org/10.13523/j.cb.20150706
-
文章历史
- 收稿日期:2015-02-26
- 修回日期:2015-04-15
2. 长江师范学院生命科学与技术学院 重庆 408100
2. Life Science and Technology Institute, Yangtze Normal University, Chongqing 408100, China
木质纤维素是地球上最丰富的生物乙醇生物原料,世界各国争相开发以木质纤维素为原料的生物乙醇生产技术[1, 2]。但是Saccharomyces cerevisiae、Zymomonas mobilis等传统乙醇生产菌种不能合成纤维素和半纤维素降解酶,而且也不能有效利用来源于半纤维素组分的木糖等戊糖[3, 4]。与这些传统乙醇菌株相比,有些高温厌氧菌的底物利用范围广,不仅可以合成多糖水解酶,还可以代谢来源于木质纤维素的五碳糖和六碳糖发酵生产乙醇[5]。因其具有可将传统乙醇发酵工艺中的酶生产、糖化和乙醇发酵等过程高度统合完成的潜在优势,从而被视为是构建统合生物工艺(consolidated bioprocessing,CBP)的理想微生物[6]。
目前提高高温厌氧菌乙醇产量的主要策略是采用敲除旁路代谢的关键酶基因乳酸脱氢酶基因(ldh)和磷酸乙酰转移酶 (pta)基因的工程手段。Desai等[7]于2004年首次成功敲除了嗜热厌氧解糖杆菌(Thermoanaerobacterium saccharolyticum)的乳酸脱氢酶基因(ldh),他们在 2008年完成了同一菌株的ldh基因和pta基因的连续敲除工作,成功的阻断了乳酸和乙酸的生成途径,获得的突变菌株 ALK2在7%木糖培养基(55℃)中连续培养时,最高乙醇浓度达到33g/L,乙醇得率为 0.46g/g木糖[8]。Taylor等[9]以一种高乙醇耐受性的兼性厌氧高温菌热葡糖苷酶地芽孢杆菌(Geobacillus thermoglucosidasius)为出发菌株,在敲除ldh基因的同时上调表达丙酮酸脱氢酶基因(pdh),加快了丙酮酸代谢速率,获得了乙醇得率为0.42g/g葡萄糖的突变株。而Yao和Mikkelsen[10]在Thermoanaerobacter mathranii中敲除ldh基因的同时过量表达了乙醇脱氢酶基因adhE,突变株的乙醇产量提高了 10%~13%。华南理工大学的研究组[11]也通过敲除嗜热厌氧杆菌Thermoanaerobacterium aotearoense的乳酸脱氢酶基因,提高了突变株的氢气和乙醇产量。但是,高温厌氧菌工程菌株的乙醇产量还是远达不到传统发酵菌的水平。而微生物细胞拥有可调节的高度耦合的代谢网络,能对外界影响做出相应的调节和适应[12],选择某一个或数个基因进行过量表达或敲除,必然会对突变株的生长和代谢等生命活动带来一系列的影响,这也往往是代谢途径改造达不到预期目的的主要原因[12, 13],因此为了进一步提高高温厌氧菌代谢工程菌株的乙醇产量,达到商业化生产的要求,需要系统研究相关基因的敲除对其细胞的生长和代谢造成的影响。
本实验室筛选的高温厌氧菌T. calidifontis Rx1是革兰氏阳性严格厌氧芽孢杆菌,不仅能利用葡萄糖等己糖发酵产乙醇,还能利用木糖,乙醇产率最高能达到理论产值的81%[14]。乳酸和乙酸是其生产乙醇中的主要副产物,不仅与乙醇生成途径争夺碳源和还原力,而且有机酸的积累对细胞的生长具有很强的抑制作用。通过同源重组插入失活的方式,成功敲除了合成乙酸的基因(ack),获得乙酸产量大幅度减少的△ack突变菌株,利用该突变菌株对4种不同的底物进行发酵,研究其生长和代谢特性,为进一步的代谢工程改造提供理论依据。
1 材料与方法 1.1 菌种与质粒高温厌氧温泉菌Rx1 (Thermoanaerobacterium calidifontis Rx1),本实验室分离保存[14]。质粒pMD-19 T Simple Vector、pBluescript II SK (-)购自宝生物(上海)生物工程有限公司。pUC18-HTK购自日本Riken DNA Bank公司,所携带的热稳定性卡那霉素抗性基因来自pUB110质粒[15]。
1.2 培养基、培养条件及试剂 1.2.1 培养基MM640培养基:主要成分参照文献[16]。
发酵培养基:不加维生素的MM640培养基,碳源分别为10g/L的葡萄糖、木糖、纤维二糖。
玉米芯水解液发酵培养基:酵母膏3g/L,蛋白胨4g/L,玉米芯水解液为碳源(按木糖浓度计算),不加维生素,其他成分含量及其具体配制方法同MM640培养基。
1.2.2 玉米芯预处理玉米芯采自云南省昆明市,自然晾干。75℃烘箱烘干,粉碎机粉碎后用目筛筛选,选择18~40目玉米芯在75℃烘箱烘至衡重,放入干燥器中冷却待用。
响应面法优化出玉米芯酸处理的最优条件: 0.73% H2SO4溶液按固液比1∶10加入到含有50g玉米芯的三角瓶中,高压蒸汽灭菌锅124℃处理1h,布氏漏斗过滤分开固相和液相,固相用100ml蒸馏水洗涤两次,洗涤液和液相混合后作为玉米水解液,并用HPLC测定其糖类、乙酸的含量。
1.2.3 培养条件将活化的Rx1接种到100ml含有50ml发酵培养液的厌氧瓶中,55℃培养,定期取样。
1.2.4 主要试剂限制性内切核酸酶PstⅠ、 XbaⅠ、 SacⅠ、 XhoⅠ、Hind Ⅲ 购自美国Fermentas公司;pfu高保真酶、Taq聚合酶、dNTP购自北京全式金生物技术有限公司;胶回收和质粒DNA小量提取试剂盒购自北京百泰克生物技术有限公司。
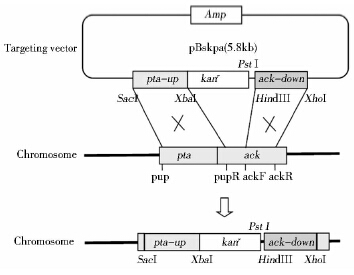
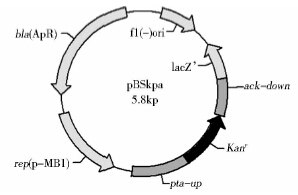
1.3 基因克隆与质粒构建本研究采取了敲除ack基因达到阻断乙酸合成途径的策略。对T. calidiforntis Rx1全基因组测序结果(未公布)进行分析发现该菌乙酸合成途径的磷酸转乙酰酶(pta)和乙酸激酶(ack)的基因是相邻的,利用同源重组的原理将卡那霉素抗性基因(kanr)片段插入其pta/ack中间使其失活(图 1),以kanr作为正筛选标记获得突变菌株。首先利用引物kmF-kmR(表 1)从质粒pUC18-HTK中扩增获得卡那霉素抗性基因(1 081bp),克隆到pBluescript II SK (-)质粒的多克隆位点PstⅠ、 XbaⅠ之间,得到中间载体pBS-HTK。然后如图 2所示,以Rx1的染色体为模板,用引物对pupF-pupR和adnF-adnR(表 1)分别扩增pta/ack的上游片段pta-up(1 223bp)和下游片段ack-down(496bp)作为同源重组的同源臂,连接到pBS-HTK中kanr片段的上游和下游[17, 18],构建重组质粒pBSkpa。
|
| 图 1 基因敲除的原理图 Fig. 1 Schematic diagram of the knockout strategy for the ack gene |
| Primer name | Sequence 5′ to 3′ | Size(bp) |
| kmF | 5′GCTCTAGAGGTACCCGTTGACGGC 3′ | 24 |
| kmR | 5′CTGCAGCTGCAGCGTAACCAACATG 3′ | 25 |
| pupF: | 5′CGAGCTCCGAGGACATTAAAGGCTG 3′ | 25 |
| pupR: | 5′GCTCTAGACTCCTCCATGAACAACTC 3′ | 26 |
| adnF: | 5′CCCAAGCTTGCCAGCAAATTATGCCAA 3′ | 27 |
| adnR: | 5′CCGCTCGAGGCTCTTCCATCTCCAT 3′ | 24 |
|
| 图 2 重组质粒pBSkpa简图 Fig. 2 Sketch diagram of the recombinant vector |
根据Mait Wiegel[19]、Tripathi等[20]的报道,采用电转化方法将重组质粒PBSkpa转入Rx1细胞。电转化条件:电压1 250V,电阻400Ω,电容25uF,电脉冲4~8ms。厌氧罐中培养3~5d后挑取单菌落到新的平板上划线,待长出菌斑后挑取细胞到2ml卡那霉素为50μg/ml的MM640培养基中,24~36h后进行PCR扩增检测和测序验证[21]。
1.5 分析方法 1.5.1 细胞干重的测定取不同培养时间的培养液,用分光光度计[UV-4802,尤尼柯(上海)仪器有限公司]于600nm处测其吸光值。通过校正曲线计算其细胞干重,DCW(g/L)=0.5×A600-0.06(R2=0.996 6)。
1.5.2 残糖及发酵代谢产物分析残糖和发酵产物分析运用高效液相色谱仪(AT-20,岛津日本)进行分析。检测器为RID-10A型示差折光检测器;色谱柱为Aminex HPX-87H column(300×7.8mm)(Bio-RAD);流动相:5mmol/L H2SO4;流速: 0.6ml/min;柱温: 55℃。所有实验都设3个重复。
1.6 发酵参数定义C回收率(%)=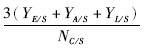
YE/S、YA/S、YL/S分别为乙醇、乙酸、乳酸的得率,葡萄糖和木糖的NC/S分别为6、5。
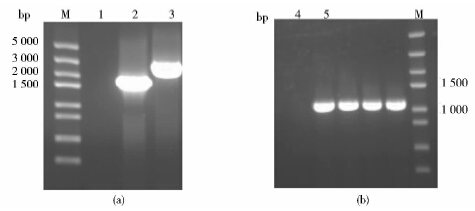
2 结果与分析 2.1 T.calidiforntis Rx1 Δack突变菌株的构建在含有50μg/ml卡那霉素的MM640培养基上挑选转化子,分别以野生型菌株和转化子的染色体DNA为模板,用pupF-adnR为引物进行PCR扩增pta-up-kanr-ack-down片段,电泳检测PCR扩增片段大小,结果如图 3(a)所示:野生型菌株获得1 830bp的片段,而转化子扩增到2.8kb的片段,说明卡那霉素抗性基因通过同源重组插入到pta、ack基因之间,使其PCR产物的长度增加了近1kb;为了进一步确认基因组中存在卡那霉素抗性基因,以kmF-kmR为引物,再进行PCR扩增kanr片段,野生型菌株扩增不出任何片段,而重组菌株出现1 081bp的片段[图 3(b)],对扩增片段的测序结果也证明卡那霉素抗性基因插入到同源臂之间。
|
| 图 3 Δack突变转化子的PCR鉴定电泳图 Fig. 3 Identification of Δack mutants by PCR (a) Primer pupF-adnR 1: ddH2O PCR product; 2: Wild type PCR product; 3: Mutant type PCR product; M: Marker (b) Primer kmF-kmR 4: Wild type PCR product; 5: Mutant type PCR product; M: Marker |
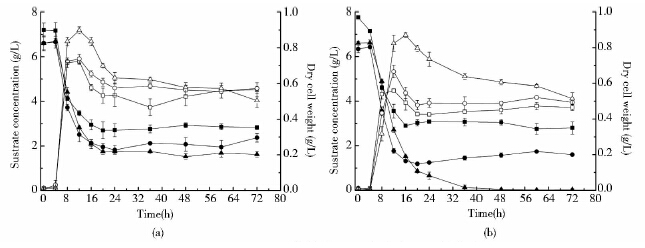
T.calidiforntis Rx1的乙酸合成基因(ack)敲除后,突变菌株Δack对不同碳源的利用和生长情况如图 4所示。由图 4中可以看出,野生菌株和突变菌株在24h左右停止利用底物(突变菌株对纤维二糖的利用在36h左右停止),此时野生菌株的葡萄糖、木糖和纤维二糖的利用率分别为0.187g/(L·h)、0.199g/(L·h)、0.202g/(L·h),突变菌株对3种糖的利用率均高于野生菌株,分别为0.195g/(L·h)、0.212g/(L·h)、0.248g/(L·h)。培养72h后,与野生菌株相比,突变菌株的底物消耗量增加,葡萄糖、木糖、纤维二糖的消耗量分别为5.00g/L、5.24g/L、6.60g/L,高出野生菌株11.14%、27.41%、8.49%。虽然突变菌株的底物利用率和消耗量都增高,但突变菌株的生长速率却相对减缓。在4~8h细胞旺盛生长,野生菌株的生长速率为0.174g/(L·h)、0.173g/(L·h)、0.206g/(L·h),而突变菌株的生达速率为0.132g/(L·h)、0.107g/(L·h)、0.078 7g/(L·h)。以葡萄糖为单一底物时,野生菌和突变菌株分别在第10h、12h达到最大生物量,干重为0.73g/L和 0.59g/L; 以木糖为唯一碳源时,突变菌株的干重最大值为0.67g/L,低于野生菌株的0.74g/L;以纤维二糖为底物时,细胞需要先把纤维二糖分解为葡萄糖后才能利用,所以生长相对缓慢,野生菌株12h达到最大值0.90g/L,突变菌株16h最大为0.87g/L,且是3种底物中最高的。T.calidiforntis Rx1敲除ack基因后,菌株的生长速率会减慢,但底物利用率增高。
|
| 图 4 野生菌株和突变菌株在不同底物中的生长曲线 Fig. 4 Substrate concentrations and growth curves for wild-type and mutant-type on glucose,xylose and cellobiose (a) Wild-type (b) Mutant-type Glucose concentration (■); Cellobiose concentration (▲); Xylose concentration(●); Growth curve on glucose(□); Growth curve on cellobose(△); Growth curve on xylose(○) |
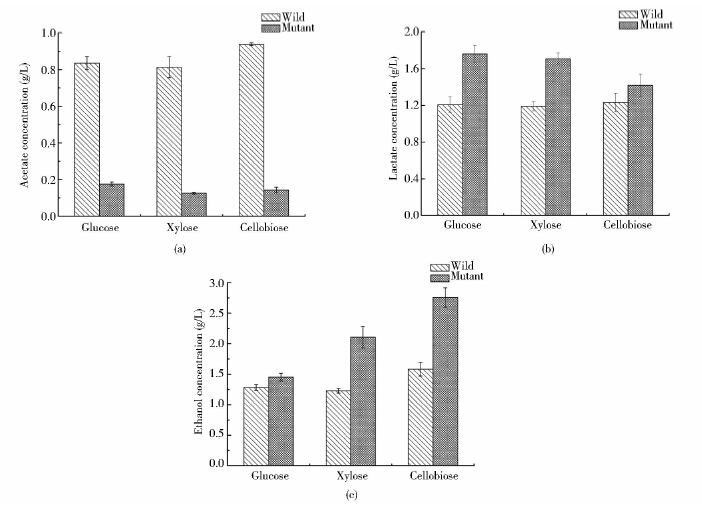
野生菌株和突变菌株以葡萄糖、木糖和纤维二糖为碳源培养24h的代谢产物乙酸、乳酸和乙醇的产量如图 5所示。从图 5(a)中可以看出在3种底物中,突变菌株的乙酸代谢受到抑制,分别为野生菌株的21.07%、15.46%、15.29%。图 5(b)、(c)的结果显示,ack基因敲除后,乳酸和乙醇的产量有不同程度的提高。以葡萄糖为底物培养结束时,野生菌的代谢产物乳酸和乙醇的最大产量分别为1.32g/L、1.37g/L,转化率分别为29.14%、30.39%;相比之下,突变菌株的乳酸的产量为1.74g/L,高野生菌株31.82%,乙醇的产量为1.45g/L,与野生菌株差异不显著,而且转化率为29.02%,反而稍低于野生菌株。当以木糖为底物时,野生菌株的乳酸、乙醇分别为1.22g/L、1.44g/L,转化率分别为25.31%、29.74%;△ack突变菌株的乳酸和乙醇的产量为1.65g/L、2.27g/L,分别提高了35.25% 和57.64%。以纤维二糖为底物时,野生菌株的产物乳酸、乙醇含量分别为1.34g/L、1.70g/L,转化率分别为25.46%、32.87%;突变菌株的发酵液中乳酸的含量为1.46g/L,与野生菌株相比没有显著地提高,而乙醇的浓度为3.60g/L,比野生菌株提高了1.1倍,转化率也增高了21.66%。
|
| 图 5 不同底物发酵24h代谢产物分析 Fig. 5 End products of T. calidiforntis Rx1 wild type and Δack mutant on different substrate at 24h |
T. calidiforntis Rx1既能利用己糖又能利用戊糖发酵生产乙醇,而且乙醇产量相当[图 5(c)]。玉米芯是一种半纤维素含量较高的农业废弃物,利用Saccharomyces cerevisiaedeng进行乙醇生产是对原料的浪费,而且可在相对温和的条件进行玉米芯的预处理,因此将半纤维素水解,用于生物乙醇生产具重要的应用价值。实验中采用0.73%硫酸,124℃水解玉米芯1h,产物浓度如表 2所示,水解液中木糖含量为24.70g/L,得率为32.11g/100g玉米芯。通过稀释调整玉米芯水解液中的木糖含量至10g/L,配制玉米芯水解液发酵培养基,研究突变菌株和野生菌株对玉米芯水解液的发酵情况。
| Corncob hydrolysate | Xylose | Gluccose | Cellobose | Acetate | Lactate |
| Concentration(g/L) | 24.70 | 2.77 | 0.64 | 2.44 | 0.33 |
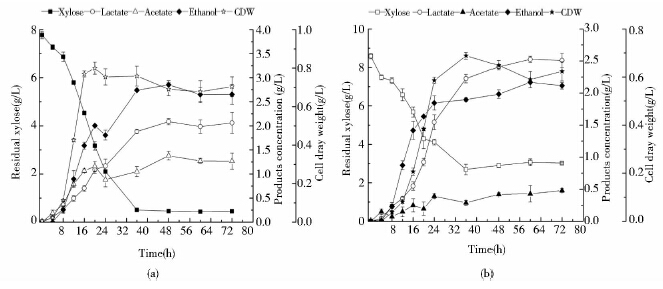
如图 6(a)所示,野生菌株前8h生长缓慢,直到20h细胞干重才达到最大值0.80g/L,这可能是玉米芯液预处理过程中产生了抑制菌株生长代谢的物质所致,玉米芯水解后除了主要产物木糖外,还含有少量的葡萄糖、纤维二糖、阿拉伯糖,以及乙酸、糠醛和5-羟甲基糠醛等产物。发酵72h后野生菌乳酸、乙酸、乙醇的产量分别为2.09g/L、1.38g/L、2.85g/L,转化率分别为28.40%、18.81%、38.82%,与木糖为单一碳源发酵相比,各产物均有明显地提高,而且转化率也增加,这可能是由于玉米芯水解酸处理过程中产生的葡萄糖和阿拉伯糖等其他单糖作为碳源被利用。另外,酸水解过程中产生的乙酸能提高菌株产量的浓度。尚淑梅等[22]研究了外源乙酸对T. calidiforntis Rx1发酵的影响,发现外源乙酸的加入提高了T. calidiforntis Rx1乙醇、乳酸的产量。He等[23]的研究也发现外源乙酸的加入既促进了Thermoanaerobacter ethanolicus细胞的生长和底物的利用率,也提高了乙醇产量。突变菌株发酵玉米芯水解液,与木糖发酵相比,乙酸的产量有所提高,为0.48g/L,但仍远低于野生菌株的发酵产物;乳酸、乙醇的产量为2.53g/L、2.17g/L,转化率为42.90%、36.83%,与野生菌株相比乙醇产量降低,乳酸产量提高;但是与野生菌株发酵单一木糖相比,乳酸、乙醇产量是增高的,与突变菌株发酵单一木糖相比,只有乳酸产量有了很明显的升高,且乙醇产量略有降低。以玉米芯水解液发酵,水解液中的乙酸促进了野生菌株乳酸、乙醇的产量,且ack基因敲除后的乳酸产量仍有显著地升高。
|
| 图 6 以玉米芯水解液为碳源时野生菌(a)、△ack突变菌株(b)的代谢产物分析 Fig. 6 End ptoducts of T. calidiforntis wild type(a) and △ack mutant(b)by corncob hydrolysate |
近年来,嗜热厌氧菌的末端终产物代谢工程研究已经引起了国内外研究工作者的极大关注,但是当前嗜热厌氧菌基因操作体系不够完善,滞缓了其在生物乙醇工业化中的应用,主要的瓶颈在于没有合适的耐热稳定的筛选标记来构建合适的打靶载体。已经报道的耐热稳定标记主要有卡那抗性基因、红霉素抗性基因和氯霉素抗性基因,而且一般在筛选时要降低温度才能筛选到较多的转化子[6, 7, 8, 9, 10, 15, 24]。本实验使用卡那抗性基因作为筛选标记,筛选时在48℃进行,低于T. calidiforntis Rx1的最适生长温度55℃。
乙酸是高温厌氧菌发酵产乙醇的主要副产物之一,敲除乳酸和乙酸代谢合成途径是当前常见的提高乙醇转化率的策略。本研究中敲除T. calidiforntis Rx1的ack基因后,当以单一底物发酵时,与野生菌株相比,突变菌株的生长速率和最大生物量都降低,这种现象在高温厌氧菌的ldh和pta/ack基因敲除工程菌中普遍存在[18, 21];但是突变菌株的碳源消耗量却增加,这可能是因为T. calidiforntis Rx1产乙酸的过程是伴随着三磷酸腺苷(ATP)的产生,△ack突变菌株因乙酸代谢途径受阻,使细胞内的ATP合成量降低,细胞的生长受到抑制,因此细胞需要更多的碳源通过EMP途径合成足够的ATP满足菌株的生命活动需要,各底物的消耗量分别增加了11.14%、27.41%、8.49%。发酵不同碳源,菌株的乳酸、乙酸、乙醇的得率如表 3所示。从表 3中可以看出,当发酵单一底物时,突变菌株的乙醇产量在3种产物中的比例都高于野生菌株;而C的回收率高于100%可能是因为培养基中除了碳源的还有酵母提取物和蛋白胨的存在。除以纤维二糖为底物外,突变菌株的乳酸得率都高于野生菌株的;乙醇的得率是在以纤维二糖、木糖为底物时高于野生菌株的,而且以纤维二糖为底物时突变菌株的乙醇产量和得率都有显著地增加。以玉米芯水解液为底物时,与野生菌株发酵单一木糖相比,突变菌株乳酸、乙醇的产量增加,而与野生菌株发酵水解液相比,只有乳酸得率增加,而外源乙酸是可以提高Rx1的乳酸、乙醇产量[22],所以外源乙酸对突变菌株产物的影响还有待验证。
| Strains | Yield(g/g) | Glucose | Cellobiose | Xylose | Hydrolysate |
| YL/S | 0.29 | 0.25 | 0.25 | 0.28 | |
| YA/S | 0.19 | 0.18 | 0.18 | 0.19 | |
| Wild | YE/S | 0.30 | 0.33 | 0.30 | 0.39 |
| YE/S/(YE/S+ YA/S+ YL/S) | 0.51 | 0.55 | 0.53 | 0.57 | |
| Carbon recover(%) | 117.72 | 110.39 | 110.63 | - | |
| YL/S | 0.35 | 0.22 | 0.32 | 0.43 | |
| YA/S | 0.033 | 0.021 | 0.024 | 0.081 | |
| Δack mutant | YE/S | 0.29 | 0.55 | 0.43 | 0.37 |
| YE/S/(YE/S+ YA/S+ YL/S) | 0.59 | 0.81 | 0.71 | 0.57 | |
| Carbon recover(%) | 96.56 | 124.98 | 120.01 | - |
菌株T. calidiforntis Rx1中,乙酸激酶 (ack) 基因的敲除大幅度降低了副产物乙酸的合成,华南理工大学[18]的研究者敲除Thermoanaerobacterium aotearoense乙酸代谢基因后,HPLC没有检测到乙酸,或许T. calidiforntis Rx1编码的Ack蛋白仍有部分活性,也或许细胞中存在其他乙酸途径。大肠杆菌在厌氧发酵产乙醇的过程中除了pta、ack途径合成乙酸外,丙酮酸在丙酮酸氧化酶的作用下释放CO2产生乙酸,而且tdcD基因编码丙酮酸激酶,同时具有乙酸激酶的活性[25]。在T. calidiforntis Rx1的全基因测序结果中没有发现丙酮酸氧化酶基因,但是发现了丙酮酸氧化还原酶和丙酮酸激酶基因,因此需要再设计实验验证T. calidiforntis Rx1中是否存在其他的乙酸代谢途径。
| [1] | Kumar A, Singh L K, Ghosh S, et al. Bioconversion of lignocellulosic fraction of water-hyacinth hemicelluloses acid hydrolysate to ethanol by pickier styptic. Bioresource Technology, 2009, 100(13): 3293-3297. |
| [2] | Lynd L R, Laser M S, Bransby D, et al. How biotech can transform biofuels. Nat Biotechnol, 2008, 26(2):169-172. |
| [3] | Menon V, Rao M. Trends in bioconversion of lignocellulose: biofuels, platform chemicals & biorefinery concept. Progress in Energy and Combustion Science, 2012, 38(14):522-550. |
| [4] | EI-Zawawy W K, Ibrahim M M, Abdel-Fattah Y R, et al. Acid and enzyme hydrolysis to convert pretreated lignocellulosic materials into glucose for ethanol production. Carbohydrate Polymers, 2011, 84(3):865-871. |
| [5] | Sommer P, Georgieva T, Ahring B K. Potential for using thermophilic anaerobic bacteria for bioethanol production from hemicellulose. Biochem Soc Trans, 2004, 32(2):283-289. |
| [6] | Olson D G, McBride J E, Shaw A J, et al. Recent progress in consolidatedbioprocessing. Curr Opin Biotechnol, 2012, 23(3):396-405. |
| [7] | Desai S G, Guerinot M L, Lynd L R. Cloning of L-lactate dehydrogenase and elimination of lactic acid production via gene knockout in Thermoanaerobacterium saccharolyticum JW/SL-YS485. Appl Microbiol Biotechnol, 2004, 65(5): 600-605. |
| [8] | Shaw A J, Podkaminer K K, Desai S G, et al. Metabolic engineering of a thermophilic bacterium to produce ethanol at high yield. Proc Natl Acad Sci USA, 2008, 105(37): 13769-13774. |
| [9] | Taylor M P, Eley K L, Martin S, et al. Thermophilic ethanologenesis: future prospects for second-generation bioethanol production. Trends Biotechnol, 2009, 27(7): 398-405. |
| [10] | Yao S, Mikkelsen M J. Identification and overexpression of a bifunctional aldehyde/alcohol dehydrogenase responsible for ethanol production in Thermoanaerobacter mathranii. J Mol Microbiol Biotechnol, 2010, 19(3): 123-133. |
| [11] | Li S, Lai C, Cai Y, et al. High efficiency hydrogen production from glucose/xylose by the ldh-deleted Thermoanaerobacterium strain. Bioresour Technol, 2010, 101(22): 8718-8724. |
| [12] | Park J M, Kim T Y, Lee S Y. Constraints-based genome-scale metabolic simulation for systems metabolic engineering. Biotechnol Adv, 2009, 27(6): 979-988. |
| [13] | Patnaik R. Engineering complex phenotypes in industrial strains. Biotechnol Prog, 2008, 24(1): 38-47. |
| [14] | Shang S M, Qian L, Zhang X, et al. Thermoanaerobacterium calidifontis sp. nov., a novel anaerobic, thermophilic, ethanol producing bacterium from hot springs in China. Arch Microbiol, 2013, 195(6):439-445. |
| [15] | Hoseki J, Yano T, Y Koyama, et al. Directed evolution of thermostable kanamycin-resistance gene: a convenient selection marker for Thermus thermophilus. J Biochem, 1999, 126(5): 951-956. |
| [16] | Romano I, Dipasquale L, Orlando P, et al.Thermoanaerobacterium thermostercus sp.nov. a new anaerobic thermophilic hydrogen-producing bacterium from buffalo-dung. Extremophiles, 2010,14(2): 233-240. |
| [17] | Argyros D A, Tripathi S A, Barrett T F, et al. High ethanol titers from cellulose by using metabolically engineered thermophilic, anaerobic microbes. Applied and Environmental Microbiology, 2011,77(23):8288-8294. |
| [18] | Yang X, Lai Z, Lai, C, et al. Efficient production of l-lactic acid by an engineered Thermoanaerobacterium aotearoense with broad substrate specificity. Biotechnol Biofuels, 2013,6(1):124. |
| [19] | Mai V, Wiegel J. Advances in development of a genetic system for Thermoanaerobacterium spp.: expression of genes encoding hydrolytic enzymes, development of a second shuttle vector, and integration of genes into the chromosome. Applied and Environmental Microbiology, 2000,66(11): 4817-4821. |
| [20] | Tripathi S A, Olson D G, Argyros D A, et al. Development of pyrF-based genetic system for targeted gene deletion in clostridium thermocellum and creation of a pta mutant. Applied and Environmental Microbiology, 2010,76(19): 6591-6599. |
| [21] | Shaw A J, Podkaminer K K, Desai S G, et al. Metabolic engineering of a thermophilic bacterium to produce ethanol at high yield. Proc Natl Acad Sci USA, 2008,105(37): 13769-13774. |
| [22] | 尚淑梅,申冬玲,李坤志,等. 高温菌发酵甘露醇高效产乙醇的代谢途径研究. 中国生物工程杂志, 2013,33(10): 73-80. Shang S M, Shen D L, Li K Z, et al. Study on metabolic pathway of efficiently producting ethanol by thermophilic bacterium using mannitol. China Biotechnology, 2013, 33(10): 73-80. |
| [23] | He Q, Lokken P M, Chen S, et al. Characterization of the impact of acetate and lactate on ethanolic fermentation by Thermoanaerobacter ethanolicus. Bioresour Technol, 2009, 100(23): 5955-5965. |
| [24] | Mai V, Lorenz W W, Wiegel J. Transformation of Thermoanaerobacterium sp. Strain JW/SL-YS485 with plasmid pIKM1 conferring kanamycin resistance. FEMS Microbiology Letters, 1997, 148(2):163-167. |
| [25] | Jantama K, Zhang X, Moore J C, et al. Eliminating side products and increasing succinate yields in engineered strains of Escherichia coli. Biotechnology and Bioengineering, 2008,101(5): 881-893. |
 2015, Vol. 35
2015, Vol. 35




