文章信息
- 肖仕圆, 许敬亮, 陈小燕, 杨柳, 袁振宏
- XIAO Shi-yuan, XU Jing-liang, CHEN Xiao-yan, YANG liu, YUAN Zhen-hong
- 在大肠杆菌中表达酮酸脱羧酶产异戊醇
- Production of the Isoamyl Alcohol in E.coli by Expression of kivD Gene
- 中国生物工程杂志, 2015, 35(4): 60-65
- China Biotechnology, 2015, 35(4): 60-65
- http://dx.doi.org/10.13523/j.cb.20150409
-
文章历史
- 收稿日期:2015-01-14
2. 中国科学院大学 北京 100049
全球环境的恶化、能源的不足等问题促进了对可再生生物燃料能源的研究[1]。目前,研究的主要热点方向是生物燃料乙醇,在2011年,美国的产量达到了10亿加仑[2]。然而,乙醇具有高蒸汽压、腐蚀性等性质,使其作为汽油代替燃料仍然存在一定的缺陷,异戊醇等高级醇比乙醇具有更高的能量密度、更低的蒸汽压、更高的辛烷值等特点,其性质更接近于汽油[3],成为新一代可再生能源的研究方向。
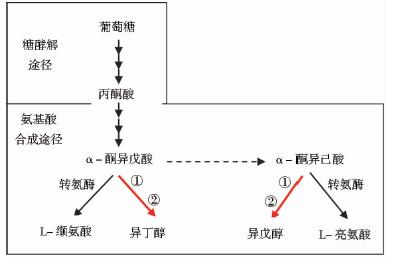
过去一直没有微生物能够经由葡萄糖直接大量合成异戊醇等高级醇的报道。在2008年,美国加利福尼亚大学的研究团队在Nature上率先报道了通过非发酵途径合成高级醇的方法[4]。他们以氨基酸合成的共同前体物α-酮酸作为底物,在α-酮酸脱羧酶和醇脱氢酶的作用下生产出异丁醇、异戊醇和2-甲基-1-丁醇等高级醇(图 1)。而大肠杆菌作为研究得最为详尽的原核宿主菌,具有遗传背景清楚、生长周期短、培养条件温和、代谢易于控制等优点。近年来,研究者利用非发酵途径,通过相关基因的表达,在大肠杆菌中成功地合成了异丁醇、异戊醇等高级醇[5, 6, 7]。但由于关键基因酮酸脱羧酶的低表达量,使其成为了阻碍高级醇大量生产的瓶颈。
|
| 图 1 异戊醇生物合成途径 Fig. 1 The pathway for isoamyl alcohol production ① Keto acid decarboxylase; ② Alcohol dehydrogenase |
本研究拟通过增加核糖体结合位点rbs优化表达条件,利用大肠杆菌强启动等策略,将乳酸乳球菌的酮酸脱羧酶基因kivD通过PCR扩增连接到大肠杆菌高效表达载体pET-28a(+)上,以实现其高效表达,为今后构建高产异戊醇工程菌株奠定基础。
1 材料与方法 1.1 材 料 1.1.1 菌株和质粒本实验使用的菌株、质粒见表 1。
| 菌株/质粒 | 相关特性 | 来源/参考 |
| Lactococcus lactis | 野生型 | 本实验室 |
| subsp. Lactis | ||
| E.coli TRANS1 | F-φ80 lac ZΔM15 | 北京全式金生物公司 |
| Δ(lacZYA-arg F) U169 | ||
| endA1 recA1 hsdR17(rk-,mk+) | ||
| supE44-thi-1gyrA96relA1phoA | ||
| F-ompThsdSB(r B-,m-) | ||
| E.coli BL21(DE3) | gal(cI857,ind1,sam7,nin5, | 北京全式金生物公司 |
| lacUV5-T7gene1) dcm | ||
| pEASY-T1 | PT7 Kan+ Amp+ LacZ | 北京全式金生物公司 |
| pET-28a(+) | PT7 Kan+ LacI | 本实验室 |
| pET-kivD | PT7 Kan+ LacI KivD | 本实验 |
| pET-kivD-rbs | PT7 Kan+ LacI KivD-rbs | 本实验 |
乳酸乳球菌MRS培养基:1%酪蛋白,1%牛肉膏,0.5%酵母提取物,0.5%乙酸钠,0.2% 柠檬酸二钠,0.1% 吐温80,0.2% 磷酸氢二钾,0.02%七水硫酸镁,0.005% 水合硫酸锰;大肠杆菌LB培养基:1%胰蛋白胨,0.5%酵母提取物,1%氯化钠。固体培养基加入2%的琼脂粉。
Trans Start Taq聚合酶链式反应试剂盒、DNA凝胶回收试剂盒、DNA Loading Buffer、DNA Marker、卡那霉素、Bradford蛋白质定量试剂盒等购自北京全式金生物公司;T4 DNA Ligase、限制性内切核酸酶购自Fermentas公司; IPTG购自生物生工;Trypton 和Yeast Extract购自Oxoid;丙烯酰胺、甲叉双丙烯酰胺、SDS、Tris、溴酚蓝、过硫酸铵、甘氨酸、TEMED、考马斯亮蓝R250均购自Amresco;琼脂糖购自Biowest公司;其余试剂均为国产分析纯或生化级。
1.2 方 法 1.2.1 乳酸乳球菌酮酸脱羧酶基因kivD的克隆Lactococcus lactis subsp Lactis菌株划线于固体平板上,挑取单菌落于10 ml MRS液体培养基中37℃、200 r/min过夜培养,2~3 ml离心收集菌体,基因组的提取方法参照TIANGEN 细菌基因组 DNA 提取试剂盒说明书。
根据NCBI 中乳酸乳球菌的酮酸脱羧酶kivD基因序列信息,利用premier 5.0设计引物,并在引物的两端加上SacI 和SalI酶切位点,其中一个另加rbs(核糖体结合位点)(表 2)。
| Primer | Sequence (5′→3′) | Restriction | Size (bp) |
| F1 | CGAGCTCATGTATACAGTAGGAGATTACC | SacI | 29 |
| F2 | CGAGCTC AAGAAGGAGATATACATGTATACAGTAGGAGATTACC | SacI | 44 |
| R1 | GTCGACTTATGATTTATTTTGTTCAGCAAAT | SalI | 31 |
以乳酸乳球菌基因组DNA为模板,按照Taq聚合酶链式反应试剂盒的反应体系进行PCR实验,反应程序:95 ℃预变性 5 min,95 ℃变性 30 s,55 ℃ 退火 30 s,72 ℃ 延伸 2 min,72 ℃延长10 min,4 ℃终止反应;循环数 35次。
1.2.2 载体的构建和阳性克隆子筛选PCR产物连接到克隆载体pEASY-T1上,得到重组质粒T-kivD和T-kivD-rbs,转化进E.coli TRANS1,挑取单菌落,经菌落PCR初步鉴定,菌液送去测序,结果在NCBI中进行比对。
pET-28a(+)、T-kivD和T-kivD-rbs分别用SacⅠ和SalⅠ双酶切,回收pET-28a酶切片段,回收T-kivD和T-kivD-rbs凝胶中的小片段,用T4 DNA Ligase连接。连接产物转化后,挑取单菌落过夜培养,提质粒,得到表达载体pET-kivD和pET -kivD-rbs,双酶切验证。
利用北京全式金生物公司提取的方法把pET-28a(+)、pET-kivD和pET -kivD-rbs 经过42 ℃热击转化进E.coli BL21(DE3)感受态细胞中,培养于含卡那霉素终浓度为 50 μg/ml的LB培养基中,菌落PCR鉴定,验证是否为阳性克隆子。其中,转化进载体pET-28a(+)的菌为空载菌,转化进载体pET-kivD的菌为重组菌1,转化进载体pET-kivD-rbs的菌为重组菌2。
1.2.3 目的蛋白的表达和发酵条件优化分别挑取平板上的空载菌、重组菌1和重组菌2的单菌落于含kan+的3 ml LB培养基中37℃、200 r/min过夜培养,1%转移到含kan+的10 ml LB培养基中37℃、200 r/min培养3 h,加入终浓度为1 mmol/L IPTG诱导发酵4 h后,各取培养液2 ml,4℃下8000 r/min离心10 min,收集菌体,上清液作为发酵液做成分分析。用双蒸水500 μl洗涤菌体2次,接着用600 μl磷酸缓冲液(pH 7.4)重悬菌体,置于冰水浴中进行超声波破碎,处理5s,停歇5s,直至重悬液变澄清。将超声处理后的菌体重悬液4℃下12 000 r/min离心15 min,收集上清液,进行十二烷基磺酸钠-聚丙烯酰胺凝胶电泳,确定酶的表达情况。
将大肠杆菌重组菌2的种子液接种到10 ml LB发酵培养基中进行摇瓶培养,起始OD600值为0.3,37℃、200 r/min培养1~2 h后至OD600值为0.6~0.8,加入1mmol/L IPTG诱导,然后在不同温度下培养,每隔一个时间段分别取样一次,通过测定溶液的OD365值来考察温度和时间对发酵的影响。
1.2.4 发酵液成分分析发酵上清液经0.22 μm 滤膜过滤后,用气相色谱-质谱联用仪检测发酵产物成分。气相程序:分流比1∶50,上样量1 μl,柱温60℃平衡1 min,10℃/min 上升至260℃,保持2 min。H2气压达到0.4 MPa,空气气压达到0.4 MPa,氩气气压达到0.6 MPa,加热器200℃。
1.2.5 酮酸脱羧酶酶活测定由于检测到KivD酶对酮异己酸具有更优的偏好性,所以酶活的测定参照文献[8]。底物为酮异己酸,测定的相应生成物为异戊醛。异戊醛与2,4-二硝基苯肼反应,生成 2,4-二硝基苯腙,在碱性溶液中呈暗红色,用分光光度法在365 nm处测光密度值。粗酶液中蛋白质含量使用Bradford蛋白质定量试剂盒测定,重复测定3 次取平均值。
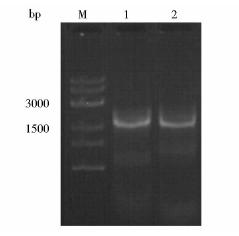
2 结 果 2.1 kivD基因的克隆以乳酸乳球菌的基因组DNA为模板,用引物对F1、R1和F2、R1进行PCR扩增,用1.0%的琼脂糖凝胶对产物进行电泳,得到与理论大小1647接近的目的条带(图 2)。
|
| 图 2 kivD基因克隆Fig. 2 kivD gene cloning M:8k DNA marker; 1: kivD; 2:kivD-rbs |
经PCR扩增的产物和pEASY-T1连接,转化进感受态细胞E.coli TRANS1 中,菌落PCR获得阳性克隆子,菌液测序,测序结果经比对正确,目的基因、酶切位点和核糖体结合位点均成功扩增。
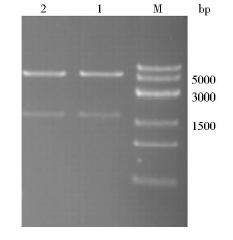
表达质粒pET-kivD和pET-kivD-rbs经过SacⅠ和SalⅠ双酶切,用1.0%琼脂糖凝胶进行电泳,得到图 3,大小约为5400 bp和1650 bp,符合理论大小。
|
| 图 3 酶切结果Fig. 3 The results of enzyme digestion M:8k DNA marker 1: pET-kivD 2: pET-kivD-rbs |
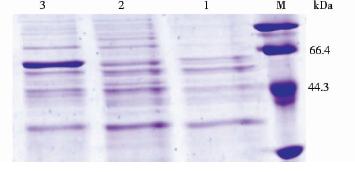
L. lactis subsp. Lactis的酮酸脱羧酶基因kivD的分子质量大小约为61 kDa[8].经过SDS-PAGE电泳(图 4),在菌株其他蛋白质表达含量基本相同的情况下,三种工程菌的蛋白质分子质量在61 kDa表达含量各不相同,空载工程菌几乎没有目的条带,重组菌株中有明显的目的条带,经过Bradford法对细胞总蛋白质量进行测定(表 3),表达量依次增加,说明酮酸脱羧酶基因表达菌种初步构建成功。
|
| 图 4 蛋白质电泳结果Fig. 4 The results of SDS-PAGE M:Low molecular weight protein maker; 1: pET-28a(+); 2: pET-kivD; 3: pET-kivD-rbs |
| 菌株 | 蛋白质含量/(mg/ml) |
| 空载菌 | 0.100±12 |
| 重组菌1 | 0.158±15 |
| 重组菌2 | 0. 220±10 |
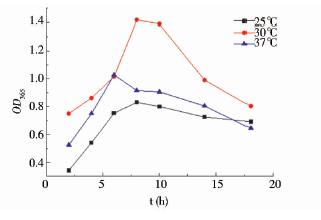
选取酮酸脱羧酶表达更好的大肠杆菌重组菌2进行优化表达。根据文献[9]和[10]的报道,温度对异源基因的表达有很大的影响,低温会抑制酶活,而高温会加速细胞的老化,从而不利于发酵。因此,本实验选取了25℃,30℃,37℃三个不同的温度,每隔2 h取样一次,后期每隔4 h取样。从图 5中可以知道,在30℃发酵8 h时,有最大光密度值,即酶活达到最大值。
|
| 图 5 不同诱导温度对粗酶液KivD酶促反应的影响Fig. 5 Effect of different temperature on KivD activity in crude extract |
发酵液经GC-MS联用仪测定以后,结果如表 4所示。与标准液测定结果相比,大肠杆菌空载菌[含pET-28a(+)]没有检测到相应的目标产物,而大肠杆菌重组菌株1(含pET-kivd)、大肠杆菌重组菌株2(含pET-kivd-rbs)检测到异戊醇,而没有检测到异戊醛和异丁醇。由此可知,目的基因在大肠杆菌中成功表达和大肠杆菌本身就具有醇脱氢酶基因,且表现出相应的活性。
| 菌株 | 异戊醛含量 | 异丁醇含量 | 异戊醇含量(mg/L) |
| 空载菌 | ○ | ○ | ○ |
| 重组菌1 | ○ | ○ | 72 |
| 重组菌2 | ○ | ○ | 115 |
| Note: ○ is no | |||
本研究在大肠杆菌BL21的基础上,成功地构建了含有kivD基因的大肠杆菌重组菌。通过IPTG诱导,使其在重组菌中成功表达,但是表达量各有差异。造成差异的原因一方面是菌株本身并没有含有目的基因;另一方面是加入了核糖体结合位点rbs。核糖体结合位点的长短、菌种特异性、离起始位点的位置等特点对翻译起着重要的作用[11, 12]。翻译开始的效果是影响基因表达的一个重要因素,核糖体结合位点的选用不会使目的基因 5′端形成“茎环”结构,从而有利于 mRNA 5′端与核糖体 30S 亚基结合,促进翻译开始[13, 14]。从实验的结果来看,加入了rbs的菌株其表达量明显高于没有加入rbs的菌株,推测其原因主要在于rbs位点离起始密码子的距离近,导致了起始翻译的密码子多,翻译量相应地增加。尽管载体本身具有rbs位点,但是距离起始密码子较远,核糖体结合后在一些载体上会翻译,而在另外一些载体上的核糖体也许会因为距离太远而脱落,从而造成表达量出现差异。
3.2 酮酸脱羧酶特异性作为异戊醇生物合成过程中的关键酶—α-酮酸脱羧酶(KivD),其来源不同,对底物催化专一性也不一样[15, 16]。工程菌转化进了乳酸乳球菌KivD表达以后,对其发酵产物进行分析,没有检测到有关文献报道的异丁醇[17, 18],而是检测到了异戊醇。从实验结果可以推测,在载体pET-28a(+)的作用下,该酮酸脱羧酶对异戊醇的底物(酮异已酸)可能有更好的偏好性。基于此实验结果,本实验室成员对其进行了专利申请[19]。
4 结论和展望本实验研究的结果表明,在强启动子T7的作用下,菌株浓度OD600值为0.6~0.8,加入1 mmol/L IPTG在30℃条件下诱导发酵8 h,酮酸脱羧酶的活性达到了最大值。发酵产物异戊醇的出现,也表明此基因在大肠杆菌高效表达载体pET-28a(+)的作用下,表达的脱羧酶对酮异已酸具有更好的偏好性。
目前还没有报道有关野生型的大肠杆菌能产异戊醇,但是通过代谢工程的改造,美国Liao等[20]实现了在大肠杆菌中产异戊醇。将来在进一步构建高产异戊醇菌株方面,可以对相关路径的关键基因进行表达,同时也可以通过基因敲除来降低底物竞争途径。
| [1] | Ingram L O, Aldrich H C, Borges A C C, et al. Enteric bacterial catalysts for fuel ethanol production.Biotechnology Progress, 1999, 15(5): 855-866. |
| [2] | 蔡海龙,王秀清.美国燃料乙醇产量快速增长的原因及对国际玉米市场的影响.中国农业大学学报,2013,30(4):127-132 Cai H L, Wang X Q.The reasons of U.S. fuel ethanol production increase and its impact on international maize market. Journal of China Agricultural University, 2013,30(4):127-132. |
| [3] | Savage N.Fuel options:the ideal biofuel.Nature,2011,474(7352):9-11. |
| [4] | Atsumi S,Hanai T,Liao J C.Non-fermentative pathways for synthesis of branched-chain higher alcohols as biofuels. Nature,2008,451(7174):86-89. |
| [5] | 潘超强,高强,郑春阳,等.产异丁醇关键基因在大肠杆菌中表达的研究.微生物学报,2012,39(7):912-920. Pan C Q, Gao Q, Zheng C Y,et al.Coexpression of two essential isobutanol synthesis genes in Escherichia coli. Microbiology China, 2012,39(7):912-920. |
| [6] | 郑丽娟,陈少云,徐刚,等.利用双启动子载体构建产异丁醇大肠杆菌.中国生物工程杂志,2013,33(8):66 -72 Zheng L J, Chen S H, Xu G, et al. Engineering E.coli for isobutanol production by two-promoter vectors. China Biotechnology, 2013,33(8):66-72. |
| [7] | Nicole N E,Shuchi S H,Anna A E,et al.Metabolic engineering for higher alcohol production.Metabolic Engineering,2014,25:174-183. |
| [8] | Martadela P, Pilar F P, Carmen P.Biochemical and molecular characterization of a-ketoisovalerate decarboxylase, an enzyme involved in the formation of aldehydes from amino acids by Lactococcus lactis. FEMS Microbiology Letters,2004,238(2):367-374 |
| [9] | Sorensen H P, Mortensen K K. Soluble expression of recombinant proteins in the cytoplasm of Escherichia coli. Microbial Cell Factories, 2005,4(1): 1-8. |
| [10] | Williams R E, Bruce N C. 'New uses for an old enzyme'——the old yellow enzyme family of flavoenzymes. Annals of Microbiology, 2002,148(6): 1607-1614. |
| [11] | Shine J,Dalgarno L.The 3'-terminal sequence of Escherichia coli 16S ribosomal RNA:complementarity to nonsense triplets and ribosome binding sites.National Academy of Sciences,1974,71(4): 1342-1346. |
| [12] | Mary V M,Maurille J F,David A T.Depletion of Free 30S ribosomal subunits in Escherichia coli by expression of RNA containing shine-dalgarno-like sequences.Jouranl of Bacteriology,2002,184(2):494-502. |
| [13] | 李育阳.基因表达技术.北京:科学出版社,2001.15-16. Li Y Y. Gene Expression Technology. Beijing: Science Press, 2001.15-16. |
| [14] | 吴乃虎.基因工程原理(下).北京:科学出版社,1989.113. Wu N H. Genetic Engineering Principles. Beijing: Science Press,1989.113. |
| [15] | König S. Subunit structure, function and organisation of pyruvate decarboxylases from various organisms. Biochimica et Biophysica Acta (BBA)-Protein Structure and Molecular Enzymology,1998, 1385(2):271-286. |
| [16] | Ezeji T, Qureshi N, Blaschek H P.Production of acetone-butanol-ethanol (ABE) in a continuous flow bioreactor using degermed corn and Clostridium beijerinckii.Process Biochemistry,2007, 42(1):34-39. |
| [17] | 林丽华, 郭媛, 庞浩,等.大肠杆菌中表达关键基因产异丁醇的研究. 生物技术,2011, 21(3):19-23. Lin L H, Guo Y, Pang H, et al. The construction of recombinant E.coli producing isobutanol. Biotechnology Bulletin, 2011, 21(3):19-23. |
| [18] | Kevin M S,Kwang M C,James C L.Engineering Corynebacterium glutamicum for isobutanol production. Appl Microbiol Biotechnol,2010, 87(3):1045-1055. |
| [19] | 袁振宏,许敬亮,陈小燕,等.一种α-酮酸脱羧酶KIVD-LL及其编码基因和应用,中国, 中华人民共和国国家产权局, CN201410309574,2014,7. Yuan Z H, Xu J L, Chen X Y, et al. An alpha keto acid decarboxylase KIVD-LL and its coding gene,application. China, The national property office of the People's Republic of China, CN201410309574,2014,7. |
| [20] | Liao J C, Connor M R. Engineering of an Escherichia coli strain for the production of 3-methyl-1-butanol. Applied and Environmental Microbiology, 2008, 74(18): 5769-5775. |
 2015, Vol. 35
2015, Vol. 35




