2. 中国科学院机器人与智能制造创新研究院,沈阳 110169;
3. 中国科学院大学,北京 100049;
4. 辽宁省微创手术机器人重点实验室,沈阳 110179;
5. 中国医科大学,沈阳 110122
2. Institutes for Robotics and Intelligent Manufacturing, Chinese Academy of Sciences, Shenyang 110169, China;
3. University of Chinese Academy of Sciences, Beijing 100049;
4. Liaoning Province Key Laboratory of Minimally Invasive Surgical Robot, Shenyang 110179, China;
5. China Medical University, Shenyang 110122, China
脉管穿刺介入手术是通过专业的导丝或导管等器械,配合医学影像设备通过脉管介入后到达病患部位,达到检查或治疗目的的一种现代化高科技微创治疗方式[1],具有创伤小,恢复快等特点。传统的血管穿刺技术没有可视化引导,主要依赖体表标志定位血管,当出现定位不清、穿刺部位有感染或者包块、极细血管穿刺等穿刺困难情况时,盲穿刺风险高。在血管穿刺时使用超声引导,可清晰看到血管结构及血管周围的神经、肌肉等毗邻结构,可迅速识别血管、提高穿刺成功率、缩短穿刺时间、避免严重并发症等。但在临床穿刺操作中,外科医生一只手拿着超声探头扫描目标脉管,另一只手进行穿刺针插入,协调双手使穿刺针准确地插入到脉管中是一个难点。同时,在一些紧急条件下需要快速建立脉管通路,例如脉管闭合止血、输液、急救等, 但目前的一些辅助脉管穿刺设备由于体积大,结构复杂并不能应用于病情紧急,环境简陋的非临床环境。
目前,在穿刺机器人领域有以下几种研究:在穿刺活检方向,Mahmoud等[2]研制了超声引导的用于乳腺穿刺活检的机器人;Lim等[3]研制了通过超声引导的前列腺穿刺活检机器人;Jiang等[4]、Dan等[5]研制了在CT放射性环境下肺部穿刺活检机器人。在微创介入治疗方向,Gao等[6]研制了超声引导经皮关节穿刺机器人辅助系统;Taguchi等[7]研制了通过超声引导的肾脏穿刺机器人——这些机器人普遍体积较大,不能便携使用。在小型的穿刺设备领域,Becker等[8]研制了图像引导手持机器人视网膜血管插管设备;Gijbels等[9]研制了视网膜静脉插管机器人辅助系统,此类机器人仅适用于眼科手术;Chen等[10]研制了超声引导经皮穿刺机器人,采用超声平面内穿刺方法,主要用于穿刺活检。
在脉管穿刺机器人领域,一些机器人系统和穿刺设备也被研究出来。例如,He等[11]研制了使用近红外视觉而不是超声辅助穿刺的静脉穿刺机器人。Perry[12]研制了通过超声引导的手臂静脉穿刺机器人,该机器人固定在一个大的机械臂上,对患者的心理上带来较大的挑战。Balter等[13]和Chen等[14]先后提出两代超声引导的静脉穿刺机器人,该机器人主要用于手臂的静脉穿刺采血,将采集的血液进行后续化验等操作[15];此后,又对第二代穿刺采血机器人进行简化,研制了一种小型化的手持式超声引导静脉穿刺设备[16],该设备体积较小,可便携使用,但仅具有2个自由度,工作范围有一定的局限性。Kobayashi等[17]研制的中心静脉置管针插入机器人具有3个主动自由度,可以实现对静脉的自动穿刺,由于体积较大,并不能在非临床的条件下便携使用。Ahmad和Yi[18]研制了一种用于动脉穿刺的被动超声探头支架,采用被动的7自由度支架将超声探头和穿刺针导丝置于支架之上,提高了穿刺精度,但并不具有主动穿刺的能力。本设计与其他团队研制的穿刺机器人在重量、穿刺深度、自由度上对比如表 1所示。
|
|
表 1 本设计与其他穿刺机器人参数对比表 Table 1 Comparison of parameters between this paper's and other puncture robots |
本文设计一种超声引导的便携式脉管穿刺的机器人,采用平面外穿刺方法扫描目标脉管,通过机械结构将超声图像、穿刺针和目标脉管对准。通过调节上下移动距离实现不同深度的脉管穿刺。该机器人的体积和超声探头大小相当,总重量在单手可持的范围内,便于在非临床条件下便携使用, 具有较大的穿刺角度调整范围,方便适应不同条件下的穿刺需求。
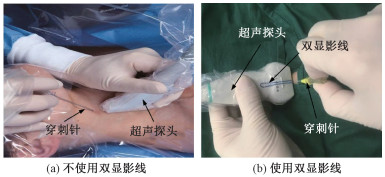
1 超声引导脉管穿刺的过程和参数 1.1 超声引导脉管穿刺过程目前,使用超声引导脉管穿刺主要有2种方式,方法1:先定位再穿刺。先通过超声影像定好穿刺部位;(将血管放置到图像中心)沿着血管走形移动,再重复标注,然后连线得到血管的走形图;最后,根据连线得到的脉管走形图进行穿刺。此方法无法确定脉管的深度,在穿刺过程中仅靠操作者的感觉确定穿刺深度。方法2:穿刺同时使用超声探头,如图 1(a)所示。第1步,根据穿刺目标脉管的位置,选择合适的穿刺部位;第2步,把超声探头放入加入无菌耦合剂的无菌护套内,抚平探头表面护套;第3步,在皮肤上涂抹无菌超声耦合剂;第4步,操作者一手持超声探头,另一只手持穿刺针进行穿刺。此方法也在很大程度上依靠穿刺操作者的经验和感觉,一次性穿刺成功率低,对患者的伤害大,操作者学习时间长。
|
Download:
|
| 图 1 超声引导穿刺图片 Fig. 1 Ultrasound-guided puncture images | |
超声引导脉管穿刺的新方法[19]提高了脉管穿刺的成功率,如图 1(b)所示,在超声探头上固定双显影线。平行的双显影线在超声探头中点处与其长轴垂直固定,通过双显影线确定超声探头和目标脉管的相对位置。将双显影线移动到目标穿刺脉管的正上方,穿刺针在皮肤外2根双显影线之间进行穿刺。经实验表明,此种穿刺方法很大程度上提高了第一次穿刺的成功率。但操作者依然无法确定穿刺深度,具有一定的穿刺失败率。
本文设计穿刺机器人取消了双显影线,通过机械结构将穿刺针布置在超声探头的中心正上方,通过超声图像的中心线确定穿刺针和目标脉管的相对位置。移动超声探头使超声图像的中心线对齐目标脉管,由于超声图像的中心线就是超声探头的中心,因此穿刺针在目标脉管的正上方。读取超声图像中的脉管深度信息后,输入到机器人。机器人根据脉管深度信息计算穿刺针达到目标脉管的移动距离,完成穿刺动作。
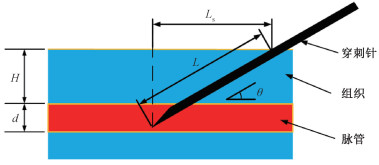
1.2 脉管穿刺的参数设计脉管穿刺介入手术的主要目的是针对穿刺困难的颈动脉、桡动脉和股动脉进行穿刺置管及介入导丝操作。在穿刺过程中对穿刺针、组织、脉管进行建模,如图 2所示。
|
Download:
|
| 图 2 穿刺针插入脉管模型 Fig. 2 Model of needle insertion into a vessel | |
插入进针长度L表示从其接触皮肤的点到其在脉管内的中心位置沿针轴向的距离,可计算为
| $ L=(H+d / 2) / \sin \theta . $ | (1) |
其中: H表示脉管的深度,d表示脉管的直径,θ表示穿刺针和组织表面的穿刺角度。根据穿刺的部位和脉管的种类不同,其参数信息[20]如表 2所示。使用超声探头进行平面外穿刺,当穿刺针针尖出现在超声扫描平面的图像时,停止进针。此时,穿刺针接触皮肤的点与超声扫描平面的垂直距离Ls为
| $ L_{\mathrm{s}}=(H+d / 2) / \tan \theta \text {. } $ | (2) |
根据表 2的脉管穿刺参数信息,我们设计了符合工作范围的脉管穿刺机器人尺寸参数。
|
|
表 2 脉管穿刺环境参数的取值范围 Table 2 Value range of environmental parameters for vessel puncture |
机器人采用平面外穿刺的方法,将穿刺针通过机械结构布置在超声探头的中心正上方。机器人通过快速拆卸机构连接在超声探头上。包括2个直线移动自由度和1个被动旋转自由度。2个直线移动自由度分别由上下移动机构和进针机构实现,被动旋转自由度由角度调节机构实现。穿刺针通过可快速拆卸机构连接到进针机构上,机器人构型如图 3所示。

|
Download:
|
| 图 3 脉管穿刺机器人的结构图和实物图 Fig. 3 Structure diagram and physical prototype image of the venous puncture | |
上下移动机构由伺服电机皮带传动驱动丝杠滑块实现机器人的上下移动自由度X,用于调整不同的穿刺深度。角度调节机构内嵌阻尼铰链连接在上下移动机构和进针机构之间,操作者可以根据以往的穿刺经验手动调节到合适的穿刺角度θ,减少学习时间。进针机构由伺服电机皮带传动驱动丝杠滑块实现进针自由度Y,完成穿刺针的刺入动作。此外,机器人与超声探头连接处使用快拆机构,可用于搭载不同型号的超声探头。穿刺针与机器人的连接处也使用了快拆机构,用于穿刺完成后,穿刺针快速脱离机器人后留置,建立脉管通路。机器人的各部分之间配合关系如图 4所示。

|
Download:
|
| 图 4 穿刺机器人的爆炸图和零件标注 Fig. 4 Explosion drawing and parts marking of puncture robot | |
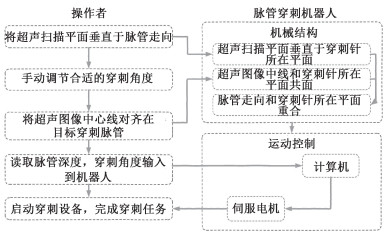
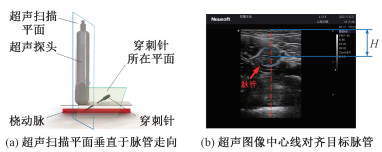
根据超声引导脉管穿刺的需求,穿刺机器人的使用方法及工作原理如图 5所示:第1步, 操作者手持连接穿刺机器人的超声探头,根据临床经验初步确定穿刺目标脉管的位置和走向,将穿刺机器人的超声探头扫描平面垂直于脉管走向放置在目标穿刺部位的上方,如图 6(a)所示。根据脉管穿刺机器人的机械结构可以确定,超声扫描平面垂直于穿刺针所在平面。
|
Download:
|
| 图 5 脉管穿刺机器人的使用流程及原理图 Fig. 5 Working process and schematic diagram of the vessel puncture robot | |
|
Download:
|
| 图 6 脉管穿刺机器人的使用方法 Fig. 6 The application method of the vessel puncture robot | |
第2步, 操作者根据患者的胖瘦和被穿刺脉管的种类,手动调节穿刺机器人到一个合适的穿刺角度(穿刺角度的确定可以根据医生的以往的操作经验,减少了学习时间)。
第3步, 操作者将超声图像的中心线对齐在目标穿刺脉管,如图 6(b)所示。由于穿刺机器人的超声图像中心线就是超声探头的中心,穿刺针在超声探头中心的正上方,可以确定脉管走向平面和穿刺针所在平面在同一平面。此时,读取超声图像的脉管的深度信息H、穿刺机器人的角度信息θ、输入到机器人。
第4步, 操作者启动穿刺机器人。机器人根据穿刺角度信息θ,脉管深度信息H,以及内置的穿刺针长度信息Lz,计算穿刺针针尖刚好可以达到超声探头扫描平面的上下移动距离D和进针距离L
| $ D=H-40 / \tan \theta-25 / \sin \theta+68, $ | (3) |
| $ L=84+40 / \sin \theta+25 / \tan \theta-L_z \text {. } $ | (4) |
机器人上下移动机构的伺服电机和进针机构的伺服电机旋转相应的圈数,完成穿刺动作。
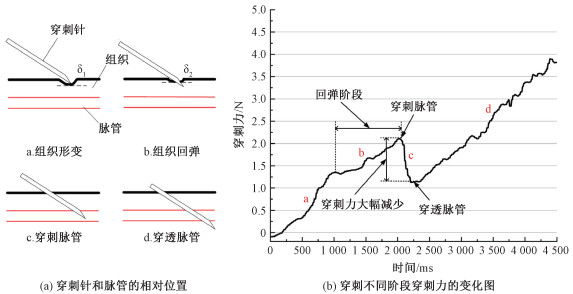
2.3 穿刺力感设计本文设计了穿刺力感机构,用于保证穿刺的准确性和安全性。在穿刺机器人末端安装力传感器实时检测穿刺力的变化以感知机器人的穿刺状态。经过对仿生脉管组织的穿刺实验,得到穿刺力变化图,如图 7(b)所示。根据穿刺针和脉管的相对位置,获得脉管穿刺不同阶段穿刺力的变化特点,如图 7(a)所示。经过分析,脉管组织穿刺过程可以分为4个阶段:穿刺针接触组织引起组织形变,穿刺针刺破组织引起组织表面回弹,穿刺针穿刺到脉管,穿刺针穿透脉管刺入另一侧组织中。
|
Download:
|
| 图 7 穿刺针位置和穿刺力变化对照图 Fig. 7 Control diagram of changes in puncture needle position and puncture force | |
我们设计穿刺机器人通过检测穿刺过程中的穿刺力变化来判断穿刺针所处的状态。当检测到穿刺力大幅减少时,停止进针动作,确保穿刺的准确性。当检测到穿刺力异常变化时,及时停止机器人,确保穿刺的安全性。
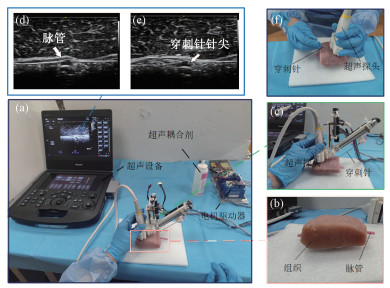
3 实验验证我们进行了2组对比试验,验证脉管穿刺机器人的实用性。实验操作者具有临床超声穿刺经验,简单学习后即可掌握穿刺机器人的使用方法。机器人脉管穿刺实验平台如图 8所示。第1组,使用超声设备辅助脉管穿刺,操作者一只手持超声探头进行脉管观测,另一只手持穿刺针进行穿刺操作。第2组,使用脉管穿刺机器人进行脉管穿刺操作(图 8(a))。每组分别进行10次脉管穿刺操作,从穿刺针接触组织开始记录穿刺所用时间和一次性穿刺是否成功。
|
Download:
|
| 图 8 机器人脉管穿刺实验台 Fig. 8 Robot vasculature lab | |
使用医用直径5mm的仿生血管作为穿刺目标,首先将仿生脉管嵌入到硅胶基质中,起固定作用,然后在硅胶基质上部分固定猪肉组织,模仿真实的脉管穿刺场景(图 8(b))。其超声图像与真实的脉管环境相似,在脉管的超声图像中可以清晰的观测到脉管的圆形截面(图 8(d))。
第1组,操作者左手握持超声探头扫描目标脉管,当超声图像中出现清晰的脉管腔后,保持超声探头不动。右手持18G股动脉穿刺针的针柄进行穿刺操作,协调双手使穿刺针穿刺到脉管腔中(图 8(f))。
第2组,使用穿刺机器人的穿刺过程(图 8(c)),操作者在学习使用方法后仅需要单手持连接有穿刺机器人的超声探头,扫描到目标脉管,将超声图像的中心线与脉管图像对齐,读取超声图像脉管深度信息,输入给穿刺机器人,启动穿刺机器人使之携带18 G股动脉穿刺针自动穿刺到目标脉管位置,穿刺完成后可以在超声图像中清晰地观测到穿刺针的针尖(图 8(e))。穿刺完成后,按动穿刺针连接机构的快拆按钮,穿刺针快速脱离机器人,留置在脉管组织中,为后续脉管插入导丝等操作建立通道。
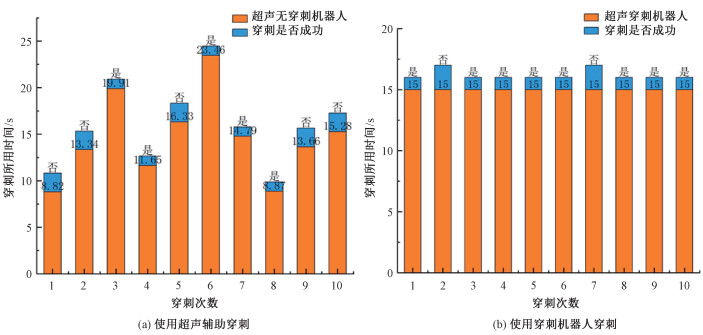
4 结果及讨论每组进行10次穿刺试验,分别记录穿刺所用时间和一次性穿刺成功率。使用超声设备辅助脉管穿刺的实验结果如图 9(a)所示,穿刺所用平均时间为14.6s,10次穿刺过程中有5次在脉管影像中观测到针尖的影像。在穿刺操作过程中虽然可以实时观测到超声图像,但超声图像仅仅是组织和脉管的一个截面,并且不能同时观测到穿刺针和脉管,不能确定穿刺针和脉管的相对位置,很大程度上是凭借感觉穿刺到脉管。
|
Download:
|
| 图 9 使用超声辅助穿刺与使用穿刺机器人在穿刺时间和成功率上的对比 Fig. 9 Comparison of puncture time and success rate between ultrasound-guided and robotic-assisted puncture | |
使用穿刺机器人进行穿刺实验的实验结果如图 9(b)所示,穿刺所用平均时间为15.0s,10次穿刺实验中有8次都在超声图像的脉管中央观测到穿刺针针尖的影像。由于设置以恒定速度进针,因此每次穿刺完成的时间均为15.0s。在机器人的穿刺过程中,操作者仅仅单手持安装穿刺机器人的超声探头,另一只手不需要额外操作,很大程度上减少了穿刺难度和学习时间。
根据实验穿刺成功率结果的对比,相较于仅使用超声设备,在时间接近的情况下,使用穿刺机器人穿刺成功率有所提高。可以说明,使用超声辅助穿刺的方法需要依靠操作者经验和感觉,操作难度大;而使用穿刺机器人进行穿刺操作,不但操作难度小,而且穿刺成功率高,具有一定的实用性。
本文设计了一种脉管穿刺机器人,用于解决脉管穿刺过程中创伤大、成功率低的问题。该机器人体积小、重量轻,可连接超声探头后便携使用。该机器人使用平面外穿刺的方法,通过机械结构使超声图像、穿刺针、脉管对准,实现准确穿刺目标脉管的功能,操作过程简单,穿刺成功率高,解决了目前手工穿刺过程中穿刺成功率低以及过分依赖操作者的经验和感觉的问题。通过实验验证了穿刺机器人的优势。下一步拟将穿刺机器人的控制系统小型化,促进穿刺机器人从原理样机到实际应用的进一步转化。
| [1] |
Eggemann H, Costa S D, Ignatov A. Ultrasound-guided versus wire-guided breast-conserving surgery for nonpalpable breast cancer[J]. Clinical Breast Cancer, 2016, 16(1): e1-e6. Doi:10.1016/j.clbc.2015.09.001 |
| [2] |
Mahmoud M Z, Aslam M, Alsaadi M, et al. Evolution of Robot-assisted ultrasound-guided breast biopsy systems[J]. Journal of Radiation Research and Applied Sciences, 2018, 11(1): 89-97. Doi:10.1016/j.jrras.2017.11.005 |
| [3] |
Lim S, Jun C H, Chang D, et al. Robotic transrectal ultrasound guided prostate biopsy[J]. IEEE Transactions on Bio-Medical Engineering, 2019, 66(9): 2527-2537. Doi:10.1109/TBME.2019.2891240 |
| [4] |
Jiang S, Yuan W, Yang Y P, et al. Modelling and analysis of a novel CT-guided puncture robot for lung brachytherapy[J]. Advanced Robotics, 2017, 31(11): 557-569. Doi:10.1080/01691864.2017.1298465 |
| [5] |
Stoianovici D, Jun C H, Lim S, et al. Multi-imager compatible, MR safe, remote center of motion needle-guide robot[J]. IEEE Transactions on Bio-Medical Engineering, 2018, 65(1): 165-177. Doi:10.1109/TBME.2017.2697766 |
| [6] |
Gao L, Zhang Y, Wang S, et al. An ultrasound-guided robot assisted system for percutaneous facet joint puncture: an experimental study[J]. Chinese Journal of Orthopaedic Trauma, 2022, 24(10): 869-73. |
| [7] |
Taguchi K, Hamamoto S, Okada A, et al. Robot-assisted fluoroscopy versus ultrasound-guided renal access for nephrolithotomy: a phantom model benchtop study[J]. Journal of Endourology, 2019, 33(12): 987-994. Doi:10.1089/end.2019.0432 |
| [8] |
Becker B C, Voros S, Lobes L A, et al. Retinal vessel cannulation with an image-guided handheld robot[C]//2010 Annual International Conference of the IEEE Engineering in Medicine and Biology. August 31-September 4, 2010, Buenos Aires, Argentina. IEEE, 2010: 5420-5423. DOI: 10.1109/IEMBS.2010.5626493.
|
| [9] |
Gijbels A, Willekens K, Esteveny L, et al. Towards a clinically applicable robotic assistance system for retinal vein cannulation[C]//2016 6th IEEE International Conference on Biomedical Robotics and Biomechatronics (BioRob). June 26-29, 2016, Singapore. IEEE, 2016: 284-291. DOI: 10.1109/BIOROB.2016.7523639.
|
| [10] |
Chen S H, Wang F, Lin Y P, et al. Ultrasound-guided needle insertion robotic system for percutaneous puncture[J]. International Journal of Computer Assisted Radiology and Surgery, 2021, 16(3): 475-484. Doi:10.1007/s11548-020-02300-1 |
| [11] |
He T B, Guo C Q, Jiang L. Puncture site decision method for venipuncture robot based on near-infrared vision and multiobjective optimization[J]. Science China Technological Sciences, 2023, 66(1): 13-23. Doi:10.1007/s11431-022-2232-5 |
| [12] |
Perry T S. Profile: Veebot drawing blood faster and more safely than a human can[J]. IEEE Spectrum, 2013, 50(8): 23-23. Doi:10.1109/mspec.2013.6565554 |
| [13] |
Balter M L, Chen A I, Maguire T J, et al. The system design and evaluation of a 7-DOF image-guided venipuncture robot[J]. IEEE Transactions on Robotics: a Publication of the IEEE Robotics and Automation Society, 2015, 31(4): 1044-1053. Doi:10.1109/TRO.2015.2452776 |
| [14] |
Chen A I, Balter M L, Maguire T J, et al. Real-time needle steering in response to rolling vein deformation by a 9-DOF image-guided autonomous venipuncture robot[J]. Proceedings of IEEE/RSJ International Conference on Intelligent Robots and Systems, 2015, 2633-2638. Doi:10.1109/IROS.2015.7353736 |
| [15] |
Balter M L, Chen A I, Fromholtz A, et al. System design and development of a robotic device for automated venipuncture and diagnostic blood cell analysis[J]. Proceedings of IEEE/RSJ International Conference on Intelligent Robots and Systems, 2016, 514-520. Doi:10.1109/IROS.2016.7759102 |
| [16] |
Leipheimer J M, Balter M L, Chen A I, et al. First-in-human evaluation of a hand-held automated venipuncture device for rapid venous blood draws[J]. Technology, 2019, 7(3/4): 98-107. Doi:10.1142/S2339547819500067 |
| [17] |
Kobayashi Y, Hong J, Hamano R, et al. Development of a needle insertion manipulator for central venous catheterization[J]. The International Journal of Medical Robotics + Computer Assisted Surgery: MRCAS, 2012, 8(1): 34-44. Doi:10.1002/rcs.420 |
| [18] |
Ahmad Khan M U, Yi B J. Design and clinical test of a passive ultrasound probe holder mechanism for arterial puncturing[J]. International Journal of Control, Automation and Systems, 2020, 18(1): 29-37. Doi:10.1007/s12555-019-0233-z |
| [19] |
Quan Z F, Zhang L, Zhou C, et al. Acoustic shadowing facilitates ultrasound-guided radial artery cannulation in young children[J]. Anesthesiology, 2019, 131(5): 1018-1024. Doi:10.1097/ALN.0000000000002948 |
| [20] |
Kimori K, Sugama J. Investigation of vasculature characteristics to improve venepuncture techniques in hospitalized elderly patients[J]. International Journal of Nursing Practice, 2016, 22(3): 300-306. Doi:10.1111/ijn.12430 |
 2025, Vol. 42
2025, Vol. 42 


