2. 临沂科技职业学院,山东 临沂 276000;
3. 山东高速集团有限公司创新研究院,山东 济南 250001
厌氧氨氧化(Anaerobic Ammonium Oxidation,ANAMMOX)是一种新型生物脱氮工艺,相较于传统的生物脱氮工艺,具有不需供氧、无需外加有机碳源、污泥产量低、脱氮效率高等优势,从而节省运行费用和能源消耗,可实现高效生物脱氮[1]。ANAMMOX工艺在废水脱氮领域特别是高氨氮、低C/N废水脱氮中具有广阔的应用潜力。厌氧氨氧化菌(Anaerobic Ammonia Oxidation Bacteria,AnAOB)是ANAMMOX反应的功能菌,在厌氧条件下,AnAOB利用NO2--N作为电子受体、NH4+-N作为电子供体进行生化反应,将氮污染物转化为N2形式从反应体系中逸出从而去除[2]。
AnAOB生长缓慢(μmax仅为0.002 7 h-1),倍增时间长(15~30 d),其生长速率、代谢活性易受环境、水质条件等影响[3],从而难以获得ANAMMOX种泥,导致工艺启动时间长且极易失稳,限制了该工艺的大规模工程化应用。2002年,世界上首个大规模ANAMMOX反应器在鹿特丹启动,耗时3.5年[4]。大多数序批式活性污泥反应器以活性污泥作为接种物,在约4个月或更长时间内才可成功启动ANAMMOX工艺[5]。食品加工、工业生产和畜禽养殖等行业均产生高氨氮废水,且同时具有高盐属性[6],AnAOB对盐度较为敏感[7],高盐会影响AnAOB的生长繁殖,抑制AnAOB的活性,导致ANAMMOX工艺更难启动及长期稳定高效运行。因此,实现高盐下ANAMMOX工艺的快速启动及稳定运行将提升我国氮污染防治工作实效与进度,具有重要的环境效益和社会意义。
目前,针对ANAMMOX工艺启动研究集中于无盐或低盐含氮废水,少有高盐环境下的启动研究。Jiang等[8]通过细胞固定富集和保留部分反硝化-ANAMMOX过程的关键功能细菌,实现无盐条件下ANAMMOX工艺的快速启动,经ANAMMOX过程的脱氮贡献高达77.10%。Li等[9]通过接种无盐的硝化污泥和ANAMMOX颗粒污泥混合物,于120 d成功启动UASB-ANAMMOX反应器。Zhang等[10]在接种污泥中加入增强的ANAMMOX颗粒,促进了ANAMMOX生物膜工艺在无盐低温下的成功启动。高盐下ANAMMOX的研究主要集中于高盐对ANAMMOX工艺性能及稳定性影响方面。Li等[11]研究得出,当盐浓度提升至18 g/L时,ANAMMOX-UASB反应器总氮(Total Nitrogen,TN)去除率降至50%。Wang等[12]研究发现,盐浓度低于12 g/L时AnAOB活性较无盐环境下略有提高,而当盐浓度高于12 g/L时会显著抑制AnAOB活性。
ANAMMOX工艺在高盐含氮废水中应用所采取的策略为:首先在低盐含氮废水中启动ANAMMOX工艺以获取种泥,然后通过逐步提高盐度驯化种泥来提高AnAOB耐盐性及脱氮活性,进而实现高盐下ANAMMOX工艺的稳定运行。在实际工程中,ANAMMOX种泥甚少,无法满足工程需求,且逐步提高盐度驯化种泥耗时长。因此,若在高盐下实现ANAMMOX工艺启动,则可同步解决耗时长、种泥少的难题。厌氧反硝化颗粒污泥来源广泛、易于获取、高氨氮适应性强、沉降性能好,且高盐下具有较高的脱氮活性[13]。Tsushima等[14]在反硝化污泥中发现了ANAMMOX活性。研究表明,氨可以被用作代替电子供体来改善厌氧反硝化反应,这为厌氧体系中由反硝化反应转变成ANAMMOX反应提供了理论依据[15]。据此,本研究以耐高盐的高活性厌氧反硝化颗粒污泥作为启动种泥,在高盐环境下富集AnAOB菌群,研究高盐下ANAMMOX工艺启动特性,考察高盐下ANAMMOX-UASB启动运行过程中的脱氮性能,以期为ANAMMOX工艺在高盐含氮废水脱氮处理工程中的应用提供理论依据与技术支持。
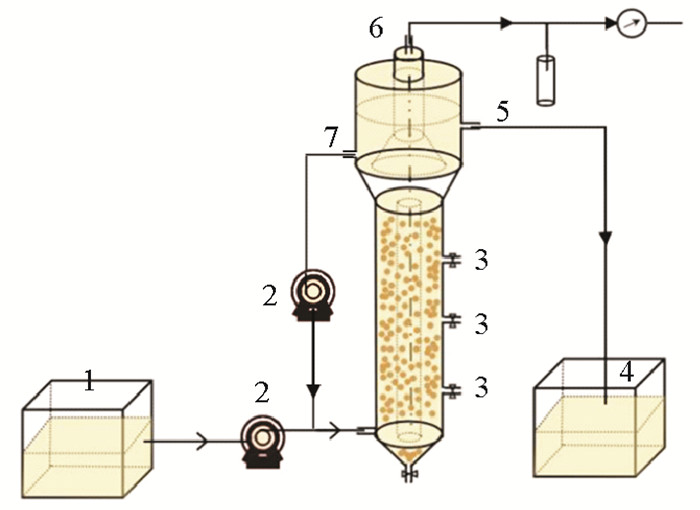
1 材料与方法 1.1 试验装置高盐环境下ANAMMOX工艺启动所采用的升流式厌氧污泥床(Upflow anaerobic sludge blanket,UASB)反应器由有机玻璃制成(见图 1),UASB反应器由进水区、反应区、沉淀区三部分组成,整体呈圆柱状。UASB反应装置的有效体积为1.4 L,高度为80 cm,其中反应区内径为6 cm,高度为50 cm。试验废水由进水蠕动泵连续泵入UASB反应器进水区,经布水器均匀布水后进入反应区,并在此与颗粒污泥进行充分接触、反应。废水中的污染物在反应区进行有效降解后进入沉淀区,在沉淀区三相分离器作用下气、液、固得以有效分离,反应器污泥重新回到反应区,反应产生的气体由反应器顶端排气孔排出并收集,经处理后的废水部分由回流蠕动泵重新泵入反应器,其它部分则经溢流堰排出。UASB反应器试验期间维持(35±1) ℃恒温条件,同时为避免光照对ANAMMOX反应的不利影响反应器整体用黑布裹覆。
|
( 1.进水箱;2.蠕动泵;3.取样口;4.出水箱;5.出水口;6.排气口;7.回流口。1. Influent tank; 2. Peristaltic pump; 3. Sample ports; 4. Effluent tank; 5. Effluent outlet; 6. Exhaust biogas; 7. Recycling port. ) 图 1 ANAMMOX-UASB试验装置系统 Fig. 1 Schematic diagram of ANAMMOX-UASB reactor system |
试验接种污泥为实验室厌氧反硝化UASB反应器中的颗粒污泥,该反应器已在高盐环境下稳定运行一年多,氮容积负荷(Nitrogen loading rate,NLR)、氮容积去除负荷(Nitrogen removal rate,NRR)分别为24.00 kg/(m3·d)、23.06 kg/(m3·d)。接种污泥平均粒径为2.50 mm,混合液悬浮固体浓度(Mixed liquor suspended solids,MLSS)约为68.13 g/L,混合液挥发性悬浮固体浓度(Mixed liquor volatile suspended solids,MLVSS)约为53.82 g/L,MLVSS/MLSS为0.79。ANAMMOX-UASB反应器启动试验的颗粒污泥接种量为1.20 L。
1.3 试验废水试验所用高盐含氮废水为人工配制,成分为(mg/L):KH2PO427.2,NaHCO3 500,CaCl2·2H2O 136,MgSO4·7H2O 300,海水晶30 000(含盐量3%);废水中微量元素Ⅰ和Ⅱ溶液含量为1 mL/L,NH4+-N和NO2--N分别由NH4Cl和NaNO2按需提供(见表 1);废水初始pH调至7.5~7.8之间。微量元素Ⅰ溶液组成成分及含量(mg/L):EDTA 5 000,FeSO4·7H2O 5 000。微量元素Ⅱ溶液组成成分及含量(mg/L):EDTA 15 000,MnCl2·4H2O 990,CuSO4·5H2O 250,ZnSO4·7H2O 430,H3BO4 14,NiCl2·6H2O 190,Na2MoO4·2H2O 220。
|
|
表 1 试验运行方案 Table 1 Experiment operation strategy |
常规指标包括NH4+-N、NO2--N、NO3--N、pH等测定,均采用国家标准方法[16],其中,NH4+-N:纳氏试剂分光光度法;NO2--N:N-(1-萘基)乙二胺分光光度法;NO3--N:紫外分光光度法;pH:玻璃电极法;MLSS、MLVSS:重量法。
氮容积负荷(NLR)、氮容积去除负荷(NRR)分别按式(1)和式(2)计算:
| $ N L R=\frac{c_{\text {inf }} \times 24}{H R T}, $ | (1) |
| $ N R R=\frac{\left(c_{\text {inf }}-c_{\text {eff }}\right) \times 24}{H R T} 。$ | (2) |
式中:cinf、ceff分别为进、出水TN浓度(mg/L);HRT为水力停留时间(h)。
1.4.2 Heme c的测定采用吡啶血红素分光光度法[17]测定Heme c(血红素C)含量。取1 g湿污泥用10 mmol·L-1 PBS缓冲液冲洗3次后定容至12 mL,碾磨成匀浆后用超声细胞破碎仪进行破碎(功率130 W,超声5 s,间隔5 s,总时间4 min),低温高速(4 ℃、10 000 r·min-1)离心15 min后获取样品上清液。向两个比色管中均加入1.5 mL样品上清液、1.5 mL混合液(200 mmol·L-1 NaOH+40%吡啶),向一个比色管中加入0.03 mmol·L-1的铁氰化钾溶液20 μL,测定550、535 nm波长下样品吸光值,记为A5503+、A5353+。向另一个比色管中加入0.04 g连二亚硫酸钠、20 μL超纯水,测定550、535 nm波长处样品吸光值,记为A5502+、A5352+。Heme c含量按式(3)计算。
| $ C=\frac{12 \times\left[\left(A_{550}^{2+}-A_{550}^{3+}\right)-\left(A_{535}^{2+}-A_{535}^{3+}\right)\right]}{M L V S S \times 23.97} 。$ | (3) |
酶的提取依据Lin等[18]的提取方法。AnAOB中硝酸盐还原酶(Nitrate reductase,Nar)、亚硝酸盐还原酶(Nitrite reductase,Nir)活性测定采用Michael等[19]的方法,以单位时间、单位蛋白下NO2--N的生成量和消耗量表示。联氨氧化酶(Hydrazine oxidase,HZO)活性测定采用联氨-细胞色素c分光光度法[20],以单位时间、单位蛋白还原细胞色素c的量来表征。联氨合成酶(Hydrazine synthase,HZS)活性利用双抗体夹心酶联免疫吸附(ELISA)方法[21]测定。
1.4.4 微生物群落分析采集的污泥样品委托北京诺禾致源生物信息科技有限公司进行样品DNA提取、PCR扩增及高通量测序。采用细菌16S rRNA基因V3+V4扩增区域,引物为341F(CCTACGGGNGGCWGCAG)和805R(GACTACHVGGGTATCTAATCC),PCR扩增体系、条件参照文献[22]方法,采用Illumina HiSeq高通量测序技术进行测序。
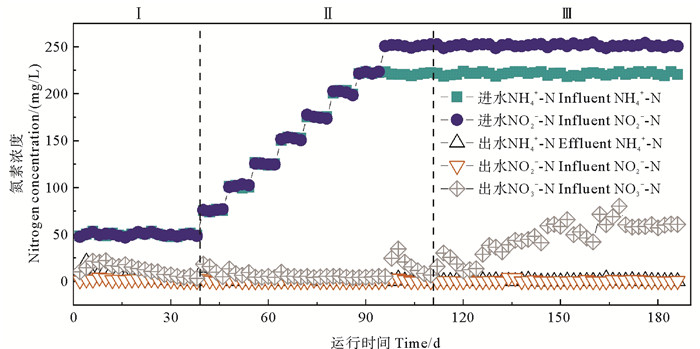
2 结果与讨论 2.1 高盐环境下ANAMMOX-UASB启动过程脱氮特性 2.1.1 氮污染物去除高盐环境下成功启动ANAMMOX-UASB反应器耗时186 d,具体试验方案见表 1,启动过程氮污染物变化如图 2所示。ANAMMOX-UASB反应器高盐启动过程依据氮素变化特征[23-24]可分为:ANAMMOX活性迟滞期(见图 2中Ⅰ)、活性提高期(见图 2中Ⅱ)、活性稳定期(见图 2中Ⅲ)。
|
图 2 高盐下ANAMMOX-UASB启动过程中的氮素变化 Fig. 2 Nitrogen pollutants changes during ANAMMOX-UASB startup process under high salinity |
在活性迟滞期(0~39 d),进水NH4+-N和NO2--N浓度均为50 mg/L,HRT为24 h。在此阶段,出水NH4+-N浓度先升后降,由9.01 mg/L(第1天)逐步升至20 mg/L(第4天)后缓慢降低,逐步降至0.85 mg/L(第39天)。不同于无盐环境下启动ANAMMOX工艺,此阶段出水NH4+-N浓度始终低于进水浓度,而无盐环境下启动ANAMMOX工艺的初期常出现出水NH4+-N浓度高于进水NH4+-N浓度现象[10, 25]。原因可能为高盐会抑制氨化细菌活性,菌体自溶过程产生的有机氮无法转化成NH4+-N,致使高盐下活性迟滞期出水NH4+-N浓度较无盐环境低。出水NO2--N浓度较低(4.05~0.24 mg/L),初期NO2--N去除率有所波动,从78.52%(第1天)降至56.14%(第10天),后逐渐提高至93.35%(第39天)。因接种污泥为厌氧反硝化污泥,可直接利用异养菌自溶过程产生的内源有机物进行厌氧反硝化,因而出水NO2--N浓度较低。出水NO3+-N浓度为先升后降,第10天出水NO3+-N浓度最大,为22 mg/L,推测可能与NO2--N的氧化有关,研究表明高盐环境下NO2--N的氧化可催化电子补充醌池产生还原力,为自身合成代谢供能[26]。ANAMMOX反应的特征是NH4+-N和NO2--N的同步去除并伴有NO3--N的生成,此阶段出水NH4+-N和NO2--N浓度出现同步下降,且降幅逐步变大,结合2.2.2和2.2.3中Heme c含量、功能酶活性也较接种污泥有所增加,2.2.4中厌氧氨氧化菌属丰度变高,表明此阶段已经逐步显现ANAMMOX反应,受此影响NH4+-N和NO2--N消耗量之比(Rs)、NH4+-N消耗量与NO3+-N生成量之比(Rp)变化均出现较大波动(见图 3)。但因出水NO3--N浓度较低,反应体系仍以厌氧反硝化过程为主。
|
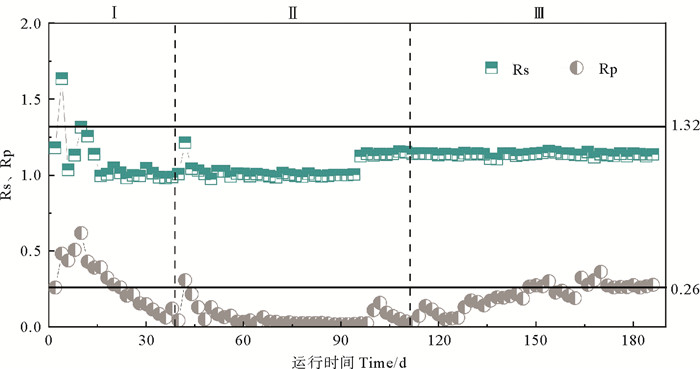
图 3 高盐下ANAMMOX-UASB启动过程的反应化学计量比 Fig. 3 The stoichiometric ratio of ANAMMOX during start-up processunder high salinity |
在活性提高期(40~110 d),以25 mg/L的浓度步幅分别将进水NH4+-N、NO2--N浓度由50 mg/L逐渐提升至225和250 mg/L,HRT保持不变。在此阶段,出水NH4+-N、NO2--N浓度均会因进水基质浓度的改变出现短暂波动后稳定,随着运行时间的延长,提升基质浓度所产生的出水NH4+-N、NO2--N浓度波动幅度逐渐降低,从而反应体系可逐步适应进水负荷变化引起的冲击。在此阶段,进水NH4+-N、NO2--N浓度由50 mg/L提升至225 mg/L,出水NH4+-N和NO2--N浓度较低(分别为0.32 mg/L、0.37 mg/L),NH4+-N和NO2--N平均去除率分别为99.86%、99.83%;出水NO3--N浓度为4.59 mg/L,出水TN浓度为5.28 mg/L,TN去除率为98.81%。当进水NH4+-N、NO2--N浓度最终各自提升至225 mg/L、250 mg/L时,出水NH4+-N和NO2--N浓度仍维持在较低浓度水平(1.62和1.23 mg/L),出水NO3--N浓度由5.37 mg/L增至34.49 mg/L后下降至6.69 mg/L,有所波动但整体呈升高趋势。活性提高阶段出水NH4+-N、NO2--N浓度较低且NO3--N浓度有所升高,结合此阶段中Rp逐渐升高(见图 3),Heme c含量、功能酶活性、厌氧氨氧化菌属丰度持续增加,故ANAMMOX活性逐渐提高,污泥反应体系的主导反应已向着ANAMMOX反应转变。朱晓桐等[23]于无盐条件下启动ANAMMOX-UASB工艺,在NH4+-N和NO2--N浓度开始出现同步下降且降幅渐大,同时出水NO3--N浓度上升时,得出结论ANAMMOX作用逐步增强并最终成为主导反应,与本试验结论一致。不过因NO3--N浓度升高后又发生降低现象,表明仍存在一定的反硝化作用消耗ANAMMOX过程中生成的NO3--N,此时的ANAMMOX反应不太稳定。
在活性稳定期(111~186 d),进水NH4+-N、NO2--N浓度维持在22、250 mg/L,HRT由24 h逐步缩至12 h。在此阶段,出水NH4+-N、NO2--N浓度稳定在0.52、0.65 mg/L,出水NO3--N浓度波动上升,由6.69 mg/L(HRT=24 h)增至58.43 mg/L(HRT=12 h)后保持稳定。研究表明厌氧反硝化菌的存在可提高AnAOB的活性从而有利于ANAMMOX工艺的启动[24],这与本试验现象一致。随着ANAMMOX-UASB的启动,Heme c含量、功能酶活性、AnAOB含量均显著增加,反硝化菌属的丰度占比总体呈下降趋势,Rs和Rp最终分别稳定在1.13和0.26,符合ANAMMOX反应的理论值(见图 3),由此可得此阶段ANAMMOX反应完全占据了主导地位并保持活性稳定,高盐条件下ANAMMOX-UASB启动成功。
因启动接种污泥、运行条件不同,无盐环境下启动ANAMMOX工艺耗时不同,时间跨度60~365 d[25]。Peng等[27]在(35±1) ℃下以成熟的厌氧颗粒污泥为接种污泥,无盐启动ANAMMOX工艺,耗时131 d。Deore R等[28]在无盐条件下利用改装过的容量为1 L的试剂瓶,以反硝化污泥作为接种污泥进行AnAOB的批量富集和ANAMMOX工艺的启动,耗时93 d。本研究在高盐环境下耗时186 d可成功启动ANAMMOX工艺,且工艺表现出良好的脱氮性能,未出现因高盐抑制而无法启动或耗时过长等问题,为高盐含氮废水的ANAMMOX工艺脱氮处理提供了新思路。
2.1.2 高盐下ANAMMOX-UASB启动过程化学计量比NH4+-N和NO2--N消耗量之比(Rs)、NH4+-N消耗量与NO3--N生成量之比(Rp)的变化可反映ANAMMOX-UASB的启动情况,高盐环境下Rs、Rp的变化情况见图 3。活性迟滞期(见图 3中Ⅰ),Rs、Rp呈较大波动,阶段后期Rs、Rp均明显低于ANAMMOX反应的理论值(1.32与0.26),此阶段以厌氧反硝化作用为主。活性提高期(见图 3中Ⅱ),Rs与Rp波动幅度变小且趋于稳定,但其值同样低于ANAMMOX反应的理论值,在阶段后期(96~110 d),Rs升至1.13,Rp由0.07最终变为0.04,表明ANAMMOX反应已在竞争中获得优势,但同时仍存在一定的厌氧反硝化作用。活性稳定期(见图 3中Ⅲ),Rs稳定在1.13左右,Rp逐步提升并最终稳定在0.26左右,ANAMMOX反应在竞争中获胜,完全占据主导地位。
ANAMMOX反应在实际运行过程中受操作参数、接种种泥、微生物菌群等影响,Rs、Rp常常会偏离理论值。Zhang等[10]在无盐条件下启动ANAMMOX工艺,启动成功后Rs在1~1.8之间,Rp在0.13~0.26之间。无盐环境下ANAMMOX反应的Rs常略低于理论值[22],本试验高盐环境下ANAMMOX工艺启动成功后的Rs也低于其理论值,Rp与理论值基本一致。
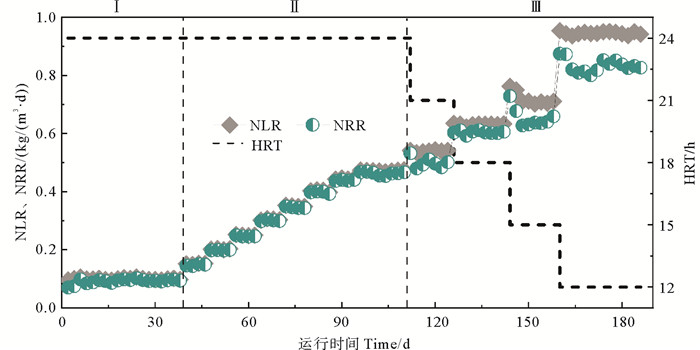
2.1.3 NLR、NRR特性ANAMMOX-UASB启动过程中NLR、NRR变化如图 4所示。活性迟滞期(见图 4中Ⅰ),NLR为0.10 kg/(m3·d),NRR为0.09 kg/(m3·d),由2.1.1分析可知此阶段出水NH4+-N、NO2--N、NO3--N浓度较低故NRR较高,此时ANAMMOX活性较低,反应体系仍以厌氧反硝化过程为主。活性提高期(见图 4中Ⅱ),NLR从0.15 kg/(m3·d)逐步提升至0.47 kg/(m3·d),相应的NRR从0.14 kg/(m3·d)增至0.46 kg/(m3·d),TN去除率维持在95.79%以上。此阶段出水NH4+-N、NO2--N浓度持续降低但NO3--N浓度有所升高,表明AnAOB活性逐步提高。由于厌氧反硝化的“伴随”,TN去除率较高,此阶段NRR为反硝化与ANANNOX共同作用的结果。活性稳定期(见图 4中Ⅲ),在NLR提升过程中NRR变幅较大,当NLR最终提至0.94 kg/(m3·d)时,因出水NO3--N浓度升高,NRR为0.83 kg/(m3·d),TN去除率为88.30%,逐步接近ANAMMOX作用的TN理论去除率(88.79%)。此阶段ANAMMOX反应完全占据了主导地位并保持活性稳定,以往研究也表明缩短HRT的方式更利于ANAMMOX工艺的快速启动[22]。NRR达到0.5 kg/(m3·d)时即可认为ANAMMOX工艺启动成功[22],本试验在进入活性稳定期后NRR超过0.5 kg/(m3·d),高盐环境下仅需186 d即可成功启动ANAMMOX-UASB反应器。
|
图 4 高盐下ANAMMOX-UASB启动过程NLR及NRR变化 Fig. 4 The characteristics of NLR and NRR during ANAMMOX-UASB startup process under high salinity |
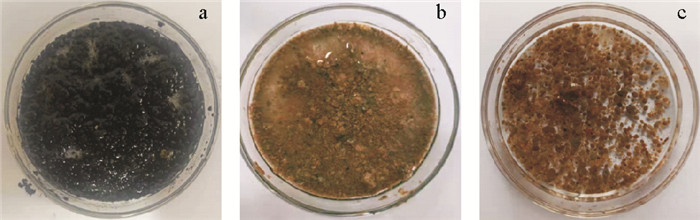
高盐环境下ANAMMOX-UASB启动过程中的污泥表观形态如图 5所示。活性迟滞期污泥(见图 5a)为黑色颗粒,颗粒大小均匀,表面光滑。活性提高期污泥(见图 5b)颜色大部分变为棕黄色,仍存在部分灰色污泥,颗粒与絮体并存,且颗粒大小不一。主要为异养微生物死亡使污泥颗粒化程度下降,并解散为絮状,异养微生物自溶形成的有机物具有粘性,使近邻污泥相互粘附,且因长HRT下水流剪切力不足,导致颗粒大小存在较大差异。活性稳定期污泥(见图 5c)已呈现出AnAOB特有的红褐色[29],且因水流剪切力的加大,可明显看出污泥的颗粒化形态,此阶段颗粒化较好。与无盐环境下ANAMMOX工艺启动相比,高盐环境下ANAMMOX工艺成功启动后污泥具有的红褐色相对较浅,初判为高盐对AnAOB活性的抑制使Heme c含量较无盐环境下含量低所致。
|
图 5 高盐下ANAMMOX-UASB启动过程污泥形态特征 Fig. 5 Sludge morphologycharacteristics during ANAMMOX-UASB start-up process under high salinity |
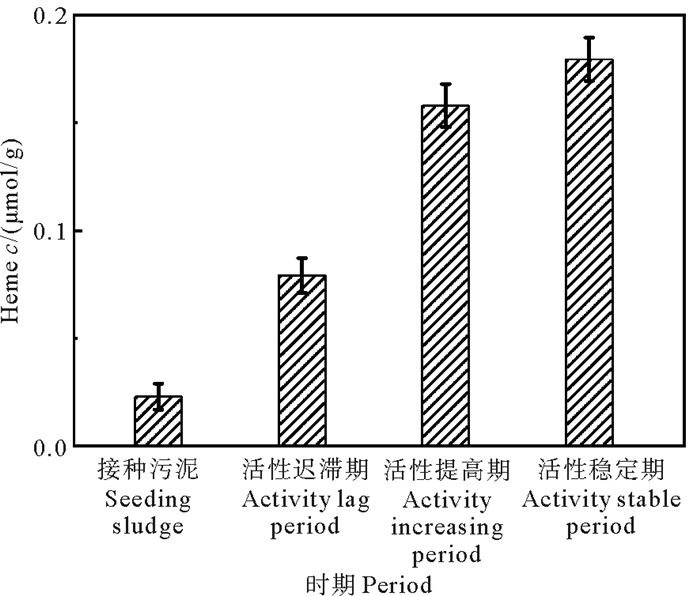
Heme c是AnAOB功能酶的重要辅基,其含量与ANAMMOX反应中功能菌的酶活密切相关,也是ANAMMOX反应中污泥呈红色的重要指示物[29]。各阶段污泥中Heme c含量见图 6。由图可得,在ANAMMOX-UASB启动过程中污泥的Heme c含量逐步增加,接种污泥、活性迟滞期污泥、活性提高期污泥和活性稳定期污泥中Heme c含量分别为0.02、0.08和0.16 μmol/g VSS、0.18 μmol/g VSS。活性稳定期污泥中Heme c含量分别是前三个时期污泥中Heme c含量的9.00、2.25和1.13倍。Zhang等[10]研究得出,无盐环境下启动ANAMMOX工艺过程中,Heme c的含量呈指数增长,与本试验的高盐环境下启动ANAMMOX工艺结果较为一致。Pearson(皮尔森)相关系数表明Heme c含量与HZO活性具有显著相关性(R=0.936,p < 0.01),Heme c含量与ANAMMOX反应的脱氮性能直接相关,在AnAOB代谢中起重要作用[28]。
|
图 6 高盐下ANAMMOX-UASB启动过程的Heme c含量 Fig. 6 Heme c content ofAnAOB during ANAMMOX-UASB start-up process under high salinity |
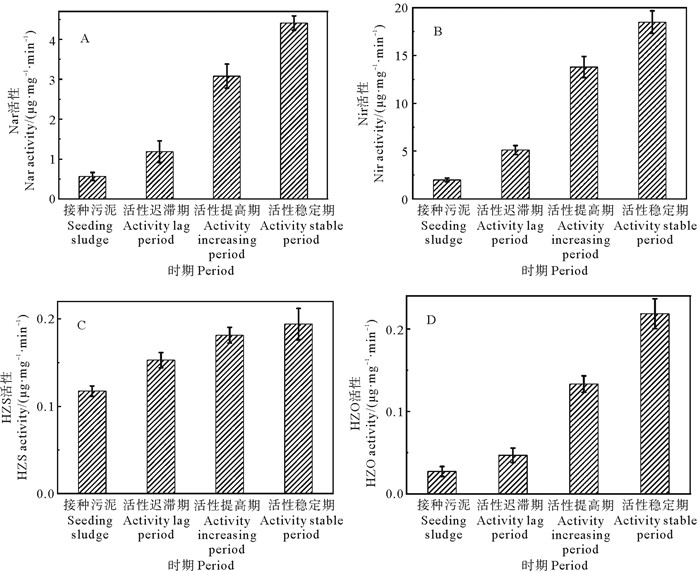
ANAMMOX反应是在多种功能酶协同作用下完成的,所涉及的脱氮功能酶主要有硝酸盐还原酶(Nar)、亚硝酸盐还原酶(Nir)、联氨氧化酶(HZO)、联氨合成酶(HZS),均位于AnAOB的菌体内部[18, 30]。在高盐环境下ANAMMOX-UASB启动过程中AnAOB脱氮功能酶活性均逐步提高(见图 7),其变化趋势与Heme c含量变化一致,Nir,HZS和HZO中均含有Heme c作辅酶[18]。Zhao等[31]研究得出,无盐环境下启动ANAMMOX工艺过程中,脱氮功能基因的丰度不断增加。
|
图 7 高盐下ANAMMOX-UASB启动过程中AnAOB功能酶活性 Fig. 7 Functional enzyme activity ofAnAOB during ANAMMOX-UASB start-up process under high salinity |
ANAMMOX-UASB启动过程中,活性迟滞期污泥、活性提高期污泥和活性稳定期污泥中Nar活性(见图 7A)较接种污泥分别增长了1.09、4.40、6.74倍,Nir活性(见图 7B)较接种污泥分别增长了1.58、5.97、8.34倍,Nar和Nir活性指示了高盐环境下ANAMMOX-UASB启动过程中亚硝酸盐的氧化与还原过程,两种酶活性的增强反映了亚硝酸盐转化动力的提高。活性迟滞期污泥、活性提高期污泥和活性稳定期污泥中HZS活性(见图 7C)较接种污泥分别增长了0.25、0.50、0.58倍,HZO活性(见图 7D)较接种污泥分别增长了0.67、3.33和6.00倍。HZS与HZO是ANAMMOX反应特有的酶,HZS催化NO与NH4+-N结合生成N2H4,HZO催化ANAMMOX反应中N2H4还原为N2[32]。相比较于其他功能酶活性,HZS酶活升幅缓慢,可推测高盐环境下NO与NH4+-N结合生成N2H4会成为高盐环境下ANAMMOX反应脱氮性能显著提升的限速反应。
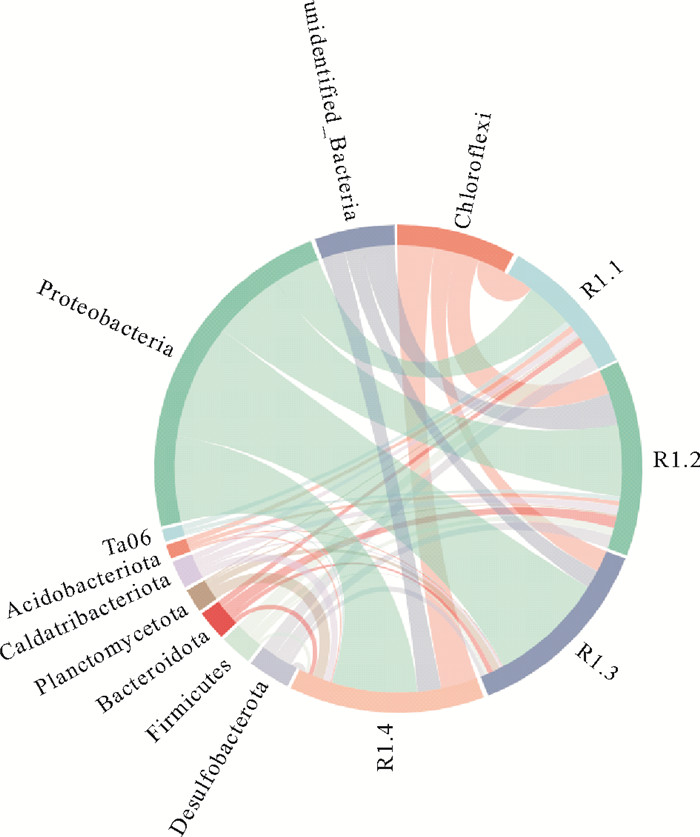
2.2.4 微生物群落结构高盐环境下ANAMMOX-UASB启动过程中,门水平下的微生物丰度分布如图 8所示。门水平下的主要优势菌门为变形菌门(Proteobacteria)、绿弯菌门(Chloroflexi)、脱硫菌门(Desulfobacterota)、厚壁菌门(Firmicutes)、拟杆菌门(Bacteroidetes)和浮霉菌门(Planctomycetes),高盐环境下ANAMMOX工艺启动过程中微生物优势菌群结构与无盐环境下启动基本一致[31]。AnAOB属于浮霉菌门,高盐环境下ANAMMOX-UASB启动阶段接种污泥、活性迟滞期污泥、活性提高期污泥、活性稳定期污泥中浮霉菌门占比分别为0.99%、1.06%、4.26%、6.05%,浮霉菌门丰度不断增加,活性稳定期污泥中浮霉菌门占比为接种污泥的6.11倍。
|
( R1.1为接种污泥;R1.2为活性迟滞期;R1.3活性提高期;R1.4活性稳定期。R1.1 was seeding sludge; R1.2 was activity lag period; R1.3 was activity increasing period; R1.4 was activity stable period. ) 图 8 高盐下ANAMMOX-UASB启动过程中门水平微生物分布 Fig. 8 Microbial distribution at phylum level during ANAMMOX-UASB start-up process under high salinity |
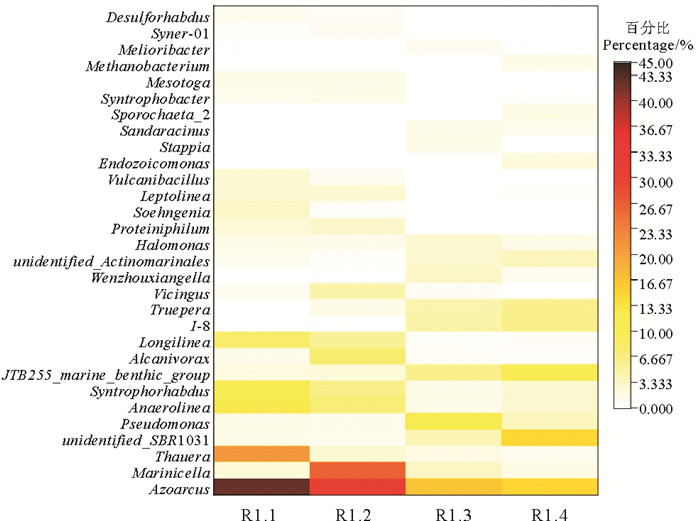
高盐环境ANAMMOX-UASB启动过程,微生物属水平(前30)丰度图见图 9。具有反硝化功能的相对高丰度的菌属包括固氮弧菌(Azoarcus)、陶厄氏菌属(Thauera)、绿脓杆菌(Pseudomonas)。反硝化功能菌在接种污泥、活性迟滞期污泥、活性提高期污泥、活性稳定期污泥的丰度占比分别为37.61%、20.58%、56.26%、35.46%,ANAMMOX-UASB启动过程其丰度呈下降趋势。浮霉菌门属水平上的丰度情况见图 10,共发现了3个属的AnAOB,分别为Candidatus_Anammoximicrobium,Candidatus_Jettenia和Candidatus_Brocadia。AnAOB菌属丰度持续增加,在活性迟滞期、活性提高期、活性稳定期的丰度占比分别是接种污泥的1.26、1.62、2.12倍。接种污泥中虽含微量AnAOB,但因其丰度低无法具备厌氧氨氧化脱氮能力。启动过程反硝化菌属丰度逐渐下降,厌氧氨氧化菌属丰度占比逐步提升。
|
( R1.1为接种污泥;R1.2为活性迟滞期;R1.3活性提高期;R1.4活性稳定期。R1.1 was seeding sludge; R1.2 was activity lag period; R1.3 was activity increasing period; R1.4 was activity stable period. ) 图 9 高盐下ANAMMOX-UASB启动过程中微生物属水平丰度 Fig. 9 Microbial abundance at genus level during ANAMMOX-UASB start-up process under high salinity |
|
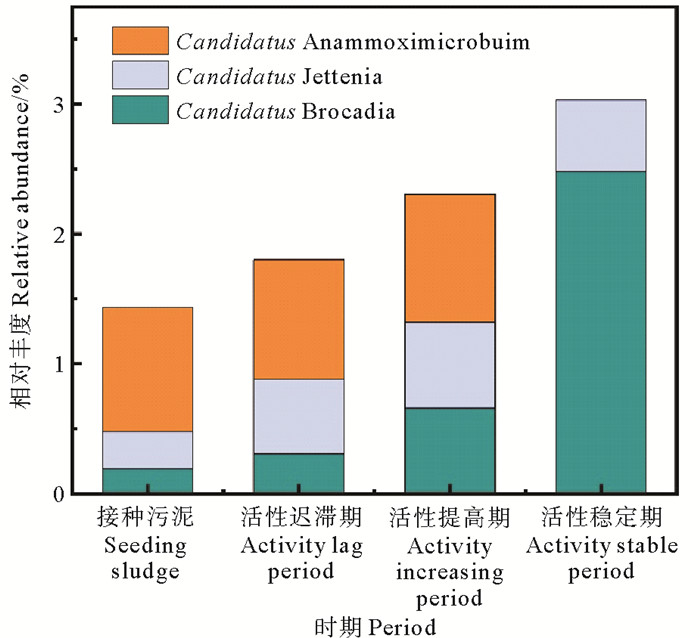
图 10 高盐下ANAMMOX-UASB启动过程中AnAOB丰度 Fig. 10 AnAOB abundance during ANAMMOX-UASB start-up process under high salinity |
活性迟滞期、活性提高期的优势菌均为Candidatus_Anammoximicrobium,但Candidatus_Jettenia、Candidatus_Brocadia丰度较接种污泥均逐步提升,Candidatus_Jettenia分别增长了1.03、1.32倍;Candidatus_Brocadia分别增长了0.58、2.45倍。在活性稳定期,Candidatus_Brocadia成为优势菌群,丰度是接种污泥的12.98倍。Candidatus_Jettenia丰度较活性提高期降低了16.39%,且不存在Candidatus_Anammoximicrobium。在无盐环境下启动ANAMMOX工艺过程中,Candidatus_Kuenenia常为优势菌属[8, 10, 24],与本试验高盐环境下启动的优势菌属差异较大,这也与接种的高盐厌氧反硝化颗粒污泥中的土著微生物有关。Candidatus_Brocadia属于r-策略型细菌,具有相对较高的增长速率和较低的基质亲和性[33],高盐环境下AnAOB细胞生长缓慢,较高的生长速率利于其生长繁殖成为优势菌属,因此高盐环境下Candidatus_Brocadia在与Candidatus_Jettenia、Candidatus_Anammoximicrobium竞争过程中更具优势从而成为优势菌群。
3 结论(1) 高盐环境下可成功启动ANAMMOX-UASB反应器,耗时仅为186 d,解决了高盐抑制无法启动或耗时过长问题。脱氮效能未受高盐环境影响,TN去除率为87.5%以上,成功启动后的Rs、Rp值分别稳定在1.13、0.26。
(2) 高盐环境下ANAMMOX-UASB启动过程中Heme c含量、功能酶活性不断提升,启动成功后Heme c含量、Nar活性、Nir活性、HZS活性、HZO活性分别为接种污泥的9.00倍、7.74、9.34、1.58和7.00倍。
(3) 高盐环境下ANAMMOX-UASB启动过程中,AnAOB所属的浮霉菌门占比由0.99%增至6.05%。反硝化菌属的丰度占比下降,厌氧氨氧化菌属丰度占比增加,活性稳定期的丰度总占比是接种污泥的2.12倍。高盐环境下启动成功后的厌氧氨氧化优势菌属为Candidatus_Brocadia,占比为2.48%。
| [1] |
McCarty P L. What is the best biological process for nitrogen removal: When and why?[J]. Environmental Science & Technology, 2018, 52(7): 3835-3841. (  0) 0) |
| [2] |
Liu Y X, Xu W, Bao L, et al. Cell surface characterization and trace metal adsorptive properties of anaerobic ammonium-oxidizing (anammox) consortia[J]. Chemosphere, 2019, 221: 11-20. DOI:10.1016/j.chemosphere.2019.01.025 (  0) 0) |
| [3] |
Lu Y Y, Wang J T, Feng Y, et al. Nitrogen removal performance and rapid start-up of anammox process in an electrolytic sequencing batch reactor (ESBR)[J]. Chemosphere, 2022, 308: 136293. DOI:10.1016/j.chemosphere.2022.136293 (  0) 0) |
| [4] |
van der Star W R L, Abma W R, Blommers D, et al. Startup of reactors for anoxic ammonium oxidation: Experiences from the first full-scale anammox reactor in rotterdam[J]. Water Research, 2007, 41(18): 4149-4163. DOI:10.1016/j.watres.2007.03.044 (  0) 0) |
| [5] |
Wang T, Zhang H M, Yang F L, et al. Start-up of the anammox process from the conventional activated sludge in a membrane bioreactor[J]. Bioresource Technology, 2009, 100(9): 2501-2506. DOI:10.1016/j.biortech.2008.12.011 (  0) 0) |
| [6] |
Zhang A Y, Wang S, Yang M M, et al. Influence of NaCl salinity on the aggregation performance of anammox granules[J]. Journal of Water Process Engineering, 2021, 39: 101687. DOI:10.1016/j.jwpe.2020.101687 (  0) 0) |
| [7] |
Wu D, Li G F, Shi Z J, et al. Co-inhibition of salinity and Ni(Ⅱ) in the ANAMMOX-UASB reactor[J]. Science of The Total Environment, 2019, 669: 70-82. DOI:10.1016/j.scitotenv.2019.03.130 (  0) 0) |
| [8] |
Jiang H, Wang Z, Ren S, et al. Enrichment and retention of key functional bacteria of partial denitrification-Anammox (PD/A) process via cell immobilization: A novel strategy for fast PD/A application[J]. Bioresource Technology, 2021, 326: 124744. DOI:10.1016/j.biortech.2021.124744 (  0) 0) |
| [9] |
Li Y, Cui N, Xuan K, et al. Start-up performance and process kinetics of a UASB-Anammox reactor at low substrate concentration[J]. Journal of Environmental Chemical Engineering, 2021, 9(6): 106726. DOI:10.1016/j.jece.2021.106726 (  0) 0) |
| [10] |
Zhang Y, Zhang J, Li J, et al. Fast start-up of ANAMMOX biofilm processes at low temperatures by economical quorum sensing regulation: The importance of endogenous N-acyl-homoserine lactones from enhanced inoculated sludge[J]. Environmental Research, 2022, 214: 114097. DOI:10.1016/j.envres.2022.114097 (  0) 0) |
| [11] |
Li X, Yuan Y, Yuan Y, et al. Effects of salinity on the denitrification efficiency and community structure of a combined partial nitritation-anaerobic ammonium oxidation process[J]. Bioresource Technology, 2018, 249: 550-556. DOI:10.1016/j.biortech.2017.10.037 (  0) 0) |
| [12] |
Wang G J, Tang Z K, Wei J, et al. Effect of salinity on anammox nitrogen removal efficiency and sludge properties at low temperature[J]. Environmental Technology, 2020, 41(22): 2920-2927. DOI:10.1080/09593330.2019.1588384 (  0) 0) |
| [13] |
于冰洁, 朱晓桐, 栾亚萍, 等. 盐度对上流式厌氧污泥反应器脱氮性能的影响[J]. 中国海洋大学学报(自然科学版), 2021, 51(12): 97-106. Yu B J, Zhu X T, Luan Y P, et al. The influence of salinity on the denitrification performance of DN-UASB reactor[J]. Periodical of Ocean University of China, 2021, 51(12): 97-106. DOI:10.16441/j.cnki.hdxb.20210010 (  0) 0) |
| [14] |
Tsushima I, Ogasawara Y, Kindaichi T, et al. Development of high-rate anaerobic ammonium-oxidizing (anammox) biofilm reactors[J]. Water Research, 2007, 41(8): 1623-1634. DOI:10.1016/j.watres.2007.01.050 (  0) 0) |
| [15] |
Cervantes F J, De la Rosa D A, Gómez J. Nitrogen removal from wastewaters at low C/N ratios with ammonium and acetate as electron donors[J]. Bioresource Technology, 2001, 79(2): 165-170. DOI:10.1016/S0960-8524(01)00046-3 (  0) 0) |
| [16] |
国家环境保护总局《水和废水监测分析方法》编委会. 水和废水监测分析方法第四版[M]. 北京: 中国环境科学出版社, 2002: 261-282. Editorial Board of Water and Wastewater Monitoring and Analysis Method, State Environmental Protection Administration. Water and Wastewater Monitoring and Analysis Method 4th ed[M]. Beijing: China Environmental Science Press, 2002: 261-282. (  0) 0) |
| [17] |
Berry E A, Trumpower B L. Simultaneous determination of hemes a, b, and c from pyridine hemochrome spectra[J]. Analytical Biochemistry, 1987, 161(1): 1-15. DOI:10.1016/0003-2697(87)90643-9 (  0) 0) |
| [18] |
Lin Q J, Kang D, Zhang M, et al. The performance of anammox reactor during start-up: Enzymes tell the story[J]. Process Safety and Environmental Protection, 2019, 121: 247-253. DOI:10.1016/j.psep.2018.10.029 (  0) 0) |
| [19] |
Meincke M, Bock E, Kastrau D, et al. Nitrite oxidoreductase from Nitrobacter hamburgensis: Redox centers and their catalytic role[J]. Archives of Microbiology, 1992, 158(2): 127-131. DOI:10.1007/BF00245215 (  0) 0) |
| [20] |
Shimamura M, Nishiyama T, Shigetomo H, et al. Isolation of a multiheme protein with features of a hydrazine-oxidizing enzyme from an anaerobic ammonium-oxidizing enrichment culture[J]. Applied and Environmental Microbiology, 2007, 73(4): 1065-1072. DOI:10.1128/AEM.01978-06 (  0) 0) |
| [21] |
戴劲. 大环内酯类抗生素对Anammox脱氮性能的影响及机理研究[D]. 湘潭: 湘潭大学环境与资源学院, 2020. Dai J. Effect of Macrolide Antibiotic on Anammox Nitrogen Removal Performance and Its Mechanism[D]. Xiangtan: College of Environment and Resources, Xiangtan University, 2020. (  0) 0) |
| [22] |
Tao Y Q, Shi R, Peng L R, et al. Start-up characteristics and microbial nitrogen removal mechanisms in ANAMMOX systems with different inoculations under prolonged starvation[J]. Process Safety and Environmental Protection, 2022, 167: 423-433. DOI:10.1016/j.psep.2022.09.029 (  0) 0) |
| [23] |
朱晓桐, 于冰洁, 林久淑, 等. ANAMMOX-UASB反应器启动特性[J]. 环境科学与技术, 2020, 43(12): 143-150. Zhu X T, Yu B J, Lin J S, et al. Startup characteristics of ANAMMOX-UASB reactor[J]. Environmental Science & Technology, 2020, 43(12): 143-150. DOI:10.19672/j.cnki.1003-6504.2020.12.020 (  0) 0) |
| [24] |
王思琦, 李贇, 陈福明, 等. 低接种量条件下实现厌氧氨氧化快速启动的策略[J]. 环境工程学报, 2022, 16(3): 999-1007. Wang S Q, Li Y, Chen F M, et al. Strategy on fast start-up of anaerobic ammonia oxidation under low inoculation conditions[J]. Chinese Journal of Environmental Engineering, 2022, 16(3): 999-1007. (  0) 0) |
| [25] |
张海芹, 陈重军, 王建芳, 等. 厌氧氨氧化启动过程及特性研究进展[J]. 化工进展, 2014, 33(8): 2180-2186. Zhang H Q, Chen C J, Wang J F, et al. Start-up and related characteristics of anaerobic ammonia oxidation processes: A review[J]. Chemical Industry and Engineering Progress, 2014, 33(8): 2180-2186. (  0) 0) |
| [26] |
Kartal B, van Niftrik L, Keltjens J T, et al. Anammox-growth physiology, cell biology, and metabolism[J]. Advances in Microbial Physiology, 2012, 60: 211-262. (  0) 0) |
| [27] |
Peng L R, Shi R, Tao Y Q, et al. Starting up anammox system with high efficiency nitrogen removal at low temperatures: Performance optimization, sludge characterization and microbial community analysis[J]. Journal of Environmental Management, 2023, 325: 116542. DOI:10.1016/j.jenvman.2022.116542 (  0) 0) |
| [28] |
Deore R, Kumar R, Waqqas Mirza M, et al. Selecting suitable seed sludge for anammox enrichment: Role of influent characteristics and reactor operational conditions[J]. Bioresource Technology, 2022, 347: 126719. DOI:10.1016/j.biortech.2022.126719 (  0) 0) |
| [29] |
Ma H Y, Zhang Y L, Xue Y, et al. Relationship of heme c, nitrogen loading capacity and temperature in anammox reactor[J]. Science of The Total Environment, 2019, 659: 568-577. DOI:10.1016/j.scitotenv.2018.12.377 (  0) 0) |
| [30] |
Zhang Q, Lin J G, Kong Z, et al. A critical review of exogenous additives for improving the anammox process[J]. Science of The Total Environment, 2022, 833: 155074. DOI:10.1016/j.scitotenv.2022.155074 (  0) 0) |
| [31] |
Zhao Y, Li J W, Liu Q Y, et al. Fast start-up and stable operation of mainstream anammox without inoculation in an A2/O process treating low COD/N real municipal wastewater[J]. Water Research, 2023, 231: 119598. DOI:10.1016/j.watres.2023.119598 (  0) 0) |
| [32] |
白刃, 贺纪正, 沈菊培, 等. 厌氧铵氧化过程中关键酶及相关分子标记在生态学研究中的应用进展[J]. 生态学报, 2016, 36(13): 3871-3881. Bai R, He J Z, Shen J P, et al. Review of the key enzymes in the anammox process and ecological inferences derived from related molecular markers[J]. Acta Ecologica Sinica, 2016, 36(13): 3871-3881. (  0) 0) |
| [33] |
van der Star W R, Miclea A I, van Dongen U G, et al. The membrane bioreactor: A novel tool to grow anammox bacteria as free cells[J]. Biotechnology and Bioengineering, 2008, 101(2): 286-294. DOI:10.1002/bit.21891 (  0) 0) |
2. Linyi Vocational College of Science and Technology, Linyi 276000, China;
3. Shandong Hi-speed Group Innovation Research Institute, Jinan 250001, China
 2023, Vol. 53
2023, Vol. 53


