湿地生态系统是地球上生产力最高、结构最复杂的生态系统之一[1], 拥有丰富的物质资源并进行着复杂的物质交换[2],凭借其高生产力和显著的碳汇潜力,它在海岸带碳固存中占据着不可替代的地位[3]。滨海湿地作为介于陆地生态系统和海洋生态系统之间的过渡区域,是指受海陆交互作用下经常被静止或流动的水体所浸淹的沿海低地,主要包括滩涂、盐沼、浅海水域等[4]。受海陆交互作用干扰,滨海湿地生态系统已成为全球环境变化的敏感区和生态系统的脆弱区[5]。
红树林是分布于热带、亚热带潮间带、以红树植物为主体的特殊植物群落[6]。该群落的土壤和生物中均储存着大量的碳,且碳存储周期长,可视为一个高效的长期自然碳汇,对缓解区域和全球气候变化有重要意义[7]。受全球气候变化及人类活动的叠加影响,红树林资源持续退化,数据显示,1973—2000年全球红树林面积锐减30 199 hm2[8],导致大气CO2浓度攀升,进而引发气温异常、海平面上升等连锁环境效应,为应对这一危机,滨海地区已通过大规模造林实施生态修复,目前也取得了阶段性进展,其中人工红树林恢复成为当前主要的修复手段[9]。
红树林湿地的碳汇功能核心依赖于生物固碳过程,而卡尔文循环是自然界中最主要的生物固碳途径[10],其运转效率直接决定了红树林生态系统的固碳能力,其中核酮糖-1,5-二磷酸羧化酶/加氧酶(RubisCO)是该循环的关键限速酶[11],其活性与分布特征对红树林固碳效率具有决定性影响。目前已知RubisCO (Ⅰ、Ⅱ、Ⅲ、Ⅳ)存在4种类型,其中RubisCO Ⅰ广泛存在于光合和化能自养生物体中[12]。RubisCO Ⅰ又可细分为4类,分别是Form Ⅰ A、Ⅰ B、Ⅰ C、Ⅰ D。RubisCO酶大亚基由cbbL基因编码,95%以上的固碳生物含有该基因[13],因此作为靶标来表征固碳细菌[14-15]。在美洲[16]、东南亚[17]及我国广东[18]、广西[19]、海南[20]等红树林分布区,学者们围绕红树林湿地的固碳功能开展了大量研究,关注到固碳细菌通过提升土壤碳储量和改善土壤环境的作用。尽管现有研究已逐步开始关注人工红树林湿地,但仍存在明显局限:多数研究集中于自然红树林的泥质土壤生境,且多以红树林碳储量为核心研究对象,尚未涉及热带海洋性季风气候下沙质土壤生境中固碳细菌的系统研究。
本研究以老爷海潟湖人工红树林为对象,该区域兼具热带海洋性季风气候与沙质土壤的独特生境组合,目前国内针对该类特殊生境下固碳细菌群落结构、功能特征及其调控机制的研究仍较为匮乏。为此,本研究以cbbL基因为标记物,采用实时荧光定量PCR技术与高通量测序技术,对比分析老爷海人工红树林湿地的光滩与红树林地土壤中固碳细菌基因丰度、群落结构多样性与差异,并探讨影响该区域土壤固碳细菌群落变化的关键环境因子。研究结果不仅有助于揭示人工红树林湿地独特的固碳机制,完善湿地生态系统碳循环理论,还能为进一步优化人工红树林湿地的生态修复和管理,提升其固碳能力,应对全球气候变化提供科学依据和理论支撑。
1 材料与方法 1.1 研究区概况老爷海位于海南岛东南部万宁市东澳镇(18°39′N— 18°42′N,110°19′E—110°25′E),形状狭长,呈东西向延伸,是一个典型的潟湖,属于热带海洋性季风气候,年平均温度为22~25 ℃,年降水量为1 500~2 500 mm,受季风气候影响,降水具有明显季节差异,自然环境优越。该区域人工红树林的种植年限为3~4年,造林平均密度约5 347株/hm2。初始造林物种以本土适生红树植物为主,除当前群落中占主导的白骨壤(Avicennia marina)、少量掺杂的木榄(Bruguiera gymnorrhiza)外,还包括桐花树(Aegiceras corniculatum)、红海榄(Rhizophora stylosa)等。但该区域当前人工红树林湿地植被类型仍较为单一,植株稀疏细弱,土壤类型为沙质土,颜色呈现灰色[21]。
|
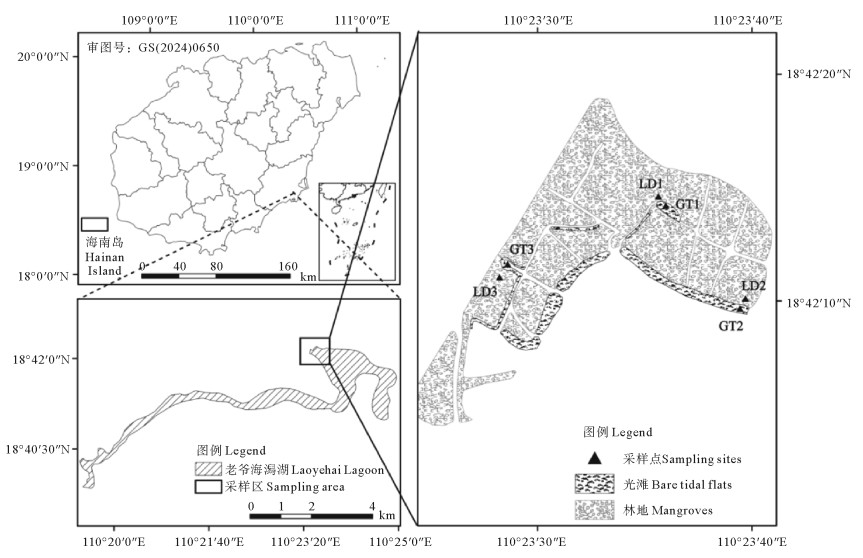
图 1 研究区域采样点分布示意图 Fig. 1 Schematic diagram of sampling point distribution in the study area |
2024年8月7—8日,在万宁市东澳镇老爷海沿岸人工红树林湿地开展土壤采样工作。采样地的选取兼顾光滩与红树林两种生境,设置光滩与红树林(20 m×20 m)各3个采样点。采样前,仔细清除土壤表面5 cm的地表层枯枝落叶及杂质,采用五点采样法,使用土钻钻取0~20 cm深度的土壤,将采集的5钻土壤混合均匀,每块样点设置6个重复,采集了36个(2×3×6)土样。
采集后的土样分为两部分处理:一部分用于分子的生物学分析,每样品取10~20 g土壤进入无菌离心管并密封,置于-80 ℃的干冰桶。另一部分土样装入密封袋,常温下带回实验室,部分样品风干后过2 mm筛用于土壤理化性质的测定,部分样品测定含水量。光滩采集各样品分别命名GT1、GT2、GT3,红树林地采集的各样品分别命名为LD1、LD2、LD3。
1.3 分析方法 1.3.1 土壤样品理化性质测定土壤pH采用酸度计测定(水土比(V∶m)为2.5∶1)[22];土壤含水率采用105 ℃烘箱中连续烘干8~12 h至恒重后测定的方法进行测定,其值用质量分数表示[22];土壤有机质含量采用重铬酸钾氧化-油浴加热测定;土壤有机碳采用重铬酸钾-浓硫酸加热法测定[22];土壤全氮采用凯氏定氮法测定;土壤全磷采用消解钼锑抗分光光度法测定[23];土壤易氧化有机碳采用高锰酸钾氧化法测定[24];土壤粒径使用激光粒度仪测定[25]。
1.3.2 土壤总DNA提取为获取土壤微生物的DNA,我们选用了土壤微生物总DNA提取试剂盒(PowerSoil DNA Isolation Kit)开展抽提工作。该试剂盒由Molecular BioProducts, Incorporated生产,整个抽提流程严格按试剂盒说明书操作。待DNA提取工作完成后,利用超微量紫外可见分光光度计(Nanodrop ND1000,美国)对提取得到的DNA进行浓度和纯度的检测。同时,借助1%琼脂糖凝胶电泳技术来评估DNA的完整性。经过检测,将符合质量要求的DNA样品置于-80 ℃环境下保存,以备后续的PCR扩增实验使用。
1.3.3 土壤固碳功能基因cbbL的扩增与测序固碳基因cbbL扩增的上游引物为K2f(ACCAYCAAGCCSAAGCTSGG),下游引物为V2r(GCCTTCSAGCTTGCCSACCRC), 片段长度为492~495 bp,扩增区为cbbL-a[26]。PCR扩增反应体系(25 μL):5×Q5 Reaction Buffer 5 μL,2.5 mmol/L dNTPs 2 μL,10 μmol/L Forward Primer 1 μL,10 μmol/L Reverse Primer 1 μL,Q5 High-Fidelity DNA Polymerase 0.25 μL,5×Q5 High GC Enhancer (optional) 5 μL,Template DNA 2 μL,ddH2O 8.75 μL。PCR反应条件:98 ℃预变性3 min,进入扩增循环,98 ℃保持30 s使模板变性,降温至65 ℃退火和延伸,重复循环30次,大量累积DNA片段,最后在72 ℃延伸5 min。PCR产物纯化后,送至上海派森诺公司采用Illumina平台对群落DNA片段进行双端(Paired-end)测序,测序平台中使用Vsearch方法[27]对测序得到的原始数据进行数据质控、序列拼接、变异检测等处理和分析。在97%相似度水平对高质量序列聚类,输出代表序列和操作分类单元(Operational taxonomic unit,OTU)表,对其长度分布进行统计,检查这些序列的长度是否和测序目的片段的长度范围相当,最后与序列数据库进行比对得出结果[28-29]。
1.3.4 土壤固碳细菌测定本研究运用实时荧光定量PCR(Real-time quantitative PCR)技术,对固碳细菌的cbbL基因丰度展开检测,所用引物与1.3.3中一致,为K2f/V2r。具体的反应体系如下:2×SYBR Real-time PCR premixture 10 μL,10 μmol/L浓度的上游、下游引物各添加0.4 μL。反应条件:95 ℃进行预变性处理,时长为5 min;之后正式进入扩增循环阶段,循环过程中,95 ℃下保持15 s实现变性,接着将温度降至60 ℃,在此温度下退火30 s,完成一次循环,共进行40个循环。
1.3.5 数据处理使用Microsoft Excel 2010对数据进行预处理,用SPSS19.0进行统计学分析,利用单因素方差分析(one-way ANOVA)和邓肯法(α=0.05)对不同地表覆盖类型土壤基本理化性质、固碳细菌cbbL基因丰度和多样性指数进行方差分析及多重比较;使用上海派森诺生物科技股份有限公司提供的云平台进行门、属水平的群落组成分析,采用R 4.3.0软件的ape包、Vegan包以及Python的scikit-bio包进行PCoA分析、PERMANOVA分析、ANOSIM分析以及冗余分析;使用Origin 2024软件包绘制微生物群落丰度图、误差柱状图等;使用ArcGIS软件绘制研究区域采样点分布示意图。
2 结果与分析 2.1 土壤理化性质由表 1可知,老爷海人工湿地中光滩和红树林地的理化性质存在差异。GT1的有机碳、全氮、易氧化有机碳、粉粒、有机质含量高于LD1;GT2和GT3的pH、细砂含量高于LD2和LD3。总体而言,红树林地的有机碳、全氮、全磷、易氧化有机碳、含水率、黏粒、粉粒及有机质含量普遍高于光滩,仅个别采样点红树林地(如LD1)的有机碳、全氮、易氧化有机碳、粉粒、有机质含量低于光滩,但细砂的含量红树林地低于光滩(GT1除外)。可见,红树林地养分相对充足,更利于生物生长;而光滩细砂含量高,土壤通气性良好,但水分和养分易流失。
|
|
表 1 土壤理化性质 Table 1 Soil physicochemical properties |
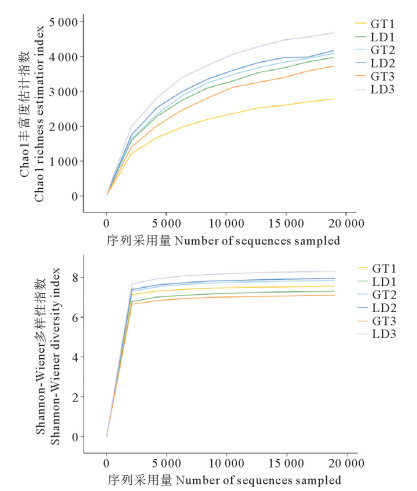
对光滩和红树林地样品进行高通量测序,数据进行抽平后,光滩三块样地分别得到38 697、32 224、49 673条优化序列,红树林地三块样地分别得到40 205、32 913、38 118条优化序列。可以看出,随着平台深度的不断加深,Chao1丰富度估计指数和Shannon-Wiener多样性指数逐渐趋于平缓,表明测序结果足够反映当前样本物种的多样性,已基本覆盖土壤中的物种(见图 2)。
|
图 2 土壤固碳细菌多样性稀释曲线 Fig. 2 Rarefaction curves of soil carbon-fixing bacterial diversity |
采用预测物种丰富度的Chao1指数、反映物种多样性的Simpson指数和Shannon-Wiener指数以及衡量物种分布均匀度的Pielou均匀度指数来表征土壤固碳细菌群落多样性。两种生境中Chao1丰富度估计指数显示红树林地>光滩,Simpson多样性指数显示GT1>LD1、GT2=LD2、GT3<LD3,而Shannon-Wiener多样性指数和Pielou均匀度指数皆为GT1>LD1、GT2<LD2、GT3<LD3(见表 2)。
|
|
表 2 土壤固碳细菌α多样性指数 Table 2 Alpha diversity indices of soil carbon-fixing bacteria |
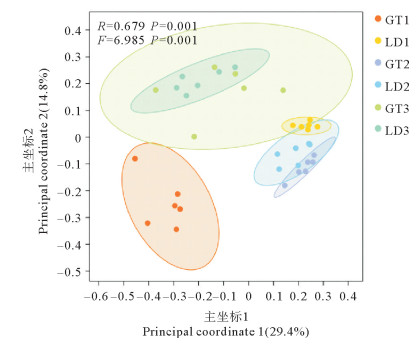
基于Bray-Curtis距离的PCoA显示(见图 3),样本点分布呈现明显的分组聚类特征,GT1和LD1相距较远,即土壤固碳细菌群落结构差异大;GT2和LD2、GT3和LD3部分重合,土壤固碳细菌群落结构存在明显差异。ANOSIM与PERMANOVA分析结果显示,组间差异大于组内差异,群落结构存在显著差异。
|
图 3 基于OTU的主坐标分析、相似性分析和置换多元方差分析的结果 Fig. 3 Results of OTU-based principal coordinates analysis, analysis of similarities, and permutational multivariate analysis of variance |
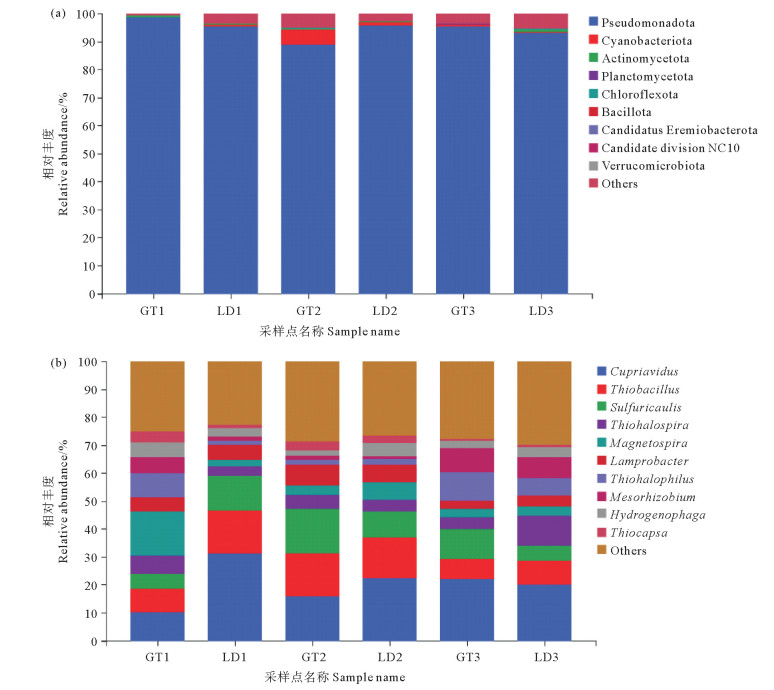
在本研究中,两个生境所得到的序列共注释到的微生物归属于9个门、10个纲、10个目、10个科、10个属、10个种。如图 4(a)所示,门水平上主要的菌门为假单胞菌门(Pseudomonadota)和蓝细菌门(Cyanobacteriota),光滩分别占比为94.46%、2.00%,红树林地分别占比为94.87%、0.77%。如图 4(b)所示,属水平上两者丰度均大于1%的有贪铜菌属(Cupriavidus,16.11%~24.66%)、硫杆菌属(Thiobacillus,10.39%~ 12.77%)、硫杆状菌属(Sulfuricaulis,9.13%~10.54%)、硫卤螺旋菌属(Thiohalospira,5.42%~6.06%)、磁螺旋菌属(Magnetospira,3.94%~7.23%)、闪杆菌属(Lamprobacter,5.20%~5.26%)、嗜盐硫杆菌属(Thiohalophilus,3.23%~6.85%)、中慢生根瘤菌属(Mesorhizobium,3.25%~5.26%)、氢噬胞菌属(Hydrogenophaga,3.37%~3.79%)、荚硫菌属(Thiocapsa,1.62%~2.41%)。其中,光滩优势菌属为贪铜菌属(16.11%)、硫杆菌属(10.39%)、硫杆状菌属(10.54%),红树林地优势菌属为贪铜菌属(24.66%)、硫杆菌属(12.77%)。
|
图 4 土壤固碳细菌在门(a)、属(b)水平上的群落结构组成 Fig. 4 Community structure of soil carbon-fixing bacteria at the phylum (a) and genus (b) levels |
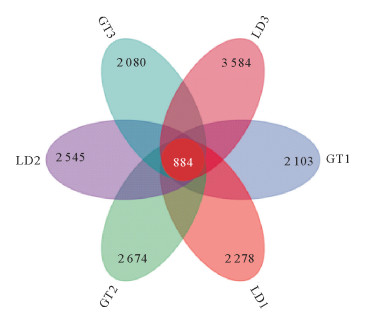
在97%的序列相似水平下,共获得50 906个OTU,光滩总OTU有19 726个,采样点GT1、GT2、GT3独有OTU分别为2 103、2 674、2 080个,红树林地总OTU有31 180个,采样点LD1、LD2、LD3独有OTU分别为2 278、2 545、3 584个,两种生境有共同OUT为884个(见图 5)。
|
图 5 土壤固碳细菌OTU花瓣图 Fig. 5 Petal diagram of OTUs of soil carbon-fixing bacteria |
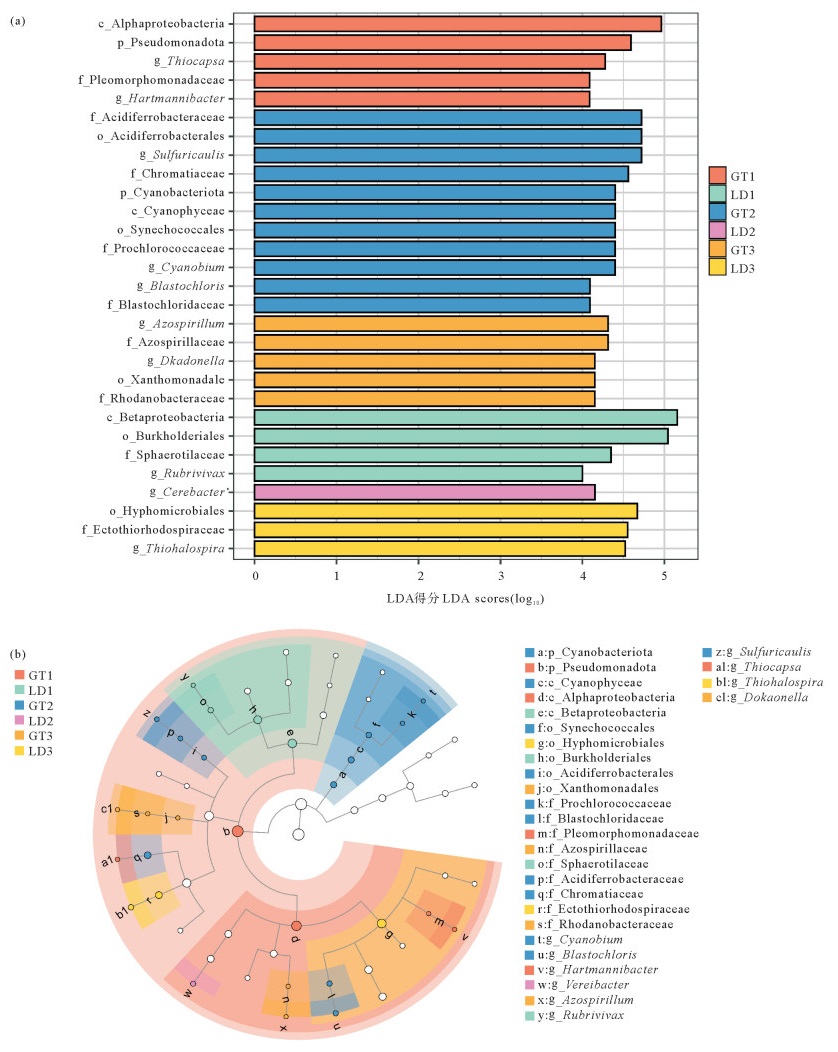
为进一步确定各生境的差异标志物种,基于物种相对丰度进行了LEfSe分析(LDA>4),结果如图 6所示,不同的生境中共有29个标志差异物种。在属水平上,光滩的差异标志物种包括α-变形菌纲的哈特曼氏杆菌属(Hartmannibacter)、芽绿菌属(Blastochloris)、固氮螺菌属(Azospirillum)、γ-变形菌纲的荚硫菌属(Thiocapsa)、硫杆状菌属、独岛杆菌属(Dokdonella)以及蓝藻纲的蓝杆藻属(Cyanobium);红树林地的差异物种包括β-变形菌纲的红长命菌属(Rubrivivax)、α-变形菌纲的Cereibacter属和γ-变形菌纲的硫卤螺旋菌属。
|
( (a):LDA柱状图,得分大于4的显示其中,得分越高表明差异越显著;(b):为进化分支图,从内到外表示门至属的分类学水平,节点圆圈大小对应平均相对丰度,空心节点表示不显著,有颜色的点表示显著,图中字母则标识了组间存在显著差异的分类单元的名称。(a): LDA bar chart, only taxa with an LDA score>4 are displayed, higher scores indicate more significant differences. (b): Evolutionary cladogram, taxonomic levels from phylum to genus are represented from the inside out. The size of each node circle corresponds to the average relative abundance, hollow nodes indicate nonsignificant differences, while colored nodes represent significant differences, letters in the figure denote taxonomic units with significant differences between groups. ) 图 6 土壤差异物种的LDA得分情况(a)和进化分支图(b) Fig. 6 LDA scores (a) and cladogram (b) of differentially abundant soil species |
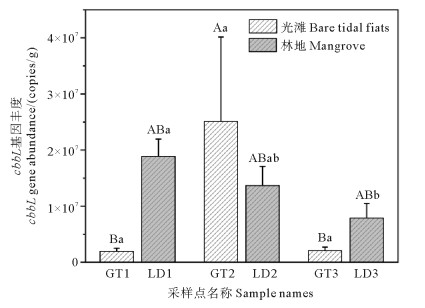
绝对定量PCR结果显示(见图 7),人工湿地中光滩的固碳细菌基因丰度为0.19×107~2.51×107 copies/g,红树林湿地的固碳细菌基因丰度为0.79×107~ 1.89×107 copies/g。其中GT1(0.19×107 copies/g)<LD1(1.89×107 copies/g)、GT2(2.51×107 copies/g)>LD2(1.37×107 copies/g)、GT3(0.21×107 copies/g)<LD3(0.79×107 copies/g),且GT2显著高于GT1和GT3,两种湿地类型下固碳细菌基因丰度未表现出统一的变化规律,仅在距离海洋较近的GT2位点光滩高于对应红树林位点,不同采样点之间差异明显。
|
( 柱状图上方不同大写字母所有采样点之间差异显著,不同小写字母表示各生境内差异显著(光滩或林地)(P<0.05)。Different uppercase letters above the bars indicate significant differences among all sampling sites, while different lowercase letters indicate significant differences within each habitat (i.e., mudflat or mangrove forest) (P < 0.05). ) 图 7 各生境土壤cbbL基因丰度 Fig. 7 The abundance of cbbL gene in soils of various habitats |
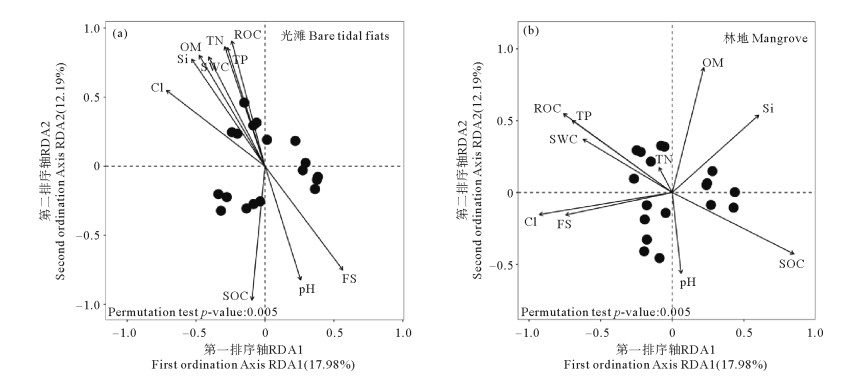
为分析影响万宁老爷海人工湿地固碳细菌群落的影响因素,基于属水平对土壤固碳细菌群落结构与环境因子进行了RDA分析(见图 8)。结果表明,光滩的第一、二排序轴共解释了30.17%的固碳细菌群落差异,固碳细菌群落组成与环境因子显著相关,其中有机碳(R2=0.895,P=0.001)、全氮(R2=0.788,P=0.001)、全磷(R2=0.767,P=0.001)、易氧化有机碳(R2=0.833,P=0.001)、pH(R2=0.706,P=0.003)、含水率(R2=0.747,P=0.001)、黏粒(R2=0.760,P=0.001)、粉粒(R2=0.832,P=0.001)、细砂(R2=0.832,P=0.001)、有机质(R2=0.822,P=0.001)显著影响(见图 8(a)),R2越大对土壤固碳细菌群落的影响越大,影响顺序为有机碳>易氧化有机碳>粉粒=细砂>有机质>全氮>全磷>黏粒>含水率>pH。
|
( TN:全氮;TP:全磷;SOC:有机碳;ROC:易氧化有机碳;SWC:土壤含水量;Cl:黏粒;Si:粉粒;FS:细砂;OM:有机质。TN: Total nitrogen; TP: Total phosphorus; SOC: Soil organic carbon; ROC: Readily oxidizable carbon; SWC: Soil water content; Cl: Clay; Si: Silt; FS: Fine sand; OM: Organic matter. ) 图 8 土壤固碳细菌群落结构与环境因子的冗余分析 Fig. 8 Redundancy analysis of soil carbon-fixing bacterial community structure and environmental factors |
红树林地的第一、二排序轴共解释38.47%的固碳细菌群落差异,土壤固碳细菌群落受到有机碳(R2=0.899,P=0.001)、全氮(R2=0.038,P=0.72)、全磷(R2=0.733,P=0.001)、易氧化有机碳(R2=0.870,P=0.001)、pH(R2=0.313,P=0.07)、含水率(R2=0.522,P=0.006)、黏粒(R2=0.880,P=0.001)、粉粒(R2=0.645,P=0.001)、细砂(R2=0.574,P=0.003)、有机质(R2=0.783,P=0.001)显著影响(见图 8(b)),影响顺序为有机碳>黏粒>易氧化有机碳>有机质>全磷>粉粒>细砂>含水率,其中全氮(R2=0.038,P=0.72)和pH(R2=0.313,P=0.07)影响不显著。
3 讨论植被作为陆地生态系统的重要组成部分,通过改变微环境条件,对土壤微生物群落结构和多样性产生显著影响[30-31]。本研究发现,两种生境下的土壤固碳细菌群落结构存在明显差异。基于Chao1丰富度估计指数,红树林地的固碳细菌物种丰富度高于光滩。在Simpson多样性指数、Shannon-Wiener多样性指数和Pielou均匀度指数方面,呈现复杂的变化规律:在距离海洋较远的采样地,其多样性指数光滩高于红树林地;在距离海洋近且水流量较大的区域,则表现为红树林地高于光滩(GT1>LD1,GT2<LD2、GT3<LD3)。此外,研究还发现有机碳与土壤固碳细菌呈现负相关,这与韩知序等[32]对热带农田的研究结果一致。这些现象可能与潮汐和微地形等因素紧密相关。如张雯雯等[33]的研究指出,频繁的海水淹没和退却导致土壤盐度剧烈变化,高盐环境对许多固碳细菌的生存和代谢产生抑制作用,限制了微生物的多样性。总体来看,红树林地具有独特的植被缓冲系统、稳定的细颗粒土壤以及丰富的有机碳,使土壤微生物数量和多样性高于光滩[34],这也印证了土壤微生物数量随着植被恢复而增加[35]。
本研究结果显示,土壤固碳细菌主要属于假单胞菌门和蓝细菌门,这与任笑瀛等[36]的研究结果一致。两类生境的优势菌属由化能自养菌与化能异养菌构成,其中贪铜菌属为化能异养菌,硫杆菌属和硫杆状菌属为化能自养菌。该结果与袁庆等[37]在福建泉州湾红树林沉积物研究中提出的“化能自养菌是红树林沉积物重要类群”的结论一致,且本研究进一步发现化能自养菌与化能异养菌在红树林沉积物中具有同等重要的生态位。红树林地中贪铜菌属与硫杆菌属的相对丰度显著高于光滩,这可能与光滩生境中有机碳输入匮乏、元素循环效率较低有关,此类环境条件难以维持化能异养菌与化能自养菌的高丰度共存。这一现象既体现了微生物群落对生境资源禀赋及功能需求的适应性演化,亦从微生物生态角度佐证了红树林湿地在区域元素循环中的关键驱动作用。
通过绝对定量PCR技术检测发现,人工红树林湿地的光滩与红树林地生境均存在一定数量的土壤固碳细菌。两类生境中cbbL基因丰度(见图 7)低于稻田[38]、农田[32]、森林[39]等生态系统,高于雨林[29]和旱地[40];其中红树林地总体cbbL基因丰度显著高于光滩,表明红树林地土壤固碳潜力更强,对区域碳汇能力的贡献更大[41]。值得注意的是,两者cbbL基因丰度差异幅度较小,推测与该研究区域人工红树林处于初级发育阶段、种植年限较短且植株个体较小密切相关。进一步分析显示,本研究中固碳细菌数量与土壤有机碳呈显著正相关,这与Yuan等[42]的研究结论一致,王蕊等[43]研究表明,部分区域固碳细菌数量与土壤有机碳呈负相关,这可能与研究区域的环境异质性密切相关,反映出不同生态系统中固碳细菌与碳基质的互作机制存在显著差异。
土壤微生物群落结构和多样性是多种环境因子综合作用的结果[44],其组成与多样性受环境因子显著影响[45]。在本研究中通过RDA分析发现,在光滩生境中,有机碳、易氧化有机碳、粉粒、细砂、有机质、全氮、全磷、黏粒、含水率、pH解释了固碳细菌群落的主要差异,成为驱动光滩固碳细菌群落结构变化的关键环境因子,这与前人研究结论一致[46-47];而在红树林地生境中,有机碳、黏粒、易氧化有机碳、有机质、全磷、粉粒、细砂、含水率为固碳细菌群落环境变化的重要环境因子,而全氮(P>0.05)和pH(P>0.05)的影响未达到显著水平。土壤中的氮与pH对植物生长具有重要的影响[48],是影响土壤固碳菌群落结构的重要因子[49-50]。而本研究中红树林地生境下全氮与pH未表现出显著影响效应,其内在驱动机制尚需进一步验证。后续研究需补充土壤盐度等关键环境因子的测定,结合多维度环境数据与高通量微生物组学技术,进一步解析光滩生境中固碳细菌群落结构变化的核心驱动机制,以完善该生境下固碳细菌群落与环境因子的关联理论。
4 结语本研究通过对海南岛老爷海人工红树林湿地两种生境(光滩和红树林地)的固碳细菌群落特征及环境影响因子进行分析,得出以下结论:人工种植红树林可显著改变土壤性质。红树林地的有机碳、全氮、全磷、易氧化有机碳、含水率、黏粒、粉粒及有机质含量普遍高于光滩,仅个别采样点红树林地(如LD1)的有机碳、全氮、易氧化有机碳、粉粒、有机质含量低于光滩;红树林地的细砂含量低于光滩。光滩与红树林地土壤固碳细菌的基因丰度、物种丰富度及多样性存在整体差异,红树林湿地表现更优;二者群落结构分化明显,且组间差异高于组内差异;假单胞菌门和蓝细菌门为主要固碳菌门,贪铜菌属、硫杆菌属等为优势菌属,这些优势菌群以化能异养菌和化能自养菌为主;两类生境间存在29个标志差异物种。土壤粒度与有机碳是影响固碳细菌群落结构的主要环境因子,全氮和pH在红树林地中影响不显著,而在光滩中影响显著。本研究表明,人工红树林湿地在生态修复和碳汇方面具有较大潜力与可操作性,这为应对全球气候变化提供了重要的实践方向。但本研究仍存在一定局限性:研究区域仅聚焦于海南岛老爷海单一人工红树林湿地,空间尺度较窄;研究周期未涉及不同季节、不同红树林生长年限的动态变化监测,难以揭示固碳细菌群落与环境因子的长期相互作用规律。基于此,未来研究可拓展至不同气候带、不同林龄的人工红树林湿地,通过长期定位观测明确固碳细菌群落的时空动态特征,进一步完善人工红树林湿地碳汇功能的调控理论,为提升湿地生态系统的固碳效益提供更精准的科学依据。
| [1] |
Wu C Y, Chen W, Cao C X, et al. Diagnosis of wetland ecosystem health in the Zoige Wetland, Sichuan of China[J]. Wetlands, 2018, 38(3): 469-484. DOI:10.1007/s13157-018-0992-y (  0) 0) |
| [2] |
Ramesh R, Chen Z, Cummins V, et al. Land-ocean interactions in the coastal zone: Past, present&future[J]. Anthropocene, 2015, 12: 85-98. DOI:10.1016/j.ancene.2016.01.005 (  0) 0) |
| [3] |
Bouillon S, Borges A V, Castaneda-Moya E, et al. Mangrove production and carbon sinks: A revision of global budget estimates[J]. Global Biogeochemical Cycles, 2008, 22(2): 1-12. (  0) 0) |
| [4] |
曹磊, 宋金明, 李学刚, 等. 中国滨海盐沼湿地碳收支与碳循环过程研究进展[J]. 生态学报, 2013, 33(17): 5141-5152. Cao L, Song J M, Li X G, et al. Research progresses in carbon budget and carbon cycle of the coastal salt marshes in China[J]. Acta Ecologica Sinica, 2013, 33(17): 5141-5152. (  0) 0) |
| [5] |
Webb E L, Friess D A, Krauss K W, et al. A global standard for monitoring coastal wetland vulnerability to accelerated sea-level rise[J]. Nature Climate Change, 2013, 3(5): 458-465. DOI:10.1038/nclimate1756 (  0) 0) |
| [6] |
郭欢敏, 沈小雪, 李瑞利. 深圳湾福田红树林自然保护区物种共存特征与物种分布概率研究[J]. 植物生态学报, 2025, 49(11): 1833-1843. Guo H M, Shen X X, Li R L. Species co-occurrence and distribution probability in Futian Mangrove Nature Reserve of Shenzhen Bay[J]. Journal of Plant Ecology, 2025, 49(11): 1833-1843. (  0) 0) |
| [7] |
Alongi D M. Carbon sequestration in mangrove forests[J]. Carbon Management, 2012, 3: 313-322. (  0) 0) |
| [8] |
贾明明, 王宗明, 毛德华, 等. 面向可持续发展目标的中国红树林近50年变化分析[J]. 科学通报, 2021, 66(30): 3886-3901. Jia M M, Wang Z M, Mao D H, et al. Spatial-temporal changes of China's mangrove forests over the past 50 years: An analysis towards the Sustainable Development Goals (SDGs)[J]. Chinese Science Bulletin, 2021, 66(30): 3886-3901. (  0) 0) |
| [9] |
彭逸生, 庄雪茵, 赵丽丽, 等. 树种选择和滩地高程对红树林修复早期系统碳储量的影响[J]. 中山大学学报(自然科学版), 2023, 62(2): 37-46. Peng Y S, Zhuang X Y, Zhao L L, et al. Influence of species choice and tidal flat elevation on the carbon sequestration of early mangrove restoration[J]. Acta Scientiarum Naturalium Universitatis Sunyatseni, 2023, 62(2): 37-46. (  0) 0) |
| [10] |
Tabita F R. Molecular and cellular regulation of autotrophic carbon dioxide fixation in microorganisms[J]. Microbiological Reviews, 1988, 52(2): 155-189. DOI:10.1128/mr.52.2.155-189.1988 (  0) 0) |
| [11] |
陈为钧, 赵贵文, 顾月华. RubisCO的研究进展[J]. 生物化学与生物物理进展, 1999, 5(5): 433-436. Chen W J, Zhao G W, Gu Y H. Advance of Ribulose 1,5 Bisphosphate Carboxylase/Oxygenase(RubisCO)[J]. Progress in Biochemistry and Biophysics, 1999, 5: 433-436. (  0) 0) |
| [12] |
Tabita F R, Satagopan S, Hanson T E, et al. Distinct form Ⅰ, Ⅱ, Ⅲ, and Ⅳ Rubisco proteins from the three kingdoms of life provide clues about rubisco evolution and structure/function relationships[J]. Journal of Experimental Botany, 2008, 59(7): 1515-1524. (  0) 0) |
| [13] |
Uchino Y, Yokota A. "Green-like" and "red-like" RubisCO cbbL genes in Rhodobacter azotoformans[J]. Molecular Biology and Evolution, 2003, 20(5): 821-830. DOI:10.1093/molbev/msg100 (  0) 0) |
| [14] |
Zhou Z, Wei W, Shi X, et al. Twenty-six years of chemical fertilization decreased soil RubisCO activity and changed the ecological characteristics of soil cbbL-carrying bacteria in an entisol[J]. Applied Soil Ecology, 2019, 141: 1-9. (  0) 0) |
| [15] |
Wang F, Guo R, Zhang N, et al. Soil organic carbon storages and bacterial communities along a restored mangrove soil chronosequence in the Jiulong River Estuary: From tidal flats to mangrove afforestation[J]. Fundamental Research, 2023, 3(6): 880-889. DOI:10.1016/j.fmre.2022.08.019 (  0) 0) |
| [16] |
Siuling C C, Jorge S H, Luis J M M, et al. Carbon stock in different ecological types of mangroves in a karstic region (Yucatan, México): An opportunity to avoid site scale emissions[J]. Frontiers in Forests and Global Change, 2023, 6(6): 1181542. (  0) 0) |
| [17] |
Sahari I S M, Razali M A N, Redzuan S N, et al. Carbon stock variability of Setiu Lagoon mangroves and its relation to the environmental parameters[J]. Global Ecology and Conservation, 2024, 53: e02994. DOI:10.1016/j.gecco.2024.e02994 (  0) 0) |
| [18] |
周治刚, 岳文, 李辉权, 等. 树种类型和潮滩高程对广东湛江高桥红树林碳储量的影响[J]. 热带海洋学报, 2024, 43(2): 108-120. Zhou Z G, Yue W, Li H Q, et al. Influence of tree species and intertidal elevations on the carbon storage of the Gaoqiao mangrove area in Zhanjiang, Guangdong Province[J]. Journal of Tropical Oceanography, 2024, 43(2): 108-120. (  0) 0) |
| [19] |
莫莉萍, 周慧杰, 刘云东, 等. 广西红树林湿地土壤有机碳储量估算[J]. 安徽农业科学, 2015, 43(15): 81-84. Mo L P, Zhou H J, Liu Y D, et al. An estimation of soil organic carbon storage in mangrove wetlands of Guangxi[J]. Journal of Anhui Agricultural Sciences, 2015, 43(15): 81-84. (  0) 0) |
| [20] |
褚梦凡, 肖晓彤, 丁杨, 等. 海南儋州湾红树林区沉积有机质来源及碳储量[J]. 海洋科学, 2021, 45(2): 22-31. Chu M F, Xiao X T, Ding Y, et al. Sediment organic matter sources and carbon stock associated with a mangrove reserve in Danzhou Bay, Hainan, China[J]. Marine Sciences, 2021, 45(2): 22-31. (  0) 0) |
| [21] |
孙天成, 马梓程, 黄赞慧, 等. 基于碳储存变化的海岸带生态系统修复策略——以海南岛东南海岸带为例[J]. 热带地理, 2023, 43(3): 443-458. Sun T C, Ma Z C, Huang Z H, et al. Coastal ecosystem restoration strategy based on carbon storage change: A case study of the southeast coastal zone of Hainan Island[J]. Tropical Geography, 2023, 43(3): 443-458. (  0) 0) |
| [22] |
鲍士旦. 土壤农化分析[M]. 3版. 北京: 中国农业出版社, 2000. Bao S D. Soil and Agricultural Chemistry Analysis[M]. 3rd ed. Beijing: China Agricultural Press, 2000. (  0) 0) |
| [23] |
鲁如坤. 土壤农业化学分析方法[M]. 北京: 中国农业科技出版社, 2000. Lu R K. Analytical Methods for Soil and Agro-Chemistry[M]. Beijing: China Agricultural Science and Technology Press, 2000. (  0) 0) |
| [24] |
Blair G J, Lefroy R D B, Lise L. Soil carbon fractions based on their degree of oxidation, and the development of a carbon management index for agricultural systems[J]. Australian Journal of Agricultural Research, 1995, 46(7): 1459-1466. DOI:10.1071/AR9951459 (  0) 0) |
| [25] |
庞奖励, 乔晶, 黄春长, 等. 前处理过程对汉江上游谷地"古土壤"粒度测试结果的影响研究[J]. 地理科学, 2013, 33(6): 748-754. Pang J L, Qiao J, Huang C C, et al. Pretreatment methods and their influences on grain-size measurement of palaeosol in the upper reaches of the Hanjiang River valley, China[J]. Scientia Geographica Sinica, 2013, 33(6): 748-754. (  0) 0) |
| [26] |
Walker N J. Real-time and quantitative PCR: Applications to mechanism-based toxicology[J]. Journal of Biochemical and Molecular Toxicology, 2001, 15(3): 121-127. DOI:10.1002/jbt.8 (  0) 0) |
| [27] |
Caporaso J G, Kuczynski J, Stombaugh J, et al. QIIME allows analysis of high-throughput community sequencing data[J]. Nature Methods, 2010, 7(5): 335-336. DOI:10.1038/nmeth.f.303 (  0) 0) |
| [28] |
张红雪, 朱巧莲, 郭力铭, 等. 烟秆生物质炭与化肥配施对植烟土壤有机碳组分及微生物的影响[J]. 土壤, 2022, 54(6): 1149-1156. Zhang H X, Zhu Q L, Guo L M, et al. Effects of combined application of tobacco stem biochar and chemical fertilizers on organic carbon fractions and microorganism in tobacco-growing soil[J]. Soils, 2022, 54(6): 1149-1156. (  0) 0) |
| [29] |
陈红利, 赵志忠, 吴丹, 等. 海南岛尖峰岭热带雨林土壤固碳细菌群落特征[J]. 土壤, 2024, 56(1): 64-72. Chen H L, Zhao Z Z, Wu D, et al. Soil carbon sequestering microbial communities in Jianfengling tropical rainforests of Hainan Island[J]. Soils, 2024, 56(1): 64-72. (  0) 0) |
| [30] |
Lin X G, Yin R, Zhang H Y, et al. Changes of soil microbiological properties caused by land use changing from rice-wheat rotation to vegetable cultivation[J]. Environmental Geochemistry and Health, 2004, 26(2): 119-128. DOI:10.1023/B:EGAH.0000039574.99651.65 (  0) 0) |
| [31] |
Lv X F, Ma B, Yu J B, et al. Bacterial community structure and function shift along a successional series of tidal flats in the Yellow River Delta[J]. Scientific Reports, 2016, 6(1): 36550. DOI:10.1038/srep36550 (  0) 0) |
| [32] |
韩知序, 赵志忠, 陈红利, 等. 海南岛不同撂荒年限的热带农田土壤固碳细菌群落特征[J]. 西南农业学报, 2024, 37(8): 1771-1779. Han Z X, Zhao Z Z, Chen H L, et al. Characteristics of carbon fixing bacteria community in tropical farmland soils with different abandoned years in Hainan Island[J]. Southwest China Journal of Agricultural Sciences, 2024, 37(8): 1771-1779. (  0) 0) |
| [33] |
张雯雯. 滩涂土壤盐分梯度对微生物群落结构影响的研究[D]. 扬州: 扬州大学, 2009. Zhang W W. Study on the Influence of Soil Salinity Gradient in Tidal Flat on Microbial Community Structure[D]. Yangzhou: Yangzhou University, 2009. (  0) 0) |
| [34] |
陈骏马, 殷荣宾, 任笑瀛, 等. 土壤固碳细菌群落对互花米草治理后红树林替代的响应[J]. 环境科学学报, 2025, 45(5): 424-433. Chen J M, Yin R B, Ren X Y, et al. Response of soil carbon-fixing microbial community to mangrove replacement after Spartina alterniflora management[J]. Acta Scientiae Circumstantiae, 2025, 45(5): 424-433. (  0) 0) |
| [35] |
Xiaofei L, Bin M, Junbao Y, et al. Bacterial community structure and function shift along a successional series of tidal flats in the Yellow River Delta[J]. Scientific Reports, 2016, 6(1): 36550. DOI:10.1038/srep36550 (  0) 0) |
| [36] |
任笑瀛, 殷荣宾, 陈骏马, 等. 互花米草二次入侵对土壤碳库管理指数及固碳菌群落特征的影响[J]. 环境科学学报, 2025, 45(4): 434-446. Ren X Y, Yin R B, Chen J M, et al. Impact of Spartina alterniflora re-invasion on soil carbon pool management index and carbon fixing bacterial community characteristics[J]. Acta Scientiae Circumstantiae, 2025, 45(4): 434-446. (  0) 0) |
| [37] |
袁庆, 王俊, 李雨霏, 等. 福建泉州湾红树林沉积物中化能自养细菌的分布特征及其驱动的潜在固碳过程[J]. 应用海洋学学报, 2025, 44(3): 423-432. Yuan Q, Wang J, Li Y F, et al. Distributional characteristics of chemolithoautotrophic bacteria and their potential drivers of carbon sequestration processes in mangrove sediments of Quanzhou Bay, Fujian[J]. Journal of Applied Oceanography, 2025, 44(3): 423-432. (  0) 0) |
| [38] |
袁红朝, 秦红灵, 刘守龙, 等. 长期施肥对稻田土壤固碳功能菌群落结构和数量的影响[J]. 生态学报, 2012, 32(1): 183-189. Yuan H C, Qin H L, Liu S L, et al. Abundance and composition of CO2 fixating bacteria in relation to long-term fertilization of paddy soils[J]. Acta Ecologica Sinica, 2012, 32(1): 183-189. (  0) 0) |
| [39] |
刘茗, 曹林桦, 刘彩霞, 等. 亚热带4种典型森林植被土壤固碳细菌群落结构及数量特征[J]. 土壤学报, 2021, 58(4): 1028-1039. Liu M, Cao L H, Liu C X, et al. Characterization of population and community structure of carbon-sequestration bacteria in soils under four types of forest vegetations typical of subtropical zone[J]. Acta Pedologica Sinica, 2021, 58(4): 1028-1039. (  0) 0) |
| [40] |
Tang Z X, Fan F L, Wan Y F, et al. Abundance and diversity of RuBisCO genes responsible for CO2 fixation in arid soils of northwest China[J]. Pedosphere, 2015, 25(1): 150-159. DOI:10.1016/S1002-0160(14)60085-0 (  0) 0) |
| [41] |
陆章欣, 严飞扬, 吴酬飞, 等. 仙山湖国家湿地公园土壤中固碳细菌的群落与功能基因特征[J]. 水土保持通报, 2025, 45(1): 235-243+275. Lu Z X, Yan F Y, Wu C F, et al. Community and functional gene characteristics of soil carbon sequestration microorganisms in Xianshanhu National Wetland Park[J]. Bulletin of Soil and Water Conservation, 2025, 45(1): 235-243+275. (  0) 0) |
| [42] |
Yuan H C, Ge T, Wu X, et al. Long-term field fertilization alters the diversity of autotrophic bacteria based on the ribulose-1, 5-biphosphate carboxylase/oxygenase (RubisCO) large-subunit genes in paddy soil[J]. Applied Microbiology and Biotechnology, 2012, 95(4): 1061-1071. DOI:10.1007/s00253-011-3760-y (  0) 0) |
| [43] |
王蕊, 李刚, 修伟明, 等. 抗虫-耐除草剂转基因玉米种植对土壤固碳细菌群落的影响[J]. 天津师范大学学报(自然科学版), 2022, 42(1): 31-36. Wang R, Li G, Xiu W M, et al. Effects of the plantation of insect-resistant and herbicide-tolerant transgenic maize on soil carbon-fixing bacterial community[J]. Journal of Tianjin Normal University (Natural Science Edition), 2022, 42(1): 31-36. (  0) 0) |
| [44] |
刘芳, 叶思源, 汤岳琴, 等. 黄河三角洲湿地土壤微生物群落结构分析[J]. 应用与环境生物学报, 2007, 13(5): 691-696. Liu F, Ye S Y, Tang Y Q, et al. Analysis of microbial community structure in coastal wetland soil of the Yellow River Delta[J]. Chinese Journal of Applied and Environmental Biology, 2007, 13(5): 691-696. (  0) 0) |
| [45] |
邓娇娇, 周永斌, 殷有, 等. 辽东山区典型人工针叶林土壤细菌群落多样性特征[J]. 生态学报, 2019, 39(3): 997-1008. Deng J J, Zhou Y B, Yin Y, et al. Soil bacterial community structure characteristics in coniferous forests of montane regions of eastern Liaoning Province, China[J]. Acta Ecologica Sinica, 2019, 39(3): 997-1008. (  0) 0) |
| [46] |
王浩骅, 张鹏, 罗帅, 等. 祁连山国家公园青海片区河流和湿地原生生物多样性研究[J]. 水生态学杂志, 2024, 45(5): 9-19. Wang H H, Zhang P, Luo S, et al. Protist diversity of rivers and wetlands in Qilian Mountain National Park (Qinghai region) based on metagenomics[J]. Journal of Hydroecology, 2024, 45(5): 9-19. (  0) 0) |
| [47] |
杨渐. 青藏高原湖泊微生物群落演替及其环境指示意义[D]. 武汉: 中国地质大学, 2015. Yang J. Microbial Response to Environmental Changes in Qinghai-Tibetan Lakes and Its Environmental Implications[D]. Wuhan: China University of Geosciences, 2015. (  0) 0) |
| [48] |
陈小弯, 田华川, 常军军, 等. 杞麓湖中河河口表流湿地净化河道污染水的效果及其微生物群落特征[J]. 生态环境学报, 2022, 31(9): 1865-1875. Chen X W, Tian H C, Chang J J, et al. Purification efficiency for polluted river water and microbial community characteristics of a surface-flow wetland located at Zhonghe River estuary near Qilu Lake[J]. Ecology and Environmental Sciences, 2022, 31(9): 1865-1875. (  0) 0) |
| [49] |
Chu H, Fierer N, Lauber C L, et al. Soil bacterial diversity in the arctic is not fundamentally different from that found in other biomes[J]. Environmental Microbiology, 2010, 12: 2998-3006. DOI:10.1111/j.1462-2920.2010.02277.x (  0) 0) |
| [50] |
Tripathi B M, Kim M, Laihoe A, et al. pH dominates variation in tropical soil archaeal diversity and community structure[J]. FEMS Microbiology Ecology, 2013, 86: 303-311. DOI:10.1111/1574-6941.12163 (  0) 0) |
 2026, Vol. 56
2026, Vol. 56


