鱼类生活在富含多种病原微生物的水环境中,其皮肤、鳃、肠和鼻腔等黏膜相关淋巴组织是病原感染鱼体时最先接触的部位,这些黏膜组织及其表面的黏液组成了鱼类抵御外界病原入侵的第一道防线,在鱼类的生长过程中发挥着至关重要的防御作用[1-2]。硬骨鱼的黏膜相关淋巴组织由先天性和适应性免疫细胞和分子组成,它们共同维持黏膜的稳态[3]。鱼类皮肤、鳃及肠上皮中分布有大量的黏液细胞,黏液细胞分泌的黏液不仅可以协助调节鱼类渗透压平衡[4],也是鱼体抵御病原微生物入侵的第一道物理和化学屏障。黏液中含有黏多糖、溶菌酶、抗体和凝集素等免疫防御因子,这些因子在鱼类的免疫防御中发挥作用[5-7]。
有关鱼类黏液细胞的研究已有很多[8-11],特别是近年来对鱼类皮肤[12-14]和肠道[15]黏液细胞的研究较多,关于花鲈(Lateolabrax japonicus)[16]、鲤(Cyprinus carpio)[17]、大菱鲆(Scophthalmus maximus)[18]、哲罗鱼(Hucho taimen)[19]、胡子鲶(Clarias fuscus)[20]、波纹唇鱼(Cheilinus undulatus)[21]、南方鲇(Silurus meridionalis)[22]、牙鲆(Paralichthys olivaceus)[23]等鱼类黏液细胞的类型与分布情况已有报道。鱼类的幽门盲囊位于肠的起始端,是鱼类特有的消化器官,幽门盲囊的存在是增加肠道表面的一种适应[24]。一般肉食性鱼类具有这一结构,其出现是仔鱼消化系统发育完全的一个重要形态标志[25]。不同鱼类中幽门盲囊的数量差别很大,由几个至数百个不等。研究发现鱼类幽门盲囊也具有免疫功能,如:虹鳟(Oncorhynchus mykiss)接种疫苗后幽门盲囊固有层中IgM+和IgT+细胞数量增加[24]; Toll样受体在鳜(Siniperca chuatsi)幽门盲囊的免疫应答反应中发挥作用[26]; 幽门盲囊还是鳜蛙虹彩病毒(Mandarin fish ranavirus, MRV)感染的主要靶组织[27]。然而,目前对于鱼类幽门盲囊的免疫功能还了解甚少,幽门盲囊中黏液细胞特性及其免疫防御作用尚待研究。
牙鲆是我国北方重要的经济养殖鱼类。我们实验室前期研究了牙鲆皮肤、鳃和肠黏膜相关淋巴组织中黏液细胞对疫苗的应答变化[23]; 克隆表达了牙鲆黏蛋白Muc2和Muc5ac,制备了其多克隆抗体,发现牙鲆肠中表达Muc2,不表达Muc5ac; 皮肤中表达Muc5ac,不表达Muc2;而鳃中表达Muc2和Muc5ac[28]。本研究通过制备牙鲆幽门盲囊组织的石蜡切片,利用苏木精-曙红(Hematoxylin-eosin,HE)染色研究幽门盲囊的组织结构; 利用阿尔新蓝(Alcian blue,AB)-过碘酸雪夫氏反应(Periodic acid Schiff,PAS)研究幽门盲囊黏液细胞类型; 以及间接免疫荧光技术研究幽门盲囊表达的黏蛋白种类; 利用迟缓爱德华氏菌灭活疫苗注射免疫牙鲆,通过AB-PAS染色、间接免疫荧光技术、实时荧光定量反转录PCR(qRT-PCR)以及酶联免疫吸附试验(ELISA),研究了免疫前后不同时间点牙鲆幽门盲囊中黏液细胞的种类和数量变化、增殖情况,以及黏液细胞分泌的黏蛋白在基因和蛋白水平上的表达变化。以期为深入了解鱼类幽门盲囊的免疫功能及黏液细胞在黏膜免疫防御中的作用提供理论依据。
1 材料与方法 1.1 实验动物及抗体健康牙鲆150尾,体质量(50±5) g,体长15~20 cm,购买于山东日照某养殖场,养殖场养殖条件稳定。实验前将鱼置于连续曝气的海水养殖箱中进行驯化,养殖温度保持在(21±1) ℃,每天喂食商品化饲料一次,每天换一半海水,暂养驯化1周后进行免疫实验。
鼠抗牙鲆黏蛋白Muc2和Muc5ac多克隆抗体[28]由本实验室制备并保存。
1.2 实验菌株培养及灭活将本实验室保存的迟缓爱德华氏菌菌株取出,室温解冻后接种于Lysogeny Broth(LB)液体培养基,于28 ℃摇床上振荡培养过夜,次日将菌液转至500 mL的LB液体培养基中继续扩大培养,于28 ℃摇床上振荡培养24 h,培养结束后离心(8 000g,10 min),倒去上清培养液,用无菌磷酸盐缓冲液(PBS,0.01 mol/L,pH=7.4)重悬沉淀,离心(8 000g,5 min),如此清洗3次。再用0.5%甲醛(v/v)于4 ℃灭活处理菌液48 h,将灭活菌液涂在固体培养基上培养,确认无菌后,再用PBS清洗3次,并调整菌液浓度至1×108 CFU/mL,放于4 ℃冰箱保存备用。
1.3 牙鲆免疫及取样将150尾健康牙鲆随机分为2组(实验组和对照组),每组75尾。用迟缓爱德华氏菌灭活疫苗注射免疫实验组牙鲆,每尾牙鲆腹腔注射浓度为1×108 CFU/mL的疫苗100 μL,对照组牙鲆每尾注射等量的PBS。分别于免疫前(0 d)以及免疫后1、2、3、5、7、10和14 d从两组牙鲆中各随机选取3尾,解剖取其幽门盲囊,并放入Bouin氏液中固定24 h左右,固定结束后用70%酒精换液。固定后的样品采用常规石蜡包埋切片法制备连续切片,并对切片进行组织学和组织化学染色。分别于免疫前(0 h)及免疫后4、8、12、24、48、72、96和120 h从各组中随机选取3尾牙鲆,解剖后将幽门盲囊放入组织保护液中,保存于-20 ℃冰箱备用,用于qRT-PCR检测。另外,分别于免疫前(0 d)及免疫后1、2、3、4、5和7 d从各组中随机选取3尾牙鲆,解剖后将幽门盲囊纵向剪开,剪成小段,放入装有PBS的离心管中,放于4 ℃冰箱中静置2 h,期间震荡数次。静置结束后,将黏液于4 ℃离心机中离心,用移液枪吸取上清液,放于-80 ℃保存备用,用于ELISA检测。
1.4 组织学与组织化学染色对切片进行HE染色,具体步骤如下:切片经常规脱蜡、复水后,浸入苏木精染液中染色10~20 min,蒸馏水冲洗,梯度酒精脱水, 95%酒精脱水后,切片放入曙红染液染色数秒,然后放入95%酒精中数秒,经常规脱水、透明、封片,即可在显微镜下观察牙鲆幽门盲囊组织结构。对切片进行AB-PAS染色来观察黏液细胞,具体步骤如下:切片经常规脱蜡、复水后,放入1% AB液(pH=2.5)中染色30 min,蒸馏水洗去染料后用1%过碘酸水溶液氧化处理5~10 min,蒸馏水清洗切片,将切片放入Schiff试剂中并在暗处密闭染色30 min,不经水洗直接放入亚硫酸氢钠溶液中清洗3次,每次2 min,流水冲洗,最后常规脱水、透明、封片,显微镜下观察黏液细胞。对于免疫后各时间点的牙鲆幽门盲囊样品,利用AB-PAS染色观察不同种类黏液细胞的变化。从各时间点的切片中随机选取3张进行观察,每张切片随机观察3个以上视野,对视野中不同种类的黏液细胞进行观察并统计。
1.5 间接免疫荧光技术健康牙鲆幽门盲囊的石蜡切片经脱蜡复水,在高压灭菌锅内进行抗原修复后,用5%的牛血清白蛋白(BSA)孵育45 min以阻断非特异性结合。然后分别将鼠抗牙鲆Muc2和Muc5ac抗体(1∶1 000,PBS稀释)作为一抗涂在切片上,37 ℃孵育90 min,之后用PBST(PBS含0.05% Tween 20)洗涤3次每次5 min,洗去一抗后,用Alexa Fluor 488标记的羊抗鼠IgG(1∶1 000,PBS稀释)作为二抗涂在切片上,37 ℃孵育45 min。然后用PBST洗涤3次,用4’, 6-二氨基-2-苯基吲哚(DAPI,1∶2 000稀释,购自Thermo Fisher Scientific)在25 ℃下染细胞核10 min,滴加抗荧光淬灭封片剂封片。对于免疫后各时间点的牙鲆幽门盲囊样品,利用鼠抗Muc2抗体进行染色,计数黏液细胞数量变化。使用未免疫小鼠血清代替一抗作为阴性对照。各时间点随机取3张切片观察,每张切片随机观察3个以上视野,对黏液细胞进行计数并统计。
1.6 扫描电子显微镜标本制备取健康牙鲆幽门盲囊,用PBS(pH=7.4)冲洗干净,在4 ℃下用2.5%戊二醛进行前固定,再用2%(v/v) 四氧化锇进行后固定。PBS冲洗3次后,将样品放在梯度酒精中脱水,临界点干燥,离子溅射镀膜仪镀金,扫描电子显微镜下观察幽门盲囊黏膜及黏液细胞。
1.7 黏液细胞的增殖检测取样前48 h对牙鲆腹腔注射胸腺嘧啶脱氧核苷类似物(EdU),取样后将组织包埋于冰冻切片包埋剂(OCT)中,-80 ℃冷冻,使用冷冻切片机制备6 μm厚的冰冻切片。根据EdU细胞增殖试剂盒说明书配制Click反应液。5% BSA孵育结束后,将Click反应液滴加到切片上,黑暗中孵育30 min。然后用鼠抗牙鲆Muc2抗体(1∶1 000,PBS稀释)作为一抗,在37 ℃下避光孵育90 min,PBST洗涤3次,每次5 min。之后使用Alexa Fluor 649标记的羊抗鼠IgG(1∶1 000,PBS稀释)作为二抗,37 ℃条件下避光孵育1 h,PBST洗涤3次,每次5 min。利用DAPI染细胞核10 min,最后使用抗荧光淬灭封片剂封片。以未免疫小鼠血清代替一抗作为阴性对照。
1.8 qRT-PCR检测黏蛋白muc2基因水平变化提取不同时间点的幽门盲囊组织样品的总RNA,利用反转录试剂盒反转为cDNA。qRT-PCR反应体系为:SYBR Premix Ex Taq 10 μL,DEPC水7.2 μL,正向引物0.4 μL,反向引物0.4 μL和cDNA模板2 μL,共20 μL。qRT-PCR反应条件为:95 ℃预变性30 s; 95 ℃变性20 s,56 ℃退火20 s,72 ℃延伸20 s,进行45个循环; 95 ℃ 5 s,60 ℃ 1 min,72 ℃ 10 s。以β-actin基因为内参基因。采用2-△△Ct法分析免疫后不同时间点牙鲆黏蛋白muc2基因的相对表达量。所用引物如表 1所示。
|
|
表 1 实时荧光定量反转录PCR所用引物 Table 1 Primers used in real-time quantitative reverse transcription PCR |
将收集好的各时间点的幽门盲囊黏液包被在96孔酶标板中,每孔加黏液100 μL,每个样品设置3个重复,酶标板放于4 ℃冰箱过夜。次日甩去黏液,用PBST洗涤各样品孔3次,每次5 min。每孔加入100 μL 5%的BSA,放入37 ℃培养箱中孵育1 h,用PBST洗涤各样品孔3次,每次5 min。将100 μL的鼠抗牙鲆Muc2抗体(1∶500,PBS稀释)加入到样品孔中,以未免疫鼠血清作为阴性对照,放于37 ℃培养箱中孵育1 h。PBST洗涤各样品孔3次后,将100 μL的碱性磷酸酶标记的羊抗鼠IgG抗体(1∶2 000,PBS稀释)加入到样品孔中,放于37 ℃培养箱中孵育1 h,再将100 μL含0.1%的4-硝基苯磷酸二钠(pNPP)的发色液加入到样品孔中并避光反应10 min,最后每孔加入2 mol/L NaOH终止发色,在405 nm条件下测定每个样品的平均吸光度值(Optical density,OD)。
1.10 统计学分析用Excel和SPSS 20软件进行数据统计分析,统计学比较采用单因素方差分析(One-way ANOVA)检验,以P<0.05作为差异显著水平。
2 结果 2.1 牙鲆幽门盲囊组织结构牙鲆幽门盲囊位于胃和肠之间,是胃与肠相连的部位。牙鲆的幽门盲囊由4个管状突起组成,其中3个盲管靠近胃的方向,位于同一个圆面上,第四个盲管靠近肠的方向(见图 1(a))。牙鲆幽门盲囊各盲管由内向外依次为黏膜层、黏膜下层、肌肉层和浆膜层(见图 1(b))。黏膜上皮层由单层柱状上皮细胞构成,上皮细胞游离端具有微绒毛,上皮细胞间分布着经HE染色后呈空泡状的黏液细胞(见图 1(e))。黏膜层向肠腔内延伸,形成纵向褶皱,无规则弯曲排列,上皮下为固有层(见图 1(f))。黏膜下层由疏松结缔组织构成,其中分布有大量的血管(见图 1(d)、(g))。肌肉层由两层平滑肌组成,分别为内层的环肌和外层的纵肌(见图 1(g))。浆膜层由薄层疏松结缔组织和间皮组成(见图 1(g))。

|
( (a) 牙鲆幽门盲囊; (b) 牙鲆幽门盲囊横切面,标尺=1 mm; (c)、(h) 牙鲆幽门盲囊整体纵切面,标尺=3 mm; (d)、(e)、(f)、(g) 牙鲆幽门盲囊纵切面局部放大,标尺=50 μm。Lu:肠腔; EC:上皮细胞; LP:固有层; GC:杯状细胞; BV:血管; SM:黏膜下层; CM:环肌; LM:纵肌; S:浆膜层。(a) Pyloric caeca of flounder; (b) Transverse section of the pyloric caeca of flounder, bar=1 mm; (c), (h) Overall longitudinal section of the pyloric caeca of flounder, bar=3 mm; (d), (e), (f), (g) Longitudinal section of the pyloric caeca of flounder, bar=50 μm. Lu: lumen; EC: epithelial cell; LP: lamina propria; GC: goblet cell; BV: blood vessel; SM: submucosa; CM: circular muscle; LM: longitudinal muscle; S: serosa. ) 图 1 牙鲆幽门盲囊HE染色 Fig. 1 HE staining of pyloric caeca of flounder |
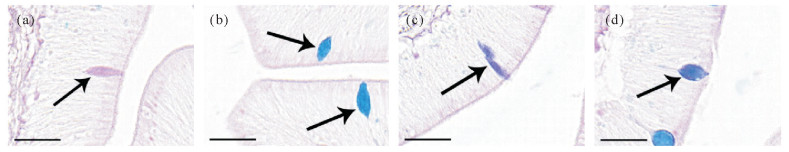
根据AB-PAS染色结果可将黏液细胞分为4种类型:Ⅰ型黏液细胞,呈红色含有中性黏多糖(见图 2(a)); Ⅱ型黏液细胞,呈蓝色含酸性黏多糖(见图 2(b)); Ⅲ型黏液细胞,呈紫红色,含有的黏多糖以中性为主同时含有少量酸性黏多糖(见图 2(c)); Ⅳ型黏液细胞,呈蓝紫色,含有的黏多糖以酸性为主同时含有少量中性黏多糖(见图 2(d))。健康牙鲆幽门盲囊中黏液细胞以Ⅱ型为主,Ⅰ型次之,Ⅲ、Ⅳ型数量较少。
|
( 牙鲆幽门盲囊黏膜上皮中Ⅰ(a)、Ⅱ(b)、Ⅲ(c)和Ⅳ(d)型黏液细胞,分别被AB-PAS染成红色、蓝色、紫红色和蓝紫色(箭头),标尺=25 μm。Four types of mucous cells, Ⅰ (a), Ⅱ (b), Ⅲ (c) and Ⅳ (d), in the pyloric caeca of flounder, which was stained magenta, blue, purple and blueviolet (arrow) by AB-PAS staining, respectively, bar=25 μm. ) 图 2 牙鲆幽门盲囊黏液细胞分类 Fig. 2 Classification of mucous cells in the pyloriccaeca of flounder |
黏液细胞位于黏膜褶的上皮细胞之间,在各盲管间的种类和分布情况并无太大差别,黏膜褶顶部的黏液细胞数量较多,底部的黏液细胞数量较少(见图 3A)。扫描电镜下,黏液未从黏液细胞排出时,可在细胞顶部观察到聚集的黏液颗粒(见图 3B(a)),黏液由黏液细胞排出后,散布在细胞表面,呈颗粒状或束状(见图 3B(b))。间接免疫荧光结果显示,牙鲆幽门盲囊4个盲管的黏液细胞均呈现Muc2阳性荧光(见图 3C(a)),但未观察到Muc5ac阳性荧光(见图 3C(b)),表明其表达黏蛋白Muc2,但不表达黏蛋白Muc5ac; 阴性对照中均未观察到阳性荧光(未展示图片)。

|
( A. 牙鲆幽门盲囊HE染色图(a)以及AB-PAS染色图(b),标尺=150 μm。B. 牙鲆幽门盲囊黏膜表面的扫描电镜图,箭头所指为黏液细胞分泌的黏蛋白颗粒,标尺=10 μm。C. 黏液细胞呈现黏蛋白Muc2阳性(a),但是黏蛋白Muc5ac为阴性(b),标尺=50 μm。A. HE staining of pyloric caeca of flounder (a) and AB-PAS staining (b), bar=150 μm. B. Scanning electron microscope image of the mucosa of pyloric caeca in flounder, the arrow indicated the mucin granules secreted by mucous cells, bar=10 μm. C. Mucous cells were stained mucin Muc2-positive (a) but Muc5ac-negative (b), bar=50 μm. ) 图 3 牙鲆幽门盲囊黏液细胞及其分泌黏蛋白 Fig. 3 Mucous cells and mucin secretion in the pyloric caeca of the flounder |
使用灭活迟缓爱德华氏菌注射免疫牙鲆后,AB-PAS染色结果显示,免疫后不同时间点牙鲆幽门盲囊中黏液细胞的种类以及数量发生了变化,但4个盲管之间无明显差异(见图 4A)。免疫前,幽门盲囊中黏液细胞多数为Ⅱ型黏液细胞,少量为Ⅰ型黏液细胞,Ⅲ、Ⅳ型黏液细胞含量较少(见图 4A); 免疫后,Ⅰ型黏液细胞数量相对减少,而Ⅱ、Ⅲ和Ⅳ型黏液细胞数量增多(见图 4A),表明黏液成分由中性黏多糖逐渐转变为酸性黏多糖。幽门盲囊中Ⅱ和Ⅳ型黏液细胞数量在第3和5天时达到最高值,Ⅲ型黏液细胞数量在第5天时达到最高值(见图 4B)。

|
( A. 黑色实心箭头表示Ⅰ型黏液细胞(红色),虚线空心箭头表示Ⅱ型黏液细胞(蓝色),无末端黑色箭头表示Ⅲ型黏液细胞(紫红色),黑色空心箭头表示Ⅳ型黏液细胞(蓝紫色)。B. 免疫后不同时间点牙鲆幽门盲囊中不同类型黏液细胞数量变化。+表示很少; ++表示较少; +++表示中度; ++++ 表示较多; +++++表示很多。A. The black solid arrows showed type Ⅰ mucous cells (magenta), the dotted hollow arrow showed type Ⅱ mucous cells (blue), the black arrowhead showed type Ⅲ mucous cells (purple), the black hollow arrow showed type Ⅳ mucous cells (blueviolet). B. Changes of different types of mucous cell numbers in pyloric caeca of flounder at different time points after injection immunization. + very few; ++ a few; +++ moderate; ++++ many; +++++ a great many. ) 图 4 迟缓爱德华氏菌灭活疫苗注射免疫后不同时间点牙鲆幽门盲囊AB-PAS染色结果 Fig. 4 The result of AB-PAS staining of pyloriccaeca of flounder at different time points after immunization with inactivated E. tarda |
间接免疫荧光结果观察到,Muc2黏蛋白从黏液细胞顶部释放至盲囊腔中,以及已排空或部分排空的黏液细胞(见图 5A)。牙鲆幽门盲囊中Muc2+黏液细胞数量在免疫后开始增多,并在第3天达到最高值(见图 5B)。

|
( A. 白色实心箭头所指为充满黏液的黏液细胞,白色空心箭头所指为已排出黏液的黏液细胞,无末端白色箭头所指为未排空黏液的黏液细胞。B. 免疫后不同时间点黏液细胞数量的变化情况(表示P<0.05)。各时间点随机取3张切片观察,每张切片随机观察3个以上视野,对黏液细胞进行计数并统计。A. The white solid arrow pointed to mucous cells filled with mucus, the white hollow arrow indicated the empty mucous cells that had released the mucus, the white arrowheads indicated mucous cells that had not emptied completely. B. Changes of mucous cell numbers in pyloric caeca of flounder at different time points after injection immunization (indicates P < 0.05). At each time point, 3 slices were randomly taken for observation, and for each slice more than 3 fields of view were randomly examined to count and analyze the mucous cells. ) 图 5 迟缓爱德华氏菌灭活疫苗注射免疫后不同时间点牙鲆幽门盲囊中黏液细胞数量变化 Fig. 5 Changes of mucous cell numbers in pyloriccaeca of flounder at different time points after injection immunization with inactivated E. tarda |
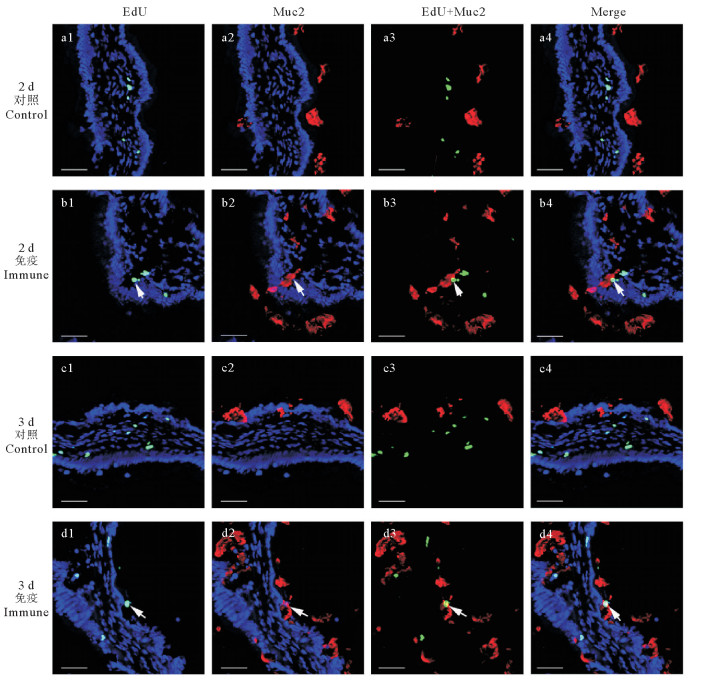
使用灭活迟缓爱德华氏菌疫苗注射免疫牙鲆后,间接免疫荧光结果显示,在第2天(见图 6 b1—b4)和第3天(见图 6 d1—d4)牙鲆幽门盲囊中Muc2+黏液细胞和EdU+细胞存在共定位,Muc2+-EdU+双阳性荧光表明存在增殖性黏液细胞,这说明注射免疫引起了黏液细胞增殖。对照组中,观察到EdU+细胞,这说明存在细胞增殖现象,但未观察到双阳性细胞。
|
( a1—d1:绿色荧光表示牙鲆幽门盲囊中EdU阳性细胞。a2—d2: 红色荧光表示牙鲆幽门盲囊中Muc2阳性细胞。a3—d3:牙鲆幽门盲囊中EdU和Muc2双阳性细胞。a4—d4:合并图,蓝色荧光为DAPI衬染的细胞核。白色箭头所指为EdU和Muc2阳性细胞,bar=20 μm。a1—d1: Green fluorescence indicated EdU positive cells in pyloric caeca of flounder. a2—d2: Red fluorescence indicated Muc2 positive cells in pyloric caeca of flounder. a3—d3: EdU and Muc2 double positive cells in pyloric caeca of flounder. a4—d4: Merge graphs, showing the cell nucleus was stained blue by DAPI. White arrows indicated EdU and Muc2 positive cells, bar=20 μm. ) 图 6 迟缓爱德华氏菌灭活疫苗免疫后牙鲆幽门盲囊中EdU和Muc2共定位分析 Fig. 6 Colocalization analysis of EdU and Muc2 in pyloric caeca of flounder after injection immunization with inactivated E. tarda |
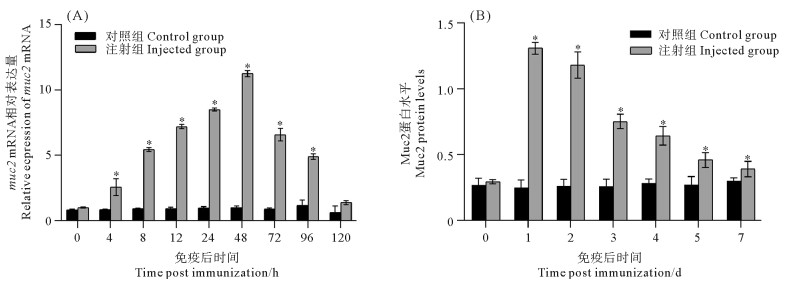
灭活迟缓爱德华氏菌疫苗注射免疫牙鲆后,幽门盲囊组织中muc2基因的表达从4 h开始显著升高(P<0.05),呈先上升后下降的趋势,在免疫后48 h达到峰值,是对照组的11.3倍(见图 7(A)),然后逐渐降低到对照水平(120 h)。ELISA法检测牙鲆幽门盲囊黏液中Muc2蛋白水平变化,结果表明幽门盲囊黏液中Muc2蛋白水平升高(P<0.05),在7 d内呈先上升后下降的趋势,在第1天到达峰值,第7天仍高于对照组水平(见图 7(B))。
|
( 表示P<0.05。indicates P < 0.05. ) 图 7 迟缓爱德华氏菌灭活疫苗注射免疫后不同时间点黏蛋白Muc2在基因(A)和蛋白(B)水平的表达变化 Fig. 7 Changes of Muc2 expression at gene (A) and protein (B) levels after injection immunization with inactivated E. tarda at different time points |
本研究中,我们针对牙鲆幽门盲囊的组织结构以及黏液细胞的免疫应答进行了研究。鱼类的幽门盲囊位于肠的起始端,实质上是肠道的分支,是鱼类特有的消化器官。肉食性鱼类具有幽门盲囊[25]。我们发现牙鲆的幽门盲囊共有4根盲管,前3根盲管靠近胃的方向,且位于同一圆面上,第4根盲管位于前3根盲管的后侧。幽门盲囊的数量因鱼种类的不同而存在很大差别,大黄鱼(Larimichthys crocea)的幽门盲囊有数十个盲管[29],鳜的幽门盲囊有一百多条盲管[30],虫纹鳕鲈(Maccullochella peelii)的幽门盲囊有4~5个盲管[31]。幽门盲囊不仅增加了消化和吸收面积,而且在腹腔的有限空间里增加了肠的功能[25]。研究表明,斑点拟绯鲤(Pseudupeneus maculatus)[32]、虎利齿脂鲤(Hoplias malabaricus)[33]的幽门盲囊中检测到消化酶活性。本文通过对牙鲆幽门盲囊进行横向和纵向切片观察,发现4个盲管无组织结构上的差异,其组织学结构分为黏膜层、黏膜下层、肌肉层和浆膜层。黏膜上皮层由单层柱状上皮细胞组成,游离端具有微绒毛,其间分布着黏液细胞,黏膜层向肠腔延伸形成大量纵向褶皱,与肠道组织结构相似。因此,虽然不同鱼类幽门盲囊在盲管数量上差异较大,但在组织结构方面基本相似。
黏液细胞普遍存在于鱼类黏膜相关淋巴组织中,在病原微生物入侵时能分泌大量黏液[34-35],与其中的补体物质、抗体等一起在鱼类免疫防御中发挥着重要作用[4, 17]。黏液细胞中的黏液主要成分为黏多糖,可分为中性黏多糖和酸性黏多糖两大类。由于不同黏液细胞中所含黏多糖的成分不同,经AB-PAS染色后可呈现不同颜色,由此可将黏液细胞分为Ⅰ、Ⅱ、Ⅲ和Ⅳ型4种类型[17]。Ⅰ型黏液细胞呈红色,含中性黏多糖; Ⅱ型黏液细胞呈蓝色,含酸性黏多糖; Ⅲ型黏液细胞呈紫红色,主要含中性黏多糖同时含有少量酸性黏多糖; Ⅳ型黏液细胞呈蓝紫色,主要含有酸性黏多糖同时含有少量中性黏多糖。本研究发现健康牙鲆幽门盲囊的黏液细胞以Ⅱ型为主,Ⅰ型较少,Ⅲ型和Ⅳ型黏液细胞含量较少,各盲管间所含黏液细胞种类无显著差异。研究表明,鱼类消化道黏液细胞类型与其功能有着密切联系。在有胃鱼中,胃黏液细胞以Ⅰ型黏液细胞为主,Ⅰ型黏液细胞中含有中性黏液,可以调节胃中的pH平衡,与胃的功能相适应[34]。食道和后肠中存在大量Ⅱ型黏液细胞,Ⅱ型和Ⅳ型黏液细胞主要含有酸性黏液,酸性黏液可以保持管腔润滑,发挥促进食物的吞咽、蛋白质的消化等作用[36]。硬骨鱼类肠道黏液细胞分泌的黏液与食物的润滑和消化、营养物质运输与吸收、阻止细菌入侵等功能密切相关[22]。牙鲆幽门盲囊黏液细胞以Ⅱ型为主,Ⅰ型次之,与肠的黏液细胞类型更为相似[23]。本文中,牙鲆黏液细胞的分布在盲管的顶部、中部和基部并无明显差别,但在幽门盲囊的黏膜褶中,黏液细胞在褶皱基部分布较少,而在顶部分布较多,这可能更利于其分泌黏液清除外来物质。目前为止,对于鱼类幽门盲囊黏液细胞分泌的黏蛋白组成尚不清楚。我们利用前期制备的黏蛋白Muc2和Muc5ac抗体检测牙鲆幽门盲囊中黏蛋白的表达情况,发现其黏液细胞表达黏蛋白Muc2,而不表达Muc5ac。这一结果与牙鲆肠道表达的黏蛋白类型一致,但不同于牙鲆皮肤(仅表达Muc5ac)和鳃(表达Muc2和Muc5ac)的黏蛋白组成[28]。鲤的Muc2只在肠中表达,在鳃中不表达[37]。人的Muc2黏蛋白主要存在于肠道,在支气管中表达水平较低[38]。这可能与不同黏蛋白成分及不同动物组织的功能差异有关。
本研究结果显示,经迟缓爱德华氏菌灭活疫苗注射免疫后牙鲆幽门盲囊中黏液细胞种类发生了变化,Ⅰ型黏液细胞减少,Ⅱ、Ⅲ、Ⅳ型黏液细胞增多,含酸性黏多糖的黏液细胞数量总体增多,说明疫苗免疫诱导黏液细胞中黏液的特性由中性黏多糖向酸性黏多糖转变,表明黏液细胞的功能发生了改变。我们实验室前期研究发现,经免疫刺激后牙鲆鳃、肠和皮肤黏膜相关淋巴组织中Ⅰ型黏液细胞减少,Ⅱ、Ⅲ和Ⅳ型黏液细胞逐渐增多[23]。这与本研究的结果相似。在有关花鲈[16]、鲤[17]、鲫(Carassius auratus)[39]、胡子鲶[20]、重口裂腹鱼(Schizothorax davidi)[40]肠道黏液细胞及黏液特性的研究中也观察到相似现象。中性黏液物质可形成一层不易被酸液破坏的黏液层,起到一定的缓冲作用以及调节pH值的作用,从而保护黏膜上皮[41]。酸性黏液则与黏液的黏度有关,大多数病原菌的最适生长pH值为弱碱性,因此酸性黏液的增多可更好地溶解、抑制或杀死病原菌来增强黏液的保护作用[42-44]。牙鲆幽门盲囊黏液细胞中黏多糖特性的变化如何影响黏液的保护作用还需进一步研究。
李学军等[43]采用ConA或PHA对鲇(Silurus asotus)进行浸泡和注射刺激后,发现皮肤和鳃中黏液细胞数量均明显增多。Marel等[13]研究发现,在高浓度菌液浸泡刺激下,鲤体表黏液分泌量及黏液细胞数量均显著增多。路珍等[23]研究发现牙鲆在疫苗浸泡免疫后肠、皮肤和鳃黏膜相关淋巴组织中黏液细胞数量均呈增多趋势。同样地,在本研究中,经疫苗注射免疫后牙鲆幽门盲囊中黏液细胞的数量增多,在第3天达到峰值后逐渐下降至免疫前水平,并且在免疫后的第2天和第3天均可看到Muc2和EdU双阳性的黏液细胞,说明免疫刺激诱导了黏液细胞的增殖,从而使细胞数量增多。有证据表明,刺激后黏液细胞可以加速黏液从细胞基部到顶部的运输速率[45]。鱼类在感染病原微生物后,可引起黏膜相关淋巴组织中的黏液细胞分泌黏液增多,说明鱼类黏液细胞对外界病原微生物有一定的抵抗作用[42-43]。此外,黏液细胞可以调节黏蛋白由基础分泌向刺激型胞外分泌的转变,在短时间内迅速产生大量黏蛋白[46]。关于硬骨鱼黏液分泌特性和调节机制的研究较少。我们实验室前期发现牙鲆浸泡免疫后,肠、皮肤和鳃黏膜相关淋巴组织中Muc2和Muc5ac在基因水平和蛋白水平均显著上调[28]。本研究发现牙鲆在免疫刺激后,幽门盲囊中Muc2在基因和蛋白水平同样出现了显著上调的趋势,结合幽门盲囊中黏液细胞数量增加,说明黏液细胞的增殖和黏蛋白的加速分泌可能有利于补充消耗的黏蛋白,增强黏液屏障作用,有助于维持黏膜稳态,这证明了牙鲆幽门盲囊具有重要的免疫防御功能,其中黏液细胞在其非特异性免疫中扮演了关键角色。
硬骨鱼类的黏膜免疫对于系统免疫是很好的补充[5-7, 47-48]。了解黏膜免疫系统的功能和作用机制是黏膜疫苗免疫接种的基础,近年来对黏膜免疫的研究越来越多,但仍有很多问题没有解决[49]。本研究探讨了疫苗注射免疫诱导的牙鲆幽门盲囊中黏液细胞种类和数量变化及黏蛋白表达变化,为进一步研究牙鲆黏液细胞在黏膜免疫中的作用提供重要参考。
4 结语牙鲆幽门盲囊有4个盲管,其组织结构由黏膜层、黏膜下层、肌肉层和浆膜层构成,其中含有4种类型的黏液细胞。迟缓爱德华氏菌灭活疫苗免疫诱导牙鲆幽门盲囊中黏液细胞增多,黏液特性由中性向酸性变化,黏蛋白在基因表达和蛋白水平上均上调,这些变化在鱼体抵御外界病原入侵过程中发挥着重要作用。本文结果为阐明鱼类幽门盲囊的免疫功能以及黏液细胞及其分泌黏液在黏膜免疫防御中的作用提供了重要参考。
| [1] |
Salinas I, Zhang Y A, Sunyer J O. Mucosal immunoglobulins and B cells of teleost fish[J]. Developmental & Comparative Immuno-logy, 2011, 35(12): 1346-1365. (  0) 0) |
| [2] |
Esteban M Á. An overview of the immunological defenses in fish skin[J]. International Scholarly Research Notices Immunology, 2012, 2012: 3-4. (  0) 0) |
| [3] |
Salinas I. The mucosal immune system of teleost fish[J]. Biology, 2015, 4(3): 525-539. DOI:10.3390/biology4030525 (  0) 0) |
| [4] |
杨桂文, 安利国. 鱼类粘液细胞研究进展[J]. 水产学报, 1999, 23(4): 403-408. Yang G W, An L G. A review on the researches of fish mucous cells[J]. Journal of Fisheries of China, 1999, 23(4): 403-408. (  0) 0) |
| [5] |
Di C J, Halliday W J. Relationship of catfish serum antibodies to immunoglobulin in mucus secretion[J]. Australian Journal of Experimental Biology and Medical Science, 1971, 49(5): 517-519. DOI:10.1038/icb.1971.56 (  0) 0) |
| [6] |
Gona O. Mucous glycoproteins of teleostean fish: A comparative histochemical study[J]. The Histochemical Journal, 1979, 11(6): 709-718. DOI:10.1007/BF01004734 (  0) 0) |
| [7] |
Estévez J, Leiro J, Tornazo A E, et al. Role of serum antibodies in protection of vaccinated turbot (Scophthalmus maximus) against vibriosis[J]. Aquaculture, 1994, 123(3-4): 197-204. DOI:10.1016/0044-8486(94)90058-2 (  0) 0) |
| [8] |
Fletcher T C, Grant P T. Immunoglobulins in the serum and mucus of the plaice (Pleuronectes platessa)[J]. Biochemical Journal, 1969, 115(5): 65. DOI:10.1042/bj1150065P (  0) 0) |
| [9] |
Singh B R, Guha G, Munshi J S. Mucous cells of the respiratory sac in an air-breathing fish Saccobranchus fossilis (Bloch)[J]. Cellule, 1974, 70(1): 5-15. (  0) 0) |
| [10] |
Kitzan S M, Sweeny P R. A light and electron microscope study of the structure of Protopterus annectens epidermis. I. Mucus production[J]. Canadian Journal of Zoology, 1968, 46(4): 767-772. DOI:10.1139/z68-106 (  0) 0) |
| [11] |
Zaccone G. Effect of osmotic stress on the chloride and mucous cells in the gill epithelium of the fresh-water teleost Barbus filamentosus (Cypriniformes, Pisces): A structural and histochemical study[J]. Acta Histochemica, 1981, 68(2): 147-159. DOI:10.1016/S0065-1281(81)80070-0 (  0) 0) |
| [12] |
Subramanian S, Mackinnon S L, Ross N W. A comparative study on innate immune parameters in the epidermal mucus of various fish species[J]. Comparative Biochemistry and Physiology-Part B: Biochemistry and Molecular Biology, 2007, 148(3): 256-263. DOI:10.1016/j.cbpb.2007.06.003 (  0) 0) |
| [13] |
Marel M V D, Caspari N, Neuhaus H, et al. Changes in skin mucus of common carp, Cyprinus carpio L., after exposure to water with a high bacterial load[J]. Journal of Fish Diseases, 2010, 33(5): 431-439. DOI:10.1111/j.1365-2761.2010.01140.x (  0) 0) |
| [14] |
Pittman K, Pittman A, Karlson S, et al. Body site matters: An eva-luation and application of a novel histological methodology on the quantification of mucous cells in the skin of Atlantic salmon, Salmo salar L[J]. Journal of Fish Diseases, 2013, 36(2): 115-127. DOI:10.1111/jfd.12002 (  0) 0) |
| [15] |
Neuhaus H, Marel V D M, Caspari N, et al. Biochemical and histochemical effects of perorally applied endotoxin on intestinal mucin glycoproteins of the common carp Cyprinus carpio[J]. Diseases of Aquatic Organisms, 2007, 77(1): 17-27. (  0) 0) |
| [16] |
谢湘筠, 林淑慧, 林树根. 花鲈消化道粘液细胞的类型及分布[J]. 福建农业学报, 2007, 22(3): 271-275. Xie X Y, Lin S H, Lin S G. Types and distribution of mucous cells in the digestive tracts of Lateolabrax japonicus[J]. Fujian Journal of Agricultural Sciences, 2007, 22(3): 271-275. (  0) 0) |
| [17] |
尹苗, 安利国, 杨桂文, 等. 鲤鱼粘液细胞类型的研究[J]. 动物学杂志, 2000, 35(1): 8-9. Yin M, An L G, Yang G W, et al. Study on the type of mucous cells in carps (Cyprinus carpio)[J]. Chinese Journal of Zoology, 2000, 35(1): 8-9. (  0) 0) |
| [18] |
黄智慧, 马爱军. 大菱鲆体表粘液细胞组化研究及高温胁迫对其类型和分布的影响[J]. 水产学报, 2010, 34(5): 719-725. Huang Z H, Ma A J. Effects of high temperature on the type and distribution of turbot (Scophthalmus maximus) skin mucous cells[J]. Journal of Fisheries of China, 2010, 34(5): 719-725. (  0) 0) |
| [19] |
关海红, 尹家胜. 哲罗鱼的消化道黏液细胞形态及分布[J]. 水产学杂志, 2010, 23(2): 42-45. Guan H H, Yin J S. Morphology and distribution of the alimentary canal mucous cells in Hucho taimen[J]. Chinese Journal of Fisheries, 2010, 23(2): 42-45. (  0) 0) |
| [20] |
尹苗, 杨桂文, 安利国. 胡子鲶粘液细胞类型及其在消化道中的分布[J]. 动物学报, 2001, 47: 116-119. Yin M, Yang G W, An L G. Study on the type of mucous cells and it's distribution in alimentary tract of Clarias fuscus[J]. Acta Zoologica Sinica, 2001, 47: 116-119. (  0) 0) |
| [21] |
王永波, 陈国华, 王珺, 等. 波纹唇鱼消化道黏液细胞的类型与分布[J]. 渔业科学进展, 2010, 31(5): 22-28. Wang Y B, Chen G H, Wang J, et al. Types and distribution of mucous cells in the digestive tracts of Cheilinus undulates Rüppell[J]. Progress in Fishery Sciences, 2010, 31(5): 22-28. (  0) 0) |
| [22] |
李凤杰, 曾令清, 葛胜东, 等. 不同摄食状态下南方鲇幼鱼肠道黏液细胞的量化分析[J]. 中国水产科学, 2013, 20(1): 75-81. Li F J, Zeng L Q, Ge S D, et al. Changes in the number of intestinal mucous cells of juvenile southern catfish Silurus meridionalis following feeding, starvation, and refeeding[J]. Journal of Fishery Sciences of China, 2013, 20(1): 75-81. (  0) 0) |
| [23] |
路珍, 绳秀珍, 唐小千, 等. 浸泡免疫迟钝爱德华氏菌疫苗诱导牙鲆黏液细胞的动态变化[J]. 水产学报, 2016, 40(3): 414-427. Lu Z, Sheng X Z, Tang X Q, et al. Dynamic changes of mucous cells in Paralichthys olivaceus induced by immersion immunization with inactivated Edwardsiella tarda[J]. Journal of Fisheries of China, 2016, 40(3): 414-427. (  0) 0) |
| [24] |
Ballesteros N A, Castro R, Abos B, et al. The pyloric caeca area is a major site for IgM+ and IgT+ B cell recruitment in response to oral vaccination in rainbow trout[J]. Fish & Shellfish Immunology, 2013, 34(6): 1695-1696. (  0) 0) |
| [25] |
杜佳, 徐革锋, 韩英, 等. 鱼类消化道组织学研究进展[J]. 水产学杂志, 2009, 22(4): 56-64. Du J, Xu G F, Han Y, et al. Research progress in the histology of the digestive tract of fish[J]. Chinese Journal of Fisheries, 2009, 22(4): 56-64. (  0) 0) |
| [26] |
Wang K L, Chen S N, Huo H J, et al. Identification and expression analysis of sixteen Toll-like receptor genes, TLR1, TLR2a, TLR2b, TLR3, TLR5M, TLR5S, TLR7-9, TLR13a-c, TLR14, TLR21-23 in mandarin fish Siniperca chuatsi[J]. Developmental and Comparative Immunology, 2021, 121: 104100. DOI:10.1016/j.dci.2021.104100 (  0) 0) |
| [27] |
Zhang W F, Deng H W, Fu Y T, et al. Production and characterization of monoclonal antibodies against mandarin fish ranavi-rus and first identification of pyloric caecum as the major target tissue[J]. Journal of Fish Diseases, 2022, 46(3): 189-199. (  0) 0) |
| [28] |
Wang J C, Gao J L, Sheng X Z, et al. Teleost Muc2 and Muc5ac: Key guardians of mucosal immunity in flounder (Paralichthys olivaceus)[J]. International Journal of Biological Macromolecules, 2024, 277(1): 134127. (  0) 0) |
| [29] |
崔龙波, 迟爽, 李新华, 等. 大黄鱼消化系统的组织学和组织化学研究[J]. 烟台大学学报(自然科学与工程版), 2014, 27(4): 266-270. Cui L B, Chi S, Li X H, et al. Histological and histochemistrical study on digestive system of Pseudosciaena crocea Riciardson[J]. Journal of Yantai University (Natural Science and Engineering Edition), 2014, 27(4): 266-270. (  0) 0) |
| [30] |
赵亮亮, 施琳澜, 赵金良, 等. 鳜幽门盲囊早期发育的组织学特征[J]. 上海海洋大学学报, 2021, 30(4): 684-690. Zhao L L, Shi L L, Zhao J L, et al. Histological features of organogenesis of the pyloric caecum of Siniperca chuatsi[J]. Journal of Shanghai Ocean University, 2021, 30(4): 684-690. (  0) 0) |
| [31] |
安丽, 董学飒, 张延华, 等. 虫纹鳕鲈外形特征及内部消化系统结构的研究[J]. 长江大学学报(自然科学版), 2013, 10(17): 29-35. An L, Dong X S, Zhang Y H, et al. Morphological characteristics and structure of digestive system of Macculochella peeli[J]. Journal of Yangtze University(Natural Science Edition), 2013, 10(17): 29-35. (  0) 0) |
| [32] |
Rodrigo B A, Michelle M B, Paticia M G P, et al. Alkaline proteases from digestive tract of four tropical fish[J]. Brazilian Journal of Food Technology, 2003, 6(2): 279-284. (  0) 0) |
| [33] |
郭恩棉, 王鑫, 周培勇, 等. 短盖巨脂鲤消化系统胚后发育学的研究[J]. 莱阳农学院学报, 2002, 19(3): 161-167. Guo E M, Wang X, Zhou P Y, et al. Studies on the development of digestive system of the white achama[J]. Journal of Laiyang Agricultural College, 2002, 19(3): 161-167. (  0) 0) |
| [34] |
Harris J E, Watson A, Hunt S. Histochemical analysis of mucous cells in the epidermis of brown trout Salmo trutta L[J]. Journal of Fish Biology, 2006, 5(3): 345-351. (  0) 0) |
| [35] |
Buchmann K, Bresciani J. Microenvironment of Gyrodactylus derjavini on rainbow trout Oncorhynchus mykiss: Association between mucous cell density in skin and site selection[J]. Parasitology Research, 1997, 84(1): 17-24. DOI:10.1007/s004360050350 (  0) 0) |
| [36] |
张伟妮, 林旋, 林树根, 等. 褐牙鲆消化道粘液细胞的类型及分布[J]. 福建农林大学学报(自然科学版), 2009, 38(3): 280-284. Zhang W N, Lin X, Lin S G, et al. Types and distribution of mucous cells in the digestive tract of Paralichthys olivaceus[J]. Journal of Fujian agriculture and Forestry University (Natural Science Edition), 2009, 38(3): 280-284. (  0) 0) |
| [37] |
Marel M, Adamek M, Gonzalez F, et al. Molecular cloning and expression of two beta -defensin and two mucin genes in common carp (Cyprinus carpio L.) and their up-regulation after beta -glucan fee-ding[J]. Fish & Shellfish Immunology, 2012, 32(3): 494-501. (  0) 0) |
| [38] |
Kim J J, Khan I W. Goblet cells and mucins: Role in innate defense in enteric infections[J]. Pathogens, 2013, 2(1): 55-70. DOI:10.3390/pathogens2010055 (  0) 0) |
| [39] |
李新华, 沈锦玉, 尹文林, 等. 银鲫口服嗜水气单胞菌疫苗的免疫和免疫组化研究[J]. 水生生物学报, 2007, 31(1): 125-131. Li X H, Shen J Y, Yin W L, et al. Immunity and immunohistochemistry by oral vaccination of Carassius auratus gibelio using Aeromonas hydrophila vaccine[J]. Acta Hydrobiologica Sinica, 2007, 31(1): 125-131. (  0) 0) |
| [40] |
何敏, 张宇, 方静. 重口裂腹鱼消化道黏液细胞类型及分布研究[J]. 淡水渔业, 2007, 37(2): 24-26. He M, Zhang Y, Fang J. The study of the mucous cells in the digestive of Schizothorax davidi[J]. Freshwater Fisheries, 2007, 37(2): 24-26. (  0) 0) |
| [41] |
曾令清, 李凤杰, 曹振东, 等. 南方鮎幼鱼的胃排空特征及其数学模型[J]. 水产学报, 2011, 35(2): 231-237. Zeng L Q, Li F J, Cao Z D, et al. The analysis of gastric evacuation characteristics and associated mathematical models in juvenile southern catfish (Silurus meridionalis)[J]. Journal of Fisheries of China, 2011, 35(2): 231-237. (  0) 0) |
| [42] |
林旋, 张伟妮, 林树根, 等. 欧洲鳗鲡皮肤、鳃及消化道粘液细胞的分布与类型[J]. 福建农业学报, 2008, 23(1): 39-43. Lin X, Zhang W N, Lin S G, et al. Type and distribution of mucous cells in skin, gills and digestive tracts of Anguilla anguilla[J]. Fujian Journal of Agricultural Sciences, 2008, 23(1): 39-43. (  0) 0) |
| [43] |
李学军, 彭新亮, 乔志刚, 等. ConA或PHA对鲇(Silurus asotus)皮肤和鳃粘液细胞密度的影响[J]. 河南师范大学学报(自然科学版), 2009, 37(6): 108-111. Li X J, Peng X L, Qiao Z G, et al. Effect of ConA or PHA on mucous cells density in the skin and gill of Silurus asotus[J]. Journal of Henan Normal University (Natural Science), 2009, 37(6): 108-111. (  0) 0) |
| [44] |
Vatsos I N, Kotzamanis Y, Henry M, et al. Monitoring stress in fish by applying image analysis to their skin mucous cells[J]. European Journal of Histochemistry, 2010, 54(2): 107-111. (  0) 0) |
| [45] |
Sinan S, Henrik S, Kristina S, et al. Rainbow trout gastrointestinal mucus, mucin production, mucin glycosylation and response to lipopolysaccharide[J]. Fish & Shellfish Immunology, 2022, 122: 181-190. (  0) 0) |
| [46] |
Thomsson K A, Benktander J, Quintanahayashi M P, et al. Mucin O-glycosylation and pathogen binding ability differ between rainbow trout epithelial sites[J]. Fish & Shellfish Immunology, 2022, 133: 349-357. (  0) 0) |
| [47] |
Rombout J H W M, Taverne-Thiele N, Kamp M V D, et al. Differences in mucus and serum immunoglobulin of carp (Cyprinus carpio L.)[J]. Developmental & Comparative Immunology, 1993, 17(4): 309-317. (  0) 0) |
| [48] |
Rombout J H W M, Taverne-Thiele T A J, Villena M I. The gut-associated lymphoid tissue (GALT) of carp (Cyprinus carpio L.): An immunocytochemical analysis[J]. Developmental & Comparative Immunology, 1993, 17(1): 55-66. (  0) 0) |
| [49] |
Vervarcke S, Ollevier F, Kinget R, et al. Mucosal response in African catfish after administration of Vibrio anguillarum O2 antigens via different routes[J]. Fish & Shellfish Immunology, 2005, 18(2): 125-133. (  0) 0) |
 2026, Vol. 56
2026, Vol. 56


