2. 自然资源部滨海城市地下空间地质安全重点实验室, 山东 青岛 266100;
3. 中国海洋大学海洋环境与生态教育部重点实验室, 山东 青岛 266100;
4. 中国海洋大学山东省海洋环境地质工程重点实验室, 山东 青岛 266100;
5. 水利部黄河水利委员会天桥黄河河务局, 河南 郑州 450003
土壤盐碱化严重影响植物生长,阻碍滨海生态景观构建,削弱固碳潜力[1]。滨海盐碱土壤结构板结、Na+含量高、养分贫瘠,微生物活性受限,致使植物营养不足,且吸水困难[2],最终限制植物生长,减少光合作用和垂向土壤的固碳效果[3]。因此,如何改善土壤结构状态,调节植物耐盐性能,提高土壤养分有效性是亟需解决的关键问题。
生物炭作为缓解盐胁迫的一种有效土壤改良剂[4],其多孔结构能够改善土壤通气性和渗透性,缓解土壤板结[5],在提高土壤肥力和改善土壤固碳方面具有重要影响[6]。然而,高pH值限制了生物炭在碱性土壤中的应用[7]。Duan等[8]通过研究发现,酸改性生物炭能够改善盐碱土的水盐分布和水稳性大团聚体的形成,缓解盐碱土壤的pH值,提高养分含量,展现出酸改性生物炭在盐碱土改良中的潜力。王翔宇等[9]对生物炭进行H3PO4改性,发现改性后生物炭比表面积和含氧官能团数量增加,增强土壤对养分的固持与活化效能,提高了对Na+的吸附能力,促进了盐分的向下淋洗,有效改善了根区土壤的微环境。尽管H3PO4改性生物炭在改良盐碱土方面显示出巨大潜力,但其对土壤微生物群落结构的调控作用有限,需结合功能微生物协同增效。
丛枝菌根真菌(Arbuscular mycorrhizal fungi, AMF)能够与90%的植物根系形成互惠共生[10],通过提高植物的根系活性、减少对盐的生理反应缓解盐胁迫损害,增强植物抗逆性,促进植物生长[11]。但盐碱土的极端理化环境严重制约了AMF的定植情况。将生物炭作为AMF的载体,有利于两者的协同作用。前人研究已经证明他们的联合应用能够显著提高植物的光合速率和植物生长[9, 12],但是在滨海盐碱土壤-植物系统中,两者分别作用的路径及互作机制尚不清晰,而且缺乏量化研究。
偏最小二乘路径模型(partial least squares path modeling,PLS-PM)可定量分析多个指标及其影响路径间的因果关系[13]。Kim等[14]通过利用PLS-PM评估了施用生物炭对土壤化学特性和植物毒性的影响;Han等[15]利用PLS-PM揭示了AMF如何增强杨树的耐盐性。我们假设PLS-PM和聚类分析能够探讨土壤盐浓度、pH和养分有效性和植物生长与生理特征间的关系[16],解决盐碱土壤-植物系统中Na+调控机制及养分提升的各自和相互作用路径,为滨海盐碱土植被修复增加固碳潜力提供支持。
本研究将生物炭和AMF联合应用于改良滨海盐碱土,主要达到以下3个目的:(1)探究盐胁迫下生物炭和AMF协同调控Na+的效应;(2)明确盐胁迫下生物炭和AMF对土壤-植物系统养分有效性的影响;(3)通过聚类分析和PLS-PM量化生物炭和AMF协同影响土壤-植物系统的耐盐性及提高养分有效性的作用路径。
1 材料与方法 1.1 实验材料 1.1.1 供试土壤土样样品采自山东省东营市黄河三角洲国家级自然保护区,选择不同盐碱化程度区域进行采样。轻度盐碱土(盐度为2.0)取自黄河口镇(37.69°N,118.95°E),重度盐碱土(盐度为6.8)取自大汶流管理站(37.82°N,119.30°E)。采样深度为表层0~20 cm,土壤样品自然风干,磨碎后过筛(2.0 mm),于室温下保存。供试土样的基本理化性质见表 1所示。
|
|
表 1 供试土壤基本理化性质 Table 1 Basic physical and chemical properties of test soil |
生物炭制备原材料为浒苔(Enteromorpha prolifera),浒苔粉末购自青岛中国海洋大学生物技术有限公司。将干燥的浒苔置于气氛炉(GR.AF80/14,上海)中,以10 ℃·min-1速率升温至400 ℃,在该温度下通N2热解2 h后自然冷却,将所得产物研磨后过0.6 mm筛,得到原始生物炭,记为BC。
王翔宇等[9]通过对照实验研究证实经H3PO4改性后的浒苔生物炭对滨海盐碱土壤盐分的抗逆性最好。改性步骤如下:称取30.0 g BC于锥形瓶中,加入100 mL浓度为10%的H3PO4溶液,于25 ℃下用磁力搅拌器以125 r·min-1搅拌12 h,用去离子水反复清洗至洗液pH稳定,在70 ℃下烘干至恒重,得到10% H3PO4改性生物炭,记为HBC。
1.1.3 供试植物及微生物菌剂黑麦草种子购买于江苏宿迁春满园种业有限公司。AMF提取自中国捷克诺曼环境技术股份有限公司的菌肥中,菌肥以天然黏土作为载体,AMF以孢子形式存在于其中,无其他物质。利用湿筛倾析-蔗糖离心法[17]从菌剂中筛选出AMF活性孢子,经表面消毒后,保存在含有无菌蒸馏水的玻璃瓶中,于4 ℃下贮存备用。
1.2 实验方法在中国海洋大学环境科学与工程学院水土污染分析实验室开展室内盆栽实验。在15 cm×15 cm×18 cm的实验盆中加入1 kg供试土壤样品。根据前期实验结果,生物炭和AMF的添加量分别在1.5%(w/w)时效果最好。将植物种子均匀撒在土壤基质表面,用少量供试土壤均匀覆盖种子,再用去离子水浇透土壤基质,将盆栽置于光照培养箱中,保持每天30 ℃,24 h光照,待种子萌发率达到约50%后将培养条件改为每天30 ℃,16 h光照,每3天浇灌20 mL去离子水,持续种植60 d后收获植物。实验设计如下表 2所示。
|
|
表 2 各处理组的实验设计 Table 2 Experimental design for each treatment group |
土壤pH采用pH计直接测定(土∶水=1∶5,w∶w)。采用原子吸收分光光度法(HJ 491-2019)分别在589和766.5 nm处测定Na+和K+含量,土壤有机碳(SOC)采用重铬酸钾-硫酸氧化法测定[18],全磷采用氢氧化钠熔融-钼锑抗比色法在700 nm处测定(GB 9837-88),有效磷采用碳酸氢钠浸提-钼锑抗比色法在880 nm处测定(HJ 704-2014),全钾采用碱溶-火焰分光光度法直接测定(GB 9836-88),速效钾采用乙酸铵浸提-火焰光度法测定(NY T 889-2004),阳离子交换量(CEC)采用三氯化六氨合钴浸提-分光光度法测定(HJ 889-2017)。
1.3.2 生物炭指标将生物炭与水以1∶20浸泡,使用pH计(PB-10,德国)测定生物炭的pH,通过计算生物炭在800 ℃下燃烧4 h后的重量损失确定其灰分含量[19],通过扫描电子显微镜(SEM)(GeminiSEM 500,德国)观察生物炭的表面形态,通过比表面积分析仪(ASAP2460,美国)测定其比表面积,采用元素分析仪(Elementar UNICUBE,德国)测定生物炭样品元素组成,利用傅里叶变换红外光谱(Tensor-27,德国)表征表面官能团。
1.3.3 植物指标采用生物显微镜(BM 2000,宁波)观察未接种与接种AMF情况下植物根部的显微结构。每盆选取3株植物收获幼苗,经清洗、拭干后,用直尺分别测量植物从茎基部到植株顶部和主根末端的长度作为株高和根长;随后称鲜质量,并于60 ℃烘箱中烘干72 h至恒重,记为干质量。植物中叶绿素、脯氨酸、根系活力分别采用乙醇提取分光光度法[20]、酸性茚三酮比色法[21]、TTC染色法[22]测定。植物中的磷采用钼锑抗比色法[23],Na+、K+采用火焰光度法[24]测定。
1.4 数据处理与分析在土壤-植物系统中,Na+迁移量是指土壤中Na+含量减去植物Na+含量,计算公式如下:
| $ E=C_1 \times m_1-C_0 \times m_0 \text { 。} $ | (1) |
式中:E为迁移量,mg·g-1;C1为Na+在土壤中的含量,mg·g-1;m1为干土壤质量,g;C0为Na+在植物中的含量,mg·g-1;m0为植物质量,g。
所有数据都表示为平均值±标准偏差,采用Microsoft Excel 2024计算标准偏差,SPSS 27.0进行单因素分析(ANOVA),采用Duncan检验进行不同处理组间的多重比较分析(P < 0.05)。采用Hiplot进行聚类分析,解释添加生物炭和AMF对各指标间的相关程度。采用Smart PLS 4.0进行偏最小二乘路径(PLS-PM)分析,用于量化生物炭和AMF对土壤-植物系统耐盐性及提高养分有效性的作用路径。使用Origin 2021进行绘图。
2 结果与分析 2.1 生物炭的基本特征生物炭的基本特性如表 3所示。HBC比表面积为255.57 m2·g-1,相较于BC增加了88.2%。BC的pH为8.01,HBC的pH为4.58,说明HBC具有较强的酸性特性,在盐碱土中加入HBC,能有效缓解盐碱土的pH。H3PO4分解木质纤维素、脂肪族及芳香族物质,形成丰富的孔洞,更有利于AMF的附着和生存[25]。生物炭富含营养元素,碳含量约占所有元素的53.2%~56.3%,HBC中的氢、氧、磷含量分别比BC提高了14.7%、6.7%、63.6%,H/C、O/C明显高于BC,生物炭极性增强[26],更能够为AMF的生长提供碳源和营养,促进微生物的生长[27]。
|
|
表 3 生物炭的基本特征 Table 3 Basic characteristics of Enteromorpha prolifera biochar |
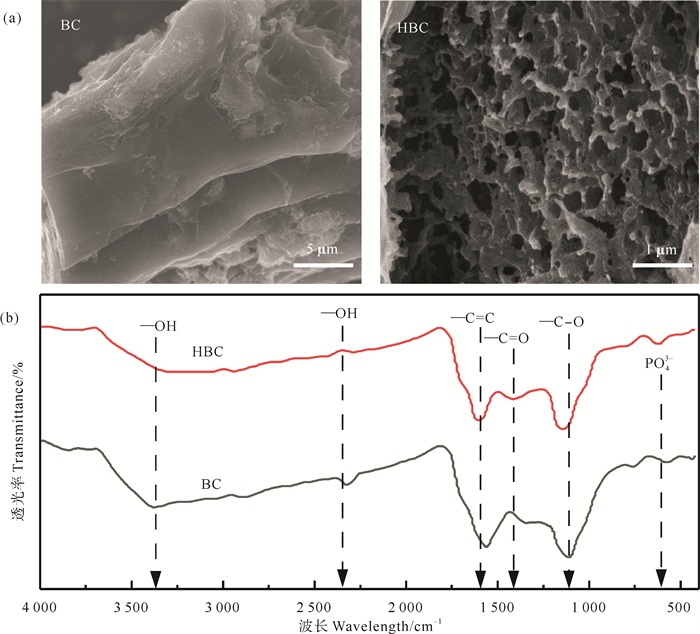
BC和HBC的表面形貌的扫描电镜图如图 1(a)所示。从图 1(a)中可知,BC表面光滑,孔隙密集且排列相对规则;而HBC表面更多的网状结构被紧密结合并逐层堆叠,形成更加稳定的碳基质骨架,有助于AMF存活[27]。
|
((a)生物炭的扫描电镜图;(b)生物炭的傅里叶红外光谱图。(a) Scanning electron micrograph (SEM) of biochar; (b) Fourier transform infrared (FTIR) spectra of biochar.) 图 1 浒苔生物炭的结构特征 Fig. 1 Structural properties of Enteromorpha prolifera biochar |
BC和HBC的傅里叶红外光谱图如图 1(b)所示。HBC在560 cm-1处观察到PO43-吸收峰[28],这表明H3PO4改性成功将含磷基团负载在生物炭表面。在1 086和1 490 cm-1处分别观察到环氧羧基(-C-O)和含氧羧基(-C=O)的伸缩振动[29],相较于BC,HBC的峰强度明显增强,表明改性成功引入了大量羧基和羟基,这些官能团通过化学键合与物理包裹双重作用使得生物炭稳定性增强[30-31],更有利于对Na+的吸附[29]。
2.2 黑麦草根际AMF定植情况未接种和接种AMF的菌根形态显微镜照片(放大400倍)见图 2。从图中可看出,未接种AMF的植物根系根表层细胞洁净透明,植物细胞呈规则排列的长椭圆形;AMF接种后,深色的胞内从枝结构密集存在于根表层细胞,与生物炭联合诱导下在根细胞及根外可观察到AMF的菌丝和泡囊等结构,表明AMF成功侵染植物根部,并对根细胞结构产生影响。

|
((a)未接种AMF的植物根部;(b)接种AMF的植物根部;(c)生物炭和AMF联合诱导下AMF侵染情况。(a) Roots of plants not inoculated with AMF; (b) Roots of plants inoculated with AMF; (c) AMF infestation under combined induction of biochar and AMF.) 图 2 AMF侵染情况显微镜照片 Fig. 2 Micrographs of AMF infestation |
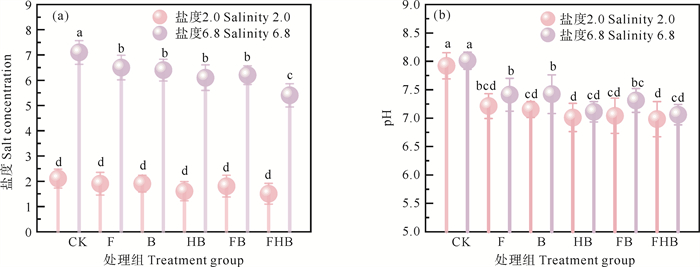
不同处理组对土壤盐浓度和pH值的影响见图 3。2.0盐度下,各处理组盐浓度无显著变化,可能是由于土壤初始盐度较低,生物炭和AMF的作用空间有限[32];6.8盐度下,盐浓度下降的趋势为FHB>HB>FB>B>F>CK。与CK组相比,两种盐度下各处理组的pH值均呈下降趋势,FHB组的pH值最低。盐浓度变化的原因是生物炭中的-COOH、-OH等含氧官能团具有吸附和离子交换能力,能够与土壤中的Na+发生相互作用,有效固定盐分,减轻土壤盐浓度[33];pH值变化的原因是:(1)HBC表面的磷酸基团(-PO43-)与土壤中的OH-发生中和反应,与CK相比,显著降低土壤pH;(2)AMF通过调控根际微环境,促进植物和微生物分泌有机酸进入根区土壤,进一步降低土壤pH[34]。2.0盐度下,各处理组对土壤pH值的改良效果相差不大,是由于土壤的缓冲能力使其变化相对稳定[35]。
|
((a)土壤盐浓度;(b)土壤pH值。(a) Soil salt concentration; (b) Soil pH.) 图 3 不同处理组对土壤盐浓度和pH值的影响 Fig. 3 Effect of different treatment groups on soil salt concentration and pH |
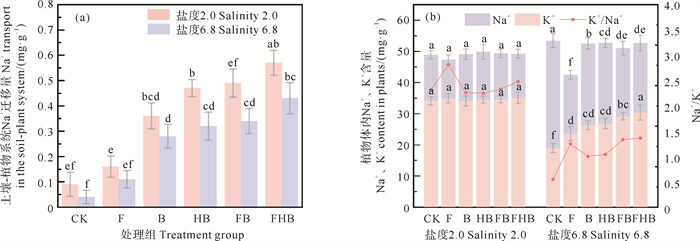
不同处理组对土壤-植物系统盐分迁移的调控效应如图 4所示。盐浓度显著影响土壤-植物系统中盐分的迁移及植物体内的Na+和K+含量。盐度越高,Na+从土壤向植物的迁移量越大,植物体内Na+含量越高。FHB组显著减少了Na+从土壤向植物的迁移,2.0盐度下,Na+变化量相比于CK组提高了5.3倍,说明生物炭的阳离子交换能力有效固定了Na+,改善了土壤的水盐分布,降低Na+向植物根系的迁移,有效缓解盐胁迫损害[36]。6.8盐度下,相较于CK组,FHB组中Na+含量降低了35.3%,K+含量升高了60.3%,K+/Na+提升了147.3%。盐碱条件下,K+/Na+是决定植物养分吸收和生物量的关键因素[37],过量盐离子会增加Na+和K+间的竞争,增加有毒Na+的积累,抑制K+的吸收,触发蛋白质合成和胞质酶活性的抑制,造成养分失衡[38]。添加AMF能够上调Na+逆向转运蛋白基因和K+/Na+协同转运蛋白基因,减少植物根对Na+的吸收,保护胞内K+介导的酶促过程免受盐胁迫损害,维持较高的K+/Na+,提高养分的选择性吸收[38]。而生物炭通过释放自身的营养物质,改善土壤团聚体,增加植物矿物质吸收,调节气孔导度和植物激素,减少Na+胁迫和细胞渗透胁迫对细胞膜的损伤,提高植物K+/Na+[39]。
|
((a)土壤-植物系统Na+迁移量;(b)植物体内Na+、K+含量变化。(a) Na+ transport in the soil-plant system; (b) Changes in Na+ and K+ content in plants.) 图 4 不同处理组对土壤-植物系统盐分迁移的调控效应 Fig. 4 Regulatory effects of different treatment groups on salt transport in the soil-plant system |
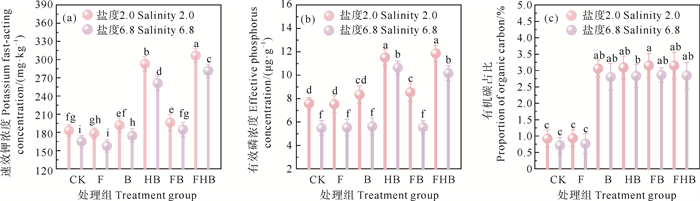
盐胁迫下生物炭和AMF对土壤养分变化的影响见图 5。各处理组中,土壤养分含量在两种盐度水平下均呈现出低促高抑的现象,其中,在2.0盐度下更为显著,与CK组相比,FHB组和HB组的速效钾含量分别提高了67.5%和60.1%,有效磷含量分别提高了56.3%和51.9%,土壤有机碳(soil organic carbon,SOC)含量分别提高了242.4%和235.9%,说明单独添加H3PO4改性生物炭对土壤养分有显著促进作用,而与AMF联合施用时促进效果最显著。生物炭的多孔结构和高比表面积能有效吸附K+,有助于土壤保水,从而改善滨海盐碱土壤结构,间接增强速效钾有效性,促进植物生长[40];H3PO4改性生物炭pH较低,可缓解盐碱土的pH值,提高土壤微生物活性,促进含钾矿物和难溶性磷的溶解,释放更多养分,形成正反馈,进而增加速效钾和有效磷含量[41]。此外,生物炭具有良好的碳稳定性,能够作为碳源保留碳[42],通过与土壤有机质、溶解有机碳和矿物质互动,促进土壤稳定团聚体形成,实现SOC的物理包封,提高土壤碳封存潜力[43]。
|
((a)速效钾浓度;(b)有效磷浓度;(c)有机碳占比。(a) Fast-acting potassium concentration; (b) Effective phosphorus concentration; (c) Proportion of organic carbon.) 图 5 不同处理组对土壤养分的影响 Fig. 5 Effect of different treatment groups on soil nutrients |
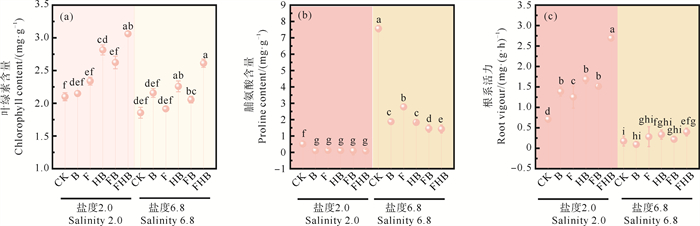
盐胁迫下生物炭和AMF对植物叶绿素、脯氨酸及根系活力含量变化的影响见图 6。各处理组在2.0盐度条件下的植物光合作用、渗透调节能力和根系活力均显著优于6.8盐度条件下的表现。2.0盐度下,与CK组相比,FHB组的叶绿素含量和根系活力分别提高了45.8%和279.8%,脯氨酸含量降低了84.3%。6.8盐度下,相较于CK组,FHB组的叶绿素含量和根系活力分别提高了40.8%和125.7%,脯氨酸含量降低了81.2%。
|
((a)叶绿素含量;(b)脯氨酸含量; (c)根系活力。(a) Chlorophyll content; (b) Proline content; (c) Root vigour.) 图 6 不同处理组对植物生理指标的影响 Fig. 6 Effects of different treatment groups on plant physiological indices |
盐胁迫主要通过破坏细胞离子的平衡,对植物光合作用、细胞分裂和整体生长产生影响。这种破坏导致叶绿素水平降低,限制光合作用效率并降低植物根系活力[44]。而接种AMF能够释放促进叶绿体形成的激素信号,在一定程度上缓解盐胁迫效应,提高植物光合作用[45]。脯氨酸在植物脱水过程中能够充当羟基自由基清除剂(FRS),通过渗透调节缓解植物盐胁迫[46]。盐度越高脯氨酸含量越高,说明脯氨酸能够充当渗透保护剂,防止蛋白质聚集和改善FRS保护植物细胞免受盐胁迫[47],进一步验证了生物炭和AMF的添加能有效缓解盐胁迫损害。
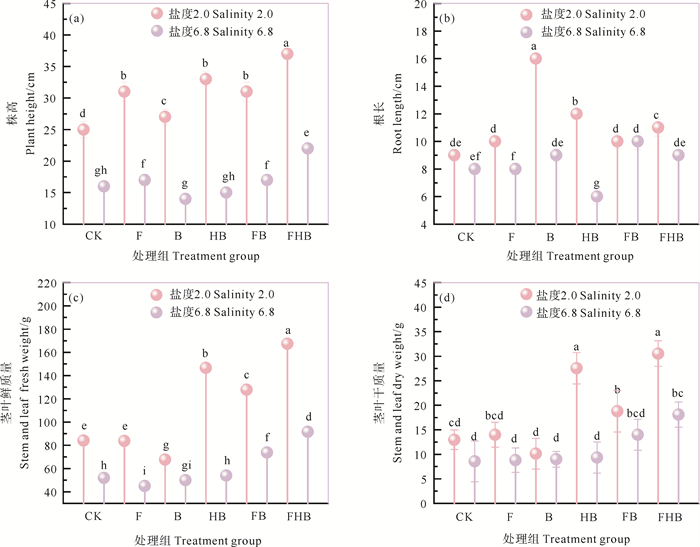
2.4.3 植物生长特征盆栽实验的植物生长60 d后的生长状态如图 7,生长指标如图 8所示。由图 7可知,各组生长状态表现为FHB>FB>F>HB>B>CK,说明生物炭与AMF联合应用效果最佳,单独添加AMF比单独添加生物炭对植株的生长更有利。此外,2.0盐度下FHB组植物生长效果比6.8盐度更佳,FHB组的株高、根长、鲜质量和干质量在2.0盐度下分别是CK组的1.5、5.5、2.0和2.4倍,表明AMF在盐胁迫环境下对植物根系生长的促进作用尤为关键。AMF通过与植物根系共生,扩展吸收面积,增强水分与养分摄取[48],进而有助于植物在盐胁迫环境中生长。此外,AMF在高盐条件下仍能有效维持植物的高干质量与鲜质量。而生物炭的存在能够优化土壤结构、增强通气与保水能力,改善与根系的相互作用,间接促进根系伸长和发育[49]。

|
图 7 60 d后不同处理组植物生长状态 Fig. 7 Plant growth status of different treatment groups after 60 d |
|
((a)植物株高;(b)植物根长;(c)茎叶鲜质量;(d)茎叶干质量。(a) Plant height; (b) Plant root length; (c) Stem and leaf fresh weight; (d) Stem and leaf dry weight.) 图 8 60 d后不同处理组植物生长指标 Fig. 8 Plant growth indexes of different treatment groups after 60 d |
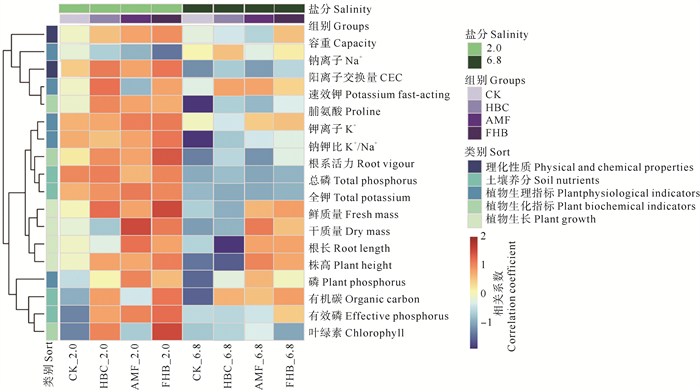
综上所述,H3PO4改性生物炭对土壤-植物系统的耐盐碱能力的优于原始生物炭。本部分仅选取CK、F、HB和FHB四个典型处理组,不考虑原始生物炭组,利用聚类热图说明在土壤-植物系统中添加H3PO4改性生物炭和AMF对土壤和植物之间的指标相关性(见图 9)。2.0盐度下,根长、株高和鲜质量的正相关关系表明,H3PO4改性生物炭和AMF的加入提升了土壤养分含量,促进植物根系生长和发育,缓解盐胁迫损害。与2.0盐度相比,6.8盐度下明显抑制了植物的生长。相关系数表明,2.0盐度下FHB组,所有指标均为正相关,只有Na+呈负相关,说明H3PO4改性生物炭和AMF对Na+具有显著抑制作用,减少了盐胁迫对植物的负面影响。H3PO4改性生物炭主要通过提高土壤CEC,竞争性吸附Na+,减少其在土壤中的迁移,降低植物对有毒Na+的吸收;AMF主要通过提升植物根系活力,增强K+吸收效率,减少Na+在植物体内的积累,同时调控植物离子分配,维持较高的K+/Na+比,这与前人的研究一致[50],具体路径通过PLS-PM进行量化。
|
图 9 盐胁迫下生物炭和AMF对土壤-植物系统指标的聚类分析 Fig. 9 Cluster analysis of biochar and AMF on soil-plant system indicators under salt stress |
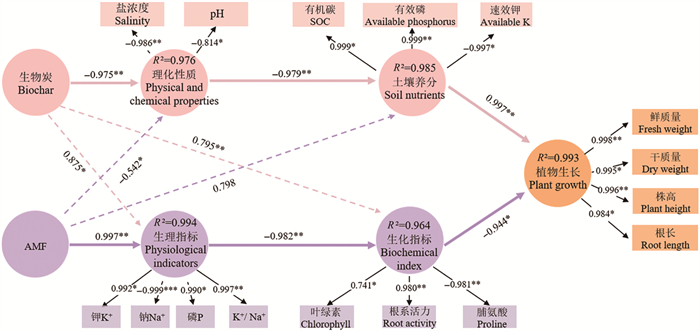
2.0盐度下各项指标优于6.8盐度,采用PLS-PM模型量化分析2.0盐度下H3PO4改性生物炭与AMF联合作用对土壤-植物系统中Na+调控机制及养分提升的作用路径(见图 10)。图 10中箭头上路径系数(β)表征潜变量总效应,正值表示对结果的正向影响,反之亦然,其绝对值大小反映了影响强度。H3PO4改性生物炭主要通过降低土壤盐浓度、pH、增加SOC等路径,增强土壤养分有效性,提高植物对水分和养分的吸收能力,间接促进植物生长(β=0.997),同时通过调控植物生理指标,有效固定Na+,产生正向效应;AMF主要调节植物生理指标(β=0.997),增强了对植物体内K+、P含量的选择性吸收,抑制Na+迁移(β=-0.999),同时强化光合作用(β=0.741),改善渗透调节(β=-0.981),提升根系活力(β=0.980),有效提高植物耐盐碱能力。联合应用下,H3PO4改性生物炭和AMF的协同效应显著增加了植物根长(β=0.984)、株高(β=0.996)及鲜质量(β=0.998),展现出滨海盐碱环境下调控Na+平衡及提升养分利用效率的综合优势。
|
(*代表P < 0.05; **代表P < 0.01; ***代表P < 0.001,R2为决定系数,表示模型对内生变量的拟合度。* stands for P < 0.05; ** stands for P < 0.01; *** stands for P < 0.001. R2 is the coefficient of determination, indicating the model's fit for the endogenous variables.) 图 10 2.0盐度下H3PO4改性生物炭和AMF调节黑麦草生长的PLS-PM模型 Fig. 10 PLS-PM modelling of biochar and AMF to regulate ryegrass growth at salinity 2.0 |
(1) H3PO4改性生物炭和AMF的协同作用在盐胁迫条件下表现出更优的促进作用。H3PO4改性生物炭通过吸附和离子交换能力固定土壤中的Na+,减少其向植物根系的迁移,改善水盐分布,显著提高K+/Na+比。AMF通过上调Na+逆向转运蛋白和K+/Na+协同转运蛋白基因,减少植物对Na+的吸收,优化离子平衡,保护胞内酶促过程。
(2) H3PO4改性生物炭通过提高微生物活性,促进含钾矿物和难溶性磷的溶解,释放更多养分,形成正反馈,增强土壤养分有效性,同时通过提高SOC含量和碳封存潜力改善土壤结构。AMF显著提升叶绿素含量和根系活力,通过渗透调节提高植物耐盐性,二者联合应用显著提升土壤-植物系统养分利用效率。
(3) 通过聚类分析和PLS-PM模型量化了H3PO4改性生物炭和AMF对土壤-植物系统中耐盐性和养分有效性的调控路径:生物炭主要通过调节土壤养分提升植物对水分和养分的吸收能力;AMF通过直接调控植物生理指标, 提高植物耐盐碱性能。
| [1] |
Güleç Şen K, Başaran U, Çopur Doǧrusöz M, et al. Growth and biochemical responses of grass pea (Lathyrus sativus L.) genotypes under salt (NaCl) stress generated by irrigation water, and changes in soil pH and EC[J]. Gesunde Pflanzen, 2023, 75(3): 667-675. DOI:10.1007/s10343-022-00732-0 (  0) 0) |
| [2] |
He K, He G, Wang C P, et al. Biochar amendment ameliorates soil properties and promotes miscanthus growth in a coastal saline-alkali soil[J]. Applied Soil Ecology, 2020, 155: 103674. DOI:10.1016/j.apsoil.2020.103674 (  0) 0) |
| [3] |
Cai J F, Fan J, Liu X S, et al. Biochar-amended coastal wetland soil enhances growth of Suaeda salsa and alters rhizosphere soil nutrients and microbial communities[J]. Science of the Total Environment, 2021, 788: 147707. DOI:10.1016/j.scitotenv.2021.147707 (  0) 0) |
| [4] |
Ei-Naggar A, Lee S S, Rinklebe J, et al. Biochar application to low fertility soils: A review of current status, and future prospects[J]. Geoderma, 2019, 337: 536-554. DOI:10.1016/j.geoderma.2018.09.034 (  0) 0) |
| [5] |
Saifullah, Dahlawi S, Naeem A, et al. Biochar application for the remediation of salt-affected soils: Challenges and opportunities[J]. Science of the Total Environment, 2018, 625: 320-335. DOI:10.1016/j.scitotenv.2017.12.257 (  0) 0) |
| [6] |
Lehmann J, Rillig M C, Thies J, et al. Biochar effects on soil biota: A review[J]. Soil Biology and Biochemistry, 2011, 43(9): 1812-1836. DOI:10.1016/j.soilbio.2011.04.022 (  0) 0) |
| [7] |
Zheng Y, Han X, Li Y, et al. Effects of biochar and straw application on the physicochemical and biological properties of paddy soils in northeast China[J]. Scientific Reports, 2019, 9(1): 16531. DOI:10.1038/s41598-019-52978-w (  0) 0) |
| [8] |
Duan M, Liu G, Zhou B, et al. Effects of modified biochar on water and salt distribution and water-stable macro-aggregates in saline-alkaline soil[J]. Journal of Soils and Sediments, 2021, 21(6): 2192-2202. DOI:10.1007/s11368-021-02913-2 (  0) 0) |
| [9] |
陈友媛, 王翔宇, 吴海霞, 等. 浒苔生物炭对滨海盐碱土Na+的吸附迁移机制研究[J]. 中国海洋大学学报(自然科学版), 2019, 49(S1): 85-92. Chen Y Y, Wang X Y, Wu H X, et al. Study on the adsorption and transport mechanism of Na+ adsorption on coastal saline soil by seagrass biochar[J]. Periodical of Ocean University of China, 2019, 49(S1): 85-92. DOI:10.16441/j.cnki.hdxb.20190142 (  0) 0) |
| [10] |
Nakmee P S, Techapinyawat S, Ngamprasit S. Comparative potentials of native arbuscular mycorrhizal fungi to improve nutrient uptake and biomass of Sorghum bicolor Linn[J]. Agriculture and Natural Resources, 2016, 50(3): 173-178. DOI:10.1016/j.anres.2016.06.004 (  0) 0) |
| [11] |
Wang Y H, Wang M Q, Li Y, et al. Effects of arbuscular mycorrhizal fungi on growth and nitrogen uptake of chrysanthemum morifolium under salt stress[J]. PLoS One, 2018, 13(4): e0196408. DOI:10.1371/journal.pone.0196408 (  0) 0) |
| [12] |
Wen Z H, Chen Y X, Liu Z Q, et al. Biochar and Arbuscular mycorrhizal fungi stimulate rice root growth strategy and soil nutrient availability[J]. European Journal of Soil Biology, 2022, 113: 103448. DOI:10.1016/j.ejsobi.2022.103448 (  0) 0) |
| [13] |
Liu H F, Xu H W, Wu Y, et al. Effects of natural vegetation restoration on dissolved organic matter (DOM) biodegradability and its temperature sensitivity[J]. Water Research, 2021, 191: 116792. DOI:10.1016/j.watres.2020.116792 (  0) 0) |
| [14] |
Kim M S, Lee S H, Kim J G. Evaluation of factors affecting arsenic uptake by Brassica juncea in alkali soil after biochar application using partial least squares path modeling (PLS-PM)[J]. Chemosphere, 2021, 275: 130095. DOI:10.1016/j.chemosphere.2021.130095 (  0) 0) |
| [15] |
Han S, Cheng Y, Wu G, et al. Enhancing salt tolerance in poplar seedlings through arbuscular mycorrhizal fungi symbiosis[J]. Plants, 2024, 13(2): 233-249. DOI:10.3390/plants13020233 (  0) 0) |
| [16] |
Guo J M, Chen Y Y, Lu P Z, et al. Roles of endophytic bacteria in Suaeda salsa grown in coastal wetlands: Plant growth characteristics and salt tolerance mechanisms[J]. Environmental Pollution, 2021, 287: 117641. DOI:10.1016/j.envpol.2021.117641 (  0) 0) |
| [17] |
Kwashie G K S, Kaba J S, Appiah-Kubi Z, et al. Synergic effect of arbuscular mycorrhizal fungi and potassium fertilizer improves biomass-related characteristics of cocoa seedlings to enhance their drought resilience and field survival[J]. Open Agriculture, 2023, 8(1): 732831-732839. (  0) 0) |
| [18] |
Walkley A, Black I A. An examination of the degtjareff method for determining soil organic matter, and a proposed modification of the chromic acid titration method[J]. Soil Science, 1934, 37(1): 28-29. (  0) 0) |
| [19] |
Fan J P, Li Y, Yu H Y, et al. Using sewage sludge with high ash content for biochar production and Cu(Ⅱ) sorption[J]. Science of the Total Environment, 2020, 713: 136663. DOI:10.1016/j.scitotenv.2020.136663 (  0) 0) |
| [20] |
Liang Y, Paris F, Tang P. Middle-late ordovician chitinozoans from the Yichang area, South China[J]. Review of Palaeobotany and Palynology, 2017, 244: 26-42. DOI:10.1016/j.revpalbo.2017.04.004 (  0) 0) |
| [21] |
Bagdi D L, Gupta S, Bagdi D K, et al. Photosynthesis, membrane stability and proline metabolism enzyme activity as potential indicators for salt tolerance in wheat[J]. Russian Journal of Plant Physiology, 2022, 69(5): 104-114. DOI:10.1134/S1021443722050028 (  0) 0) |
| [22] |
Zhang X, Huang G, Bian X, et al. Effects of root interaction and nitrogen fertilization on the chlorophyll content, root activity, photosynthetic characteristics of intercropped soybean and microbial quantity in the rhizosphere[J]. Plant, Soil and Environment, 2013, 59(2): 80-88. DOI:10.17221/613/2012-PSE (  0) 0) |
| [23] |
孙亚凯. 功能性微生物菌株的筛选及组合菌群活性研究[D]. 天津: 天津大学, 2007. Sun Y K. Screening of Functional Microbial Strains and Activity of Combined Flora[D]. Tianjin: Tianjin University, 2007. (  0) 0) |
| [24] |
Seid F, Mehari B. Elemental and proximate compositions of sesame seeds and the underlying soil from Tsegede, Ethiopia[J]. International Journal of Analytical Chemistry, 2022, 2022(1): 1083196. (  0) 0) |
| [25] |
Yang R, Liu G Q, Xu X H, et al. Surface texture, chemistry and adsorption properties of acid blue 9 of hemp (Cannabis sativa L.) bast-based activated carbon fibers prepared by phosphoric acid activation[J]. Biomass and Bioenergy, 2011, 35(1): 437-445. DOI:10.1016/j.biombioe.2010.08.061 (  0) 0) |
| [26] |
刘贺春. 酸改性生物炭对土壤氮素截留吸附效果研究[D]. 哈尔滨: 东北农业大学, 2024. Liu H C. Research on the Effect of Acid-Modified Biochar on Nitrogen Retention and Adsorption in Soil[D]. Harbin: Northeast Agricultural University, 2024. (  0) 0) |
| [27] |
Dai Z M, Xiong X Q, Zhu H, et al. Association of biochar properties with changes in soil bacterial, fungal and fauna communities and nutrient cycling processes[J]. Biochar, 2021, 3(3): 239-254. DOI:10.1007/s42773-021-00099-x (  0) 0) |
| [28] |
Zhong M, Li W, Jiang M, et al. Improving the ability of straw biochar to remediate Cd contaminated soil: KOH enhanced the modification of K3PO4 and urea on biochar[J]. Ecotoxicology and Environmental Safety, 2023, 262: 115317. DOI:10.1016/j.ecoenv.2023.115317 (  0) 0) |
| [29] |
唐恒军, 邱彪, 司马卫平, 等. 酸改性酒糟生物炭对Cr(Ⅵ)的去除性能研究[J]. 工业水处理, 2025, 45(3): 144-151. Tang H J, Qiu B, Sima W P, et al. Removal of Cr(Ⅵ) by acid-modified lees biochar[J]. Industrial Water Treatment, 2025, 45(3): 144-151. (  0) 0) |
| [30] |
Wei J, Li Y, Li J, et al. A 2-year pure biochar addition enhances soil carbon sequestration and reduces aggregate stability in understory conditions[J]. Scientific Reports, 2024, 14(1): 30122. DOI:10.1038/s41598-024-81232-1 (  0) 0) |
| [31] |
Dong W, Xing J, Chen Q, et al. Hydrogen bonds between the oxygen-containing functional groups of biochar and organic contaminants significantly enhance sorption affinity[J]. Chemical Engineering Journal, 2024, 499: 156654. DOI:10.1016/j.cej.2024.156654 (  0) 0) |
| [32] |
Wang X, Ding J, Han L, et al. Biochar addition reduces salinity in salt-affected soils with no impact on soil pH: A meta-analysis[J]. Geoderma, 2024, 443: 116845. DOI:10.1016/j.geoderma.2024.116845 (  0) 0) |
| [33] |
Ma W M, Ma L, Jiao J T, et al. Impact of straw incorporation on the physicochemical profile and fungal ecology of saline-alkaline soil[J]. Microorganisms, 2024, 12(2): 277-294. DOI:10.3390/microorganisms12020277 (  0) 0) |
| [34] |
卢建男, 张琼, 刘铁军, 等. 不同改良剂对盐碱地土壤及草地早熟禾生长的影响[J]. 草业科学, 2017, 34(6): 1141-1148. Lu J N, Zhang Q, Liu T J, et al. Effects of different amendments on growth of saline soils and grassland morning glory[J]. Grass Science, 2017, 34(6): 1141-1148. (  0) 0) |
| [35] |
Chen X, Liu L, Yang Q, et al. Optimizing biochar application rates to improve soil properties and crop growth in saline-alkali soil[J]. Sustainability, 2024, 16(6): 2523. DOI:10.3390/su16062523 (  0) 0) |
| [36] |
Mikajlo I, Lerch T Z, Louvel B, et al. Composted biochar versus compost with biochar: Effects on soil properties and plant growth[J]. Biochar, 2024, 6(1): 85-102. DOI:10.1007/s42773-024-00379-2 (  0) 0) |
| [37] |
Sun B R, Li Z Y, Wang C. Shoot K/Na ratio is the key factor for vermicompost and arbuscular mycorrhizal fungi to improve maize biomass in saline-alkali soil[J]. Journal of Soil Science and Plant Nutrition, 2024, 24(4): 6617-6629. DOI:10.1007/s42729-024-01994-5 (  0) 0) |
| [38] |
Porcel R, Aroca R, Azcon R, et al. Regulation of cation transporter genes by the arbuscular mycorrhizal symbiosis in rice plants subjected to salinity suggests improved salt tolerance due to reduced Na+ root-to-shoot distribution[J]. Mycorrhiza, 2016, 26(7): 673-684. DOI:10.1007/s00572-016-0704-5 (  0) 0) |
| [39] |
Ran C, Gulaqa A, Zhu J, et al. Benefits of biochar for improving ion contents, cell membrane permeability, leaf water status and yield of rice under saline-sodic paddy field condition[J]. Journal of Plant Growth Regulation, 2020, 39(1): 370-377. DOI:10.1007/s00344-019-09988-9 (  0) 0) |
| [40] |
Zhao W, Zhou Q, Tian Z Z, et al. Apply biochar to ameliorate soda saline-alkali land, improve soil function and increase corn nutrient availability in the songnen plain[J]. Science of the Total Environment, 2020, 722: 137428. DOI:10.1016/j.scitotenv.2020.137428 (  0) 0) |
| [41] |
Zhu Z, Zhang Y, Tao W, et al. The biological effects of biochar on soil's physical and chemical characteristics: A review[J]. Sustainability, 2025, 17(5): 2214. DOI:10.3390/su17052214 (  0) 0) |
| [42] |
Ameloot N, Graber E R, Verheijen F G A, et al. Interactions between biochar stability and soil organisms: Review and research needs[J]. European Journal of Soil Science, 2013, 64(4): 379-390. DOI:10.1111/ejss.12064 (  0) 0) |
| [43] |
Zheng H, Wang X, Luo X X, et al. Biochar-induced negative carbon mineralization priming effects in a coastal wetland soil: Roles of soil aggregation and microbial modulation[J]. Science of the Total Environment, 2018, 610-611: 951-960. DOI:10.1016/j.scitotenv.2017.08.166 (  0) 0) |
| [44] |
Hao S H, Wang Y R, Yan Y X, et al. A review on plant responses to salt stress and their mechanisms of salt resistance[J]. Horticulturae, 2021, 7(6): 132-161. DOI:10.3390/horticulturae7060132 (  0) 0) |
| [45] |
Malik J A, Alqarawi A A, Alotaibi F, et al. Alleviation of NaCl stress on growth and biochemical traits of Cenchrus ciliaris L. via Arbuscular mycorrhizal fungi symbiosis[J]. Life, 2024, 14(10): 1276. DOI:10.3390/life14101276 (  0) 0) |
| [46] |
Wu N, Li Z, Wu F, et al. Comparative photochemistry activity and antioxidant responses in male and female populus cathayana cuttings inoculated with arbuscular mycorrhizal fungi under salt[J]. Scientific Reports, 2016, 6(1): 37663. DOI:10.1038/srep37663 (  0) 0) |
| [47] |
Chen J T, Wang X R, Liu X Y, et al. Beneficial effects of biochar-based organic fertilizers on nitrogen assimilation, photosynthesis, and sucrose synthesis of sugar beet (Beta vulgaris L.)[J]. International Journal of Plant Production, 2022, 16(4): 755-768. DOI:10.1007/s42106-022-00219-y (  0) 0) |
| [48] |
Zhang Z C, Ding S L, Diao F W, et al. AMF symbiosis drives the rhizosphere microbiome to synergistically improve herbage growth in saline-alkaline soils[J]. Land Degradation & Development, 2024, 35(11): 3663-3674. (  0) 0) |
| [49] |
杨怡森, 袁小会, 廖国婷, 等. 菌根共生条件下施加生物炭对玉米根系及生长的影响[J]. 江苏农业科学, 2022, 50(17): 90-94. Yang Y S, Yuan X H, Liao G T, et al. Effects of biochar application on maize root system and growth under mycorrhizal symbiosis[J]. Jiangsu Agricultural Science, 2022, 50(17): 90-94. (  0) 0) |
| [50] |
赵新月, 孙萍, 陈友媛, 等. 盐胁迫下丛枝菌根真菌和生物炭调节黑麦草碳氮代谢的路径[J]. 中国海洋大学学报(自然科学版), 2023, 53(11): 121-130. Zhao X Y, Sun P, Chen Y Y, et al. Regulation of carbon and nitrogen metabolism of ryegrass by mycorrhizal fungi and biochar under salt stress[J]. Periodical of Ocean University of China, 2023, 53(11): 121-130. DOI:10.16441/j.cnki.hdxb.20220138 (  0) 0) |
2. Key Laboratory of Geological Safety of Subterranean Spaces in Coastal Cities, Ministry of Natural Resources, Qingdao 266100, China;
3. Key Laboratory of Marine Environment and Ecology, Ministry of Education, Ocean University of China, Qingdao 266100, China;
4. Key Laboratory of Geological Engineering for Marine Environment in Shandong Province, Ocean University of China, Qingdao 266100, China;
5. Tianqiao Yellow River Bureau, Yellow River Conservancy Commission, Ministry of Water Resources, Zhengzhou 450003, China
 2025, Vol. 55
2025, Vol. 55


