2. 青岛海洋科技中心海洋生态与环境科学功能实验室, 山东 青岛 266237
挥发性卤代烃(Volatile halocarbons, VHCs)是一类重要的痕量温室气体[1], 负担着海洋和大气平流层之间传输卤素自由基的重要作用。大气中的VHCs在紫外光的作用下, 会发生化学降解或者光化学分解产生卤素自由基(如氯和溴), 这些卤素自由基进而与大气中的臭氧反应, 造成对流层和平流层下层的臭氧层破坏[2]。此外通过口摄入、皮肤接触和呼吸道吸入等方式VHCs可在人体中长期积累[3], 可能对人体产生致癌、致畸和致突变的影响[4]。由于VHCs对大气化学、全球气候变化及人类健康的影响, 它们在大气和海洋等环境中的研究已经受到各国的广泛关注。
研究表明, 长寿命挥发性卤代烃是平流层卤素的重要来源[2]。CFCs是一类人工合成的化合物, 1932年三氯氟甲烷(CFC-11)作为一种长寿命VHCs(大气寿命>6个月)首次出现, 随后以制冷剂、气雾剂、干洗剂等工业产品的形态被大量使用[5-6], 但CFCs对于臭氧层的破坏直到20世纪70年代才被关注。随着《蒙特利尔议定书》的颁布, 长寿命的人为源消耗臭氧层物质已经逐步被淘汰[7], 因此, 以天然源为主的短寿命挥发性卤代烃(如二溴甲烷(CH2Br2))对大气卤素的相对贡献将在未来增加[8]。海洋中短寿命的溴代烃主要由海藻自然产生[7]。例如, 海水中CHBr2Cl含量主要受到浮游植物的生产释放影响。此外, 人为排放、陆源输入也对海水中CHBr2Cl浓度产生影响[9]。碘甲烷(CH3I)除了来自海洋中的浮游植物[10-13], 还能通过非生物来源形式的光化学产生[14-19]。
珠江口位于广东省中南部, 是我国第三大河口, 珠江口附近的水文特征主要受广东沿岸流、南海暖流和黑潮的影响[20-21]。按地理位置珠江可分为八大口门, 珠江冲淡水最终通过八个口门汇入南海, 口门以外还有潮汐的存在[22], 致使河口内的水文环境变得更加复杂。南海是我国最大且最深的边缘海, 位于亚洲东南部, 是太平洋的边缘海之一, 其地理位置独特, 海域辽阔, 海底地形复杂, 拥有大陆架、大陆坡以及深海盆地等海底形态, 受到沿岸上升流、淡水输入、环流及中尺度旋涡等的影响, 水文结构复杂[23]。此外, 珠江还会携带大量泥沙和营养盐等物质汇入南海, 对南海的生物地球化学循环有着十分重要的影响[24]。因此本文选择珠江口及南海西部作为研究海域, 通过测定2023年秋季珠江口和南海西部大气和海水中CFC-11、CH3I、CH2Br2、一氯二溴甲烷(CHBr2Cl)的浓度水平, 阐明该海域4种VHCs的浓度分布及控制因素, 补充全球VHCs的数据库, 进而为评估VHCs的释放对全球环境和气候变化的影响提供科学依据。
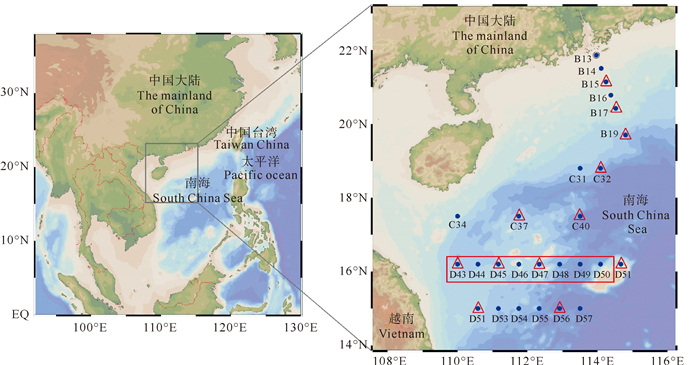
1 材料与方法 1.1 样品的采集于2023年10月4日—11月2日(秋季)搭载“实验3号”海洋调查船对珠江口-南海西部海域进行调查。调查海区和采样站位如图 1所示。本航次共采集大面站27个, 并在其中12个站位采集大气样品(三角形标记站位), 在40—53站位采集200 m以浅的垂直样品(红色方框标记站位)。表层海水(0~5 m)和200 m以浅不同深度垂直站位的海水样品(0~5、25、30、45、55、61、75、100、150和200 m), 使用安装在Seabird 911 CTD探测器上的12 L Niskin采水器采集。样品采集后, 用海水润洗135 mL玻璃瓶及聚四氟乙烯盖子3次, 将硅胶管插到瓶底, 让海水快速注入但不能产生气泡和较大涡旋。当水装满且溢出水体积约为瓶体积1/2时, 慢慢抽出硅胶管, 瓶口液面为凸液面, 滴加1~2滴饱和NaN3溶液以抑制生物活性, 用压盖器将盖子压紧, 确保不留顶空。将采集好的样品上下颠倒几次后立即放在4 ℃冰箱中冷藏保存, 返回陆地后尽快测定, 海水样品保存方法的可靠性和准确性实验表明样品浓度30 d内不发生变化[25]。
|
(△标记为大气采样站位, 红色方框内为断面站位。△ marks the atmospheric sampling stations; The section positions are in the red box.) 图 1 珠江口-南海西部采样站位示意图 Fig. 1 Schematic diagram of sampling stations in the Pearl River Estuary-Western South China Sea |
大气样品用3 L苏玛罐进行采集, 采样前用多通道采样罐清洗系统清洗采样罐并抽真空。为避免来自船体的污染, 在将要停船时将苏玛罐置于船的最顶层甲板, 迎着风向旋开苏玛罐的螺母和开关进行采样, 采样完毕后立即旋闭开关和螺母, 样品密封保存, 样品在返回陆地实验室后测定。
1.2 仪器与试剂Agilent 6890N气相色谱仪, 配置μECD(63Ni源)检测器(美国Agilent Technologies公司); G2070化学工作站(美国Agilent Technologies公司); DB-624弹性石英毛细管柱(长度60 m, 内径0.53 mm, 膜厚3 μm)(美国Restek公司); 吹扫-捕集前处理装置(实验室自行设计); 3.2 L苏码不锈钢采样罐(美国Restek公司); 2101DS多通道采样罐清洗系统(美国Nutech公司); 2202A动态稀释仪(美国Nutech公司); 8900DS低温预浓缩系统(美国Nutech公司); 气相色谱/质谱仪(Agilent7890A/5975C-GC/MSD); 日立F-4500荧光仪。100 mL气密注射器(澳大利亚SGE Analytical Science公司); VHCs气体标准样品(Spectra gases, 美国); VHCs液体混合标准样品(浓度规格, Organic stanolarols solutions international, 美国)。分析纯无水Mg(ClO4)2(国药集团化学试剂有限公司); 纯度99.99%的高纯氮气和液氮(青岛豪森气体有限公司)。
1.3 海水和大气中VHCs及相关参数的测定海水中VHCs浓度采用吹扫-捕集气相色谱法进行测定, 用气密性注射器将体积为50 mL的海水样品转移到气提室中, 用高纯氮气吹扫VHCs, 进行预浓缩处理, 去除CO2和H2O后将目标气体通过浸入液氮的不锈钢管路吹扫14 min, 将捕获了气体的不锈钢管浸入烧沸的热水中, 立即打开六通阀, 载气携带待测气体进入气相色谱仪进行分析。利用外标法进行定量分析, 该方法的检出限为0.01×10-12~0.22×10-12 mol·L-1, 相对标准偏差为1.83%~3.97%, 具体分析测定方法见文献[25]。
大气样品使用三级冷阱预浓缩系统(Nutech 8900DS, USA)-气相色谱质谱联用仪(Agilent 7890A/5975C, USA)进行分析测定。将300 mL大气样品从苏玛罐中抽入到预浓缩系统, 通过三级冷阱去除O2, CO2和H2O等气体, 对目标VHCs进行浓缩, 浓缩后的样品进入GC-MS中进行分析测定。利用外标法进行定量, 该方法的检出限为0.1×10-12~0.5×10-12 mol·L-1, 相对标准偏差小于2%, 具体分析测定方法见文献[25]。
叶绿素a(Chl a)测定参照Parsons等[26]的方法。营养盐(NH+ 4、NO3-、NO2-、PO43-)用营养盐自动分析仪(Seal Analytical AA3)测定, 具体测定方法参照文献[27]。
海水的环境参数(如温度(T)、盐度(S)和深度)由CTD探头测量获取, 风速用船载风速仪在水面上方约10 m处进行测定。利用HYSPLIT模型, 基于气象数据, 计算并绘制了气团的72 h后向轨迹图, 以分析气团的来源和传输路径。使用SPSS 27.0.1软件对表层海水中不同VHCs浓度与环境参数进行相关性分析。
1.4 海-气通量的计算测定VHCs的海-气通量可以评价海洋中VHCs对全球气候变暖的贡献[28]。目前, 大气中痕量气体在海-气界面通量的定量计算, 通常采用Liss and Slater[29]提出的双层滞膜模型:
| $ F=K_{\mathrm{w}}\left(C_{\mathrm{w}}-C_{\mathrm{a}} / H\right)。$ |
式中: F(nmol·m-2·d-1)是海-气通量; KW(m·d-1)是气体交换速率系数; CW(pmol·L-1)是VHCs在表层海水中的浓度; Ca(pmol·L-1)是VHCs在大气中的浓度; H为无量纲的亨利常数, 是海水温度T(K)的函数, CFC-11的H由Warner和Weiss[30]的公式计算得到, CH3I、CH2Br2、CHBr2Cl的H根据Moore[32]等提出的公式计算(见表 1)。
|
|
表 1 亨利常数计算公式 Table 1 Calculation formula of Henry's Law constant |
KW(m·d-1)是气体交换速率系数, 是风速(u, m·s-1)和气体常数(SC)的函数。风速(u, m·s-1)为各个站位海平面上方10 m处采样时的瞬时风速, SC是水的动力黏度与待测气体分子扩散系数之比。本文采用国际上较为常用的Wanninkhof提出的公式[33]计算KW值。
| $ K_{\mathrm{W}}=\left(0.251 u^2\right)\left(S_{\mathrm{C}} / 660\right)^{-0.5} \text { 。} $ |
气体施密特常数SC是表层海水温度t(℃)的函数, 本研究采用国际上较为常用的Wanninkhof[33]提出的公式计算, CFC-11的施密特常数(SC)采用Zheng等[34]提出的公式计算:
| $ \begin{aligned} & \quad S_{\mathrm{C}}\left(\mathrm{CH}_2 \mathrm{Br}_2\right)=335.6 \times 173.84^{0.5} \times(1-0.065 \times \\ & \left.t+0.002~043 \times t^2-2.6 \times 10^{-5} \times t^3\right), \\ & \quad S_{\mathrm{C}}\left(\mathrm{CHBr}_2 \mathrm{Cl}\right)=335.6 \times 208.3^{0.5} \times(1-0.065 \times \\ & \left.t+0.002~043 \times t^2-2.6 \times 10^{-5} \times t^3\right), \\ & \quad S_{\mathrm{C}}\left(\mathrm{CH}_3 \mathrm{I}\right)=(62.9 / 52.9)^{0.6} \times(2~004-93.5 \times \\ & \left.t+1.39 \times t^2\right), \\ & \quad S_{\mathrm{C}}(\mathrm{CFC}-11)=3~501.8-210.31 \times t+6.1851 \times \\ & t^2-0.075~13 \times t 。\end{aligned} $ |
式中t为表层海水温度, 单位为℃。
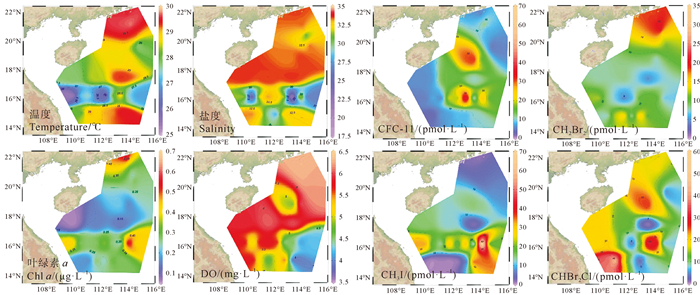
2 结果与讨论 2.1 海水中VHCs的水平分布特征及控制因素调查海域海表层海水温度范围为25.26~29.87 ℃, 平均值为(28.30±1.25) ℃; 盐度范围为19.47~33.69, 平均值为31.51±3.64。Chl a的浓度范围为0.06~0.67 μg·L-1, 平均值为(0.28±0.14) μg·L-1, 溶解氧(DO)的浓度为3.68~6.39 mg·L-1, 平均值为(5.45±0.82) mg·L-1。表层海水中温度、盐度、Chl a及DO的水平分布如图 2所示。
|
图 2 珠江口-南海西部海域表层海水中温度(℃)、盐度、Chl a(μg·L-1)、DO(mg·L-1)和4种VHCs浓度(pmol·L-1)的分布 Fig. 2 The distribution of temperature (℃), salinity, Chl a (μg·L-1), DO (mg·L-1) and concentrations of four VHCs (pmol·L-1) in the surface seawater from the Pearl River Estuary to the western South China Sea |
研究海域受南海北部沿岸上升流、南海中部冷涡和暖窝的影响, 表层海水盐度的高值区主要出现在北部和中部海域, 温度的高值区主要出现在北部、中部及西南海域, 总体而言温度与盐度的分布相似。西沙群岛地处南海中北部, 终年存在温跃层[35-36]。南海西部D45, D46, D47, D48站位均分布于西沙群岛, 受风场和岛礁自身的影响, 产生向海水表层上涌的营养盐, 导致海水表层温度有所降低, 初级生产力或Chl a含量增加, 这4个站位表层海水温度的平均值(26.93 ℃)低于其他站位的平均值(28.30 ℃), 这与赵文静等[37]在2014年的研究结果一致, 符合Doty and Oguri[38]提出的岛质效应。珠江口B14、B15站位出现温度高值, 可能是附近的台山核电站温排水对周围海域水温造成热冲击[39], 导致水温有所升高。
表层海水中的Chl a高值区出现在珠江口附近海域、越南沿岸, 总体呈现近岸高远岸低的特点。南海近岸海域的陆源性营养盐含量较丰富, 季风和海域水浅等因素易将底层营养盐推至表层, 而在中部的海盆区域, 陆源性营养盐对叶绿素贡献量极小, 并且受较弱的上升流影响, 使南海中部海域的叶绿素偏低。珠江口近岸、海南岛南部及越南东部海域DO浓度较高, 这可能主要受到水体与大气间较强气体交换的影响。另一方面, 这些海域相对较高的温度、盐度等物理因素促使氧气溶解度增加。
研究海域表层海水中CFC-11、CH2Br2、CH3I和CHBr2Cl的浓度范围和平均值分别是0.47~49.79(12.74±10.66) pmol·L-1、0.97~32.58(10.79±0.72) pmol·L-1、0.61~39.13(12.18±12.43) pmol·L-1、0.83~38.19(21.66±17.45) pmol·L-1。表层海水中CFC-11的浓度平均值高于2020年9月和2021年夏季刘志雯等[40]在珠江口-南海西部的调查研究结果, Wang等[41]调查发现CFC-11的溶解度与温度显著相关, 因此这一差异可能是因为调查季节处于秋季, 秋季较低的海水温度所致。CHBr2Cl与张颖杰等[42]于2016年6月调查的东海海域浓度相近, 高于Kurihara等[43]在北太平洋西部的调查结果, 可能是珠江口岸附近海水携带丰富的营养盐, 影响了浮游植物生物量和群落结构, 进而影响CHBr2Cl的浓度。表层海水中CH2Br2、CH3I高于陈卓等[44]报道的夏季珠江口海域浓度, 可能一方面是因为珠江口附近经济比较繁荣, 人口密集, 大量有机污染物排放在附近海域, 同时秋季东北季风给陆地带来了大量的降水, 陆源物质通过珠江被输送到附近海域, 大量营养物质的输送促进了浮游植物的生长, 造成了CH2Br2的高值; 另一方面秋季的海水温度较低, 不仅使CH3I在海水中的溶解度增加, 还会造成不同浮游植物优势藻种的差别, 从而影响排放CH3I的速率。
表层海水中4种VHCs的分布图如2所示。CFC-11的高值出现在南海西部的海南岛东部海域(C31站位)和西沙群岛海域(D45站位和D48站位)。受人类活动和工业排放的影响, 陆地径流将丰富的氯化物输送至此海域所致。此外, 西沙群岛附近海域存在一些正在使用的油气开采平台, 在油气开采过程中释放出较高浓度的CFCs, 致使CFC-11出现高值[45]。
CH2Br2的浓度分布总体呈现近岸高、远岸低的趋势。CH2Br2高值出现在珠江口附近海域, 一方面受到粤西沿岸环流的作用将沿岸产生的VHCs输送至此; 另一方面, CH2Br2主要来自浮游植物, 调查期间处于丰水期末期, 珠江冲淡水携带陆源物质(N、P等营养元素)入海导致海水中氮、磷等元素含量增加[46-48], 促进了浮游植物的生长及其释放卤代烃。CH3I的高值区出现在南海西部开阔海域的D46、D48、D50、D57站位。王凤等[49]在南海西部的超微型浮游植物的群类中调查发现, 原绿球藻所占比重最高。此外, Hughes等[50]通过实验室培养证实原绿球藻能够产生CH3I。因此推测该海域CH3I的高值与浮游植物中高丰度的原绿球藻释放有关。这一观点与Ooki等[51]报道的寡营养盐热带海域中CH3I的高浓度可能是由原绿球藻产生的结论一致。CHBr2Cl的浓度分布总体呈现近岸高, 远海低的趋势。南海开阔海域的D52、D53站位CHBr2Cl的高浓度源于受到大型浮游植物[52-54]释放。受到粤西暖流、越南沿岸流和冷涡的综合作用, 将深层营养盐输送到上层海水, 影响该区域的浮游植物生长[55]及CHBr2Cl的产生释放。此外, CHBr2Cl的高浓度还出现在珠江口近岸C31站位。珠江三角洲经济发达, 工业发展迅速, 发电厂、海水淡化设施和水消毒过程等人类活动也会影响其浓度[56-57]。
相关性分析结果如表 2所示, CH3I与Chl a不存在明显相关关系, 推测可能与人类活动输入及近岸海域的大型浮游植物释放和光化学反应影响有关[58]。CFC-11作为一种陆源指示, CH3I和CFC-11显著正相关关系(r =0.392, P=0.05), 进一步表明人类活动对CH3I浓度的显著影响。
|
|
表 2 珠江口-南海西部表层海水4种VHCs的浓度与环境参数的相关性 Table 2 Correlation between the concentrations of 4 VHCs and environmental parameters in the surface water of the Pearl River Estuary-Western South China Sea |
CH3I与温度呈现显著负相关(r=-0.49, P=0.01), 可能受上升流的影响, 海水温度较低, 次表层营养物质涌入表层海水中, 促进了表层浮游植物的生长, 导致CH3I在表层海水的溶解度较高。DO的含量代表了水体中氧化还原状态, 其与浮游植物的光合作用密切相关, CH3I与DO呈现显著负相关(r =-0.48, P=0.01), 浮游植物在进行光合作用时, 释放氧气使得水体中DO含量升高; 而当CH3I浓度升高时, DO浓度降低, 可能是CH3I的产生过程与浮游植物的呼吸作用存在关联。Chl a代表浮游植物的总生物量, 不同的浮游植物释放VHCs的速率存在较大差异, 无法反应该区域浮游植物的群落结构, 此外部分CH3I在海水来自于光化学的生成。
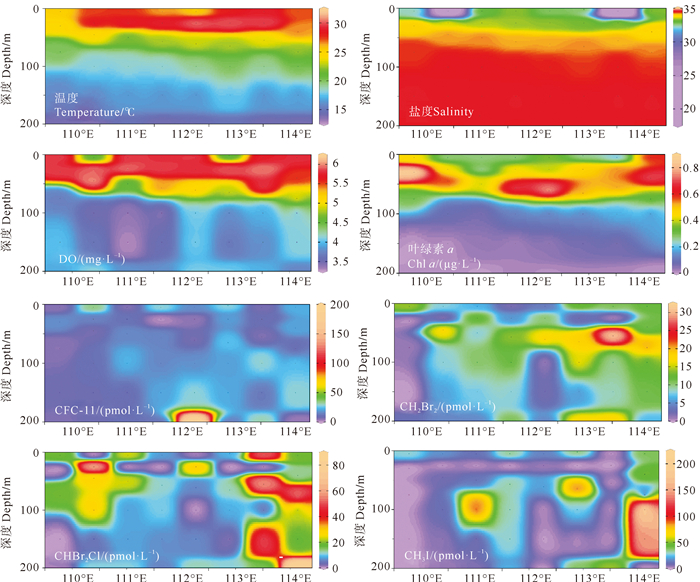
2.2 VHCs浓度的垂直分布南海西部秋季受东北季风影响, 地形和季风相互作用会产生较强的上升流, 导致海底水体涌升, 混合搅拌加剧, 海洋生态系统复杂多变。为了深入了解VHCs在南海西部的空间分布情况, 选择43—50站位全水层进行采样调查。4种VHCs浓度的及温度、盐度、DO和Chl a环境参数的垂直分布如图 3所示。
|
图 3 S断面海水中VHCs(pmol·L-1)、温度(℃)、盐度、DO(mg·L-1)和Chl a(μg·L-1)的垂直分布 Fig. 3 Vertical distributions of VHCs (pmol·L-1), temperature (℃), salinity, DO (mg·L-1) and Chl a (μg·L-1) in the seawater of Section S |
断面位于南海中西部海域, 秋季南海风场由西南季风向东北季风转换, 风力搅拌会加强上层海水垂直混合并传递热能, 形成温度跃层, 温跃层的绝热作用使上层热量不传递至深层, 致使海表温度升高, 而较高的海温反向促进温跃层强度增大[23], 海水温度随深度的增加而减小, 垂直特征明显。根据图 3可以看出, 在断面两端出现明显的温盐分层现象, 在两端50 m以上的水层出现了小范围的盐度锋面, 明显受到了上升流的影响。
DO在垂直分布上整体随着深度的增加含量减少, 可能是真光层浮游植物光合作用旺盛, 而底层浮游植物的死亡和沉降降解消耗水体中的DO所致。Chl a在该断面整体呈现出表层高底层低的特点, Chl a最大值基本位于5~50 m之间。由于南海处于热带, 光照强度极高, 过强的光照不适宜浮游植物的生长, 因此浮游植物叶绿素浓度的最大值层往往出现在温跃层[23]。
CFC-11浓度高值主要出现在沿岸表层及底层。表层的高值区与附近地区人类活动和工业排放有关。CFC-11浓度底层的高值可能与海气交换及海水垂直混合有关。Beining等[59]研究发现, 海气交换导致海洋混合层中CFC-11的浓度趋于溶解平衡, 随后CFC-11发生循环和转移过程进入更深的水层。谭娟等[60]通过模拟海洋中CFC-11的垂直分布, 发现底层CFC-11浓度增大可能是由于观测海域靠近大陆架区域, 与海水垂直混合有关。受到来源和去除途径[11, 61]及南海西部复杂的水团与热带气旋的作用, CH3I、CH2Br2和CHBr2Cl浓度在该断面中的垂直分布表现出斑块状特征。CH3I和CHBr2Cl在D50站位底层均出现浓度最大值。这可能是由于底层沉积物悬浮释放或底栖生物释放导致[9, 62]。此外, Moore等[63]指出深层海水中高浓度的CHBr2Cl是由于Cl取代CHBr3所致。2023年正值厄尔尼诺(ENSO)年, 越南东部上升流区域初级生产力的增加受ENSO的约束, 西南季风减弱, 沿岸风应力减小, 上升流被抑制, 导致表层海水不能及时补充深层营养盐, 使初级生产力受到影响, 造成表层CH3I的低值[23]。由图 3可知, CH2Br2的高值出现在混合层(50~100 m)以及断面东部的底层位置。Archer等[64]研究发现浮游植物和细菌可以产生卤代过氧化酶, 促进释放CH2Br2。此外, 菲律宾西北部海域出现的高值区可能是由南海黑潮的入侵造成, Gong等[65-67]研究发现, 入侵南海的黑潮在流经吕宋海峡时, 由于地形因素造成海水的垂直混合加剧, 丰富的营养盐被带到海水上层, 产生较高浓度的VHCs。
2.3 大气中VHCs的分布特征及控制因素珠江口-南海海域大气中CFC-11、CH3I、CH2Br2和CHBr2Cl的浓度范围分别为210.38~278.42、0.32~2.80、0.09~3.37和1.35~2.78 pptv, 平均值分别为(226.61±19.08)、(1.19±0.75)、(1.84±1.07)和(1.91±0.47) pptv。
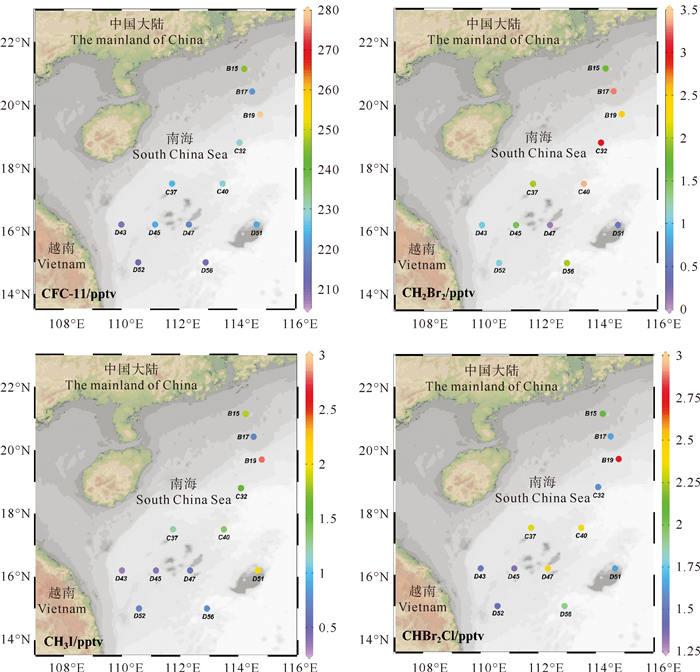
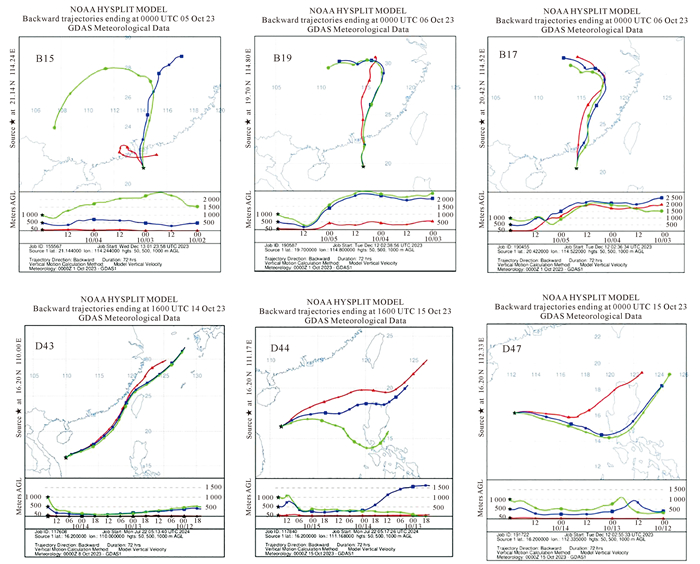
调查海域的大气中CFC-11的均值接近全球平均值[68](229.8 pptv), 高于张逸青等[69]测定的夏季珠江口-南海西部的CFC-11浓度均值(193.95 pptv), CH3I的均值高于全球平均值(0.8 pptv), 低于刘志雯等[70]2020年南海东北部的均值。大气中CFC-11和CH3I的浓度高值都出现在离岸较近的B15和B19站位, 结合72 h反轨迹分析, 气团在到达这两个站位前沿珠江三角洲地区移动(见图 5)。作为中国南部领先的制造业中心, 珠江三角洲地区空调、冰箱、汽车等制造业十分发达[71], 因此推测B15和B19站位CFC-11和CH3I的高值主要受珠江三角区较多的工业生产制造和密集人口活动排放的影响。大气中CFC-11和CH3I的浓度低值出现在离岸较远的D43站位。由后向轨迹图 5知, 气团从东海海域向东南方向, 途径台湾海峡和较为洁净的南沙海域上空, 这些海域受到人为排放的影响较小, 来自海洋的清洁气团稀释后, 使大气中CFC-11和CH3I出现浓度低值。
|
图 4 珠江口-南海西部大气中4种VHCs的浓度(pptv)的分布 Fig. 4 Distribution of four VHCs concentrations (pptv) in the atmosphere over the Pearl River Estuary-Western South China Sea |
|
图 5 B15、B19、B17、D43、D45和D47站位上方气团的72 h后向轨迹图 Fig. 5 72 hour backward trajectory diagrams of air masses above stations B15, B19, C32, B17, D43, D45 and D47 |
CH2Br2和CHBr2Cl在大气中的浓度平均值略高于全球平均水平[71](CH2Br2: 0.9 pptv; CHBr2Cl: 0.3 pptv), CHBr2Cl的平均值与尹丽菁[72]2022年4月在东海调查的结果相近(2.0 pptv), 这两个海域的调查结果均高于全球水平, 出现该结果的原因可能是所研究海域收集的样本来自受工业排放严重影响的沿海地区。CH2Br2和CHBr2Cl大气浓度总体呈现近岸高, 远海低的趋势。CH2Br2和CHBr2Cl的高值与CFC-11和CH3I的浓度高值均在雷州半岛附近海域, 分别出现在B17和B19站位。B17与B19站位的后向轨迹图大致吻合, 受陆源输入的影响较大。一方面, 气团在到达这两个站位前, 经过珠江三角洲和中国东部工业城市, 受生产制造排放和人类生产生活影响较大。另一方面, 由于受到河流输入等因素, 近岸海域的营养盐和有机质浓度一般较高[71], Chl a和DOC含量也比较大, He等[73]在黄东海的调查表明浮游植物释放的CH2Br2可以直接排放到大气中, 导致这些海域大气中CH2Br2和CHBr2Cl的浓度较高。CH2Br2和CHBr2Cl在南海北部海域的D47和D45站位出现低值, 由于72 h后向轨迹图可以看出, 气团从南海东北部分别途径菲律宾北部和中部地区最终到达这些站位, 这些区域远离陆地, 部分气团来自于海洋上空洁净空气团, 受陆源输入和人为排放影响较小, 同时气团行进的这些海域生物生产力较低, 不易受到途径城市卤代烃排放的影响。上述因素共同导致该海域大气中CH2Br2和CHBr2Cl的低值。
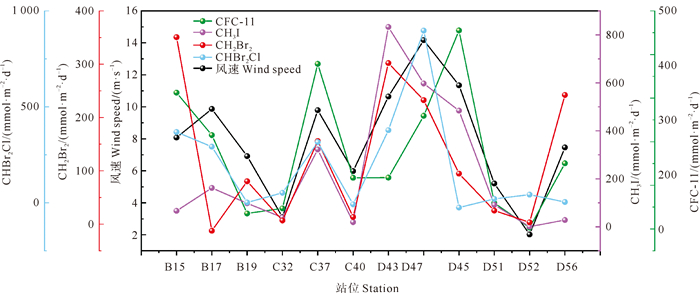
2.4 海-气通量秋季珠江口-南海西部海域CFC-11、CH3I、CH2Br2和CHBr2Cl的海-气通量范围分别为3.09~455.09、0.58~597.23、-12.60~301.99、-24.85~897.15 nmol·m-2·d-1, 海-气通量平均值分别为(179.31±145.56)、(228.43±271.89)、(124.58±128.42)、(195.06±272.69) nmol·m-2·d-1。上述结果表明, 调查期间珠江口-南海西部海域表现为大气中CH3I、CH2Br2和CHBr2Cl的源, 而作为CFC-11的汇, 与张逸青等[69]在2022年夏季南海西部海域调查结果和刘志雯等[70]在2021年夏季南海结果相同。表 3和图 6共同表明, 4种VHCs通量分布受控于多重环境因子: CFC-11、CH3I和CHBr2Cl的海-气通量与风速显著相关, 而CH3I和CH2Br2的海-气通量同时与表层海水浓度显著正相关。具体而言, 开阔海域(如D45站位)因缺乏地形屏障, 在热带气旋或季风系统影响下[74]形成高风速(12.04 m·s-1), 导致CFC-11和CHBr2Cl的通量在该海域出现最高值, 体现风速对垂直扩散过程的主导作用。相较之下, 近岸海域CH3I海-气通量最大值(D43站位597.23 nmol·m-2·d-1)的形成同时受到此海域较大风速(10.64 m·s-1)和表层高浓度(27.65 pmol·L-1)的共同驱动, 该现象与较高的生物生产力的水体促进CH3I生产释放相吻合[40]。
|
|
表 3 珠江口-南海西部海域4种VHCs的海-气通量与风速、表层海水温度和VHCs浓度的相关性分析 Table 3 Correlation analysis of sea-air fluxes of four VHCs, wind speed, temperature and concentrations of VHCs in surface seawater in the Pearl River Estuary-Western South China Sea |
|
图 6 秋季珠江口-南海西部CFC-11、CH3I、CH2Br2和CHBr2Cl的海-气通量和风速 Fig. 6 Sea-air fluxes of CFC-11, CH3I, CH2Br2 and CHBr2Cl and wind speed in the Pearl River Estuary-Western South China Sea in autumn |
珠江口近岸海域B15站位的CH2Br2海-气通量最高值受到区域环境特征的影响: 邻近陆源输入如工业与城市排放的废热经河流及直接排放入海, 以及该区域航运繁忙, 船舶发动机等释放的热量导致海水温度较高(29.87 ℃), 通过降低溶解度促进表层海水中的CH2Br2向大气扩散释放。这印证了Abrahamsson等[75]关于近岸海-气通量高于大洋区VHCs的观测结论。值得注意的是, Yokouchi等[76]在日本相模湾的调查研究发现, VHCs的海-气通量年际波动较大, 这表明本研究单一季节调查结果可能无法完全反映区域通量的年际变化特征。本研究在珠江口-南海西部海域的采样站位覆盖度不足, 一些海沟等特殊地形缺乏采样, 且海域空间异质性显著, 相邻站位间通量可能因局部因素存在差异。此外, 单季节观测难以捕捉季风转换期等关键时段的海-气交换动态以及未实现连续时间序列观测, 无法区分周日尺度变化对通量的影响, 后续研究需结合多季节航次观测与数值模拟, 系统阐明VHCs通量的时空演变机制。
3 结论(1) 表层海水VHCs的空间分布受自然过程与人类活动的协同调控。CFC-11在南海西部海域的高值主要受粤西沿岸流和南海暖流等多重水团的主导。CH3I的浓度变化则体现了浮游植物生物合成与光化学反应的复合调控机制。CH2Br2和CHBr2Cl浓度分布呈现近岸高、远岸低的趋势, 可能与珠江口城市排污、工业排放等陆源输入过程密切相关。
(2) 垂直分布特征表明, 4种VHCs浓度在底层海水均出现高值, 表明沉积物-水界面存在VHCs释放过程。其中, CH2Br2在混合层及断面东部底层的的高值可能源于浮游植物、细菌产生卤代过氧化酶促进其释放。
(3) 大气中VHCs浓度呈现显著的区域差异: CFC-11的均值与全球平均值(229.8 pptv)无显著差异, 其浓度变化受海-气扩散平衡调控; CH3I的均值高于全球平均值(0.8 pptv), 反映生物源释放的显著影响。CH2Br2和CHBr2Cl的浓度趋势(近岸>远海)印证陆源输入对近岸大气成分的显著影响。综合海-气通量数据, 本研究证实珠江口-南海西部海域在秋季表现为大气CH3I、CH2Br2和CHBr2Cl的源, 同时作为CFC-11汇。
| [1] |
Reifenhäuser W, Heumann K G. Bromo and bromochloromethanes in the Antarctic atmosphere and the south polar sea[J]. Chemosphere, 1992, 24(9): 1293-1300. DOI:10.1016/0045-6535(92)90054-U (  0) 0) |
| [2] |
Hossaini R, Atlas E, Dhomse S S, et al. Recent trends in stratospheric chlorine from very short-lived substances[J]. Journal of Geophysical Research: Atmospheres, 2019, 124(4): 2318-2335. DOI:10.1029/2018JD029400 (  0) 0) |
| [3] |
陆蓓蓓, 黄发源, 单晓梅, 等. 合肥市水源与饮用水中挥发性卤代烃健康风险评价[J]. 中国预防医学杂志, 2013, 14(4): 260-264. Lu B B, Huang F Y, Shan X M, et al. Health risk assessment of volatile halohydrocarbons in water sources and drinking water in Hefei City[J]. China Preventive Medicine, 2013, 14(4): 260-264. (  0) 0) |
| [4] |
Ramadan A, Yassin M F, Alshammari B Z. Health risk assessment associated with volatile organic compounds in a parking garage[J]. International Journal of Environmental Science and Technology, 2019, 16(8): 2549-2564. (  0) 0) |
| [5] |
Molina M J, Rowland F S. Stratospheric sink for chlorofluoromethanes: Chlorine atom-catalysed destruction of ozone[J]. Nature, 1974, 249(5460): 810-812. DOI:10.1038/249810a0 (  0) 0) |
| [6] |
Cicerone R J, Stolarski R S, Walters S. Stratospheric ozone destruction by man-made chlorofluoromethanes[J]. Science, 1974, 185(4157): 1165-1167. DOI:10.1126/science.185.4157.1165 (  0) 0) |
| [7] |
Hossaini R, Chipperfield M P, Montzka S A, et al. Efficiency of short-lived halogens at influencing climate through depletion of stratospheric ozone[J]. Nature Geoscience, 2015, 8(3): 186-190. DOI:10.1038/ngeo2363 (  0) 0) |
| [8] |
Dessens O, Zeng G, Warwick N, et al. Short-lived bromine compounds in the lower stratosphere, impact of climate change on ozone[J]. Atmospheric Science Letters, 2009, 10(3): 201-206. DOI:10.1002/asl.236 (  0) 0) |
| [9] |
何真, 倪洁, 杨桂朋. 海洋中挥发性卤代烃的研究进展[J]. 中国海洋大学学报(自然科学版), 2020, 50(3): 27-36. He Z, Ni J, Yang G P. Research progress on volatile halocarbons in the ocean[J]. Periodical of Ocean University of China, 2020, 50(3): 27-36. DOI:10.16441/j.cnki.hdxb.20190410 (  0) 0) |
| [10] |
Manley S L, Dastoor M N. Methyl halide (CH3X) production from the giant kelp, Macrocystis, and estimates of global CH3X production by kelp 1[J]. Limnology and Oceanography, 1987, 32(3): 709-715. DOI:10.4319/lo.1987.32.3.0709 (  0) 0) |
| [11] |
Itoh N, Tsujita M, Ando T, et al. Formation and emission of monohalomethanes from marine algae[J]. Phytochemistry, 1997, 45(1): 67-73. DOI:10.1016/S0031-9422(96)00786-8 (  0) 0) |
| [12] |
Manley S L, De L, Cuesta J L. Methyl iodide production from marine phytoplankton cultures[J]. Limnology and Oceanography, 1997, 42(1): 142-147. DOI:10.4319/lo.1997.42.1.0142 (  0) 0) |
| [13] |
Tegtmeier S, Krüger K, Quack B, et al. The contribution of oceanic methyl iodide to stratospheric iodine[J]. Atmospheric Chemistry and Physics, 2013, 13(23): 11869-11886. DOI:10.5194/acp-13-11869-2013 (  0) 0) |
| [14] |
Butler J H, King D B, Lobert J M, et al. Oceanic distributions and emissions of short-lived halocarbons[J]. Global Biogeochemical Cycles, 2007, 21(1): GB1023. DOI:10.1029/2006GB002732 (  0) 0) |
| [15] |
Chuck A L, Turner S M, Liss P S. Oceanic distributions and air-sea fluxes of biogenic halocarbons in the open ocean[J]. Journal of Geophysical Research: Oceans. DOI:10.1029/2004JC002741 (  0) 0) |
| [16] |
Happell J D, Wallace D W R. Methyl iodide in the Greenland/Norwegian Seas and the tropical Atlantic Ocean: Evidence for photochemical production[J]. Geophysical Research Letters, 1996, 23(16): 2105-2108. DOI:10.1029/96GL01764 (  0) 0) |
| [17] |
Moore R M, Zafiriou O C. Photochemical production of methyl iodide in seawater[J]. Journal of Geophysical Research: Atmospheres, 1994, 99(D8): 16415-16420. DOI:10.1029/94JD00786 (  0) 0) |
| [18] |
Richter U, Wallace D W R. Production of methyl iodide in the tropical Atlantic Ocean[J]. Geophysical Research Letters. DOI:10.1029/2004GL020779 (  0) 0) |
| [19] |
Yokouchi Y, Osada K, Wada M, et al. Global distribution and seasonal concentration change of methyl iodide in the atmosphere[J]. Journal of Geophysical Research: Atmospheres. (  0) 0) |
| [20] |
Zhang J, Yu Z G, Wang J T, et al. The subtropical Zhujiang (Pearl River) estuary: Nutrient, trace species and their relationship to photosynthesis[J]. Estuarine, Coastal and Shelf Science, 1999, 49(3): 385-400. DOI:10.1006/ecss.1999.0500 (  0) 0) |
| [21] |
Hu J, Jia G, Mai B, et al. Distribution and sources of organic carbon, nitrogen and their isotopes in sediments of the subtropical Pearl River estuary and adjacent shelf, Southern China[J]. Marine Chemistry, 2006, 98(2-4): 274-285. DOI:10.1016/j.marchem.2005.03.008 (  0) 0) |
| [22] |
夏维, 周争桥. 基于观测资料的珠江口附近海域夏季气象水文要素分析[J]. 海洋湖沼通报, 2021, 43(5): 60-65. Xia W, Zhou Z Q. Analysi s of summer meteorological and hydrological elements in the sea area near the Pearl River Estuary based on observational data[J]. Marine Limnological Bulletin, 2021, 43(5): 60-65. (  0) 0) |
| [23] |
林智涛. 南海北部与西部初级生产力影响因子探究[D]. 湛江: 广东海洋大学, 2017. Lin Z T. Influencing Factors of Primary Productivity in the Northern and Western Parts of the South China Sea[D]. Zhangjiang: Guangdong Ocean University, 2017. (  0) 0) |
| [24] |
Yin K, Harrison P J. Nitrogen over enrichment in subtropical Pearl River estuarine coastal waters: Possible causes and consequences[J]. Continental Shelf Research, 2008, 28(12): 1435-1442. DOI:10.1016/j.csr.2007.07.010 (  0) 0) |
| [25] |
杨桂朋, 尹士序, 陆小兰, 等. 吹扫-捕集气相色谱法测定海水中挥发性卤代烃[J]. 中国海洋大学学报(自然科学版), 2007, 37(2): 299-304. Yang G P, Yin S X, Lu X L, et al. Determination of volatile halogenated hydrocarbons in seawater by gas chromatography with purge-trap[J]. Periodial of Ocean University of China, 2007, 37(2): 299-304. DOI:10.16441/j.cnki.hdxb.2007.02.023 (  0) 0) |
| [26] |
Parsons T R. A manual of Chemical & Biological Methods for Seawater Analysis[M]. Netherlands: Elsevier, 2013.
(  0) 0) |
| [27] |
Stewart B M, Elliott P A W. Systematic salt effects in the automated determination of nutrients in seawater[J]. Water Research, 1996, 30(4): 869-874. DOI:10.1016/0043-1354(95)00245-6 (  0) 0) |
| [28] |
World Meteorological Organization (WMO), Scientificassessment of ozone depletion[R]. Ceneva, Switzerland: Switzerland Global Ozone Research and MonitoringProject-Report, 2022.
(  0) 0) |
| [29] |
Liss P S, Slater P G. Flux ofgases across the air-sea interface[J]. Nature, 1974, 247(5438): 181-184. DOI:10.1038/247181a0 (  0) 0) |
| [30] |
Warner M J, Weiss R F. Solubilities of chlorofluorocarbons 11 and 12 in water and seawater[J]. Deep Sea Research Part A, 1985, 32(12): 1485-1497. DOI:10.1016/0198-0149(85)90099-8 (  0) 0) |
| [31] |
Hunter-Smith R J, Balls P W, Liss P S. Henry's Law constants and the air-sea exchange of various low molecular weight halocarbon gases[J]. Tellus B: Chemical and Physical Meteorology, 1983, 35B(3): 170-176. DOI:10.1111/j.1600-0889.1983.tb00021.x (  0) 0) |
| [32] |
Moore R M, Geen C E, Tait V K. Determination of Henry's Law constants for a suite of naturally occurring halogenated methanes in seawater[J]. Chemosphere, 1995, 30(6): 1183-1191. DOI:10.1016/0045-6535(95)00009-W (  0) 0) |
| [33] |
Wanninkhof R. Relationship between wind speed and gas exchange over the ocean[J]. Journal of Geophysical Research: Oceans, 1992, 97(5): 7373-7382. (  0) 0) |
| [34] |
Zheng M, De Bruyn W J, Saltzman E S. Measurements of the diffusion coefficients of CFC-11 and CFC-12 in pure water and seawater[J]. Journal of Geophysical Research: Oceans, 1998, 103(1): 1375-1379. (  0) 0) |
| [35] |
林洪瑛, 韩舞鹰. 南沙群岛海域营养盐对浮游植物生长的限制研究[C]//中国海洋湖沼学会, 中科院海洋研究所. 第七届全国海洋湖沼青年学者学术研讨会论文摘要集. 青岛: 中国科学院南海海洋研究所, 2000: 16-17. Lin H Y, Han W Y. Restriction of phytoplankton growth by nutrient salts in Nansha Islands[C]//China Society of Marine Lakes and Marshes, Institute of Oceanography, Chinese Academy of Sciences. Abstracts of the Seventh National Symposium for Young Scholars on Marine Lakes and Marshes. Qingdao: South China Sea Institute of Oceanography, Chinese Academy of Sciences, 2000: 16-17. (  0) 0) |
| [36] |
陈露, 李纯厚, 戴明, 等. 西沙永兴岛附近海域秋末氮磷营养盐加富对浮游植物生长限制的影响[J]. 南方水产科学, 2016, 12(4): 125-130. Ch en, Li C H, Dai M, et al. Effects of nitrogen and phosphorus nutrient enrichment on phytoplankton growth limitation in late fall in the waters off Yongxing Island, Xisha[J]. Southern Aquatic Science, 2016, 12(4): 125-130. (  0) 0) |
| [37] |
赵文静, 姜国强, 杨静, 等. 西沙群岛及周边海域水体关键生态环境参量时空分布特征的遥感研究[C]. 2015年中国环境科学学会学术年会论文集, 北京: 中国环境科学学会, 2015: 1885-1891. Zhao W J, Jiang G Q, Yang J, et al. Remote sensing study on the spatial and temporal distribution characteristics of key ecological and environmental parameters in the water bodies of Xisha Islands and the surrounding waters[C]. Proceedings of the 2015 Annual Conference of the Chinese Society for Environmental Science, Beijing: China Environmental Science Society, 2015: 1885-1891. (  0) 0) |
| [38] |
Doty M S, Oguri M. The island mass effect[J]. ICES Journal of Marine Science, 1956, 22(1): 33-37. DOI:10.1093/icesjms/22.1.33 (  0) 0) |
| [39] |
粟丽, 黄梓荣, 徐珊楠, 等. 台山核电邻近海域春秋季浮游植物群落结构特征[J]. 海洋科学, 2016, 40(9): 61-68. Su L, Huang Z R, Xu S N, et al. Characteristics of phytoplankton community structure in the adjacent sea area of Taishan nuclear power plant in spring and fall[J]. Marine Science, 2016, 40(9): 61-68. (  0) 0) |
| [40] |
刘志雯, 何真, 邹亚文, 等. 南海东北部及吕宋海峡邻近海域海水和大气中挥发性卤代烃的浓度分布与海-气通量[J]. 中国海洋大学学报(自然科学版), 2023, 53(1): 85-94. Liu Z W, He Z, Zou Y W, et al. Concentration distribution and sea-air fluxes of volatile halogenated hydrocarbons in seawater and atmosphere in the northeastern part of the South China Sea and the neighboring waters of Luzon Strait[J]. Periodical of Ocean University of China, 2023, 53(1): 85-94. DOI:10.16441/j.cnki.hdxb.20220049 (  0) 0) |
| [41] |
Wang P, Scott J R, Solomon S, et al. On the effects of the ocean on atmospheric CFC-11 lifetimes and emissions[J]. Proceedings of the National Academy of Sciences, 2021, 118(12): e2021528118. DOI:10.1073/pnas.2021528118 (  0) 0) |
| [42] |
张颖杰, 何真, 杨桂朋. 东海海水和大气中挥发性卤代烃的分布[J]. 中国环境科学, 2018, 38(1): 14-25. Zhang Y J, He Z, Yang G P. Distribution of volatile halogenated hydrocarbons in seawater and atmosphere of the East China Sea[J]. China Environmental Science, 2018, 38(1): 14-25. (  0) 0) |
| [43] |
Kurihara M K, Kimura M, Iwamoto Y, et al. Distributions of short-lived iodocarbons and biogenic trace gases in the open ocean and atmosphere in the western North Pacific[J]. Marine Chemistry, 2010, 118(3-4): 156-170. DOI:10.1016/j.marchem.2009.12.001 (  0) 0) |
| [44] |
陈卓. 珠江口、东海和西太平洋挥发性卤代烃的分布及其影响因素研究[D]. 青岛: 中国海洋大学, 2024. Chen Z. Study on theDistribution of Volatile Halogenated Hydrocarbons in the Pearl River Estuary, East China Sea and West Pacific Ocean and their influencing factors[D]. Qingdao: Ocean University of China, 2024. (  0) 0) |
| [45] |
刘树保, 李欣, 周永文. 大港油田地区挥发性有机物分析[J]. 油气田环境保护, 2016, 26(4): 26-28. Liu S B, Li X, Zhou Y W. Analysis of volatile organic compounds in Dagang oilfield area[J]. Oil and Gas Field Environmental Protection, 2016, 26(4): 26-28. (  0) 0) |
| [46] |
Cai W J, Dai M H, Wang Y C, et al. The biogeochemistry of inorganic carbon and nutrients in the Pearl River estuary and the adjacent Northern South China Sea[J]. Continental Shelf Research, 2004, 24(12): 1301-1319. DOI:10.1016/j.csr.2004.04.005 (  0) 0) |
| [47] |
Dai M H, Zhai W D, Cai W J, et al. Effects of an estuarine plume-associated bloom on the carbonate system in the lower reaches of the Pearl River estuary and the coastal zone of the northern South China Sea[J]. Continental Shelf Research, 2008, 28(12): 1416-1423. DOI:10.1016/j.csr.2007.04.018 (  0) 0) |
| [48] |
杨威, 董园, 俎婷婷, 等. 南海北部夏季叶绿素a分布规律及影响因素[J]. 热带海洋学报, 2019, 38(6): 9-20. Yang W, Dong Y, Zu T T, et al. Distribution and influencing factors of chlorophyll-a in the northern South China Sea in summer[J]. Journal of Tropical Oceanography, 2019, 38(6): 9-20. (  0) 0) |
| [49] |
王凤. 西太平洋和南海西部超微型浮游植物群落结构的研究[D]. 济南: 山东大学, 2021. Wang F. Research on the Community Structure of Ultramicrophy Toplankton in the western Pacific Ocean and western South China Sea[D]. Jinan: Shandong University, 2021. (  0) 0) |
| [50] |
Hughes C, Franklin D J, Malin G. Iodomethane production by two important marine cyanobacteria: Prochlorococcus marinus(CCMP 2389) and Synechococcus sp[J]. Marine Chemistry, 2011, 125(1-4): 19-25. DOI:10.1016/j.marchem.2011.01.007 (  0) 0) |
| [51] |
Ooki A, Nomura D, Nishino S, et al. A global-scale map of isoprene and volatile organic iodine in surface seawater of the Arctic, Northwest Pacific, Indian, and Southern Oceans[J]. Journal of Geophysical Research: Oceans, 2015, 120(6): 4108-4128. DOI:10.1002/2014JC010519 (  0) 0) |
| [52] |
Sturges W T, Sullivan C W, Schnell R C, et al. Bromoalkane production by Antarctic ice algae[J]. Tellus B: Chemical and Physical Meteorology, 1993, 45(2): 120-126. DOI:10.3402/tellusb.v45i2.15586 (  0) 0) |
| [53] |
Moore R M, Webb M, Tokarczyk R, et al. Bromoperoxidase and iodoperoxidase enzymes and production of halogenated methanes in marine diatom cultures[J]. Journal of Geophysical Research: Oceans, 1996, 101(9): 20899-20908. (  0) 0) |
| [54] |
Laturnus F, Adams F C, Wiencke C. Methyl halides from Antarctic macroalgae[J]. Geophysical Research Letters, 1998, 25(6): 773-776. DOI:10.1029/98GL00490 (  0) 0) |
| [55] |
柴扉, 薛惠洁, 侍茂崇. 海南岛东部上升流研究[C]//中国海洋学文集——南海海流数值计算及中尺度特征研究. 青岛: 青岛海洋大学, 2001: 138-146. Chai F, Xue H J, Shi M C. Study on the upwelling in the eastern part of Hainan Island[C]//Anthology of Chinese Oceanography—Numerical Computation and Mesoscale Characterization of the South China Sea Currents. Qingdao: Qingdao Ocean University, 2001: 138-146. (  0) 0) |
| [56] |
Nieuwenhuijsen M J, Toledano M B, Eaton N E, et al. Chlorination disinfection byproducts in water and their association with adverse reproductive outcomes: A review[J]. Occupational and Environmental Medicine, 2000, 57(2): 73-85. DOI:10.1136/oem.57.2.73 (  0) 0) |
| [57] |
Quack B, Wallace D W R. Air-sea flux of bromoform: Controls, rates, and implications[J]. Global Biogeochemical Cycles. DOI:10.1029/2002GB001890 (  0) 0) |
| [58] |
张逸青, 何真, 尹丽菁, 等. 春季和秋季东海挥发性卤代烃的时空分布与海-气通量研究[J]. 海洋环境科学, 2024, 43(1): 12-26. Zhang Y Q, He Z, Yin L J, et al. Spatial and temporal distribution of volatile halogenated hydrocarbons in the East China Sea during spring and fall and sea-air fluxes[J]. Marine Environmental Science, 2024, 43(1): 12-26. (  0) 0) |
| [59] |
Beining P, Roether W. Temporal evolution of CFC 11 and CFC 12 concentrations in the ocean interior[J]. Journal of Geophysical Research: Oceans, 1996, 101(7): 16455-16464. (  0) 0) |
| [60] |
谭娟, 李清泉, 王兰宁, 等. MOM4_L40模式对全球海洋CFC-11分布的模拟及其通风能力评估[J]. 地球物理学报, 2016, 59(11): 3960-3973. Tan J, Li Q Q, Wang L N, et al. Simulation of the global oceanic CFC-11 distribution and assessment of oceanic ventilation using the MOM4_L40 model[J]. Chinese Journal of Geophysics, 2016, 59(11): 3960-3973. (  0) 0) |
| [61] |
Goodwin K D, Schaefer J K, Oremland R S. Bacterialoxidation of dibromomethane and methyl bromide in natural waters and enrichment cultures[J]. Applied and Environmental Microbiology, 1998, 64(12): 4629-4636. DOI:10.1128/AEM.64.12.4629-4636.1998 (  0) 0) |
| [62] |
Li Y, He Z, Yang G P, et al. Spatial distribution and biogeochemical cycling of methyl iodide in the Yellow Sea and the East China Sea during summer[J]. Environmental Pollution, 2021, 276: 116749. DOI:10.1016/j.envpol.2021.116749 (  0) 0) |
| [63] |
Moore R M, Tokarczyk R. Volatile biogenic halocarbons in the northwest Atlantic[J]. Global Biogeochemical Cycles, 1993, 7(1): 195-210. DOI:10.1029/92GB02653 (  0) 0) |
| [64] |
Archer S D, Posman K M, DeStefano J, et al. Fluorescent detection of bromoperoxidase activity in microalgae and planktonic microbial communities using aminophenyl fluorescein[J]. Frontiers in Marine Science, 2019, 6: 68. DOI:10.3389/fmars.2019.00068 (  0) 0) |
| [65] |
Tamg D, Ni I, Kester D, et al. Remote sensing observations of winter phytoplankton blooms southwest of the Luzon Strait in the South China Sea[J]. Marine Ecology Progress Series, 1999, 191: 43-51. DOI:10.3354/meps191043 (  0) 0) |
| [66] |
Gong G C, Liu K K, Liu C T, et al. The chemical hydrography of the South China Sea West of Luzon and a comparison with the West Philippine Sea[J]. Terrestrial, Atmospheric and Oceanic Sciences, 1992, 3(4): 561-587. (  0) 0) |
| [67] |
Peñaflor E L, Villanoy C L, Liu C T, et al. Detection of monsoonal phytoplankton blooms in Luzon Strait with MODIS data[J]. Remote Sensing of Environment, 2007, 109(4): 443-450. DOI:10.1016/j.rse.2007.01.019 (  0) 0) |
| [68] |
Fahey D, Newman P A, Pyle J A, et al. Scientific assessment of ozone depletion: 2018[M]. Geneva, Switzerland: World Meteorological Organizatio, [2018.11.5 ], doi: 10.7289/V5/CWMD,2018-06-58.
(  0) 0) |
| [69] |
张逸青. 中国东海和南海西部海域挥发性卤代烃的浓度分布与海-气通量研究[D]. 青岛: 中国海洋大学, 2022. Zhang Y Q. Concentration Distribution and Sea-air Flux of Volatile Halogenated Hydrocarbons in the East China Sea and the Western Part of the South China Sea[D]. Qingdao: Ocean University of China, 2022. (  0) 0) |
| [70] |
刘志雯. 中国东海、南海和东印度洋挥发性卤代烃的浓度分布与海-气通量研究[D]. 青岛: 中国海洋大学, 2021. Liu Z W. Concentration Distribution and Sea-air Flux of Volatile Halogenated Hydrocarbons in the East China Sea, South China Sea and East Indian Ocean[D]. Qingdao: Ocean University of China, 2021. (  0) 0) |
| [71] |
Bergesen H O, Parmann G, Thommessen ∅ B. World Meteorological Organization, 1st Edition[M]. London: London Routledge, 2018: 233-234.
(  0) 0) |
| [72] |
尹丽菁. 春季中国东海挥发性卤代烃的分布变化及海洋酸化的影响[D]. 青岛: 中国海洋大学, 2023. Yin L J. Changes in the Distribution of volatile Halogenated Hydrocarbons in the East China Sea in Spring and the Impact of Ocean Acidification[D]. Qingdao: Ocean University of China, 2023. (  0) 0) |
| [73] |
He Z, Yang G P, Lu X L, et al. Halocarbons in the marine atmosphere and surface seawater of the south Yellow Sea during spring[J]. Atmospheric Environment, 2013, 80: 514-523. DOI:10.1016/j.atmosenv.2013.08.025 (  0) 0) |
| [74] |
江文, 王东海, 张春燕, 等. 近70年不同路径的南海热带气旋的统计特征[J]. 热带气象学报, 2022, 38(3): 433-443. Jiang W, Wang D H, Zhang C Y, et al. Statistical characteristics of South China Sea tropical cyclones with different paths in the last 70 years[J]. Journal of Tropical Meteorology, 2022, 38(3): 433-443. (  0) 0) |
| [75] |
Abrahamsson K, Bertilsson S, Chierici, M, Fransson, A, et al. Variations of biochemical parameters along a transect in the Southern Ocean, with special emphasis on volatile halogenated organic compounds[J]. Deep Sea Research Part Ⅱ, Topical Studies in Oceanography, 2004, 51(22-24): 2745-2756. DOI:10.1016/j.dsr2.2004.09.004 (  0) 0) |
| [76] |
Yokouchi Y, Inagaki T, Yazawa K, et al. Estimates of ratios of anthropogenic halocarbon emissions from Japan based on aircraft monitoring over Sagami Bay, Japan[J]. Journal of Geophysical Research: Atmospheres. DOI:10.1029/2004JD005320 (  0) 0) |
2. Marine Ecology and Environmental Science Function Laboratory, Qingdao Marine Science and Technology Center, Qingdao 266237, China
 2025, Vol. 55
2025, Vol. 55


