2. 中国海洋大学海洋生物遗传学与育种教育部重点实验室, 山东 青岛 266003
密码子使用偏好(Codon usage bias)是蛋白质翻译过程中同义密码子的非随机使用, 这种现象在不同物种间普遍存在。虽然同义密码子的替换使用不会改变蛋白质的序列和结构, 但密码子使用频率与tRNA丰度的匹配程度显著影响了翻译效率, 对蛋白质合成的动态调控起着关键作用[1]。通过调整tRNA丰度和优化其对应密码子的频率能够提升tRNA配对的准确性、增加翻译速度、抑制转录本的早期剪切和多腺苷酸化以及提升mRNA的稳定性。而应用稀有密码子具有调控翻译起始以及提升蛋白质折叠准确性的作用[2]。研究表明, 密码子的使用偏好类型受到选择压力、突变和遗传漂变等因素的影响, 是自然选择和中性过程共同作用的结果[3-4]。密码子使用偏好具有生物类群的特异性, 特定的同义替代在大肠杆菌(Escherichia coli)[5]、酿酒酵母(Saccharomyces cerevisiae)[6]、黑腹果蝇(Drosophila melanogaster)[7]和人类(Homo Sapiens)[8]等多种生物体中具有显著的适应性和表型效应, 对基因组分子进化产生了重要影响。在缺乏明显选择压力的种群中, 密码子使用遵循中性演化规律, 该规律能反映基因组范围的偏向性突变特征。例如, 哺乳动物和酵母重组热点区域的GC偏向性基因转换显著影响该区域第三位密码子GC含量[9-10]。在GC与AT比例偏差较大的物种中, 碱基偏向性突变对密码子选择偏好的影响甚至超过选择压力[11]。例如, 革兰氏阳性细菌山羊支原体的基因组呈现出显著的偏向性碱基比例, GC含量仅占25%, 甚至只有2%的密码子以鸟嘌呤(G)或胞嘧啶(C)核苷酸结尾[12]。选择和突变对密码子使用偏好的影响并不互斥, 多项研究表明, 密码子使用偏好类型由选择和中性过程之间的平衡共同塑造[13]。然而, 目前尚不清楚影响这种平衡的具体因素及其在物种间或基因间的变化规律。
软体动物是无脊椎动物中的第二大类群, 现存物种超过100 000种[14]。它们在生命周期、栖息地和形态上具有高度多样性, 为研究选择和中性过程对密码子使用偏好的影响提供了独特的研究体系。然而, 尽管软体动物具有重要的生态和经济价值, 但目前对软体动物门的密码子研究仍局限于双壳纲等主要类群[15]。近年来, 随着基因组测序技术的飞速发展, 多个软体动物的基因组图谱被破译, 为系统解析其密码子使用规律奠定了基础。在本研究中, 收集了软体动物头足纲、腹足纲、双壳纲和无板纲四个主要类群动物的基因组和转录组数据, 通过分析41个物种的蛋白质编码基因, 计算了各物种的密码子频率和相对同义密码子使用度(Relative synonymous codon usage, RSCU), 鉴定了偏好和稀有密码子, 评估了物种整体水平的密码子使用偏好规律。进一步地, 本研究对比了各门类动物的密码子使用偏好差异, 探究了影响软体动物密码子使用偏好的潜在因素, 为深入理解其基因组演化驱动力提供了新的见解, 也为完善软体动物蛋白质编码基因的注释提供了参考依据。
1 材料与方法 1.1 数据来源本研究选取了41种软体动物的基因编码序列(Coding sequences, CDS), 包括12种双壳纲(Bivalves)、10种腹足纲(Gastropods)、10种头足纲(Cephalopods)和9种无板纲(Aplacophora)的物种, 具体包括: 平端深海偏顶蛤(Bathymodiolus platifrons)、菲律宾偏顶蛤(Modiolus philippinarum)、合浦珠母贝(Pinctada fucata)、秘鲁紫扇贝(Argopecten purpuratus)、海湾扇贝(A. irradians)、栉孔扇贝(Chlamys farreri)、闪耀毛皮贝(Chaetoderma nitidulum)、虾夷扇贝(Patinopecten yessonesis)、泥蚶(Tegillarca granosa)、魁蚶(Scapharca broughtonii)、螠蛏(Sinonovacula constricta)、侏儒蛤(Mulinia lateralis)、长牡蛎(Crassostrea gigas)、褐云玛瑙螺(Achatina fulica)、绿叶海蜗牛(Elysia chlorotica)、皱纹盘鲍(Haliotis discus)、加州海兔(Aplysia californica)、光滑双脐螺(Biomphalaria glabrata)、短滨螺(Littorina saxatilis)、新西兰泥蜗(Potamopyrgus antipodarum)、脉红螺(Rapana venosa)、帽贝(Lottia gigantea)、福寿螺(Pomacea canaliculata)、茎柔鱼(Dosidicus gigias)、夏威夷短尾乌贼(Euprymna scolopes)、金乌贼(Sepia esculenta)、虎斑乌贼(S. pharaonis)、仿乌贼(Sepioloidea lineolata)、环蛸(Hapalochlaena maculosa)、玛雅蛸(Octopus maya)、加州双斑蛸(O. bimaculoides)、长蛸(O. minor)、Alexandromenia crassa、Entonomenia tricarinata、Falcidens caudatus、Helluoherpia aegiri、Kruppomenia borealis、Macellomenia schanderi、Neomenia megatrapezata、Proneomenia sluiteri和Idiosepius notoides [16-27]。这41个物种中有17个有参考基因组序列的物种。对于这17个物种, 其基因组序列和基因组注释的通用特征格式(General feature format, GFF)文件是从NCBI(https://www.ncbi.nlm.nih.gov/)和GIGADB(http://gigadb.org/)数据库下载的。侏儒蛤的参考基因组和注释数据由本课题组提供。利用gffread(v0.12.7)软件从参考基因组序列中提取CDS。对于其余24个没有参考基因组序列的物种, 其CDS序列从参考转录本拼接序列(Transcriptome shotgun assembly, TSA)中提取, 其中: 15个物种(L. rugatus、B. platifrons、M. philippinarum、D. gigias、E. scolopes、H. maculosa、I. notoides、O. maya、O. minor、S. esculenta、S. pharaonic、S. lineolate、L. saxatilis、P. antipodarum、R. venosa)的TSA序列从NCBI数据库获取; 其余9个物种(A. crassa、C. nitidulum、E. tricarinata、F. caudatus、H. aegiri、K. borealis、M. schanderi、N. megatrapezata、P. sluiteri)的TSA数据从DRYAD数据库(https://datadryad.org/stash)下载。数据来源或登录号如表 1所示。使用ORFfinder(v1.0.0)软件识别其开放阅读框, 提取长于100 bp的CDS。本研究使用Blastn比对识别了其中的线粒体编码基因, 并将其去除。为保证分析准确性, 本研究剔除了密码子个数非整数或含有模糊碱基的CDS。
|
|
表 1 物种名和获取数据的网站或NCBI登录号 Table 1 Species names and the websites or NCBI access numbers for available data |
有效密码子数量(Effective number of codons, ENC)是评估基因或基因组密码子使用偏好程度的常用参数[28]。ENC取值范围为20~61:若取值20, 则表示密码子完全偏好, 即每个氨基酸只使用一种密码子; 若取值61, 则表示密码子使用没有偏好。本研究使用EMBOSS软件的CHIPS(Codon heterozygosity in a protein-coding sequence)子程序计算了各物种基因以及基因组水平上的ENC[29]。在无选择压力的假设下, ENC的期望值可以由第三位密码子的GC含量(GC3)近似计算, 即当偏向性突变是导致生物体中密码子使用偏好程度的主要因素时, 基因的ENC的观测值与期望值非常接近。而如果大量基因的真实值与预期值差异较大, 则表明自然选择等其他因素在塑造密码子使用偏好类型中起到了关键作用[28]。因此, 本研究进一步分析了ENC与GC3的相关性, 以评估偏向性突变对密码子使用偏好的影响程度。
1.3 同义密码子使用频率分析同义密码子相对使用频率由Sharp等[6]提出, 是一个被广泛应用于评估密码子使用偏好的指标。RSCU是特定密码子的实际频率与无使用偏好情况下预期频率的比值, 其计算公式如下:
| $ r_{\mathrm{RSCU}}=\frac{a_{i j}}{\sum\limits_j^{b_i} a_{i j}} b_i 。$ | (1) |
式中: aij为编码第i种氨基酸的第j个同义密码子的出现次数; bi为第i种氨基酸的同义密码子数量。当RSCU大于1时, 表明该密码子的使用频率高于预期。相反, 当RSCU小于1时, 则表明该密码子的使用频率低于预期。从64个密码子中排除没有同义编码的蛋氨酸密码子(ATG)和色氨酸密码子(TGG)以及3个终止密码子(TAA、TAG和TGA)后, 本研究使用CodonW(v1.4.7)软件计算各物种剩余的59个密码子的RSCU[30]。为探索密码子使用偏好与进化状态的关系, 本研究进一步利用Cluster3.0软件对各物种的RSCU进行了分层聚类分析[27]。
1.4 中性演化检验中性图(Neutrality plot)是一种被广泛用于检验中性演化对密码子使用偏好影响的方法。该方法通过分析基因第一和第二密码子位置的总GC含量(GC12)与GC3之间的相关性, 评估突变压力、选择压力以及遗传漂变等因素对同义密码子使用偏好的影响。当突变是导致密码子使用偏好的主要因素时, 密码子内的3个位置受到同等突变压力, 导致GC12与GC3之间的回归系数趋近1;若回归系数显著偏离1, 则表明自然选择、遗传漂变和基因表达水平等其他因素在塑造特定同义密码子的偏好中起更突出的作用[28-29]。本研究使用CodonW(v1.4.7)软件和编写的Perl脚本计算了基因和基因组水平的GC12和GC3, 并进一步在软体动物四个主要类群中评估了其与ENC之间的关系。
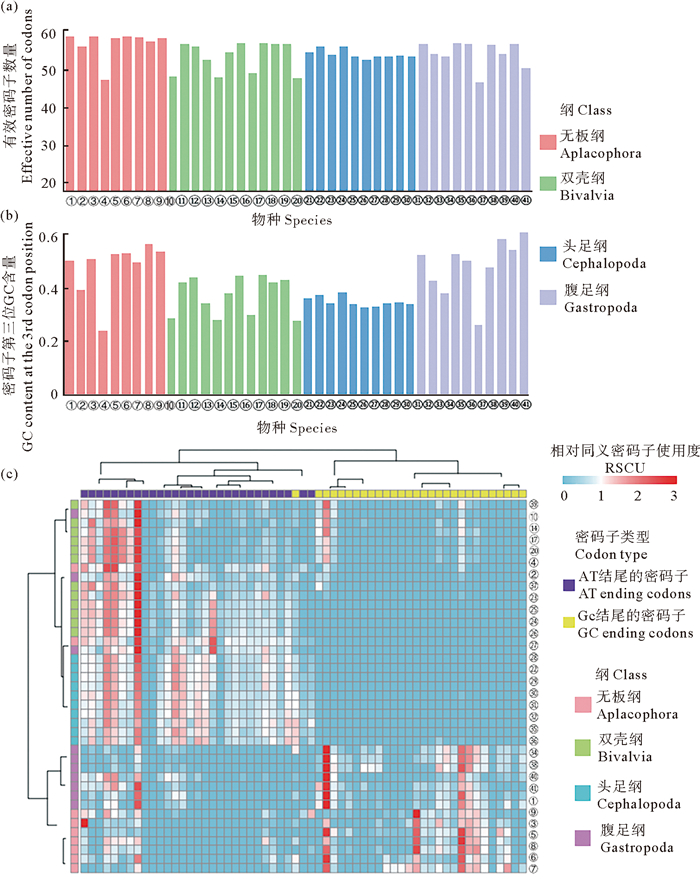
2 结果 2.1 软体动物密码子使用偏好类型本研究所涉及的41种软体动物的密码子偏好水平普遍较弱, 其中腹足纲帽贝(L. gigantea)的偏好性最强, 其有效密码子数为46.83, 而无板纲动物A. crassa的偏好性最弱, 其有效密码子数高达59.16(见图 1(a))。在四个主要类群中, 无板纲的密码子偏好水平最低, 然后依次是头足类、双壳类和腹足类, 但各门类间的差异并不显著(单因素方差分析, P > 0.05)。碱基构成分析表明, 软体动物的GC3差异较大, 其中脉红螺(R. venosa)的GC3超过0.617, 而帽贝(L. gigantea)的GC3仅为0.264(见图 1(b))。无板纲和腹足纲的GC3显著高于头足纲和双壳纲(单因素方差分析, P < 0.05)。
|
(①: Alexandromenia crassa; ②: Chaetoderma nitidulum; ③: Entonomenia tricarinata; ④: Falcidens caudatus; ⑤: Helluoherpia aegiri; ⑥: Kruppomenia borealis; ⑦: Macellomenia schanderi; ⑧: Neomenia megatrapezata; ⑨: Proneomenia sluiteri; ⑩: Bathymodiolus platifrons; ⑪: Chlamys farreri; ⑫: Crassostrea gigas; ⑬: Mulinia lateralis; ⑭: Modiolus philippinarum; ⑮: Pinctada fucata; ⑯: Patinopecten yessonesis; ⑰: Scapharca broughtonii; ⑱: Sinonovacula constricta; ⑲: Argopecten irradians; ⑳: Argopecten purpuratus; ㉑: Tegillarca granosa; ㉒: Dosidicus gigias; ㉓: Euprymna scolopes; ㉔ Hapalochlaena maculosa; ㉕: Idiosepius notoides; ㉖: Octopus maya; ㉗: Octopus bimaculoides; ㉘: Octopus minor; ㉙: Sepia esculenta; ㉚: Sepia pharaonis; ㉛ Sepioloidea lineolata; ㉜ Aplysia californica; ㉝ Achatina fulica; ㉞ Biomphalaria glabrata; ㉟: Elysia chlorotica; ㊱: Haliotis discus; ㊲: Lottia gigantea; ㊳: Pomacea cananiculata; ㊴: Littorina saxatilis; ㊵: Potamopyrgus antipodarum; ㊶: Rapana venosa.) 图 1 软体动物41个物种按四个纲排列的ENC(a)、GC3(b)以及基于密码子RSCU的欧几里得距离聚类(c) Fig. 1 ENC(a), GC3(b), and Euclidean distance similarity of RSCU(c)of 41 molluscan species |
密码子相对使用频率分析表明, 除编码亮氨酸的密码子TGG外, 软体动物密码子使用明显分为GC结尾密码子偏好型和AT结尾密码子偏好型。同时, 物种的密码子使用频率也呈现出按分类阶元聚集的分层现象, 其中: 双壳纲和头足纲动物偏向于使用以AT结尾的密码子; 无板纲和腹足纲动物则对以GC结尾的密码子呈现更高的使用频率(见图 1(c))。这种现象可能与无板纲和腹足纲的基因组GC含量普遍较高有关。值得注意的是, 腹足纲的陆生褐云玛瑙螺(A. fulica)、两栖光滑双脐螺(B. glabrata)和生活在潮间带的帽贝(L. gigantea)同双壳动物类似, 偏向于使用以AT结尾的密码子, 三者的生态分布均包含陆生环境, 而本研究所涉及的其余腹足动物则完全营水生生活。无板纲闪耀毛皮贝(C. nitidulum)和F. caudatus也偏向于使用以AT结尾的密码子, 这两种尾腔动物(Caudofoveata)在海底沉积层中营固着滤食生活, 而本研究所分析的其余无板纲物种则属于运动能力更强的沟腹动物(Solenogastres), 主要分布于海底沉积物或藻类覆盖的岩石以及珊瑚礁中的细小缝隙等生境, 营捕食生活。研究结果暗示, 生境与习性的多样性会导致密码子使用偏好的差异。此外, 腹足纲和无板纲中有5个物种的GC3均明显低于其所属类群(见图 1(b)), 这表明密码子使用偏好类型主要受到GC含量而非其分类地位的影响。这一点与基因组碱基比例的差异趋势一致, 双壳纲和头足纲动物的GC含量较为均一, 密码子使用偏好类型也更相似; 而腹足纲和无板纲动物基因组中GC含量差异较大, 密码子使用偏好类型也更加多变。
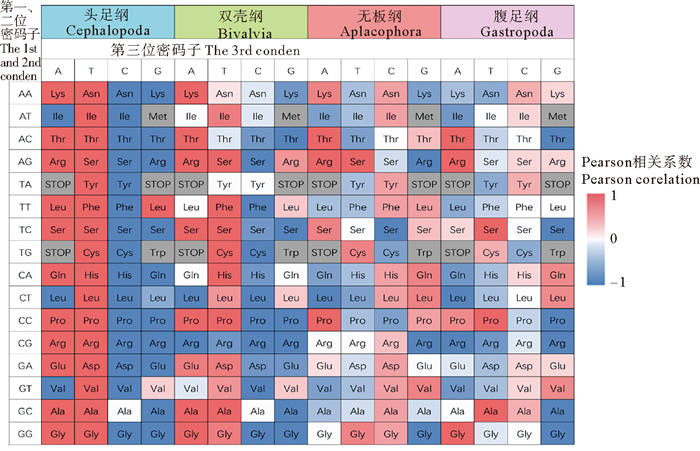
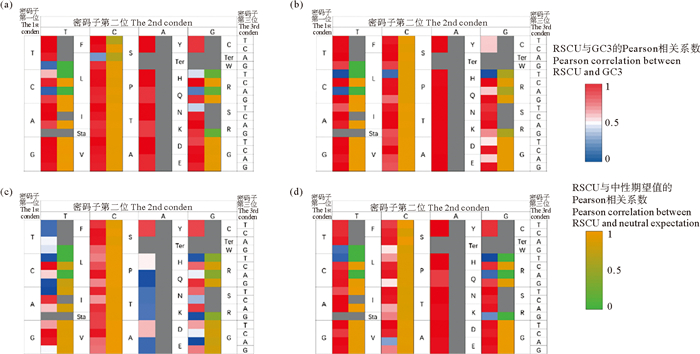
2.2 软体动物密码子使用偏好性差异基于每个密码子的RSCU所进行的聚类分析表明, 软体动物在密码子使用上存在明显的偏好类型, 本研究进一步计算了软体动物四个纲内各个密码子的RSCU与ENC负值的Pearson相关系数(见图 2)。其中, 多数密码子的RSCU与密码子偏好程度线性相关, 只有头足纲的密码子ATT(I)、ATG(M)、GCG(A)、GGA(G), 双壳纲的ATA(I)、GTT(V), 无板纲的AAG(K)、GTA(V)以及腹足纲的TTT(F)、GTA(V)的使用频率与密码子偏好程度相关性较弱。在头足纲、双壳纲和无板纲中, 多数以AT结尾的密码子的RSCU与ENC负值正相关、而GC结尾的密码子则呈现负相关; 在腹足纲的情况则完全相反, 明显呈现出对GC结尾密码子的偏好性。为进一步探究影响软体动物特定密码子使用偏好类型的主要因素, 本研究检验了密码子的RSCU与GC3s之间的相关性, 以及AT结尾或GC结尾密码子的RSCU总和与中性期望之间的相关性, 并评估了各个密码子的使用偏好是否符合Palidwor等[30]的中性演化模型。如图 3所示, 在四个纲中, 大多数简并密码子AT结尾或GC结尾密码子的RSCU总和与中性期望的相关性较强, 表明其大致符合中性演化过程。值得注意的是, 编码精氨酸的CGA、CGT与AGG在腹足纲中的使用偏好类型明显偏离了中性演化, 其影响因素还需进一步探究。
|
图 2 软体动物无板纲、双壳纲、头足纲和腹足纲中RSCU与ENC负值间的Pearson相关系数 Fig. 2 Pearson correlation coefficient of the RSCU and negative ENC value in, in mollusks Aplacophora(a), Bivalvia(b), Cephalopoda(c) and Gastropoda(d) |
|
(图中左侧、上侧与右侧分别代表密码子的第一、第二与第三位基因型。每一个密码子有三列值: 第一列为每个密码子RSCU和GC3之间的Pearson相关系数, 第二列为一个氨基酸中所有以AT结尾或GC结尾密码子的RSCU与中性期望值的比较, 第三列为密码子的名称。Genotype of the 1st, 2nd, and 3rd codon positions are displayed on the left, top, and right sides of the figure, each codon has three columns of values: The first column shows the Pearson correlation coefficient between the RSCU and GC3 values, the second column the compares the summed RSCU values for all AT-ending or GC-ending codons within an amino acid to the neutral expectations and the third column displays the codon name. The first and second columns with colors closer to red indicate a greater influence of neutral mutations.) 图 3 软体动物无板纲(a)、双壳纲(b)、头足纲(c)和腹足纲(d)密码子使用偏好类型的中性演化检验 Fig. 3 Neutral expectation test for codon usage preference type in mollusks Aplacophora(a), Bivalvia(b), Cephalopoda(c) and Gastropoda(d) |
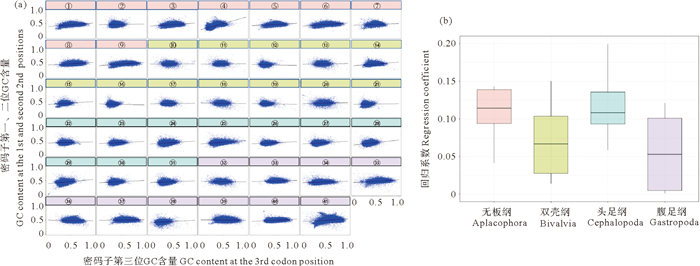
偏向性突变理论认为突变并非随机, 其倾向于增加或减少基因组中的GC含量, 这种突变压力更多集中于基因组的中性区域。由于密码子的简并性, 其GC含量在一定程度上反映了中性区域受到的突变压力, 因此若密码子GC12与GC3间的相关性很高, 则代表突变压力在三个位点间并无显著差异, 密码子使用偏好主要受中性突变、遗传漂变和tRNA丰度的中性进化等因素影响, 反之则代表第三位密码子受到选择压力、翻译选择和表观遗传修饰等其他因素的影响。为深入探讨在物种密码子使用偏好类型的演化驱动机制, 本研究以物种内单个基因的编码序列为单位, 检验了GC12与GC3的相关性。分析结果显示, 在四个类群中, 大部分物种GC12与GC3的回归系数均低于0.2(见图 4(a)), 这表明软体动物的密码子使用偏好类型受中性演化、自然选择和表观遗传修饰等多重因素共同影响。腹足纲的物种中, GC12与GC13的回归系数明显低于其他三个纲的动物(见图 4(b)), 其中褐云玛瑙螺(A. fulica)和皱纹盘鲍(H. discus)受到的突变压力明显低于其他物种。
|
((a)软体动物41个物种的中性图, 其中黑色线条代表回归线。(b)根据所属类群分组后的回归系数分布。(a) Neutrality plots of 41 molluscan species. Lines in black represent the regression lines. (b) Distribution of regression coefficients of species grouped by classes. ①: Alexandromenia crassa; ②: Chaetoderma nitidulum; ③: Entonomenia tricarinata; ④: Falcidens caudatus; ⑤: Helluoherpia aegiri; ⑥: Kruppomenia borealis; ⑦: Macellomenia schanderi; ⑧: Neomenia megatrapezata; ⑨: Proneomenia sluiteri; ⑩: Argopecten irradians; ⑪: Argopecten purpuratus; ⑫: Bathymodiolus platifrons; ⑬: Chlamys farreri; ⑭: Crassostrea gigas; ⑮: Mulinia lateralis; ⑯: Modiolus philippinarum; ⑰: Pinctada fucata; ⑱: Patinopecten yessonesis; ⑲: Scapharca broughtonii; ⑳: Sinonovacula constricta; ㉑: Tegillarca granosa; ㉒: Dosidicus gigias; ㉓: Euprymna scolopes; ㉔: Hapalochlaena maculosa; ㉕: Idiosepius notoides; ㉖: Octopus bimaculoides; ㉗: Octopus maya; ㉘: Octopus minor; ㉙: Sepia esculenta; ㉚: Sepia pharaonis; ㉛: Sepioloidea lineolata; ㉜: Achatina fulica; ㉝: Aplysia californica; ㉞: Biomphalaria glabrata; ㉟: Elysia chlorotica; ㊱: Haliotis discus; ㊲: Littorina saxatilis; ㊳: Lottia gigantea; ㊴: Potamopyrgus antipodarum; ㊵: Pomacea canaliculata; ㊶: Rapana venosa.) 图 4 软体动物41个物种的中性图分析 Fig. 4 Neutrality plots of 41 molluscan species |
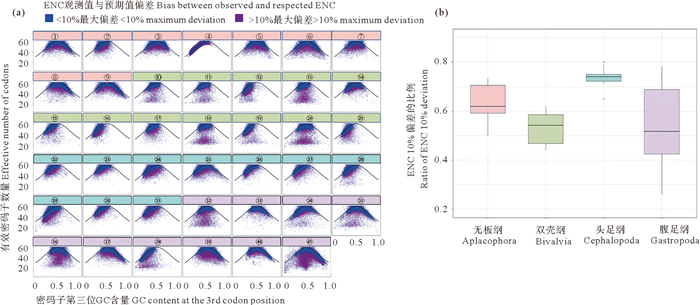
在缺乏选择压力的中性演化过程中, ENC的期望值可以由GC3近似计算, 因此ENC的观测值与期望值的差异程度能够反映偏向性突变压力[28]。本研究根据物种内每个基因编码序列的GC3, 计算了其ENC期望值, 并进一步探索了软体动物驱动密码子使用偏好类型演化的因素(见图 5(a))。在双壳纲、无板纲、头足纲和腹足纲中, ENC真实值与GC3的相关系数分别为0.987、0.925、0.986以及0.532(见图 5(a)), ENC观测值与期望值的偏差为-10%~10%的基因占比分别为0.740、0.638、0.560以及0.516(见图 5(b))。本研究结果与基于密码子GC含量相关性的中性检验分析结果一致, 这表明偏向性突变对腹足动物密码子使用偏好类型的影响较其他三个类群更小, 即驱动其密码子使用偏好类型的因素与其他三个类群存在显著差异。腹足动物中褐云玛瑙螺、皱纹盘鲍、帽贝(L. gigantea)以及脉红螺(R. venosa)中大量基因的ENC观测值明显偏离其期望值, 这暗示这些基因可能受到较强的选择压力作用。
|
((a)软体动物41个物种的ENC分布图, 其中ENC预期值和ENC观测值分别以黑色曲线和散点表示, 其中蓝色散点表示ENC观测值与预测值之差小于最大值的10%, 其余则为红色散点(a) ENC plots of 41 molluscan species. ENC expected values are displayed as black curve. ENC observations are represented by scatter points, in which points in blue indicating the difference between expected and observed ENC less than 10% of the maximum, with the remaining marked in red; 根据所属类群分组后, ENC观测值与预期值偏差小于最大值的10%的基因占比分布(b) The distribution of the proportion of genes with ENC observation values deviating from expected values by less than 10% of the maximum, grouped by their respective classes. ①: Alexandromenia crassa; ②: Chaetoderma nitidulum; ③: Entonomenia tricarinata; ④: Falcidens caudatus; ⑤: Helluoherpia aegiri; ⑥: Kruppomenia borealis; ⑦: Macellomenia schanderi; ⑧: Neomenia megatrapezata; ⑨: Proneomenia sluiteri; ⑩: Argopecten irradians; ⑪: Argopecten purpuratus; ⑫: Bathymodiolus platifrons; ⑬: Chlamys farreri; ⑭: Crassostrea gigas; ⑮: Mulinia lateralis; ⑯: Modiolus philippinarum; ⑰: Pinctada fucata; ⑱: Patinopecten yessonesis; ⑲: Scapharca broughtonii; ⑳: Sinonovacula constricta; ㉑: Tegillarca granosa; ㉒: Dosidicus gigias; ㉓: Euprymna scolopes; ㉔: Hapalochlaena maculosa; ㉕: Idiosepius notoides; ㉖: Octopus bimaculoides; ㉗: Octopus maya; ㉘: Octopus minor; ㉙: Sepia esculenta; ㉚: Sepia pharaonis; ㉛: Sepioloidea lineolata; ㉜: Achatina fulica; ㉝: Aplysia californica; ㉞: Biomphalaria glabrata; ㉟: Elysia chlorotica; ㊱: Haliotis discus; ㊲: Littorina saxatilis; ㊳: Lottia gigantea; ㊴: Potamopyrgus antipodarum; ㊵: Pomacea canaliculata; ㊶: Rapana venosa.) 图 5 软体动物41个物种的ENC分布图 Fig. 5 ENC plots of 41 molluscan species |
软体动物是动物界中第二大门类, 是化石记录中最早出现的两侧对称动物之一, 其出现标志着大约5.4亿年前的寒武纪出现动物大爆发[31]。凭借着形态结构、行为模式和生存策略的高度多样性, 软体动物在多次大规模灭绝事件中幸存下来, 成为最古老且进化上最成功的无脊椎动物类群之一, 广泛分布于海洋、淡水和陆地生态系统。尽管软体动物在生物学、进化学和生态学方面具有重要地位, 但长期以来, 因缺乏数据, 针对其密码子使用偏好类型的研究相对较少。高通量测序技术的快速发展推进了长牡蛎(C. gigas)、合浦珠母贝(P. fucata)和虾夷扇贝(P. yessonesis)等多个软体动物精细基因组图谱的绘制, 为深入解析其分子演化特征提供了重要的数据资源。在此, 本研究系统收集了近年来发表的软体动物基因组序列数据, 探究了头足纲、腹足纲、双壳纲和无板纲四大类群的密码子使用偏好特征。结果显示, 软体动物中每个物种平均超过50个密码子被频繁利用, 大多数密码子的相对使用频率接近1。相比之下, 果蝇和线虫中仅有45~48个密码子被频繁使用, 这表明大多数软体动物的密码子使用偏好性较弱[32-34]。
Gerdol等[15]发现, 双壳动物中以AT结尾的密码子普遍比以GC结尾的密码子使用频率更高, 从而推测这是软体动物的普遍特征。而本研究通过纳入更多物种, 首次发现软体动物的密码子使用偏好类型呈现出按分类阶元聚集的分层现象, 其中: 双壳纲和头足纲动物的密码子使用偏好类型相近, 偏向于使用以AT结尾的密码子; 而腹足纲和无板纲动物则更偏向于使用以GC结尾的密码子。这可能与物种特异性的基因组GC含量偏倚有关[35]。
本研究还发现, 腹足纲动物呈现出多样化的密码子使用偏好类型, 其中褐云玛瑙螺(A. fulica)、帽贝(L gigantea)和福寿螺(P. cananiculata)三种营陆生或两栖的动物同其余水生的腹足类动物不同, 呈现出同双壳纲和头足纲动物类似的AT结尾密码子偏好性, 这暗示其可能受生活环境和自然选择的影响。然而, 在原核生物和部分真核生物的研究中, 普遍认为偏向性突变是决定密码子使用偏好类型的核心因素[36-38]。本研究通过中性检验证实, 偏向性突变和选择压力的影响作用在软体动物的不同类群中存在差异。腹足纲动物较双壳纲、头足纲和无板纲受到的选择压力更大。其中, 在褐云玛瑙螺(A. fulica)、帽贝(L gigantea)和皱纹盘鲍(H.discus)等腹足动物中, 大量基因编码序列的有效密码子数量明显偏离其期望值, 这暗示其可能受到较强的选择压力。在密码子层面的检验进一步表明, 腹足纲动物中精氨酸密码子CGT、CGA和AGG显著偏离了Palidwor的中性演化模型, 这暗示此类型密码子受到的选择压力更大。在研究酵母和节肢动物中发现, 同义突变相比非同义突变更有利于生物的适应性, 因此在变化的栖息环境中, 密码子偏好性通常会表现出显著的非中性特征[39-40]。这在很大程度上解释了随着生境的多样化, 为何中性演化对密码子使用偏好的影响逐渐减弱。然而, 由于目前软体动物的数据资源的局限性, 本研究在收集各栖息地的物种数据时存在一定的偏差, 无法完全排除抽样误差造成的影响。随着未来测序数据的不断积累, 我们期待能通过更系统的分析来克服这些局限性。
4 结语本研究系统分析了41种软体动物的基因编码序列, 旨在探究头足纲、腹足纲、双壳纲和无板纲这四个主要类群的密码子使用偏好特征和演化动力。研究结果显示: 大部分软体动物的密码子偏好性较弱, 且呈现出按分类阶元和基因组GC含量分层的密码子使用偏好, 其中双壳纲和头足纲动物偏向于使用以AT结尾的密码子, 而腹足纲和无板纲动物偏向于以GC结尾的密码子; 软体动物的密码子使用偏好类型主要受中性演化和自然选择共同影响, 但是这种影响在这四个类群间存在差异, 其中腹足动物较双壳纲、头足纲和无板纲受到的选择压力更大, 且选择压力集中于编码精氨酸的三种密码子的使用偏好上。本研究系统绘制了软体动物的密码子使用偏好图谱, 为深入理解其遗传多样性和基因组演化提供了重要见解。
| [1] |
Liu Y. A code within the genetic code: Codon usage regulates co-translational protein folding[J]. Cell Communication and Signaling, 2020, 18(1): 145. DOI:10.1186/s12964-020-00642-6 (  0) 0) |
| [2] |
Hanson G, Coller J. Codon optimality, bias and usage in translation and mRNA decay[J]. Nature reviews Molecular cell biology, 2018, 19(1): 20-30. DOI:10.1038/nrm.2017.91 (  0) 0) |
| [3] |
Doherty A, Mcinerney J O. Translational selection frequently overcomes genetic drift in shaping synonymous codon usage patterns in vertebrates[J]. Molecular Biology and Evolution, 2013, 30(10): 2263-2267. DOI:10.1093/molbev/mst128 (  0) 0) |
| [4] |
Song H, Liu J, Song Q, et al. Comprehensive analysis of codon usage bias in seven Epichloё species and their peramine-coding genes[J]. Front Microbiol, 2017, 8: 1419. DOI:10.3389/fmicb.2017.01419 (  0) 0) |
| [5] |
Ikemura T. Correlation between the abundance of Escherichia coli transfer RNAs and the occurrence of the respective codons in its protein genes[J]. Journal of Molecular Biology, 1981, 146(1): 1-21. DOI:10.1016/0022-2836(81)90363-6 (  0) 0) |
| [6] |
Sharp P M, Tuohy T M, Mosurski K R. Codon usage in yeast: Cluster analysis clearly differentiates highly and lowly expressed genes[J]. Nucleic Acids Research, 1986, 14: 5125-5143. DOI:10.1093/nar/14.13.5125 (  0) 0) |
| [7] |
Akashi H. Synonymous codon usage in Drosophila melanogaster: Natural selection and translational accuracy[J]. Genetics, 1994, 136(3): 927-935. DOI:10.1093/genetics/136.3.927 (  0) 0) |
| [8] |
Ikemura T. Codon usage and tRNA content in unicellular and multicellular organisms[J]. Molecular Biology and Evolution, 1985, 2(1): 13-34. (  0) 0) |
| [9] |
Galtier N, Duret L. Adaptation or biased gene conversion? Extending the null hypothesis of molecular evolution[J]. Trends in Genetics, 2007, 23(6): 273-277. DOI:10.1016/j.tig.2007.03.011 (  0) 0) |
| [10] |
Mancera E, Bourgon R, Brozzi A, et al. High-resolution mapping of meiotic crossovers and non-crossovers in yeast[J]. Nature, 2008, 454(7203): 479-485. DOI:10.1038/nature07135 (  0) 0) |
| [11] |
Hershberg R, Petrov D A. Selection on codon bias[J]. Annual Review of Genetics, 2008, 42: 287-299. DOI:10.1146/annurev.genet.42.110807.091442 (  0) 0) |
| [12] |
Chen S L, Hao H F, Zhao P, et al. Genome-wide analysis of the first sequenced Mycoplasma capricolum subsp. capripneumoniae strain M1601[J]. G3 Genes Genomes Genetics, 2017, 7(9): 2899-2906. DOI:10.1534/g3.117.300085 (  0) 0) |
| [13] |
Cope A L, Gilchrist M A. Quantifying shifts in natural selection on codon usage between protein regions: A population genetics approach[J]. BMC Genomics, 2022, 23(1): 408. DOI:10.1186/s12864-022-08635-0 (  0) 0) |
| [14] |
Taylor P D, Lewis D N. Fossil Invertebrates[M]. Cambridge: Harvard University Press, 2005.
(  0) 0) |
| [15] |
Gerdol M, De Moro G, Venier P, et al. Analysis of synonymous codon usage patterns in sixty-four different bivalve species[J]. PeerJ, 2015, 3: e1520. DOI:10.7717/peerj.1520 (  0) 0) |
| [16] |
Takeshi T, Takeshi K, Ryo K, et al. Draft genome of the pearl oyster Pinctada fucata: A platform for understanding bivalve biology[J]. DNA Research, 2012, 19(2): 117-130. DOI:10.1093/dnares/dss005 (  0) 0) |
| [17] |
Zhang G, Fang X, Guo X, et al. The oyster genome reveals stress adaptation and complexity of shell formation[J]. Nature, 2012, 490(7418): 49-54. DOI:10.1038/nature11413 (  0) 0) |
| [18] |
Wang S, Zhang J, Jiao W, et al. Scallop genome provides insights into evolution of bilaterian karyotype and development[J]. Nature Ecology & Evolution, 2017, 1(5): 120. (  0) 0) |
| [19] |
Ran Z, Li Z, Yan X, et al. Chromosome level genome assembly of the razor clam Sinonovacula constricta[J]. Molecular Ecology Resources, 2019, 19(6): 1647-1658. DOI:10.1111/1755-0998.13086 (  0) 0) |
| [20] |
Xin L S, Umberto R, Wu B, et al. Chromosomallevel assembly of the blood clam, Scapharca (Anadara) broughtonii, using long sequence reads and HiC[J]. Giga Science, 2019, 8(7): giz067. DOI:10.1093/gigascience/giz067 (  0) 0) |
| [21] |
Guo Y, Zhang Y, Liu Q, et al. A chromosomal level genome assembly for the giant African snail Achatina fulica[J]. Giga Science, 2019, 8(10): giz124. DOI:10.1093/gigascience/giz124 (  0) 0) |
| [22] |
Rumpho M E, Worful J M, Lee J, et al. Horizontal gene transfer of the algal nuclear gene psbO to the photosynthetic sea slug Elysia chlorotica[J]. Proceedings of the National Academy of Sciences of the United States of America, 105(46): 17867-17871. (  0) 0) |
| [23] |
Nam B H, Kwak W, Kim Y O, et al. Genome sequence of pacific abalone (Haliotis discus hannai): The first draft genome in family Haliotidae[J]. Giga Science, 2017, 6(5): 1-8. (  0) 0) |
| [24] |
Albertin C B, Simakov O, Mitros T, et al. The octopus genome and the evolution of cephalopod neural and morphological novelties[J]. Nature, 2015, 524(7564): 220-224. DOI:10.1038/nature14668 (  0) 0) |
| [25] |
Moroz L L, Edwards J R, Puthanveettil S V, et al. Neuronal transcriptome of Aplysia: Neuronal compartments and circuitry[J]. Cell, 2006, 127(7): 1453-1467. DOI:10.1016/j.cell.2006.09.052 (  0) 0) |
| [26] |
Simakov O, Marletaz F, Cho S J, et al. Insights into bilaterian evolution from three Spiralian genomes[J]. Nature, 2013, 493(7433): 526-531. DOI:10.1038/nature11696 (  0) 0) |
| [27] |
Liu C, Zhang Y, Ren Y, et al. The genome of the golden apple snail Pomacea canaliculata provides insight into stress tolerance and invasive adaptation[J]. Giga Science, 2018, 7(9): giy101. DOI:10.1093/gigascience/giy101 (  0) 0) |
| [28] |
Wright F. The "effective number of codons" used in a gene[J]. Gene, 1990, 87: 23-29. DOI:10.1016/0378-1119(90)90491-9 (  0) 0) |
| [29] |
Wu Y, Li Z, Zhao D, et al. Comparative analysis of flower-meristem-identity gene APETALA2 (AP2) codon in different plant species[J]. Journal of Integrative Agriculture, 2018, 17: 867-877. DOI:10.1016/S2095-3119(17)61732-5 (  0) 0) |
| [30] |
Palidwor G A, Perkins T J, Xia X. A general model of codon bias due to GC mutational bias[J]. PLoS One, 2010, 5: e13431. DOI:10.1371/journal.pone.0013431 (  0) 0) |
| [31] |
Rosenberg G. A new critical estimate of named species-level diversity of the recent mollusca[J]. American Malacological Bulletin, 2014, 32(2): 308-322. DOI:10.4003/006.032.0204 (  0) 0) |
| [32] |
Powell J R, Moriyama E N. Evolution of codon usage bias in Drosophila[J]. Proceedings of the National Academy of Sciences of the United States of America, 1997, 94: 7784-7790. (  0) 0) |
| [33] |
Mitreva M, Wendl M C, Martin J, et al. Codon usage patterns in Nematoda: Analysis based on over 25 million codons in thirty-two species[J]. Genome Biology, 2006, 7: R75. DOI:10.1186/gb-2006-7-8-r75 (  0) 0) |
| [34] |
Vicario S, Moriyama E N, Powell J R. Codon usage in twelve species of Drosophila[J]. BMC Evolutionary Biology, 2007, 7: 226. DOI:10.1186/1471-2148-7-226 (  0) 0) |
| [35] |
Yang M, Liu J, Yang W, et al. Analysis of codon usage patterns in 48 Aconitum species[J]. BMC Genomics, 2023, 24: 703. DOI:10.1186/s12864-023-09650-5 (  0) 0) |
| [36] |
Bulmer M. The selection-mutation-drift theory of synonymous codon usage[J]. Genetics, 1991, 129(3): 897-907. DOI:10.1093/genetics/129.3.897 (  0) 0) |
| [37] |
Michael C A, Shafquat B, Guorong C, et al. Codon usage bias analysis within and across genomes[J]. Nucleic Acids Research, 2007, 35(2): 132-136. (  0) 0) |
| [38] |
Rao A, Chen Z, Wu D, et al. Codon usage bias in the chloroplast genomes of Cymbidium species in Guizhou, China[J]. South African Journal of Botany, 2024, 164: 429-437. DOI:10.1016/j.sajb.2023.12.009 (  0) 0) |
| [39] |
Shen X, Song S, Li C, et al. Synonymous mutations in representative yeast genes are mostly strongly non-neutral[J]. Nature, 2022, 606(7915): 725-731. DOI:10.1038/s41586-022-04823-w (  0) 0) |
| [40] |
Bailey S F, Alonso Morales L A, Kassen R. Effects of synonymous mutations beyond codon bias: The evidence for adaptive synonymous substitutions from microbial evolution experiments[J]. Genome Biology and Evolution, 2021, 13(9): evab141. DOI:10.1093/gbe/evab141 (  0) 0) |
2. Key Laboratory of Marine Genetics and Breeding, Ministry of Education, Ocean University of China, Qingdao 266003, China
 2025, Vol. 55
2025, Vol. 55


