随着工业化的发展,有毒有害物质海上运输量不断增加,因装卸作业以及海上碰撞、搁浅而造成的海上危险化学品泄漏的风险也不断增加,由此造成事故海域严重污染进而威胁到海洋生态安全。根据国际海事组织制定的《国际散装运输危险化学品船舶构造和设备规则》(International Code for the Construction and Equipment of Ships Carrying Dangerous Chemicals in Bulk,简称IBC规则)[1],烷基(C3和C4)苯属于Y类污染物,排海后会对海洋资源和人体健康有不利影响,也会对海上设施等产生危害。烷基(C3)苯,即碳九芳烃或C9芳烃,是含有9个碳原子的芳烃化合物,主要来源于石油重整与裂解生产乙烯的副产品,正丙苯(n-propylbenzene,n-PBZ)、异丙苯(isopropylbenzene,i-PBZ)是其中的2种主要组分,二者在C9芳烃中的质量占比分别为12.3%和4.2%[2]。当发生C9芳烃泄漏入海事故时,短时间内大量C9芳烃会排入周围海域。例如,2018年11月福建泉港区C9芳烃泄漏入海事故期间,约有69.1 t C9芳烃入海[3]。相应的,海水中的n-PBZ和i-PBZ浓度激增,很可能会达到或接近于其溶解度(25 ℃时分别为52.2和50.0 mg/L)[4]。本研究团队之前采用微宇宙装置模拟海洋自然环境条件开展衰减实验发现,当海水中n-PBZ和i-PBZ的初始浓度分别为27.06和26.35 mg/L时,在风速5 m/s条件下,较强的挥发作用可使二者在2 d内快速降到3 mg/L左右,但是随后衰减缓慢,分别需要20和15 d才能降至低生态风险水平;而海上风速较低(1 m/s)时,2种丙苯的衰减速度明显减慢(约为5 m/s时的一半),由此造成的中、高生态风险将持续20 d以上[5]。这表明泄漏入海的丙苯(如无特别说明,下文的丙苯特指n-PBZ和i-PBZ)将在较长时间内对海洋生物造成危害,因此必须采取人为措施加快丙苯的去除。基于微藻的环境生物修复技术具有低成本(太阳能驱动)、生态友好性(无需使用有毒有害化学物质)、能代谢有机污染物作为碳源、藻生物质可作为海洋食物链的基础(有利于生态恢复)等优点[6-8]。近年来利用微藻去除环境中有机污染物的研究日益增多[9-10]。但是,微藻的光合作用、营养物质利用以及对外源污染物代谢活动受到温度、盐度、光强等[11-14]环境因素影响,由此造成微藻在不同环境条件下对污染物的去除效果存在很大差异。然而现有研究大多采用单因子试验探究环境因素对微藻去除污染物的影响[11-14],但有毒有害物质的海上泄漏事故可能发生在不同海域和不同季节,在实际修复过程中,多种因素共同作用下的去除效果不得而知。如果当时当地的海洋环境条件不适于微藻去除目标污染物,那么采用微藻进行生物修复将不会获得良好效果。因此,实施生物修复时应考虑到环境因子对微藻去除性能的综合影响。
响应面法(Response surface methodology, RSM)是科学研究中常用的一种过程优化方法,通常用于分析多个响应变量之间的关系,能够通过模型拟合准确表达出各因子与响应指标之间的数学关系,直观预测出各实验因子的最优值[15]。例如,Dayana等[16]利用RSM法优化蛋白核小球藻(Chlorella pyrenoidosa)去除苯酚的条件,最优去除率为97%;Chen等[17]通过RSM法探究底物浓度、接种量和温度对假单胞菌(Pseudomonas sp.)降解石油污染土壤中含硫多环芳烃的影响,确定底物浓度是最重要的影响因素;Cai等[15]优化去除石油烃的环境变量,去除率提升至79.94%。
网状鼻胞藻S6A(Rhinomonas reticulata S6A)是本研究团队从大亚湾海水中筛选分离得到的一种隐藻门微藻,当其在海水中的接种密度为1 × 104 cells/mL时,7 d内可将初始浓度5 mg/L的n-PBZ和i-PBZ分别去除34.6%和38.8%[18]。随后进行的单因子试验还表明[19],盐度、温度和光强是影响其去除2种丙苯的关键因子。本研究拟在此基础上进行Box-Behnken设计(BBD),并结合RSM法,优化得到该微藻去除n-PBZ和i-PBZ的最佳环境条件,且构建多元二次回归模型,为确定微藻应用于丙苯泄漏海域生物修复的适宜时机提供依据。
1 材料与方法 1.1 材料天然海水:采自青岛沙子口近岸海域(盐度为30.0,pH=8.3),通过0.45 μm水系微孔滤膜过滤以去除杂质。
网状鼻胞藻S6A:为本研究团队前期分离得到[18]。将其接种于灭菌的F/2培养基中(配方见表 1),在温度25 ℃、光强60 μmol/(m2·s)、光暗周期14 h/10 h条件下培养至指数生长期,用于正式实验。由于后续实验期间培养体系完全密封(避免丙苯挥发对去除效果的影响),向培养基中加入250 mg/L的NaHCO3以提供微藻正常生长所需碳源。
n-PBZ、i-PBZ:均为色谱纯(纯度>99.0%),购自梯希爱化工有限公司;二氯甲烷(CH2Cl2,纯度>99.0%),色谱纯,购自科密欧化学试剂有限公司;1-氯萘(纯度=96%),色谱纯,购自上海麦克林生化科技有限公司;二甲基亚砜(DMSO,液相色谱纯)购自天津市科密欧化学试剂有限公司;海水素购自山东贝森饲料有限公司;其他药品均为分析纯,购自国药集团化学试剂有限公司。n-PBZ和i-PBZ在使用前分别采用DMSO溶解定容为浓度25 g/L的储备液。
1.2 方法 1.2.1 Box-Behnken实验设计前期单因子试验[19]表明,海水的盐度、温度和光强对微藻去除n-PBZ、i-PBZ的影响较大。因此,对于每种丙苯,以单因子试验中这三个因子各自的最佳水平为中心点,每个因子再取低(-1)和高(+1)两个水平(见表 2)。然后,按3因子3水平进行BBD实验设计,需进行17组实验,每组实验重复3次,具体实验安排见表 3和表 4。
|
|
表 2 Box-Behnken设计中的因子及水平 Table 2 Factors and levels in Box-Behnken design |
|
|
表 3 基于BBD的微藻去除n-PBZ实验设计以及相应的响应值 Table 3 Experimental design for n-PBZ removal by the microalga based on BBD and the corresponding response values |
|
|
表 4 基于BBD的微藻降解i-PBZ实验设计以及相应的响应值 Table 4 Experimental design for i-PBZ degradation by the microalga based on BBD and the corresponding response values |
将指数生长期微藻用灭菌的F/2培养基稀释至藻细胞密度为1×104 cells/mL,分装于一系列50 mL血清瓶(带四氟乙烯涂层的丁基橡胶衬垫和中空的铝盖)中,盖塞后,用微量注射器分别注入2 μL的n-PBZ或i-PBZ储备液,使其初始浓度为5 mg/L,混匀后置于光照培养箱(PGX-250D-LED,江苏天翎仪器有限公司)中,分别在17组实验的设计条件下(见表 3和表 4)连续培养7 d。其中,盐度调节时,首先采用灭菌蒸馏水稀释海水,或将适量海水素直接加入海水中,以得到所需盐度的溶液,然后用该溶液分别配制F/2培养基,最后用0.1 mol/L NaOH或0.1 mol/L HCl溶液调节pH为8.3。培养箱光强使用光量子计(3415F,美国Spectrum公司)进行测定,通过调节培养箱自身的光照度以及光源与样品瓶之间的距离来获得所需光强。对于光强为0的实验,需要将血清瓶用锡箔纸包被后再放入培养箱中。各组实验均以培养结束时n-PBZ或i-PBZ的去除率为响应值。
1.2.3 丙苯浓度测定参照Jin等[21]的方法进行萃取,按体积比2∶1(v/v)向样品中注入二氯甲烷(含5 mg/L 1-氯萘),充分混匀萃取后吸取样品中有机相,注入气相色谱质谱联用仪(GC/MS,8890/7000D,美国Agilent公司)进行测定。
气相色谱条件:HP-5MS毛细管柱(30 m×0.25 mm×0.25 μm);柱升温程序:初始温度为100 ℃,保持1 min,以25 ℃/min的速率升至150 ℃,再以30 ℃/min的速率升至200 ℃。载气为高纯氦气,流速为1.0 mL/min;进样模式为不分流进样,进样体积为1.0 μL。质谱条件:电子轰击离子源(EI),离子化能量为70 eV,离子源温度为230 ℃。接口温度为280 ℃,四级杆温度为150 ℃;扫描模式为选择离子监测(Selected ion monitoring,SIM)。以目标化合物浓度为横坐标,以目标化学物定量离子响应值与内标化合物定量离子响应值的比值为纵坐标,绘制标准曲线,计算丙苯浓度。按式(1)计算丙苯去除率,
| $ \eta=\frac{C_0-C_t}{C_0} \times 100 \%。$ | (1) |
式中:η为去除率(%);Ct为t时刻藻液中剩余丙苯浓度(mg/L);C0为藻液中初始丙苯浓度(mg/L)。
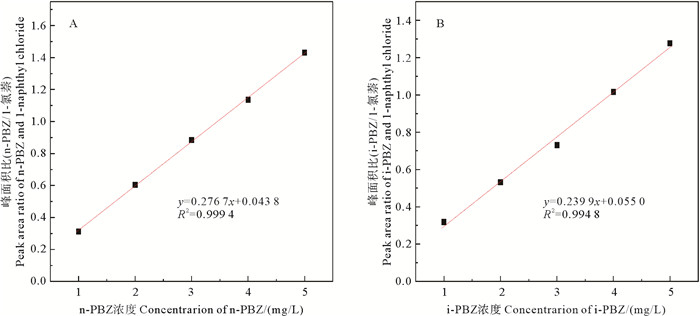
由图 1可见,n-PBZ标准曲线方程为y=0.276 7x+ 0.043 8(R2=0.999 4);3个加标水平(1、3和5 mg/L)的回收率为92.92%~109.65%,相对标准偏差为1.92%~4.39%;海水样品的检测限(LOD=3×信号/噪声)为0.08 mg/L。i-PBZ标准曲线方程为y= 0.239 9x+0.055 0(R2=0.994 8);3个加标水平(1、3和5 mg/L)的回收率为92.41%~107.31%,相对标准偏差为2.61%~7.84%;海水样品的检测限为0.02 mg/L。这表明该方法监测每种丙苯均具有良好的线性范围、精密度和准确度。
|
图 1 n-PBZ和i-PBZ标准曲线 Fig. 1 The standard curves for n-PBZ and i-PBZ |
每组实验重复3次,n-PBZ或i-PBZ的去除率以平均值表示。使用Design expert 13软件对所有实验数据进行回归拟合,得到盐度、温度和光强对响应值的二次多项式方程(模型)。使用SPSS 19.0软件对17组实验的结果进行单因素方差分析(ANOVA),P<0.05视为差异显著。根据ANOVA的结果,判断模型的有效性以及影响n-PBZ或i-PBZ去除效果的因子顺序,并获得微藻去除2种丙苯的最佳环境条件。
2 结果 2.1 模型建立与显著性分析表 3和表 4分别列出了微藻去除n-PBZ、i-PBZ的17组实验结果。经回归拟合,得到以2种丙苯的去除率(Y1、Y2)为响应值的多元二次回归方程:
| $ \begin{gathered} Y_1=-504.769~1+10.382~7 A+32.594~0 B+ \\ 0.097~3 C-0.069~2 A B+0.000~8 A C-0.002~3 B C- \\ 0.162~1 A^2-0.600~2 B^2-0.000~1 C^2\text { 。} \end{gathered} $ | (2) |
| $ \begin{gathered} Y_2=-290.275~3+8.011~8 A+15.594~5 B+ \\ 0.116~0 C-0.056~1 A B-0.000~8 A C+0.000~2 B C-\\ 0.107~8 A^2-0.276~3 B^2-0.000~1 C^2 \text { 。} \end{gathered} $ | (3) |
式中,A、B、C分别表示盐度、温度(℃)和光强(μmol/(m2·s))。
统计学分析表明(见表 5和表 6),上述两个模型均具有较高的F值(59.08和25.35),且P值均小于0.05(P < 0.000 1和P < 0.000 2),表明建立的模型有意义;失拟项不显著(P值分别为0.237 1、0.655 4,均大于0.05),表明实际值与模型预测值有较好拟合度[22]。两方程的确定系数(R2)分别为0.987 0和0.970 2,调整确定系数(Adj-R2)分别为0.970 3和0.932 0,表明两模型可信度良好,分别能解释97.03%和93.20%的响应值变化[23]。两模型的偏差系数CV分别为4.02%和3.11%,均小于10%[24];精密度分别为20.04和15.93,远大于4,符合模型建立要求[25]。
|
|
表 5 3个因子影响n-PBZ去除的显著性检验及ANOVA分析 Table 5 Significance test and ANOVA analysis of the impact of three factors on n-PBZ removal |
|
|
表 6 3个因子影响i-PBZ去除的显著性检验及ANOVA分析 Table 6 Significance test and ANOVA analysis of the impact of three factors on i-PBZ removal |
此外,根据ANOVA得到的F值可知(见表 5和表 6),影响微藻去除n-PBZ的环境因子主次顺序为:光强(10.60)>温度(3.12)>盐度(1.83);而影响i-PBZ去除的因子主次顺序为:温度(10.97)>盐度(8.51)>光强(1.00)。
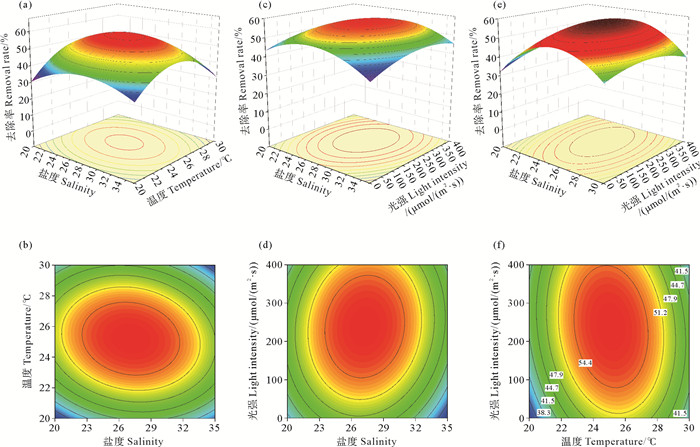
2.2 因子间的交互作用根据RSM原理,固定其中1种因子不变,可得到任意2种因子及其交互作用对丙苯去除率影响的三维响应面图和等高线图。一般认为,2种因子交互作用的响应面坡面越陡峭,表明交互作用对响应值影响越显著;反之,则表明交互作用对响应值的影响越不显著[26]。等高线的形状也能反映交互作用的强弱:椭圆形表示2种因子的交互作用显著,而圆形则表示交互作用相对不显著[27]。由图 2和图 3可知,每个响应面都有明显的峰值点,说明最佳点出现在实验范围内,表明通过RSM实验可求得每种丙苯去除的最佳条件进而获得最大去除率[28]。
|
((a)和(b): 盐度和温度; (c)和(d): 盐度和光强; (e)和(f): 温度和光强。(a) and (b): Salinity vs. temperature; (c) and (d): Salinity vs. light intensity; (e) and (f): Temperature vs. light intensity.) 图 2 因子两两交互作用对n-PBZ去除率影响的三维曲面图和等高线图 Fig. 2 The 3-D surface plots and contour maps showing the effect of pairwise interaction of three factors on the removal of n-PBZ |
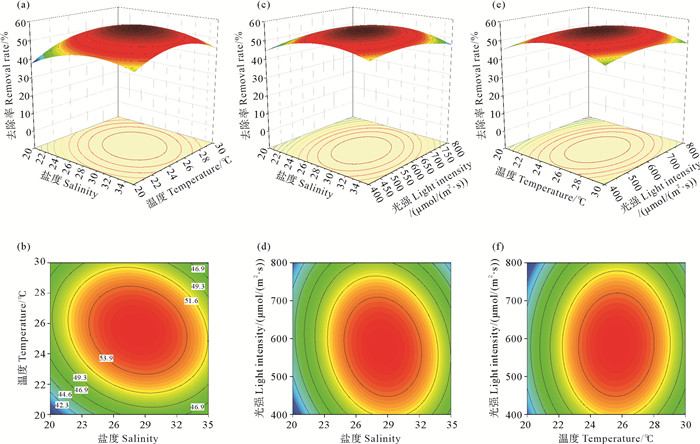
|
((a)和(b): 盐度和温度; (c)和(d): 盐度和光强; (e)和(f): 温度和光强。(a) and (b): Salinity vs. temperature; (c) and (d): Salinity vs. light intensity; (e) and (f): Temperature vs. light intensity.) 图 3 3因子两两交互作用对i-PBZ去除率影响的三维曲面图和等高线图 Fig. 3 The 3-D surface plots and contour maps showing the effect of pairwise interaction of three factors on the removal of i-PBZ |
由图 2(a)、(b)和图 2(e)、(f)可见,等高线图呈明显椭圆形,表明温度与盐度、温度与光强在n-PBZ去除过程中的交互作用明显,具体表现为:随着温度(22~26 ℃)和盐度(20.0~30.0)同步增加,或者随着光强(0~300 μmol/(m2·s))和温度(20~25 ℃)同时增大,去除率不断提高。这与表 5的结果(交互项AB、BC的P < 0.05)相符。由图 3可见,每个响应面的坡度陡峭程度均不及图 2中相应的响应面,表明因子间交互作用对i-PBZ去除率的影响较低。相对而言,盐度-温度响应面的坡度较为陡峭(见图 3(a)、(b)),随着温度(22~26 ℃)和盐度(20.0~30.0)同步增加,i-PBZ去除率不断提高,且表 6中交互项AB的P < 0.05,表明这两个因子之间存在显著交互作用。
2.3 丙苯生物去除的环境条件优化与结果验证通过Design-Expert 13软件进行计算,微藻去除n-PBZ的最适环境条件为:海水盐度27.2、温度25.1 ℃、光强237.9 μmol/(m2·s),此时的理论去除率最高(57.58%);对于i-PBZ而言,理论去除率在海水盐度为28.4、温度为25.5 ℃、光强为580.8 μmol/(m2·s)时最高(56.30%)。为检验模型的可靠性,在上述优化条件下分别进行微藻去除2种丙苯的实验(各重复3次),7 d后n-PBZ和i-PBZ的去除率分别为51.19%和54.62%,与上述理论预测值相近(相对误差分别为5.87%和1.51%),证明回归模型可以较好预测网状鼻胞藻S6A对海水中2种丙苯的去除效果。
3 讨论 3.1 在优化的环境条件下2种丙苯的去除率笔者之前的研究中[18],曾将网状鼻胞藻S6A接种于含n-PBZ和i-PBZ(初始浓度均为5 mg/L)的F/2培养基中,在盐度30.0、温度25 ℃、光强60 μmol/(m2·s) 条件下培养7 d,n-PBZ和i-PBZ的去除率分别为34.6%和38.8%。本研究中,在优化的环境条件下,微藻对n-PBZ和i-PBZ的去除率(实测值)分别提高了16.6%和15.8%,表明微藻对丙苯的去除率因环境因子的变化而变化,将其在适宜环境条件下应用于污染海域,能够获得较好的生物修复效果。这是因为,污染物的生物降解是一个动态的生物能量过程,它在很大程度上取决于生长条件的适宜性,这些条件有助于激活微藻的相应机制以代谢外源污染物[29]。
3.2 影响微藻去除2种丙苯的关键因子经过RSM优化得到的微藻去除n-PBZ的最适光强(237.9 μmol/(m2·s))约为之前研究中的4.0倍,而最适温度(25.1 ℃)和盐度(27.2)则与之前研究所用的水平接近。这表明,虽然n-PBZ的高去除率是通过联合调控多因素(光强、温度、盐度)获得的,但是,提高光强对微藻去除n-PBZ的促进作用更大。2.1节的ANOVA分析同样发现(见表 5),三因子中,光强的F值最大且其影响达到显著水平(P<0.05),而温度、盐度的F值较低且影响不显著(P>0.05),这意味着当这些因子的水平在实验设计的范围内(见表 2)发生变化时,光强是影响n-PBZ去除的关键因子,而温度、盐度的变化对n-PBZ去除的影响较小。文献[30]报道,光照对于微藻生长及其保持污染物去除能力是必要的。笔者进行单因子试验发现[19],在含n-PBZ(5 mg/L)的培养基中,光强200 μmol/(m2·s)下S6A藻的比生长速率显著高于光强为0以及400~800 μmol/(m2·s)时的水平,同时,光强200 μmol/(m2·s)下的n-PBZ去除率也最大。这是高光强下微藻生长及其代谢活性受到刺激的结果[31]。需要说明的是,虽然温度和盐度在实验设计范围内变化对n-PBZ去除的影响较小,但是,如果其变化超出上述范围,仍会造成n-PBZ去除率显著降低。例如,笔者之前通过单因子试验研究环境因子对S6A藻去除n-PBZ (5 mg/L)的影响时发现[19],当温度为5 ℃时,微藻接种7 d后的去除率(14.4%)比30 ℃时(39.76%)低得多;而盐度为5.0时的去除率(22.04%)也明显低于盐度30.0时的去除率(36.15%)。这表明,光强对n-PBZ去除的较大影响只有在温度和盐度达到一定水平时才能显现出来。2.2节中温度与光强之间存在显著的交互作用这一情况也能证明这一点。
与n-PBZ不同,根据环境因子影响i-PBZ去除的ANOVA分析(见表 6),温度和盐度对i-PBZ去除有显著影响(P<0.05),而光强的影响不显著。经RSM优化后,微藻i-PBZ去除所需的适宜光强为之前研究中所用光强(60 μmol/(m2·s))的9.7倍,也大大高于n-PBZ去除所需的适宜光强,表明S6A藻需要吸收更多光能才能有效去除i-PBZ。这可能与S6A藻对2种丙苯的降解机制不同有关,因为二者在分子结构上存在差异:n-PBZ的苯环上取代基团为直链取代基(即丙烷基),i-PBZ的苯环上则为带支链的取代基(即异丙烷基)。有些研究发现,很多芳香烃的好氧降解需要在细胞色素P450(即CYP450)等单加氧酶的催化下进行[32]。某些加氧酶(包括CYP450)属于诱导酶,即暴露于外源污染物后合成受到刺激,从而增强微生物降解有毒物质的能力[33]。但是,还有研究报道,强光会在细胞内产生光氧化逆境,导致叶绿体中产生大量ROS,包括H2O2、单线态氧(1O2)和具有强氧化性的羟基自由基(·OH)等[34-35],而水中有机物的降解与微藻细胞内的ROS有直接关系[36-37]。由此推测,当暴露于n-PBZ时,在光强不太高时即能诱导微藻合成CYP450等降解酶以代谢转化n-PBZ;而i-PBZ则不同,其难以诱导微藻合成其降解酶,但能通过在强光照下产生较多ROS使i-PBZ被氧化去除。当然,这需要进一步测定不同光强下微藻暴露于每种丙苯后的相关降解酶活性以及ROS产生量才能确定。因此,微藻对i-PBZ的去除仍是多因素(光强、温度、盐度)联合作用的结果,但主要决定于温度和盐度,而光强在较高水平(400~800 μmol/(m2·s))时波动对去除率影响不大,只是在580.8 μmol/(m2·s)时去除率稍高一些。
3.3 基于优化环境条件的S6A藻在渤海的适用性分析渤海船舶运输危险化学品的数量较大,根据原国家海洋局海洋减灾中心的评估[38],危险化学品高泄漏风险区达到渤海海域面积的48.4%,三大湾区(渤海湾、辽东湾和莱州湾)均为高风险区。因此,本研究根据上述优化结果,结合渤海的盐度、温度和光强分布特征,分析该海区发生丙苯泄漏事故后利用S6A藻进行生物修复的适宜性。
渤海的表层海水盐度在冬季(其与秋季、春季相差不大)和夏季分别介于29.5~32.0和28.0~31.0之间[39],这个盐度范围比较接近上述优化的S6A藻去除丙苯的最适盐度,因此,该海区的盐度较适合S6A藻在丙苯污染海域的应用。
温度不仅是影响i-PBZ去除的最关键因子,而且在n-PBZ、i-PBZ去除过程中与盐度和/或光强的交互作用显著,表明该因子决定着盐度、光强对2种丙苯去除率的影响程度,因此,适宜温度对于微藻净化海水中的丙苯十分重要。前人研究利用肠杆菌(Enterobacter sp. L-2)降解石油烃[40]、机油降解菌ML-1菌株降解机油[41]时同样发现,温度是影响这些污染物降解速率的主要因素。经RSM优化得到S6A藻去除2种丙苯的适宜温度分别为25.1和25.5 ℃,而当海水温度低于或高于这些优化值时丙苯去除率均会降低(见图 2(a)、2(e)和图 3(a)、3(e))。根据《中国海洋生态环境状况公报》[42],渤海表层海水的月平均温度在1.2~27.1 ℃之间,温度的季节差异性对S6A藻去除丙苯的效果会有较大影响。其中,6—9月的表层水温(21.5~27.1 ℃)适于微藻对丙苯的去除;而1—4月和11—12月的水温大多低于10 ℃,会大大降低S6A藻在丙苯污染海域生物修复中的应用效果。
光强是影响微藻生长的重要环境因子之一,但是,到达地面的太阳辐照中只有波长在380~710nm之间的光谱成分对植物光合作用有效,这部分光强被称为光合有效辐射(Photosynthetically active radiation, PAR)[43]。据文献[44]报道,渤海海域的PAR呈明显季节性变化,春、夏、秋三季(3—8月)的月均值较高,为36~51 Einstein/m2(即417~590 μmol/(m2·s)),适于微藻去除i-PBZ;而冬季(1—2月和11—12月)的PAR较低,为17~25 Einstein/m2(即197~289 μmol/(m2·s)),适于微藻去除n-PBZ。
4 结论(1) 3种环境因子对网状鼻胞藻S6A去除n-PBZ的影响顺序为光强>温度>盐度,去除i-PBZ的影响顺序为温度>盐度>光强。
(2) 适度的高光强有利于提高海水中丙苯的去除率,且i-PBZ的有效去除需要更高光强;温度与盐度、光强之间的显著交互作用表明,利用微藻去除丙苯时应重视温度的适宜性。
(3) RSM优化得到:微藻去除n-PBZ的最适环境条件为盐度27.2、温度25.1 ℃、光强237.9 μmol/(m2·s),微藻去除i-PBZ的最适环境条件为盐度28.4、温度25.5 ℃,光强580.8 μmol/(m2·s)。
(4) 在优化的环境条件下,微藻对n-PBZ和i-PBZ的去除率分别比优化前提高了16.6%和15.8%。
| [1] |
中华人民共和国海事局. 关于执行《国际散装运输危险化学品船舶构造和设备规则》2019年修正案有关事项的通知[EB/OL]. (2020-12-21)[2023-12-19]. https://www.msa.gov.cn/html/xxgk/tzgg/wgfw/20201221/7D9BE1D6-B452-4E4D-B101-2A62C99F6F41.html. Maritime Safety Administration of the People's Republic of China. Notice on the Implementation of the 2019 Amendment to the International Code for the Construction and Equipment of Ships Carrying Dangerous Chemicals in Bulk[EB/OL]. (2020-12-21)[2023-12-19]. https://www.msa.gov.cn/html/xxgk/tzgg/wgfw/20201221/7D9BE1D6-B452-4E4D-B101-2A62C99F6F41.html. (  0) 0) |
| [2] |
余强. 中国大百科全书(第三版)——碳九芳烃[EB/OL]. (2023-08-19)[2023-12-19]. https://www.zgbk.com/ecph/words?SiteID=1&ID=119455&Type=bkzyb#:~:text=%E7%A2%B3%E4%B9%9D%E8%8A%B3%E7%83%83. Yu Q. Chinese Encyclopaedia (The third edition)—C9 aromatic[EB/OL]. (2023-08-19)[2023-12-19]. https://www.zgbk.com/ecph/words?SiteID=1&ID=119455&Type=bkzyb#:~:text=%E7%A2%B3%E4%B9%9D%E8%8A%B3%E7%83%83. (  0) 0) |
| [3] |
陈鼎豪, 陈思莉, 潘超逸, 等. 福建泉港"碳九"事件中海洋水体超标面积及大气影响范围的确定[J]. 环境工程学报, 2021, 15(8): 2536-2546. Chen D H, Chen S L, Pan C Y, et al. Determination of over-standard area of marine water and atmospheric impact range in Quangang C9 Event in Fujian province[J]. Chinese Journal of Environmental Engineering, 2021, 15(8): 2536-2546. (  0) 0) |
| [4] |
Li H, Meng F, Li A. Ecological risk assessment for xylenes and propylbenzenes in aquatic environment using a species sensitivity distribution approach[J]. Ecotoxicology and Environmental Safety, 2023, 261: 115106. DOI:10.1016/j.ecoenv.2023.115106 (  0) 0) |
| [5] |
陈汕, 夏宇凡, 孟范平. 基于微宇宙系统的环境因子影响海水中正丙苯和异丙苯衰减速率的研究[J]. 中国海洋大学学报(自然科学版), 2025, 55(9): 114-124. Chen S, Xia Y F, Meng F P. A study on the influence of environmental factors on the attenuation rate of n-propylbenzene and isopropylbenzene in seawater by using microcosm system[J]. Periodical of Ocean University of China, 2025, 55(9): 114-124. DOI:10.16441/j.cnki.hdxb.20240213 (  0) 0) |
| [6] |
El-sheekh M M, Hamouda R A, Nizam A A. Biodegradation of crude oil by Scenedesmus obliquus and Chlorella vulgaris growing under heterotrophic conditions[J]. International Biodeterioration & Biodegradation, 2013, 82: 67-72. (  0) 0) |
| [7] |
Doria E, Longoni P, Scibilia L, et al. Isolation and characterization of a Scenedesmus acutus strain to be used for bioremediation of urban wastewater[J]. Journal of Applied Phycology, 2012, 24: 375-383. DOI:10.1007/s10811-011-9759-z (  0) 0) |
| [8] |
Xiong J, Kurade M B, Abou-Shanab R A I, et al. Biodegradation of carbamazepine using freshwater microalgae Chlamydomonas mexicana and Scenedesmus obliquus and the determination of its metabolic fate[J]. Bioresource Technology, 2016, 205: 183-190. DOI:10.1016/j.biortech.2016.01.038 (  0) 0) |
| [9] |
Wang Q, Liu W, Li X, et al. Carbamazepine toxicity and its co-metabolic removal by the cyanobacteria Spirulina platensis[J]. Science of the Total Environment, 2020, 706: 135686. DOI:10.1016/j.scitotenv.2019.135686 (  0) 0) |
| [10] |
Meza-escalante E R, Lepe-martinié L, Díaz-quiroz C, et al. Capacity of marine microalga Tetraselmis suecica to biodegrade phenols in aqueous media[J]. Sustainability, 2022, 14(11): 6674. DOI:10.3390/su14116674 (  0) 0) |
| [11] |
Perrineau M M, Zelzion E, Gross J, et al. Evolution of salt tolerance in a laboratory reared population of Chlamydomonas reinhardtii[J]. Environmental Microbiology, 2014, 16(6): 1755-1766. DOI:10.1111/1462-2920.12372 (  0) 0) |
| [12] |
Li H, Meng F, Wang Y, et al. Removal of phenol by Isochrysis galbana in seawater under varying temperature and light intensity[J]. Journal of Oceanology and Limnology, 2020, 38(3): 773-782. DOI:10.1007/s00343-019-9125-6 (  0) 0) |
| [13] |
Khataee A R, Zarei M, Pourhassan M. Bioremediation of malachite green from contaminated water by three microalgae: Neural network modeling[J]. Clean-Soil Air Water, 2010, 38(1): 96-103. DOI:10.1002/clen.200900233 (  0) 0) |
| [14] |
Knudsmark S K, Birch H, Hammershøj R, et al. Determining the temperature dependency of biodegradation kinetics for 34 hydrocarbons while avoiding chemical and microbial confounding factors[J]. Environmental Science & Technology, 2021, 55(16): 11091-11101. (  0) 0) |
| [15] |
Cai Y, Wang R, Rao P, et al. Bioremediation of petroleum hydrocarbons using Acinetobacter sp. SCYY-5 isolated from contaminated oil sludge: Strategy and effectiveness study[J]. International Journal of Environmental Research and Public Health, 2021, 18(2): 819. DOI:10.3390/ijerph18020819 (  0) 0) |
| [16] |
Dayana P S, Bakthavatsalam A K. Optimization of phenol degradation by the microalga Chlorella pyrenoidosa using Plackett-Burman design and response surface methodology[J]. Bioresource Technology, 2016, 207: 150-156. DOI:10.1016/j.biortech.2016.01.138 (  0) 0) |
| [17] |
Chen S, Sun S, Zhao C, et al. Optimization of biodegradation of polycyclic aromatic sulfur heterocycles in soil using response surface methodology[J]. Petroleum Science and Technology, 2018, 36(22): 1883-1890. DOI:10.1080/10916466.2018.1517165 (  0) 0) |
| [18] |
Du S, Cui J, Meng F, et al. Bioremediation of propylbenzenes by a novel marine microalga Rhinomonas reticulata S6A isolated from Daya Bay: Acute toxicity, growth kinetics and biodegradation performance[J]. Frontiers in Marine Science, 2023, 10: 1171944. DOI:10.3389/fmars.2023.1171944 (  0) 0) |
| [19] |
Cui J, Du S, Li Y, et al. Effects of inorganic nutrients and environmental factors on the removal of n-propylbenzene and isopropylbenzene in seawater by cryptophytes Rhinomonas reticulata S6A[J]. Journal of Oceanology and Limnology, 2024, 42(4): 1200-1215. DOI:10.1007/s00343-023-3203-5 (  0) 0) |
| [20] |
Guillard R R. Culture of phytoplankton for feeding marine invertebrates[M]// Culture of Marine Invertebrate Animals. [s. l. ]: Springer, 1975: 29-60.
(  0) 0) |
| [21] |
Jin H M, Choi E J, Jeon C O. Isolation of a BTEX-degrading bacterium, Janibacter sp. SB2, from a sea-tidal flat and optimization of biodegradation conditions[J]. Bioresource Technology, 2013, 145: 57-64. DOI:10.1016/j.biortech.2013.02.004 (  0) 0) |
| [22] |
马锋锋, 郑旭东, 张建, 等. 污泥生物炭对水体中磷的吸附[J]. 中国环境科学, 2024, 44(3): 1347-1356. Ma F F, Zheng X D, Zhang J, et al. Adsorption of phosphate from aqueous solution by sludge biochar[J]. China Environmental Science, 2024, 44(3): 1347-1356. (  0) 0) |
| [23] |
郗婧怡, 王双庆, 白一彤, 等. 响应面法优化黑水虻处理餐厨垃圾工艺参数研究[J]. 中国农业科技导报, 2025, 27(1): 241-249. Xi J Y, Wang S Q, Bai Y T, et al. Study on optimization of processing parameters using Hermetia illucens larva to treat food waste by response surface methodology[J]. Journal of Agricultural Science and Technology, 2025, 27(1): 241-249. (  0) 0) |
| [24] |
Ahmadi M, Vahabzadeh F, Bonakdarpour B, et al. Application of the central composite design and response surface methodology to the advanced treatment of olive oil processing wastewater using Fenton's peroxidation[J]. Journal of Hazardous Materials, 2005, 123(1): 187-195. (  0) 0) |
| [25] |
Beg Q K, Sahai V, Gupta R. Statistical media optimization and alkaline protease production from Bacillus mojavensis in a bioreactor[J]. Process Biochemistry, 2003, 39(2): 203-209. DOI:10.1016/S0032-9592(03)00064-5 (  0) 0) |
| [26] |
陈建福. 响应面优化黄槿叶总黄酮提取工艺及其抗氧化活性[J]. 食品研究与开发, 2019, 40(14): 85-91. Chen J F. Optimization extraction of total flavonoids from Hibiscus tilisceus leaves using response surface methodology and its antioxidant activity[J]. Food Research and Development, 2019, 40(14): 85-91. (  0) 0) |
| [27] |
Luo X, Bai R, Zhen D, et al. Response surface optimization of the enzyme-based ultrasound-assisted extraction of acorn tannins and their corrosion inhibition properties[J]. Industrial Crops and Products, 2019, 129: 405-413. DOI:10.1016/j.indcrop.2018.12.029 (  0) 0) |
| [28] |
Bezerra M A, Santelli R E, Oliveira E P, et al. Response surface methodology (RSM) as a tool for optimization in analytical chemistry[J]. Talanta, 2008, 76(5): 965-977. DOI:10.1016/j.talanta.2008.05.019 (  0) 0) |
| [29] |
Nazos T T, Kokarakis E J, Ghanotakis D F. Metabolism of xenobiotics by Chlamydomonas reinhardtii: Phenol degradation under conditions affecting photosynthesis[J]. Photosynthesis Research, 2017, 131: 31-40. DOI:10.1007/s11120-016-0294-2 (  0) 0) |
| [30] |
Surkatti R, Al-Zuhair S. Microalgae cultivation for phenolic compounds removal[J]. Environmental Science and Pollution Research, 2018, 25: 33936-33956. DOI:10.1007/s11356-018-3450-8 (  0) 0) |
| [31] |
Yao X, Sun J, Bai X, et al. A high-efficiency mixotrophic photoelectroactive biofilm reactor (MPBR) for enhanced simultaneous removal of nutrients and antibiotics by integrating light intensity regulation and microbial extracellular electron extraction[J]. Journal of Environmental Management, 2023, 325: 116520. DOI:10.1016/j.jenvman.2022.116520 (  0) 0) |
| [32] |
臧淑艳, 单华旭, 姚淑华, 等. 苯并(a)芘降解过程中细菌降解相关酶的蛋白应答[J]. 生态学杂志, 2018, 37(10): 3086-3091. Zang S Y, Shan H X, Yao S H, et al. Protein response of bacterial enzymes involved in degradation during BaP degradation[J]. Chinese Journal of Ecology, 2018, 37(10): 3086-3091. (  0) 0) |
| [33] |
宁大亮, 王慧, 王立华, 等. 难降解有机物对白腐真菌P450的诱导及P450的作用[J]. 中国环境科学, 2009, 29(4): 407-412. Ning D L, Wang H, Wang L H, et al. Induction and function of cytochrome P450 in degradation of refractory organic chemicals by Phanerochaete chrysosporium[J]. China Environmental Science, 2009, 29(4): 407-412. (  0) 0) |
| [34] |
Weng H X, Qin Y C, Sun X W, et al. Effects of light intensity on the growth of Cryptomonas sp. (Cryptophyceae)[J]. Environmental Geology, 2009, 57(1): 9-15. DOI:10.1007/s00254-008-1277-1 (  0) 0) |
| [35] |
Liu X, Wu F, Deng N. Photoproduction of hydroxyl radicals in aqueous solution with algae under high-pressure mercury lamp[J]. Environmental Science & Technology, 2004, 38(1): 296-299. (  0) 0) |
| [36] |
Chalifour A, Chin W Y, Leung P Y, et al. Effect of light on the transformation of BDE-47 by living and autoclaved cultures of Microcystis flos-aquae and Chlorella vulgaris[J]. Chemosphere, 2019, 233: 140-148. DOI:10.1016/j.chemosphere.2019.05.189 (  0) 0) |
| [37] |
姜盼盼. 光引发藻液形成活性氧及降解诺氟沙星[D]. 无锡: 江南大学, 2016. Jiang PP. Production of Reactive Oxygen Species and Degradation of Norfloxacin in Algae Liquid Induced by UV Irradiation[D]. Wuxi: Jiangnan University, 2016. (  0) 0) |
| [38] |
方正飞, 武江越. 绘制危化品泄漏入海风险"一张图"[N]. 中国海洋报, 2019-07-24(3). Fang Z F, Wu J Y. Mapping the Risk of Hazardous Chemical Spills into the Sea[N]. China Ocean News, 2019-07-24(3). (  0) 0) |
| [39] |
刘哲, 魏皓, 蒋松年. 渤海多年月平均温盐场的季节变化特征及形成机制的初步分析[J]. 青岛海洋大学学报, 2003, 33(1): 7-14. Liu Z, Wei H, Jiang S N. Characteristics of seasonal variation of monthly mean temperature and salinity fields in the Bohai Sea and analysis of the related dynamics[J]. Journal of Qingdao Ocean University, 2003, 33(1): 7-14. (  0) 0) |
| [40] |
孙烁, 刘其友, 陈水泉, 等. 利用响应面法对L-2菌株降解石油烃进行优化[J]. 化工进展, 2019, 38(12): 5512-5518. Sun S, Liu Q Y, Chen S Q, et al. Optimization for degradation of total petroleum hydrocarbon by the strain L-2 with response surface methodology[J]. Chemical Industry and Engineering Progress, 2019, 38(12): 5512-5518. (  0) 0) |
| [41] |
刁志龙, 辛毅, 刘坤, 等. 机油降解菌降解机油的响应面法优化及其动力学研究[J]. 重庆理工大学学报(自然科学), 2021, 35(8): 209-216. Diao Z L, Xin Y, Liu K, et al. Optimization and kinetics of engine oil degradation by engine oil degrading bacteria using response surface methodology[J]. Journal of Chongqing University of Technology (Natural Science), 2021, 35(8): 209-216. (  0) 0) |
| [42] |
中华人民共和国自然资源部. 2017年中国海洋生态环境状况公报[EB/OL]. (2018-06-06)[2023-12-11]. http://gc.mnr.gov.cn/201806/t20180619_1797652.html. Ministry of Natural Resources of the People's Republic of China. Bulletin of China Marine Ecological Environment Status (2017)[EB/OL]. (2018-06-06)[2023-12-11]. http://gc.mnr.gov.cn/201806/t20180619_1797652.html. (  0) 0) |
| [43] |
Guedes V C, Lombardi A T, Horta A C L. Polychromatic controller of photosynthetically active radiation applied to microalgae[J]. Brazilian Journal of Chemical Engineering, 2023, 40(4): 1089-1101. DOI:10.1007/s43153-022-00298-4 (  0) 0) |
| [44] |
麻书畅. 基于长时序遥感数据不同类型海区叶绿素a特征及其与环境因子关系分析[D]. 杭州: 浙江大学, 2022. Ma S C. Characteristics of Chlorophyll-a and Its Relationship with Environmental Factors in Different Types of Sea Areas Based on Long Time Series Remote Sensing Data[D]. Hangzhou: Zhejiang University, 2022. (  0) 0) |
 2025, Vol. 55
2025, Vol. 55


