2. 中国海洋大学-中国船舶集团环境发展有限公司海洋生态保护修复与可持续利用技术联合研究中心,山东 青岛 266100;
3. 自然资源部黄渤海温带海草床生态系统野外科学观测研究站,山东 青岛 266100;
4. 中华环境保护基金会,北京 100062
海草是唯一一类完全营沉水生活的海洋被子植物[1],构筑的海草床作为滨海三大典型生态系统之一,具有减缓水流、净化水体、稳固海洋底质、抑制病菌和固碳增汇等重要的生态服务价值[2-4]。然而,由于人类活动和全球气候变化等影响,全球范围内海草床正呈现严重衰退趋势,退化速度每年超过7%[5-6]。中国是世界上海草床退化最严重的国家之一,超过80%的海草床已完全消失[2, 7]。海草床人工修复技术主要包括植株移植法和种子种植法,但在绝大多数的海草床生态修复工程中,两者的供体均来自于天然草床,存在诸多潜在的生态风险[8-10]。
近年来,种苗法越来越成为关注热点,其主要是针对种子高产的海草种类,在适宜的人工促萌和幼苗培育条件下,通过种子萌发—实生苗建成—种苗培育—海区移栽的方式,实现海草床的保护修复[11],具有生态风险小、利于保持海草遗传多样性等优点[12]。其中,种子萌发和实生苗建成是植物生活周期中损失率最高的阶段[13-14],因此适宜的种子萌发和实生苗建成条件是提升种苗法修复效果的关键要素。全球海草种类超过半数均生产顽拗性种子并具有明显休眠期[15],休眠的破除(种子萌发)是种子内部状态与温度、盐度、光照、激素、溶解氧等外部环境因子共同作用的结果[16-18]。
众多研究表明,溶解氧水平对海草种子萌发和实生苗建成至关重要[14, 19]。萌发开始后种子吸水膨胀,种胚即吸收大量氧气为萌发供能[19]。氧气通过改变胚对激素的敏感性影响激素对种子萌发的调节作用,还可以通过影响活性氧浓度、乙醇代谢和蛋白质降解等代谢过程介导种子萌发[20]。与多数陆生植物种子不同,沉水植物种子一般在低氧条件(小于1 mg·L-1)下呈现出高萌发率[21]。Probert等[22]研究发现,鳗草(Zostera marina)种子在沉积物掩埋的厌氧条件下萌发率可达90%,而在有氧水培条件下的萌发率仅为40%,且种子的萌发历期更长。Kawasaki等[23]利用类似低氧条件对鳗草种子进行促萌,发现鳗草种子的萌发率可达93.9%。然而,这些研究大多仅定性研究低氧条件和常氧条件对海草种子萌发的影响,并未对溶解氧水平进行定量控制,因此促进海草种子萌发的适宜溶解氧水平尚不明确[24]。
为进一步查明溶解氧对海草种子萌发和实生苗建成的影响,在实验室条件下,设置了5个不同溶解氧水平,研究了其对温带优势海草种类—鳗草种子萌发率、萌发指标、种子内部水分和营养物质含量以及实生苗建成率、形态学参数和生理指标等的影响,明确了鳗草种子萌发和实生苗建成的最适溶解氧水平,分析了种子和实生苗对不同溶解氧水平的生理响应过程,以期为深入了解海草繁殖生物学理论和提升海草床种苗法生态修复效果提供基础数据和理论依据。
1 材料与方法 1.1 实验材料实验用鳗草种子于2022年7月采集自山东省荣成市天鹅湖海域(37.338°N—37.358°N,122.555°E—122.579°E)。采集时,海区水温(T)为(22.0±0.9) ℃、盐度(S)为30.0±0.5,溶解氧(DO)含量为(8.7±0.5) mg·L-1。选取颗粒饱满、色泽正常的种子,置于比重为1.2的盐水中,使用筛网收集沉底种子用于实验[25]。筛选后的种子经过75%酒精消毒30 s,放入尼龙网袋置于自然光照、盐度30.0±0.5、水温4.0 ℃的循环海水中保存待用[26]。
1.2 实验设计综合前期监测和调查结果,该海域的鳗草种子通常在早春萌发[27],因此实验于2023年1—4月进行,共计110 d。实验设置5个溶氧量水平:2、4、6、8(对照)和10 mg·L-1,每水平设置9个重复。使用纯度99.9%的氮气或氧气分别给低氧和高氧处理组的实验水槽海水充气,直至各处理组海水的溶解氧水平分别达到设置水平。实验期间,每天使用YSI DO 200型溶氧仪实时监测水体溶水平,并通过调整充气阀保证各处理组海水溶解氧水平的误差控制在±0.5 mg·L-1。
1.3 实验过程在待用种子中随机挑选67 500粒,平均分成45份,每份种子置于250 mL烧杯中并编号,同组的9个烧杯置于1个玻璃水槽(长×宽×高: 40 cm×40 cm× 20 cm)。依据van Lent等[28]研究结果,使用盐度15.0± 0.5的无菌海水加至水深18 cm开始种子促萌。
子叶萌出1 cm视为种子萌发[29]。每2 d观察种子的萌发情况,将萌发的种子立即移植于平铺有3 cm细砂(粒径: 0.13~0.25 mm)的250 mL烧杯中,每个烧杯移植20粒,确保细砂刚好能覆盖种子下胚轴,然后将同组的烧杯置于相同规格的玻璃水槽,加入盐度30.0±0.5的无菌海水至18 cm,最后将玻璃水槽放入光照培养箱(GXZ-280,宁波江南仪器厂)开始实生苗培育[30]。种子萌发持续60 d(萌发基本停滞,累积萌发率趋于平稳),实生苗培育持续50 d,实验共进行110 d。
1.4 实验条件根据于兵等[31]报道,种子萌发期间,水温设置为(16.0±0.5) ℃、处于黑暗条件、每2 d换水1次;实生苗培育期间,水温设置为(16.0±0.5) ℃、光照周期12 L∶12 D、光量子强度50 μmol·m-2·s-1、溶解氧水平8.0 mg·L-1、每2 d更换海水和细砂1次[30]。
1.5 样品采集与测定播种前,随机选取待用的鳗草种子1 000粒,测定种子初始的水分、总蛋白质含量和非结构性碳水化合物(可溶性糖和淀粉)含量以及α-淀粉酶活性。种子萌发实验开始后,每2天统计种子萌发数量,计算累积萌发率、平均萌发历期、发芽指数和活力指数;每20天取样1次,于每个处理组随机选择3个重复,每个重复随机采集150粒种子,混合后随机平均分为3份,分别测定每份种子样品的上述生理学指标。实生苗培育50 d后,统计各处理组实生苗存活率,计算实生苗建成率,测量和分析实生苗的形态学指标和叶片光合色素含量。每次数据统计和样本采集时均选择9:00—10:00的时间范围,以消除取样时间对实验结果的影响。
1.5.1 种子萌发累积萌发率(CGR,%)、平均萌发历期(MTG,d)、发芽指数(GI)和活力指数(VI)的计算参照Wen等[32]。水分含量(MS,%)测定采用烘干法[33];总蛋白质含量(TP,%)测定采用凯氏定氮法[34];可溶性糖含量(SS,%)和淀粉含量(S,%)测定采用蒽酮法[35];α-淀粉酶活性(α-AA,U·g-1)测定采用3, 5-二硝基水杨酸(DNS)测定还原糖法[36]。每组样品的同一指标重复测定4次。
1.5.2 实生苗建成实生苗培育结束后,统计最终存活的幼苗数量,以实生苗初始数量为基数计算实生苗存活率(SSR,%),并以播种种子数量为基数计算实生苗建成率(SER,%)。各处理组分别随机选择30株幼苗,测量幼苗的株高(SH,cm)、最大根长(RL,cm)、茎节长(IL,cm)、叶鞘长(SL,cm)和最大叶长(LL,cm)等形态学指标。剩余的幼苗采用浸提法[37-38]测定叶片的叶绿素a(Chl a,mg·g-1)、叶绿素b(Chl b,mg·g-1)、类胡萝卜素(Caro,mg·g-1)和总叶绿素(Chl a+b,mg·g-1)的含量,并计算叶绿素a和叶绿素b的比值(Chl a/b)。
1.6 数据处理实验数据以平均值±标准差表示。使用SPSS 25.0软件进行单因素方差分析(One-way ANOVA)和Tukey多重比较分析各个参数的差异显著性,差异显著水平为P < 0.05,差异极显著水平为P < 0.01。对种子萌发指标和种子生理指标进行主成分分析以揭示种子萌发与种子内含物之间的关系。采用Pearson相关分析方法探究种子萌发与实生苗建成过程中各指标之间的相关性。利用Origin 2022软件绘图。
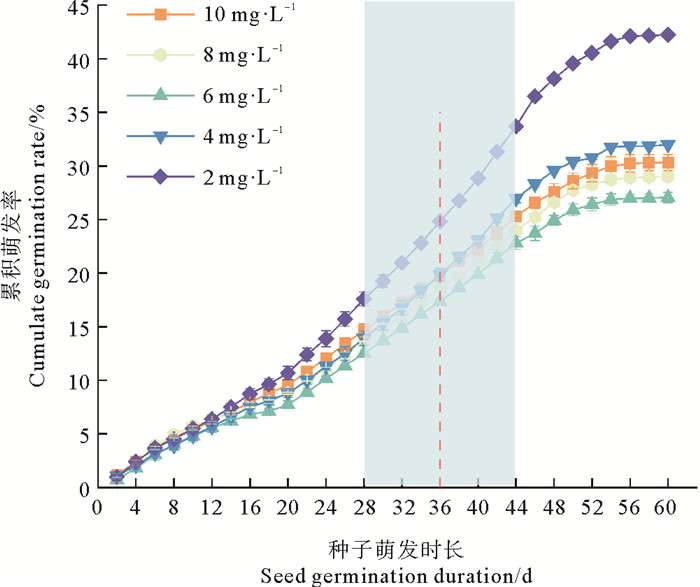
2 结果 2.1 种子萌发 2.1.1 累积萌发率随种子萌发时间增加,各处理组的累积萌发率均呈现缓慢增加-快速增加-趋于平稳的趋势(见图 1)。单因素方差分析显示,实验期间各处理组的累积萌发率均存在显著差异。至萌发60 d,2 mg·L-1处理组的种子累积萌发率显著高于其他处理组,是对照组的1.5倍(P < 0.05)。
|
图 1 不同溶解氧水平处理组鳗草种子累积萌发率的变化 Fig. 1 Change in cumulate germination rate of Z. marina seeds exposed to different dissolved oxygen levels |
种子萌发实验结束后,2 mg·L-1处理组的平均萌发历期、发芽指数和活力指数均达到最大值,显著高于其他处理组(P < 0.05,见表 1)。此外,低氧处理组(2和4 mg·L-1)的3个萌发指标均显著高于对照组,而高氧处理组(10 mg·L-1)的发芽指数显著高于对照组(P < 0.05),其他萌发指标与对照组差异不显著(P>0.05)。
|
|
表 1 不同溶解氧水平对鳗草种子萌发指标的影响(平均值±标准差) Table 1 Effects of different dissolved oxygen levels on germination indexes of Z. marina seeds(mean±SD) |
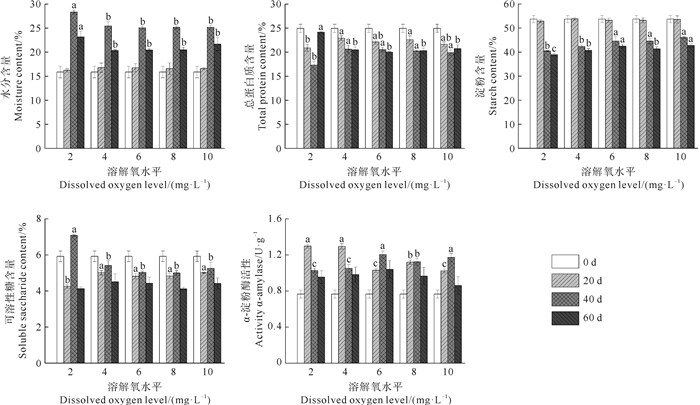
鳗草种子各项生理指标在不同萌发时期变化显著。种子萌发初期(0~20 d),所有处理组的α-淀粉酶活性显著升高,低氧处理组(2和4 mg·L-1)是对照组的1.1倍,显著高于其他各处理组(P < 0.05);至种子快速萌发期(20~40 d),与种子萌发初期相比,种子水分和可溶性糖含量明显升高而总蛋白质含量和淀粉含量显著下降(P < 0.05),其中2 mg·L-1处理组的水分和可溶性糖含量分别达到对照组的1.1和1.4倍、总蛋白质含量和淀粉含量分别降至对照组的85.5%和90.7%;至种子萌发缓滞期(40~60 d),2 mg·L-1处理组的总蛋白质含量迅速上升超过其他处理组,达到对照组的1.2倍(见图 2)。
|
(不同小写字母表示相同萌发时长同一指标组间存在显著差异(P < 0.05)。下同。Different lowercase letters indicate significant differences among treatments in the same index at the same germination time(P < 0.05). The same as below.) 图 2 不同溶解氧水平对鳗草种子生理指标的影响(平均值±标准差) Fig. 2 Effects of different dissolved oxygen levels on physiological indexes of Z. marina seeds (mean±SD) |
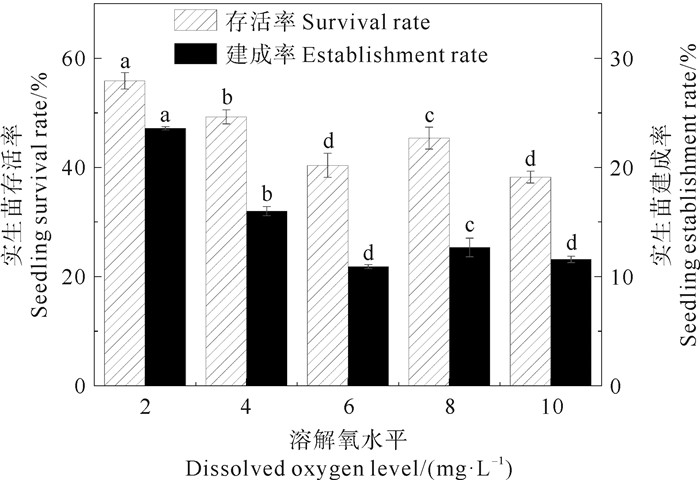
溶解氧水平对实生苗的存活率和建成率有显著影响(P < 0.05)。随溶解氧水平降低,实生苗的存活率和建成率总体呈上升趋势。经过50 d培育,2 mg·L-1处理组的存活率和建成率均最高,分别为对照组的1.2和1.9倍;而10 mg·L-1处理组的存活率最低,仅为对照组的84.2%(见图 3)。
|
图 3 不同溶解氧水平对鳗草实生苗存活率和建成率的影响(平均值±标准差) Fig. 3 Effects of different dissolved oxygen levels on survival rate and establishment rate of Z. marina seedlings (mean±SD) |
如表 2所示,经过50 d培育,2 mg·L-1处理组的根长达到最大值,显著高于6 mg·L-1对照组(P < 0.05);所有形态学参数在2 mg·L-1处理组与对照组之间无明显差异(P>0.05)。
|
|
表 2 不同溶解氧水平条件下鳗草实生苗生长指标的变化(平均值±标准差) Table 2 The change in gowth indexes of Z. marina seedlings exposed to different dissolved oxygen levels (mean±SD) |
从叶绿素含量来看,2 mg·L-1处理组实生苗的叶绿素b含量和总叶绿素含量最低,分别为对照组的75.9%和88.2%(P < 0.05);叶绿素a/b比值在2 mg·L-1处理组达到最大值,是对照组的1.2倍;但2 mg·L-1处理组的类胡萝卜素含量与对照组无显著差异(P>0.05)详见表 3。
|
|
表 3 不同溶解氧水平对鳗草实生苗光合色素含量的影响(平均值±标准差) Table 3 Effect of different dissolved oxygen levels on photosynthetic pigment contents of Z. marina seedlings (mean±SD) |
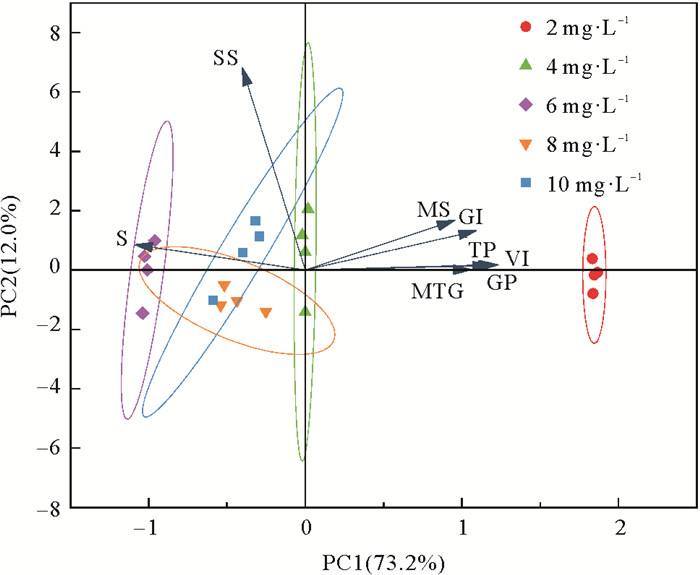
对不同溶解氧水平条件下鳗草种子的萌发参数和生理指标进行主成分分析(见图 4)。结果显示,不同溶解氧水平处理间存在显著差异;种子淀粉含量和种子萌发具有显著负相关关系,而种子水分和总蛋白质含量则与种子萌发具有显著正相关关系(P < 0.05)。
|
(GI:发芽指数;VI:活力指数;GP:萌发潜力;MTG:平均萌发历期;S:淀粉含量;SS:可溶性糖含量;MS:水分含量;TP:总蛋白质含量。GI: Germination index; VI: Vitality index; GP: Germination potential; MTG: Mean time of germination; S: Starch content; SS: Soluble sugar content; MS: Moisture content; TP: Total protein content.) 图 4 鳗草种子萌发和生理指标的主成分分析 Fig. 4 Principal component analysis of germination and physiological indexes of Z. marina seeds |
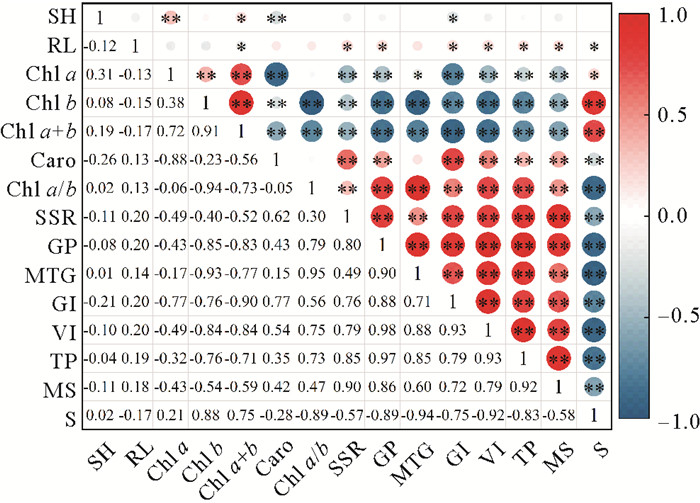
选取PCA分析中解释量较大的种子萌发和生理指标(S、MS、TP、VI、GI、MTG和GP)以及在各组间存在显著差异的植株生态学指标(SH、RL及光合色素)对实生苗存活率(SSR)进行Pearson相关性分析(见图 5)。结果显示,鳗草实生苗的存活率与种子的萌发及生理指标之间存在较强的相关性。实生苗存活率与种子总蛋白质含量、水分含量和萌发指标呈极显著正相关,与种子的淀粉含量,实生苗的叶绿素a含量、叶绿素b含量和总叶绿素含量均呈极显著负相关关系(P < 0.01);株高与总叶绿素呈显著正相关(P < 0.05)、与类胡萝卜素呈极显著负相关(P < 0.01);最大根长与总叶绿素、淀粉含量呈显著负相关(P < 0.05)。
|
(SH:株高;RL:根长;Chl a:叶绿素a;Chl b:叶绿素b;Chl a+b:总叶绿素;Caro:类胡萝卜素;Chl a/b:叶绿素a/b;SSR:实生苗存活率;GP:萌发潜力;MTG:平均萌发历期;GI:发芽指数;VI:活力指数;TP:总蛋白质含量;MS:水分含量;S:淀粉;*:P < 0.05;**:P < 0.01。SH: Seedling height; RL: Root length; Chl a: Chlorophyll a; Chl b: Chlorophyll b; Chl a+b: Total chlorophyll; Caro: Carotenoid; Chl a/b: Chlorophyll a/b; SSR: Seedling survival rate; GP: Germination potential; MTG: Mean time of germination; GI: Germination index; VI: Vitality index; TP: Total protein content; MS: Moisture content; S: Starch; * : P < 0.05; ** : P < 0.01.) 图 5 鳗草实生苗生态学指标和种子生理学指标的相关性分析 Fig. 5 Correlation analysis between seedling ecological indexes and seed physiological indexes of Z. marina |
萌发率、发芽指数和活力指数是反映种子萌发能力的关键参数[32]。本研究发现,溶解氧水平对鳗草种子的累积萌发率、发芽指数和活力指数有显著影响,2 mg·L-1处理组的种子累积萌发率是对照组的1.5倍,发芽指数和活力指数均显著高于其他处理组,这与Churchill[39]和Moore等[40]的研究结果相似。但Hootsmans等[41]研究发现,被掩埋保存在厌氧环境下30 d后,鳗草种子基本不萌发。这可能是由于该研究将种子掩埋在温度20 ℃、盐度40的有机质中,导致沉积物硫化物水平显著升高从而对种子活力和萌发产生不利影响[42],且高盐条件也会抑制种子吸水从而限制鳗草种子萌发[43]。自然环境中,鳗草种子成熟后脱离佛焰苞下沉至底质表面,在泥沙沉积、水体运动和生物扰动等多重因素影响下掩埋至底质之中形成休眠种子库,待休眠期结束后自然萌发[41, 44]。鳗草海草床的底质环境一般处于低氧条件,其间隙水溶解氧水平通常低于3 mg·L-1[22, 45]。因此本研究得到的鳗草种子最适宜萌发的溶解氧水平(2 mg·L-1)与其自然萌发条件接近。除此之外,种子萌发对氧气的需要量取决于物种本身结构、休眠类型和环境温度等多种因素[20]。采自不同地理种群的鳗草种子的萌发时间和萌发率等萌发状态存在显著差异[46]。不同环境因素也会对海草种子的萌发产生耦合影响[16, 47],有研究发现,在温度16 ℃和盐度15的条件下,有氧和厌氧处理下的累积发芽率均超过80%,低温层积和低盐条件可影响溶解氧对鳗草种子的促萌作用[29]。
种子萌发起始于水分吸收,终止于胚轴伸出,该过程包括呼吸作用和DNA修复等一系列代谢活动[13]。这些代谢活动是种子萌发的关键,在低氧时,鳗草种子萌发是通过提高渗透调节物质含量,促进种子吸水膨胀并加快代谢水平以实现对低氧环境的生理响应[48]。淀粉和可溶性糖等相互转化为成熟种子提供储能物质,并进一步成为支持种子萌发和幼苗生长的能量来源[49]。其中,淀粉是种子的重要储能物质,成熟鳗草种子的淀粉含量约占50%[50]。本研究发现,2 mg·L-1溶解氧水平条件下鳗草种子的α-淀粉酶活性在40 d时大幅度升高并显著高于对照组,淀粉含量随后急剧下降并显著低于对照组,这主要是由于α-淀粉酶在缺氧条件下仍可将淀粉转化为可溶性糖以促进种子萌发[51-52]。可溶性糖是植物细胞主要的营养物质和渗透调节物质,在不良条件下植物种子可以通过提高液泡的可溶性糖含量增加植物细胞渗透势,稳定植物细胞膜结构,维持细胞正常代谢从而提高植物细胞抵御不良环境的能力[53]。本研究发现,2 mg·L-1溶解氧水平条件下鳗草种子的可溶性糖含量在种子快速萌发时期大幅升高且显著高于其他处理组。Sugiura等[54]也发现,鳗草幼苗生长初期,下胚轴和植株内部淀粉颗粒的数目以及淀粉含量均显著降低,在淀粉酶的作用下转化为可溶性糖。此外,本研究还发现,低氧条件下种子总蛋白质含量呈现快速分解、然后又迅速合成增加的变化情况,这可能与种子应对低氧环境时进行渗透调节积累蛋白有关[55]。研究发现,在高水温、高盐度、叶片脱水和低溶解氧浓度条件下,鳗草种子的RCI2蛋白编码基因表达上调,可能参与了鳗草种子对低氧环境的适应[56]。综合种子在萌发阶段的生理响应过程可知,低氧条件下,鳗草种子通过提高α-淀粉酶活性加速淀粉分解,增加可溶性糖含量,进而促进吸水膨胀和能量供应,最终显著提升萌发率。
3.2 溶解氧对鳗草实生苗建成的影响缺氧胁迫对鳗草植株的光合和生长具有显著负面影响[39, 57]。因此,本研究的种子在低氧条件下水培萌发后即转入适宜的常氧条件进入实生苗的培育阶段。实生苗建成率取决于种子萌发率和实生苗存活率,不同溶解氧水平条件下种子萌发率的差异以及其对种子生理的潜在影响导致各处理组的实生苗存活率和建成率均存在显著差异。其中,2 mg·L-1处理组实生苗存活率达到55.9%,显著高于其他处理组。Xu等[58]研究发现,掩埋在厌氧底质(细砂)中2 cm的鳗草种子的实生苗建成率相比掩埋深度5 cm处理组升高1.7倍,但掩埋深度10 cm处理组实生苗全部死亡,说明适宜的低氧条件对海草实生苗的存活和建成具有促进作用,但溶解氧水平过低或掩埋深度过大则导致鳗草实生苗的建成受限[39, 58]。本研究发现,各溶解氧水平条件下萌发种子培育的实生苗的形态学指标与对照组无显著差异,研究结果与Churchill[39]的研究结论一致,说明低氧促萌的种子在厌氧环境缓解后,其萌发不会抑制实生苗的生长。
光合作用可为植物提供氧气,以维持植物的有氧代谢和增强生物合成活性[59]。叶绿素a和叶绿素b可以形成叶绿素循环相互转化,叶绿素b是光合天线LHCII的调控者,叶绿素a/b的比值反映了叶绿素结构体中捕光天线的比例[60-61]。本研究发现,2 mg·L-1处理条件下鳗草幼苗的Chl a/b达到对照组的1.3倍,说明鳗草初萌发幼苗能够通过改变光合色素含量等光合响应来应对种子萌发期间的低氧条件[62]。本研究还发现,植株存活率和光合色素含量之间存在极显著相关关系,鳗草早期幼苗的下胚轴和子叶组织也表现出光合能力,有利于实生苗建成[59]。
萌发阶段种子内容物的消耗和转变可为植株生活史后期发育奠定基础[63]。孙燕[64]研究发现,鳗草种子下胚轴在鳗草萌发后20 d内持续为幼苗生长提供营养物质和能量。本研究发现,鳗草实生苗存活率与种子总蛋白质含量呈极显著正相关,这与江文杰等[65]关于栓皮栎(Quercus variabilis)种子贮藏物质影响萌发成苗的结论一致。此外,鳗草实生苗不定根的最大根长与淀粉含量显著负相关,类似现象在水稻(Oryza sativa)种子的研究中也有报道,这进一步表明种子萌发阶段的营养物质储备对实生苗早期生长具有重要影响[66]。
4 结语种子萌发和实生苗建成是植物生活周期中损失率最高的阶段。本研究以温带优势海草种类——鳗草为对象,探究了不同溶解氧水平对鳗草种子萌发和实生苗建成的影响,分析了不同溶解氧水平下鳗草种子萌发及实生苗建成的生理响应。结果发现,低溶解氧水平对鳗草种子萌发和实生苗建成具有显著促进作用,其中,2 mg·L-1是种子萌发阶段的适宜溶解氧水平。综合分析生理指标的变化趋势可知,鳗草种子通过加速淀粉分解,提高可溶性糖等渗透调节物质和营养物质含量,促进种子吸水膨胀,提高物质代谢水平以实现对低氧环境的适应。研究结果进一步丰富了海草繁殖生物学理论,为提升海草种苗法的生态修复效果提供了依据。后期应采用基因组学和蛋白组学等技术进一步分析海草种子和实生苗应对低氧促萌的响应过程,以充分明确鳗草种子低氧促萌的分子生物学响应机制。
| [1] |
Ma X, Vanneste S, Chang J, et al. Seagrass genomes reveal ancient polyploidy and adaptations to the marine environment[J]. Nature Plants, 2024, 10(2): 240-255. DOI:10.1038/s41477-023-01608-5 (  0) 0) |
| [2] |
周毅, 江志坚, 邱广龙, 等. 中国海草资源分布现状、退化原因与保护对策[J]. 海洋与湖沼, 2023, 54(5): 1248-1257. Zhou Y, Jiang Z J, Qiu G L, et al. Distribution status, degradation reasons and protection countermeasures of seagrass resources in China[J]. Oceanologia et Limnologia Sinica, 2023, 54(5): 1248-1257. (  0) 0) |
| [3] |
Macreadie P I, Costa M D P, Atwood T B, et al. Blue carbon as a natural climate solution[J]. Nature Reviews Earth & Environment, 2021, 2(12): 826-839. (  0) 0) |
| [4] |
Lamb J B, Van De Water J A J M, Bourne D G, et al. Seagrass ecosystems reduce exposure to bacterial pathogens of humans, fishes, and invertebrates[J]. Science, 2017, 355(6326): 731-733. DOI:10.1126/science.aal1956 (  0) 0) |
| [5] |
Dunic J C, Brown C J, Connolly R M, et al. Long-term declines and recovery of meadow area across the world's seagrass bioregions[J]. Global Change Biology, 2021, 27(17): 4096-4109. DOI:10.1111/gcb.15684 (  0) 0) |
| [6] |
Waycott M, Duarte C M, Carruthers T J B, et al. Accelerating loss of seagrasses across the globe threatens coastal ecosystems[J]. Proceedings of the National Academy of Sciences of the United States of America, 2009, 106(30): 12377-12381. (  0) 0) |
| [7] |
Du J, Chen B, Nagelkerken I, et al. Protect seagrass meadows in China's waters[J]. Science, 2023, 379(6631): 447. (  0) 0) |
| [8] |
李森, 范航清, 邱广龙, 等. 海草床恢复研究进展[J]. 生态学报, 2010, 30(9): 2443-2453. Li S, Fan H Q, Qiu G L, et al. Review on research of seagrass beds restoration[J]. Acta Ecologica Sinica, 2010, 30(9): 2443-2453. (  0) 0) |
| [9] |
Zhang Y H, Li C, Zhao J S, et al. Seagrass resilience: Where and how to collect donor plants for the ecological restoration of eelgrass Zostera marina in Rongcheng Bay, Shandong Peninsula, China[J]. Ecological Engineering, 2020, 158: 106029. DOI:10.1016/j.ecoleng.2020.106029 (  0) 0) |
| [10] |
张沛东, 张彦浩, 张宏瑜, 等. 海草植株扩繁理论及其定植效应的研究进展[J]. 渔业科学进展, 2020, 41(4): 181-189. Zhang P D, Zhang Y H, Zhang H Y, et al. Research advances in shoot propagation theory and planting technique of seagrasses[J]. Progress in Fishery Sciences, 2020, 41(4): 181-189. (  0) 0) |
| [11] |
Tanner C E, Parham T. Growing Zostera marina (eelgrass) from seeds in land-based culture systems for use in restoration projects[J]. Restoration Ecology, 2010, 18(4): 527-537. DOI:10.1111/j.1526-100X.2010.00693.x (  0) 0) |
| [12] |
刘燕山. 大叶藻四种播种增殖技术的效果评估与适宜性分析[D]. 青岛: 中国海洋大学, 2015. Liu Y S. Assessing Establishment Success and Suitability Analysis of four Zostera marina Seed Planting Technologies[D]. Qingdao: Ocean University of China, 2015. (  0) 0) |
| [13] |
徐恒恒, 黎妮, 刘树君, 等. 种子萌发及其调控的研究进展[J]. 作物学报, 2014, 40(7): 1141-1156. Xu H H, Li N, Liu S J, et al. Research progress on seed germination and its regulation[J]. Acta Agronomica Sinica, 2014, 40(7): 1141-1156. (  0) 0) |
| [14] |
Bewley D, Bradford K J, Hilhorst H W M, et al. Seeds: Physiology of Development, Germination and Dormancy[M]. 3rd edition. Cambridge: Cambridge University Press, 2013: 247-295.
(  0) 0) |
| [15] |
Orth R J, Harwell M C, Bailey E M, et al. A review of issues in seagrass seed dormancy and germination: implications for conservation and restoration[J]. Marine Ecology Progress Series, 2000, 200: 277-288. DOI:10.3354/meps200277 (  0) 0) |
| [16] |
张沛东, 孙燕, 牛淑娜, 等. 海草种子休眠、萌发、幼苗生长及其影响因素的研究进展[J]. 应用生态学报, 2011, 22(11): 3060-3066. Zhang P D, Sun Y, Niu S N, et al. Research progress in seagrass seed dormancy, germination, and seedling growth and related affecting factors[J]. Chinese Journal of Applied Ecology, 2011, 22(11): 3060-3066. (  0) 0) |
| [17] |
Shu K, Liu X D, Xie Q, et al. Two faces of one seed: Hormonal regulation of dormancy and germination[J]. Molecular Plant, 2016, 9(1): 34-45. DOI:10.1016/j.molp.2015.08.010 (  0) 0) |
| [18] |
Meng Y, Shuai H, Luo X, et al. Karrikins: Regulators involved in phytohormone signaling networks during seed germination and seedling development[J]. Frontiers in Plant Science, 2017, 7: 2021. (  0) 0) |
| [19] |
Weitbrecht K, Müller K, Leubner-Metzger G. First off the mark: Early seed germination[J]. Journal of Experimental Botany, 2011, 62(10): 3289-3309. DOI:10.1093/jxb/err030 (  0) 0) |
| [20] |
Corbineau F. Oxygen, a key signalling factor in the control of seed germination and dormancy[J]. Seed Science Research, 2022, 32(3): 126-136. DOI:10.1017/S096025852200006X (  0) 0) |
| [21] |
高健. 沉水植物繁殖生理与组培快繁技术研究[D]. 武汉: 华中师范大学, 2007. Gao J. Study of Reproduction Physiology and Tissue Culture of Submerged Macrophytes[D]. Wuhan: Central China Normal University, 2007. (  0) 0) |
| [22] |
Probert R J, Brenchley J L. The effect of environmental factors on field and laboratory germination in a population of Zostera marina L. from southern England[J]. Seed Science Research, 1999, 9(4): 331-339. DOI:10.1017/S0960258599000343 (  0) 0) |
| [23] |
Kawasaki Y, Yamada S, Honda M. Development of Technique for Marine Macrophyte Bed Creation in the Coastal Zone Near Power Plant: Method for eelgrass (Zostera marina L.) bed creation by seeding[R]. Japan: Central Research Institute of Electric Power Industry, 1988.
(  0) 0) |
| [24] |
Valdemarsen T, Wendelboe K, Egelund J T, et al. Burial of seeds and seedlings by the lugworm Arenicola marina hampers eelgrass (Zostera marina) recovery[J]. Journal of Experimental Marine Biology and Ecology, 2011, 410: 45-52. DOI:10.1016/j.jembe.2011.10.006 (  0) 0) |
| [25] |
Xu S C, Zhou Y, Xu S, et al. Seed selection and storage with nano-silver and copper as potential antibacterial agents for the seagrass Zostera marina: Implications for habitat restoration[J]. Scientific Reports, 2019, 9: 20249. DOI:10.1038/s41598-019-56376-0 (  0) 0) |
| [26] |
田璐, 张沛东, 牛淑娜, 等. 不同处理对大叶藻种子萌发和幼苗建成的影响[J]. 生态学杂志, 2014, 33(9): 2408-2413. Tian L, Zhang P D, Niu S N, et al. Effects of different treatments on seed germination and seedling establishment of eelgrass Zostera marina L.[J]. Chinese Journal of Ecology, 2014, 33(9): 2408-2413. (  0) 0) |
| [27] |
王朋梅, 周毅, 张晓梅, 等. 天鹅湖大叶藻种苗补充情况调查[J]. 海洋科学, 2016, 40(6): 49-55. Wang P M, Zhou Y, Zhang X M, et al. Supplementary investigation of eelgrass seedlings(Zostera marina L.) in Swan Lake[J]. Marine Sciences, 2016, 40(6): 49-55. (  0) 0) |
| [28] |
Van Lent F, Verschnure J M. Comparative study on populations of Zostera marina L. (eelgrass): Experimental germination and growth[J]. Journal of Experimental Marine Biology and Ecology, 1995, 185(1): 77-91. DOI:10.1016/0022-0981(94)00132-W (  0) 0) |
| [29] |
Brenchley J L, Probert R J. Seed germination responses to some environmental factors in the seagrass Zostera capricorni from eastern Australia[J]. Aquatic Botany, 1998, 62(3): 177-188. DOI:10.1016/S0304-3770(98)00089-8 (  0) 0) |
| [30] |
王合虎, 张彦浩, 李文涛, 等. 不同栽培方式对鳗草实生苗建成和生理的影响[J]. 渔业科学进展, 2023, 44(6): 239-249. Wang H H, Zhang Y H, Li W T, et al. Effects ofdifferent cultivation methods on seedling establishment and physiology of the eelgrass Zostera marina[J]. Progress in Fishery Sciences, 2023, 44(6): 239-249. (  0) 0) |
| [31] |
于兵, 杨启文, 张彦浩, 等. 赤霉素和弱酸对鳗草种子萌发和生理特性的影响[J]. 渔业科学进展, 2023, 44(4): 26-34. Yu B, Yang Q W, Zhang Y H, et al. Effects ofgibberellin and weak acid on seed germination and physiological characteristics of the eelgrass Zostera marina[J]. Progress in Fishery Sciences, 2023, 44(4): 26-34. (  0) 0) |
| [32] |
Wen D, Xu H, Xie L, et al. Effects of nitrogen level during seed production on wheat seed vigor and seedling establishment at the transcriptome level[J]. International Journal of Molecular Sciences, 2018, 19(11): 3417. DOI:10.3390/ijms19113417 (  0) 0) |
| [33] |
李淑娴, 高莹莹, 李运红, 等. 种子含水量的测定方法及展望[J]. 种子, 2010, 29(10): 57-59, 61. Li S X, Gao Y Y, Li Y H, et al. Methold of measuring seed water content and it's expectation[J]. Seed, 2010, 29(10): 57-59, 61. (  0) 0) |
| [34] |
Hiller A, Plazin J, Van Slyke D D. A study of conditions for Kjeldahl determination of nitrogen in proteins: Description of methods with mercury as catalyst, and titrimetric and gasometric measurements of the ammonia formed[J]. The Journal of Biological Chemistry, 1948, 176(3): 1401-1420. DOI:10.1016/S0021-9258(18)57154-4 (  0) 0) |
| [35] |
Yemm E W, Willis A J. The estimation of carbohydrates in plant extracts by anthrone[J]. The Biochemical Journal, 1954, 57(3): 508-514. DOI:10.1042/bj0570508 (  0) 0) |
| [36] |
赵玉锦, 王台. 水稻种子萌发过程中α-淀粉酶与萌发速率关系的分析[J]. 植物学通报, 2001(2): 226-230. Zhao Y T, Wang T. Analysis of the relationship between α-amylase and germinating rate of rice seeds during the process of seed germination[J]. Chinese Bulletin of Botany, 2001(2): 226-230. (  0) 0) |
| [37] |
Arnon D I. Copper enzymes in isolated chloroplasts. polyphenoloxidase in Beta vulgaris[J]. Plant Physiology, 1949, 24(1): 1-15. DOI:10.1104/pp.24.1.1 (  0) 0) |
| [38] |
高俊凤. 植物生理学实验指导[M]. 北京: 高等教育出版社, 2006: 74-77. Gao J F. Experimental Guidance of Plant Physiology[M]. Beijing: Higher Education Press, 2006: 74-77. (  0) 0) |
| [39] |
Churchill A C. Growth characteristics of Zostera marina seedlings under anaerobic conditions[J]. Aquatic Botany, 1992, 43(4): 379-392. DOI:10.1016/0304-3770(92)90049-O (  0) 0) |
| [40] |
Moore K A, Orth R J, Nowak J F. Environmental regulation of seed germination in Zostera marina L. (eelgrass) in Chesapeake Bay: Effects of light, oxygen and sediment burial[J]. Aquatic Botany, 1993, 45(1): 79-91. DOI:10.1016/0304-3770(93)90054-Z (  0) 0) |
| [41] |
Hootsmans M J M, Vermaat J E, Van Vierssen W. Seed-bank development, germination and early seedling survival of two seagrass species from the Netherlands: Zostera marina L. and Zostera noltii hornem[J]. Aquatic Botany, 1987, 28(3): 275-285. (  0) 0) |
| [42] |
Pastor J, Dewey B, Johnson N W, et al. Effects of sulfate and sulfide on the life cycle of Zizania palustris in hydroponic and mesocosm experiments[J]. Ecological Applications, 2017, 27(1): 321-336. DOI:10.1002/eap.1452 (  0) 0) |
| [43] |
刘云龙, 张学雷. 盐度对大叶藻种子萌发和幼苗发育的影响[J]. 海洋学报, 2016, 38(2): 104-111. Liu Y L, Zhang X L. The effects of salinity on seed germination and seedling development of the seagrass, Zostera marina L.[J]. Haiyang Xuebao, 2016, 38(2): 104-111. (  0) 0) |
| [44] |
Jørgensen M S, Labouriau R, Olesen B. Seed size and burial depth influence Zostera marina L. (eelgrass) seed survival, seedling emergence and initial seedling biomass development[J]. PLoS One, 2019, 14(4): e0215157. DOI:10.1371/journal.pone.0215157 (  0) 0) |
| [45] |
Nakashima Y, Sonobe T, Hanada M, et al. Microbial detoxification of sediments underpins persistence of Zostera marina meadows[J]. International Journal of Molecular Sciences, 2024, 25(10): 5442. DOI:10.3390/ijms25105442 (  0) 0) |
| [46] |
Zhang Y, Xu S, Yue S, et al. Reciprocal field transplant experiment and comparative transcriptome analysis provide insights into differences in seed germination time of two populations from different geographic regions of Zostera marina L.[J]. Frontiers in Plant Science, 2022, 12: 793060. DOI:10.3389/fpls.2021.793060 (  0) 0) |
| [47] |
王明, 郭馨, 唐学玺, 等. 大叶藻种子萌发环境条件研究[J]. 海洋与湖沼, 2016, 47(3): 540-548. Wang M, Guo X, Tang X X, et al. Optimal condition for seed germination of Zostera marina[J]. Oceanologia et Limnologia Sinica, 2016, 47(3): 540-548. (  0) 0) |
| [48] |
Ma M, Cen W, Li R, et al. The molecular regulatory pathways and metabolic adaptation in the seed germination and early seedling growth of rice in response to low O2 stress[J]. Plants, 2020, 9(10): 1363. DOI:10.3390/plants9101363 (  0) 0) |
| [49] |
Zhu M, Zang Y, Zhang X, et al. Insights into the regulation of energy metabolism during the seed-to-seedling transition in marine angiosperm Zostera marina L.: Integrated metabolomic and transcriptomic analysis[J]. Frontiers in Plant Science, 2023, 14: 1130292. DOI:10.3389/fpls.2023.1130292 (  0) 0) |
| [50] |
Delefosse M, Povidisa K, Poncet D, et al. Variation in size and chemical composition of seeds from the seagrass Zostera marina—Ecological implications[J]. Aquatic Botany, 2016, 131: 7-14. DOI:10.1016/j.aquabot.2016.02.003 (  0) 0) |
| [51] |
Loreti E, Alpi A, Perata P. α-amylase expression under anoxia in rice seedlings: An update[J]. Russian Journal of Plant Physiology, 2003, 50(6): 737-743. DOI:10.1023/B:RUPP.0000003271.64810.16 (  0) 0) |
| [52] |
Damaris R N, Lin Z, Yang P, et al. The rice alpha-amylase, conserved regulator of seed maturation and germination[J]. International Journal of Molecular Sciences, 2019, 20(2): 450. DOI:10.3390/ijms20020450 (  0) 0) |
| [53] |
李桂玲, 王琦, 王金水, 等. 重金属对植物种子萌发胁迫及缓解的机制[J]. 生物技术通报, 2019, 35(6): 147-155. Li G L, Wang Q, Wang J S, et al. Mechanisms of stress and mitigation of heavy metals on seed germination of plants[J]. Biotechnology Bulletin, 2019, 35(6): 147-155. (  0) 0) |
| [54] |
Sugiura H, Hiroe Y, Suzuki T, et al. The carbohydrate catabolism of Zostera marina influenced by lower salinity during the pre-germination stage[J]. Fisheries Science, 2009, 75(5): 1205-1217. DOI:10.1007/s12562-009-0156-3 (  0) 0) |
| [55] |
孙奎香, 于遒功, 张玉凤, 等. 水分胁迫对花生种子萌发过程中贮藏物质降解的影响[J]. 中国农学通报, 2012, 28(12): 60-65. Sun K X, Yu Q G, Zhang Y F, et al. The effects of water stress on the degradation of storage materials during peanut seed germination process[J]. Chinese Agricultural Science Bulletin, 2012, 28(12): 60-65. (  0) 0) |
| [56] |
Senuma M, Dobashi S, Bando Y, et al. Overexpression of eelgrass Rare Cold Inducible 2 (RCI2) maintains chlorophyll content in Arabidopsis subjected to high salinity and dehydration[J]. Plant Stress, 2022, 6: 100116. DOI:10.1016/j.stress.2022.100116 (  0) 0) |
| [57] |
Zhang Y, Zhao P, Yue S, et al. New insights into physiological effects of anoxia under darkness on the iconic seagrass Zostera marina based on a combined analysis of transcriptomics and metabolomics[J]. Science of the Total Environment, 2021, 768: 144717. DOI:10.1016/j.scitotenv.2020.144717 (  0) 0) |
| [58] |
Xu S C, Wang P M, Wang F, et al. Responses of eelgrass seed germination and seedling establishment to water depth, sediment type, and burial depth: Implications for restoration[J]. Marine Ecology Progress Series, 2021, 678: 51-61. DOI:10.3354/meps13888 (  0) 0) |
| [59] |
Brodersen K E, Kühl M. Photosynthetic capacity in seagrass seeds and early-stage seedlings of Zostera marina[J]. New Phytologist, 2023, 239(4): 1300-1314. DOI:10.1111/nph.18986 (  0) 0) |
| [60] |
Rüdiger W. Biosynthesis of chlorophyll b and the chlorophyll cycle[J]. Photosynthesis Research, 2002, 74(2): 187-193. DOI:10.1023/A:1020959610952 (  0) 0) |
| [61] |
Voitsekhovskaja O V, Tyutereva E V. Chlorophyll b in angiosperms: Functions in photosynthesis, signaling and ontogenetic regulation[J]. Journal of Plant Physiology, 2015, 189: 51-64. DOI:10.1016/j.jplph.2015.09.013 (  0) 0) |
| [62] |
柳杰, 张沛东, 郭栋, 等. 环境因子对海草生长及光合生理影响的研究进展[J]. 水产科学, 2012, 31(2): 119-124. Liu J, Zhang P D, Guo D, et al. Research advancement in effects of environmental factors on growth and photosynthetic physiology of sea weed[J]. Fisheries Science, 2012, 31(2): 119-124. (  0) 0) |
| [63] |
Nonogaki H, Bassel G W, Bewley J D. Germination—Still a mystery[J]. Plant Science, 2010, 179(6): 574-581. DOI:10.1016/j.plantsci.2010.02.010 (  0) 0) |
| [64] |
孙燕. 大叶藻(Zostera marina L.)种子下胚轴在幼苗生长期的作用及其机制[D]. 青岛: 中国海洋大学, 2013. Sun Y. Effeet of Hypocotyl in Zostera marina L. Seed on Early Seedling Growth[D]. Qingdao: Ocean University of China, 2013. (  0) 0) |
| [65] |
江文杰, 杨钦淞, 李国雷, 等. 栓皮栎种子贮藏物质和内源激素对萌发成苗的影响[J]. 北京林业大学学报, 2024, 46(1): 19-26. Jiang W J, Yang Q S, Li G L, et al. Effects of storage substances and endogenous hormones on seed germination and seedling formation of Ouercus variabilis[J]. Journal of Beijing Forestry University, 2024, 46(1): 19-26. (  0) 0) |
| [66] |
Pan T, Lin L, Liu Q, et al. In situ degradation and characterization of endosperm starch in waxy rice with the inhibition of starch branching enzymes during seedling growth[J]. International Journal of Molecular Sciences, 2018, 19(11): 3397. DOI:10.3390/ijms19113397 (  0) 0) |
2. Joint Research Center for Conservation, Restoration & Sustainable Utilization of Marine Ecology, Ocean University of China-China State Shipbuilding Corporation Environmental Development Company Limited, Qingdao 266100, China;
3. Observation and Research Station of Yellow-Bohai Seas Temperate Seagrass Bed Ecosystem, Ministry of Natural Resources, Qingdao 266100, China;
4. China Environmental Protection Foundation, Beijing 100062, China
 2025, Vol. 55
2025, Vol. 55


