2. 中国海洋大学海洋环境与生态教育部重点实验室,山东 青岛 266100
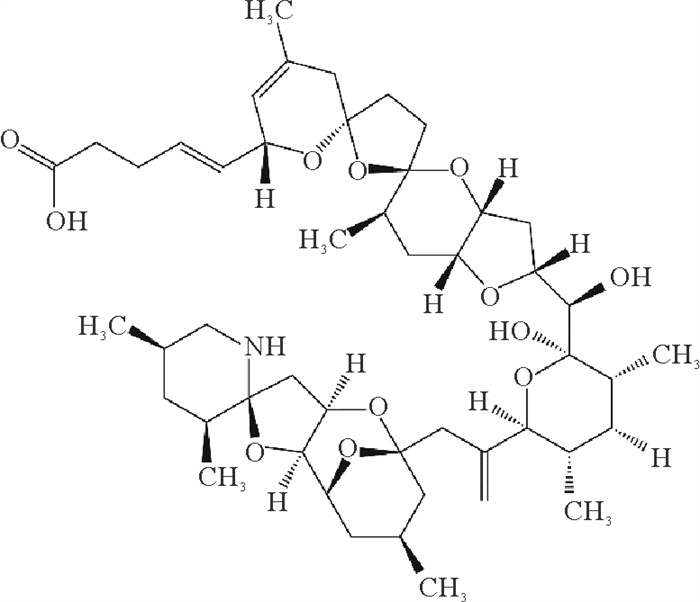
近年,随着有毒赤潮在全球邻海国家或地区近岸海域的频繁发生,藻毒素严重威胁贝类等水产品安全和人类健康。氮杂螺环酸(Azaspiracids, AZAs)是一种含氮且具独特螺环结构的聚醚类藻毒素(见图 1),目前已发现60多种AZA的同系物[1],其中AZA-1、AZA-2和AZA-3是常见组分。AZAs主要由环胺藻属(Azadinium spp.)和甲藻Amphidoma languida产生,其中常见的环胺藻属主要包括腹孔环胺藻(A. poporum)、具刺环胺藻(A. spinosum)和右侧环胺藻(A. dexteroporum)等[2-6]。环胺藻在法国、爱尔兰、朝鲜、中国以及阿根廷等国家沿海广泛分布。AZAs毒素通过食物链传递可在扇贝、贻贝、牡蛎等贝类组织中富集[7],威胁消费者健康和贝类养殖业的持续发展。消费者一旦误食含高浓度AZAs的贝类,几小时内可观察到急性中毒症状,出现恶心、呕吐、严重腹泻和胃肠部痉挛等。然而,目前有关AZAs对人体的作用机制尚不明确。为了保护消费者健康,欧洲食品安全局将贝类等水产品中AZA-1、AZA-2和AZA-3的总含量控制标准设定为160 μg·kg-1贝肉,其中AZA-1、AZA-2和AZA-3的毒性当量因子(TEF)分别为1、1.8和1.4[8]。研究还发现,AZAs对多种细胞具有细胞毒性,毒性大小与作用时间、毒素浓度有关,并且AZA-1、AZA-2的细胞毒性作用不可逆[8]。
|
图 1 AZA-2毒素的化学结构 Fig. 1 Chemical structure of AZA-2 |
由于藻毒素标准物质数量有限,价格昂贵,严重制约了藻毒素相关科学研究的进展。目前全球商业化的藻毒素标准物质主要由加拿大国家研究委员会(National research council, Canada, CNRC)和西班牙CIFGA实验室等少数几个机构提供,中国针对海洋有毒藻资源的开发非常有限,商业化的藻毒素标准品极为缺乏。国际上许多海洋生物毒素标准物质无法通过化学合成途径获取,主要以室内培养的有毒藻为毒素来源,通过分离纯化获得标准物质,但该途径面临产毒藻规模化培养的关键问题。目前关于环境因子对腹孔环胺藻生长和产毒影响的研究较少。Jauffrais等[9]报道了具刺环胺藻可以在温度10~26 ℃、盐度30~40和光照强度50~250 μmol·m-2·s-1的条件下生长,发现盐度35、温度18~22 ℃和通气时藻细胞密度最大。Li等[10]报道低浓度(0和3.6 μmol·L-1)磷酸盐会抑制腹孔环胺藻AZDY06的生长,促进稳定生长期单位细胞AZA-2的产量,而低浓度硝酸盐(88.2 μmol·L-1)对腹孔环胺藻的生长无明显影响,减少了稳定生长期单位细胞AZA-2的含量。Kilcoyne等[11]报道10和18 ℃培养条件下具刺环胺藻藻细胞的最终密度相似,而10 ℃时单位细胞毒素产量更高,低光暗比(8 h∶16 h)下藻细胞密度低,高光暗比(16 h∶8 h)下单位细胞毒素含量略高。本研究选择一株中国南海海域分离的腹孔环胺藻AZDY06,探讨不同温度、盐度和光照强度培养条件下微藻的生长、光合作用和产毒情况,为后续毒素标准物质的制备提供充足的毒素来源。
1 材料与方法 1.1 腹孔环胺藻的培养本研究使用的腹孔环胺藻(A. poporum, AZDY06)分离自中国南海,可产生AZA-2毒素。将取自青岛石老人海水浴场的新鲜海水(盐度32)过0.45 μm混合纤维滤膜,置于500 mL锥形瓶中,在121 ℃下高压灭菌20 min,待海水冷却后添加不含硅酸盐的L1培养液后,接入腹孔环胺藻,使初始浓度达到5 000 cells·mL-1,在温度22 ℃、光照强度100 μmol·m-2·s-1、光暗比为12 h∶12 h的光照培养箱进行培养。
1.2 实验设计本研究主要考察温度、盐度和光照强度对腹孔环胺藻生长及产毒水平的影响。腹孔环胺藻的室内培养温度常设置为18 ℃。因此,本研究在18 ℃的基础上设置了22和14 ℃,以探究温度变化对微藻生长和产毒影响。天然海水的盐度为30~32,本研究以盐度30为基础,分别上调和下调两个盐度梯度探究低盐(22、26)和高盐(34、38)对微藻生长和产毒的影响。室内培养海洋微藻的光照强度一般为100 μmol·m-2·s-1,本研究在此基础上调和下调光照强度,探究光照强度对微藻生长和产毒的影响。
考察不同温度对腹孔环胺藻的生长及产毒水平的影响时,在批次培养中设计22、18和14 ℃三个实验组。分别将三个光照培养箱的温度设置为22、18和14 ℃,其他参数不变,将微藻放在光照培养箱中培养,每组设置3个平行样。
考察不同盐度对腹孔环胺藻的生长与产毒水平的影响时,在批次培养中设计22、26、30、34和38五个实验组。将盐度为32的新鲜海水在高压灭菌锅中蒸煮20 min,冷却后海水盐度为38。然后采用蒸馏水将海水盐度分别稀释至22、26、30、34和38。分别取340 mL不同盐度的海水置于500 mL锥形瓶中,灭菌后添加培养液,接入适量的腹孔环胺藻细胞,在常规条件下培养,每组设3个平行样。
考察不同光照强度对腹孔环胺藻生长与产毒水平的影响时,在批次培养中设置80、100和120 μmol·m-2·s-1三个实验组。采用三组智能LED灯管装置设置相应的光照强度,温度为22 ℃,光暗比(L∶D)为12∶12,每组设3个平行样。
上述各组实验共培养28 d,期间每隔一天取样,用流式细胞仪(Accuri C6 Plus,美国BD公司)记录藻密度,用浮游植物荧光仪(PHYTO-PAM,德国Walz公司)测定光合作用参数,并在指数生长初期、指数生长后期,稳定生长期各取20 mL藻液,测定藻细胞的胞内外毒素情况。
1.3 生长曲线与光合参数的测定计数前充分摇匀培养液,移取1 mL藻液于1.5 mL离心管中,混匀后在流式细胞仪上计数,进样量为50 μL,选择多甲藻黄素-叶绿素-蛋白复合物(Percp-H)通道对藻细胞进行计数。计数时每组取三个平行样,每个平行样计数两次,取最终平均值,计算藻密度,并绘制生长曲线。
腹孔环胺藻的比增长率μ通过式(1)计算:
| $ \mu=\frac{\left(\ln N_t-\ln N_0\right)}{t-t_0} 。$ | (1) |
其中:N0表示初始的藻细胞密度,cells·mL-1;Nt表示t天后的藻细胞密度,cells·mL-1。
取1.5 mL藻液加入至浮游植物荧光仪的石英样品管中,暗适应10 min后放入样品室中,测定Fv/Fm及叶绿素a含量。
1.4 AZA-2毒素的提取采用真空抽滤器,将20 mL藻液过0.7 μm的玻璃纤维滤膜,细胞用于胞内毒素分析,滤液用于胞外毒素分析。
1.4.1 胞内毒素将过滤有藻细胞的滤膜剪碎,转移至10 mL离心管中并加入3 mL甲醇,涡旋混合1 min。首先将离心管在液氮中反复冻融3次,每次5 min;随后于冰水浴条件下超声破碎10 min,5 580g条件下离心10 min,将上清液转移至10 mL容量瓶中;再向离心管中加入3 mL甲醇,涡旋混匀后,重复离心两次,将上清液合并后,用甲醇定容。取1 mL样品,过0.22 μm尼龙滤膜于1.5 mL样品瓶中,-18 ℃保存,待液相色谱-质谱联用仪进行分析。
1.4.2 胞外毒素采用Oasis-HLB SPE柱(60 mg, 3 mL)富集培养液中胞外毒素,具体操作步骤如下:首先,依次用3 mL甲醇和3 mL 20%甲醇水溶液(v/v)活化和平衡SPE柱(约1 mL·min-1);然后,将20 mL培养液配制成含有20%甲醇的上样液加入SPE柱内(约0.5 mL·min-1);随后,用3 mL 20%甲醇水溶液进行淋洗(约1 mL·min-1),除去盐分;最后,用3 mL甲醇进行洗脱(约1 mL·min-1),收集洗脱液于5 mL容量瓶中,100%甲醇定容。取1 mL样品,过0.22 μm尼龙滤膜于1.5 mL样品瓶中,-18 ℃保存,待LC-MS/MS分析。
1.5 LC-MS/MS分析采用高效液相色谱(Ultimate 3000, Thermo)串联复合线性离子阱质谱(Qtrap 4500, AB SCIEX)联用仪分析AZA-2毒素。应用X-BridgeTM C18柱(150 mm×3 mm i.d., 5 μm)对样品进行分离,柱温为35 ℃,流动相A为超纯水,流动相B为90%乙腈水溶液,两相中均含有6.7 mmol·L-1的NH4OH,pH为11,流速为0.3 mL·min-1,进样量为5 μL,ESI离子源,气体温度为350 ℃。采用梯度洗脱的方式进行目标分析物的洗脱,洗脱梯度:0~1 min: 20% B;1~7 min: 90% B;7~9 min: 90% B;9~10 min: 20% B;10~11 min: 20% B。采用正离子模式下的MRM方法对毒素进行定量分析,定量离子对为m/z 856.5->838.5,定性离子对为m/z 856.5->672.4。
1.6 数据处理所有数据均表示为平均值±标准差(SD),采用IBM SPSS统计软件(Version 22)进行单因素方差分析(ANOVA)和最小显著性差异(LSD)检验(α=0.05)分析,GraphPad prism 8绘制数据结果。
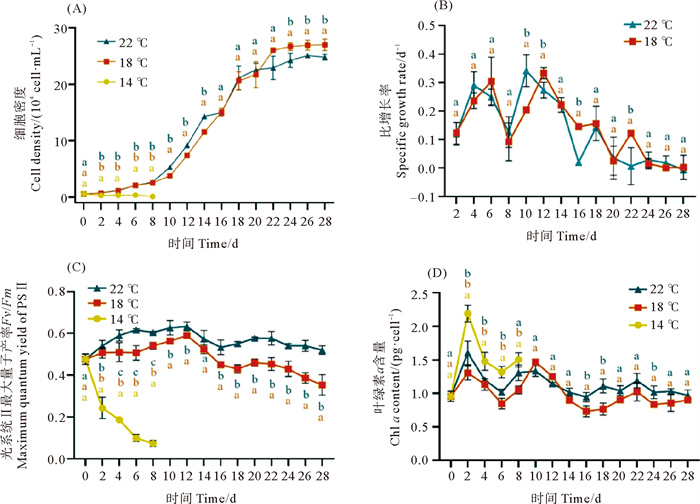
2 实验结果 2.1 不同温度对腹孔环胺藻生长和产毒的影响在不同温度条件下腹孔环胺藻的生长曲线如图 2(A)所示。结果发现,14 ℃条件下显著抑制了微藻的生长(p < 0.05),自接入藻液后藻密度持续下降,8 d时藻细胞几乎全部死亡。在18和22 ℃条件下,微藻在第10天时进入指数生长期,两个温度下指数生长期的最大比生长速率分别为0.33和0.34 d-1,无显著性差异(p>0.05)(见图 2(B))。18和22 ℃实验组中微藻基本在第22天后进入稳定生长期,第24—28天18 ℃条件下藻密度显著高于22 ℃(p < 0.05),藻密度在第28天时分别达到2.7×105和2.5×105 cells·mL-1。
|
( 不同字母代表存在显著差异p < 0.05。Different letters indicate that the difference is significant at 0.05 level. ) 图 2 不同温度条件下腹孔环胺藻AZDY06的生长曲线(A)、比增长率(B)、光系统Ⅱ最大量子产率(Fv/Fm)(C)和叶绿素a含量(Chl a)(D) Fig. 2 Growth curves (A), specific growth rate (B), maximum quantum yield of PSII (Fv/Fm) (C), and chlorophyll a content (D) of A. poporum AZDY06 at different temperatures |
在18和22 ℃组中,微藻光系统Ⅱ最大量子产率Fv/Fm随培养时间先增加后减少(见图 2(C)),在一定范围内,温度越高最大光能利用效率越高;单位细胞叶绿素a含量在整个生长周期呈上下波动的变化趋势,总体来看22 ℃单位细胞叶绿素a含量在第8、16、18和24天显著高于18 ℃组(p < 0.05)(见图 2(D)),说明22 ℃条件下藻细胞光合效率更高。在14 ℃条件下藻细胞无法正常生长,光能利用效率和叶绿素a含量持续下降。
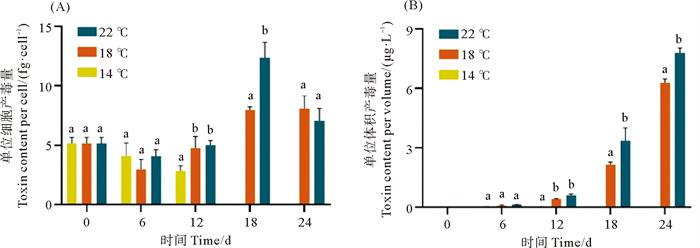
在14 ℃条件下,单位细胞产毒量逐渐减少,这与低温环境胁迫有关。在18和22 ℃条件下,单位细胞AZA-2的含量呈先降低后逐渐增加的趋势,单位细胞产毒量分别在指数生长后期的第24和18天时达到最大值,分别为8和12 fg·cell-1,含量差异显著(p < 0.05)(见图 3(A))。在稳定生长后期(第24天),单位细胞产毒量在22 ℃条件下出现了显著降低(p < 0.05),而18 ℃条件下无显著变化(p>0.05)。稳定生长期后,随着藻细胞不断主动向胞外分泌毒素,使胞外毒素占比逐渐增大(见表 1)。随着培养时间的延长,单位体积中AZA-2的含量不断增加,尤其是进入稳定生长期后毒素含量快速增加。在18和22 ℃条件下,第24天时单位体积中AZA-2的含量分别达到6和8 μg·L-1(见图 3(B))。在第18天和24天时22 ℃条件下单位体积中藻细胞合成的毒素含量明显高于18 ℃条件下的合成量(p < 0.05)。
|
( 不同字母代表存在显著差异p < 0.05。Different letters indicate that the difference is significant at 0.05 level. ) 图 3 不同温度条件下腹孔环胺藻AZDY06的单位细胞产毒量(A)和单位体积产毒量(B) Fig. 3 Toxin production per cell (A) and per unit volume (B) of A. poporum AZDY06 at different temperature |
|
|
表 1 不同培养条件下腹孔环胺藻AZDY06胞内毒素占总毒素的比例 Table 1 Table 1 Percentage of intracellular toxins to total toxins in A. poporum AZDY06 under different culture conditions |
不同盐度条件下腹孔环胺藻表现出类似的生长趋势(见图 4(A))。总体上,微藻在第8天时开始进入指数生长期,随后在第24天进入稳定生长期。在盐度为26时,微藻的生长状况相对最好,最大藻密度可达3×105 cells·mL-1,其次为盐度34、30、38和22。最低盐度和最高盐度生长状况较差,最大藻密度分别为2×105和1.7×105 cells·mL-1,比盐度26组最大藻密度降低了20%和25%。不同盐度处理组细胞比增长速率均大于0,所有盐度处理组在第6天呈现出最大的比增长速率,总体呈现出先增加后下降的趋势,比增长率最大值可达0.57 d-1(见图 4(B)),第12、16、18、20、22、26、28天比增长率在各组之间无显著差异(p>0.05)。
|
( 不同字母代表存在显著差异p < 0.05。Different letters indicate that the difference is significant at 0.05 level. ) 图 4 不同盐度条件下腹孔环胺藻AZDY06的生长曲线(A)、比增长率(B)、光系统Ⅱ最大量子产率(Fv/Fm)(C)和叶绿素a含量(Chl a)(D) Fig. 4 Growth curves (A), specific growth rate (B), maximum quantum yield of PSII (Fv/Fm) (C), and chlorophyll a (D) of A. poporum AZDY06 at different salinities |
不同盐度处理组腹孔环胺藻Fv/Fm随培养时间延长先增加到最高值后围绕其上下波动(见图 4(C)),藻细胞接种6 d后开始进入指数生长期,其到稳定生长期单位细胞叶绿素含量都比较稳定(见图 4(D))。
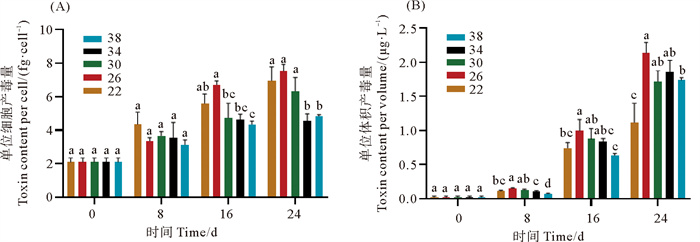
在不同盐度条件下,在整个生长周期微藻的单位细胞产毒量呈现出稳定上升的趋势(见图 5(A))。在盐度为22、26和30时,微藻在第24天时单位细胞产毒量最大,且与高盐度组(34和38)有显著差异(p < 0.05),说明AZDY06在低盐度条件下单位细胞合成的毒素更多。在微藻培养过程中,单位体积中AZA-2的含量不断增加,尤其是进入指数生长期中期后毒素含量快速增加。总体来看,盐度为26时单位体积藻液中毒素含量最高,在第24天时达到2.2 μg·L-1(见图 5(B))。
|
( 不同字母代表存在显著差异p < 0.05。Different letters indicate that the difference is significant at 0.05 level. ) 图 5 不同盐度腹孔环胺藻AZDY06的单位细胞产毒量(A)和单位体积产毒量(B) Fig. 5 Toxin production per cell (A) and per unit volume (B) of A. poporum AZDY06 at different salinities |
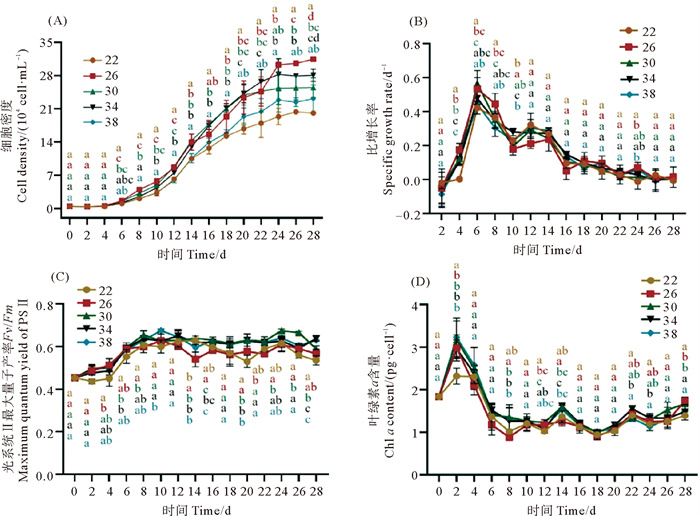
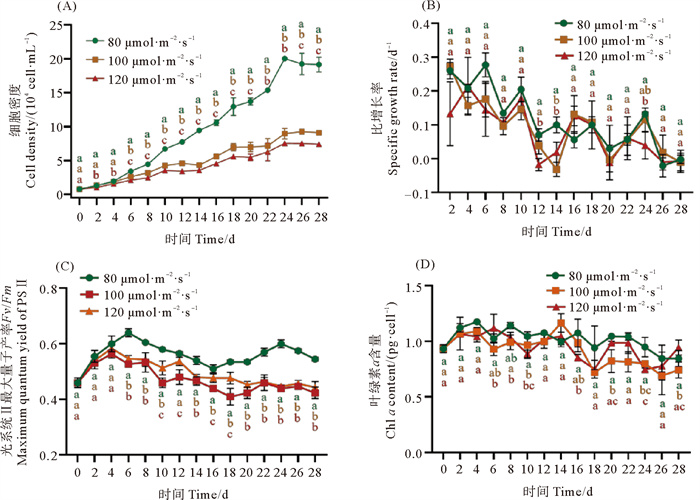
随着光照强度的增加,藻细胞生长逐渐受到抑制(见图 6(A)),光照强度为80 μmol·m-2·s-1时藻细胞生长最好,最大藻密度达到2×105 cells·mL-1,而光照强度为120 μmol·m-2·s-1时藻细胞生长情况最差,仅为1×105 cells·mL-1,且100和120 μmol·m-2·s-1光照强度条件下藻细胞分裂缓慢,生长趋势平缓。从第6天开始,除第18、22和24天外,其余测定天数不同光照强度处理组藻密度均差异显著(p < 0.05)。不同光照强度处理组比增长速率总体呈现下降的趋势,第6天80 μmol·m-2·s-1处理组比增长速率最大(0.28 d-1),到第26天比增长速率接近0,比增长速率在第12、14、24天有显著性差异(p < 0.05),其中第12天120 μmol·m-2·s-1处理组比增长速率显著低于其余两组,第14天80 μmol·m-2·s-1处理组比增长速率显著高于其余两组,第24天80 μmol·m-2·s-1处理组比增长速率显著高于120 μmol·m-2·s-1处理组(p < 0.05)(见图 6(B))。
|
( 不同字母代表存在显著差异p < 0.05。Different letters indicate that the difference is significant at 0.05 level. ) 图 6 不同光照强度条件下腹孔环胺藻AZDY06的生长曲线(A)、比增长率(B)、光系统Ⅱ最大量子产率(Fv/Fm)(C)和叶绿素a含量(Chl a)(D) Fig. 6 Growth curves (A), specific growth rate (B), maximum quantum yield of PSII (Fv/Fm) (C), and chlorophyll a (D) of A. poporum AZDY06 at different light intensities |
不同光照强度处理组腹孔环胺藻Fv/Fm随培养时间延长先增加后减少,80 μmol·m-2·s-1时最大光能利用效率最高,其次为120和100 μmol·m-2·s-1,表明腹孔环胺藻在低光强下光能利用效率更高,过高的光强会抑制藻细胞光能利用效率(见图 6(C))。单位细胞叶绿素a含量在整个生长周期上下波动,80 μmol·m-2·s-1光照强度在第24天显著高于其他处理组单位细胞叶绿素a含量(见图 6(D))。
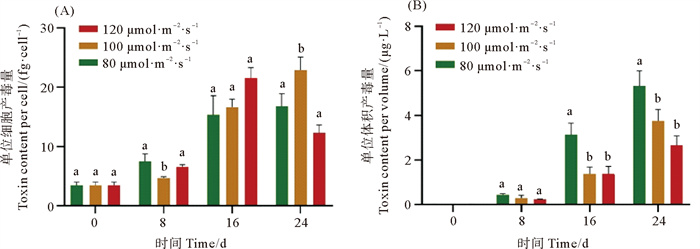
在微藻生长的前16天,不同光照强度下单位细胞产毒量不断增加。与第16天相比,第24天时80 μmol·m-2·s-1组中单位细胞产毒量无显著性差异(p>0.05),100 μmol·m-2·s-1组增加了37%,而120 μmol·m-2·s-1组降低了43%(见图 7(A))。120 μmol·m-2·s-1条件下在稳定生长期后期受光照强度影响其细胞受到损伤,藻细胞形态已经发生变化,单位细胞产毒量减少。
|
( 不同字母代表存在显著差异p < 0.05。Different letters indicate that the difference is significant at 0.05 level. ) 图 7 不同光照强度腹孔环胺藻AZDY06的单位细胞(A)和单位体积产毒量(B) Fig. 7 Toxin production per cell (A) and per unit volume (B) of A. poporum AZDY06 at different light intensities |
在微藻培养过程中,不同光照强度组中单位体积中AZA-2含量不断增加,尤其是进入指数生长期中期后毒素含量快速增加。第16和24天时光照强度为80 μmol·m-2·s-1组中单位体积藻液中毒素含量显著高于其他两组(p < 0.05)。其中第24天时,80、100和120 μmol·m-2·s-1组单位体积藻液中毒素含量分别达到6、4和3 μg·L-1(见图 7(B))。
3 讨论本研究中,腹孔环胺藻在14 ℃培养条件下生长受到了抑制,18和22 ℃培养条件下生长状况良好,指数生长期持续约14 d。前期研究报道,具刺环胺藻在10~26 ℃培养条件下藻细胞均较好生长[9],说明不同种环胺藻对温度的适应范围存在差异。最大PSII光化学量子产率(Fv/Fm)通常用于指示藻类的生理和光合作用效率。22 ℃与其他温度条件相比,藻细胞和单位细胞叶绿素a含量最大,叶绿素a会增加藻细胞光捕获能力从而促进细胞生长[12-13]。当藻细胞暴露于低温时,光合速率迅速降低,剩余电子被转移到O2生成活性氧(ROS)[14]。正常生理状态下Fv/Fm较稳定,保持在0.65左右[15]。在本研究中,14 ℃培养条件下藻细胞Fv/Fm逐渐降低至0.073。
本研究中,腹孔环胺藻在盐度为22~38的培养条件下均能生长,Fv/Fm值均稳定在0.65左右,各处理组之间无显著差异,说明该藻株对盐度具有较宽的适应范围,适于在近海淡咸水混合区生长。但不同盐度条件下腹孔环胺藻的密度存在差异,在稳定生长期阶段藻密度在盐度26组中最高,其次分别为盐度34、30、38和22组。盐度过高和过低均不利于腹孔环胺藻的生长,前期研究也发现盐度40培养条件下具刺环胺藻的藻密度明细低于盐度30、32和35组中的藻密度[11]。盐度对腹孔环胺藻生长的影响主要归因于细胞渗透压的变化,从而影响代谢速率和离子转运[16]。相比于温度和光照强度,盐度胁迫更能刺激细胞的生长,即使在盐度22条件下最大藻密度藻细胞与最适光强80 μmol·m-2·s-1最大藻密度一致。在22 ℃和盐度30条件下,藻细胞获得最大比生长速率(0.57 d-1)。
本研究中随着光照强度的增加,Fv/Fm不同程度地连续降低,高光照强度下光合效率的下降表明高光照强度抑制其生长[17],有研究表明高光照强度可以诱导微藻损伤和活性氧的产生[18]。在低光照强度下藻细胞生长更好,表明当藻细胞暴露于低光照强度时,藻细胞具有光驯化能力,即藻细胞通过积累更多的叶绿素a以弥补其光捕获能力[19],这与Azadinium caudatum藻株在低光照强度下生长更好的现象一致[20]。Jauffrais等[9]发现50~250 μmol·m-2·s-1光照强度下具刺环胺藻没有表现出光抑制生长的迹象,最高光照强度下微藻的生长速率略有下降。此处需要说明的是,实验过程中缺少足够的光照培养箱,不同光照强度的微藻培养是在恒温的藻种室进行的,腹孔环胺藻相应的生长速率和最大细胞密度均明显低于其在光照培养箱中的状态指标。
本研究显示,不同培养条件下藻细胞的单位体积毒素产量在稳定期增加,毒素的合成和释放可能是产毒藻类防御的重要组成部分[24]。从指数生长期到稳定生长期,腹孔环胺藻产生的AZA-2单位细胞毒素产量随着生长速率的降低而显著增加,并在稳定生长期达到峰值,这在不同温度、盐度和光照条件下表现出相同的规律,这与之前研究中生长速率降低增加毒素合成的结果一致[25],且与产聚醚类藻毒素的其他甲藻相似[25-27]。指数生长期细胞毒素含量较低可能是由于细胞的快速分裂不利于细胞内毒素的积累[28]。毒素合成对盐度变化的反应很复杂,在不同盐度处理组与温度和光照强度相比最大单位细胞产毒量更低,这可能是由于细胞更多能量用于细胞生长导致毒素合成减少。为了适应更高的盐度(38),更多的营养物质和能量被用来增强渗透调节,导致毒素产生减少[29]。在本研究的3个温度处理组中,22 ℃获得更高的毒素产量,在此温度条件下设置不同的光照强度,藻密度的比增长率与单位细胞AZA-2毒素的合成呈相反的变化趋势,这可能是藻细胞对环境压力的反应或由于生长速率的普遍降低导致毒素积累。具刺环胺藻3D9藻株单位细胞AZA毒素产量受到低温的显著影响,在10 ℃时单位细胞产毒量为220 fg·cell-1,比在18~26 ℃之间的产毒量高20倍[11]。许多研究表明温度也是影响麻痹性贝毒产毒藻毒素合成的主要因素[29-31],低温促进麻痹性贝毒前体精氨酸的积累从而促进麻痹性贝毒的生物合成[32]。本研究中稳定生长期细胞内毒素逐渐释放到胞外,Dai等[27]发现腹孔环胺藻(NWFSC1011和NWFSC1018)进入稳定生长期后胞外毒素占比明显增加。在稳定生长期,单位细胞毒素产量高通常与磷酸盐耗竭有关[33],这与磷限制增加AZDY06的AZA-2毒素合成结果一致[10]。
将前面所有处理组的腹孔环胺藻AZDY06在指数生长期和稳定生长期的胞内毒素占培养体系中全部毒素的比例进行汇总比较(见表 1),发现胞内AZA-2毒素占总毒素的比例在不同实验组中差异较大。尝试分析了不同实验组中胞内毒素占比与胞内毒素含量之间可能的相关性,发现不同处理组在同一生长时期并未呈现明显相关性。但在指数生长后期,不同盐度和光照强度条件下的单位细胞产毒量与胞内毒素占总毒素的比例呈负相关(p=0.058, R2=0.951 3),说明随着批次培养时间的延长藻细胞分裂活跃度降低,此时随着单位细胞内毒素含量的增加,越来越多的毒素释放至胞外,使得胞内毒素占比降低。当微藻进入稳定生长期后,藻细胞胞外毒素含量不断增加,胞外毒素占总毒素的比例最高可达78%,因此在毒素提取时应与胞内毒素一起收集。
当然,受制于实验室空间和光照培养箱数量条件的限制,本研究未能采用正交实验或响应面分析法设计不同温度、盐度和光照强度的影响因子组合实验,采用单因素分析法初步探究了不同培养条件对腹孔环胺藻生长和产毒的影响。实际培养过程中不同环境因子之间的耦合作用如何,尚有待深入研究。
4 结论(1) 14 ℃培养条件下腹孔环胺藻的生长受到抑制,18和22 ℃培养条件下微藻生长良好。在稳定生长期,18 ℃下藻细胞的密度最大,22 ℃下单位体积AZA-2产毒量最多。
(2) 在盐度为22~38的培养条件下,腹孔环胺藻生长良好。相比于其他几个盐度组,盐度为26时微藻的藻密度、单位细胞和单位体积AZA-2产毒量最高,且均随着培养时间的延长不断增大。
(3) 在80、100和120 μmol·m-2·s-1三组不同光照强度培养条件下,80 μmol·m-2·s-1组中腹孔环胺藻生长状况最好,高光强降低藻细胞的光能利用效率从而抑制细胞生长。三组不同光照强度培养条件下,单位细胞毒素产量在指数生长期均逐渐增加。
(4) 在温度22 ℃、盐度26、光强80 μmol·m-2·s-1条件下获得了最大的单体体积毒素产量。在稳定生长后期胞外毒素含量占总毒素含量的比例最高可达78%,因此在毒素提取时应当与胞内毒素一起收集。
| [1] |
Mudge E M, Miles C O, Hardstaff W R, et al. Fatty acid esters of azaspiracids identified in mussels (Mytilus edulis) using liquid chromatography-high resolution mass spectrometry[J]. Toxicon-X, 2020, 8: 100059. DOI:10.1016/j.toxcx.2020.100059 (  0) 0) |
| [2] |
Tillmann U, Salas R, Gottschling M, et al. Amphidoma languida sp. nov. (Dinophyceae) reveals a close relationship between Amphidoma and Azadinium[J]. Protist, 2012, 163(5): 701-719. DOI:10.1016/j.protis.2011.10.005 (  0) 0) |
| [3] |
Tillmann U, Elbraechter M, Krock B, et al. Azadinium spinosum gen. et sp. nov. (Dinophyceae) identified as a primary producer of azaspiracid toxins[J]. European Journal of Phycology, 2009, 44(1): 63-79. DOI:10.1080/09670260802578534 (  0) 0) |
| [4] |
Tillmann U, Jaen D, Fernandez L, et al. Amphidoma languida (Amphidomatacea, Dinophyceae) with a novel azaspiracid toxin profile identified as the cause of molluscan contamination at the Atlantic coast of southern Spain[J]. Harmful Algae, 2017, 62: 113-126. DOI:10.1016/j.hal.2016.12.001 (  0) 0) |
| [5] |
Luo Z, Krock B, Mertens K N, et al. Morphology, molecular phylogeny and azaspiracid profile of Azadinium poporum (Dinophyceae) from the Gulf of Mexico[J]. Harmful Algae, 2016, 55: 56-65. DOI:10.1016/j.hal.2016.02.006 (  0) 0) |
| [6] |
Krock B, Tillmann U, John U, et al. Characterization of azaspiracids in plankton size-fractions and isolation of an azaspiracid-producing dinoflagellate from the North Sea[J]. Harmful Algae, 2009, 8(2): 254-263. DOI:10.1016/j.hal.2008.06.003 (  0) 0) |
| [7] |
Ozawa M, Uchida H, Watanabe R, et al. Azaspiracid accumulation in Japanese coastal bivalves and ascidians fed with Azadinium poporum producing azaspiracid-2 as the dominant toxin component[J]. Toxicon, 2023, 226: 107069. DOI:10.1016/j.toxicon.2023.107069 (  0) 0) |
| [8] |
European Food Safety Authority. Opinion of the scientific panel on contaminants in the food chain on a request from the European Commission on marine biotoxins in shellfish azaspiracids group[J]. The European Food Safety Authority Journal, 2008, 6(10): 1-52. (  0) 0) |
| [9] |
Jauffrais T, Sechet V, Herrenknecht C, et al. Effect of environmental and nutritional factors on growth and azaspiracid production of the dinoflagellate Azadinium spinosum[J]. Harmful Algae, 2013, 27: 138-148. DOI:10.1016/j.hal.2013.05.009 (  0) 0) |
| [10] |
Li A, Jiang B, Chen H, et al. Growth and toxin production of Azadinium poporum strains in batch cultures under different nutrient conditions[J]. Ecotoxicology and Environmental Safety, 2016, 127: 117-126. DOI:10.1016/j.ecoenv.2016.01.017 (  0) 0) |
| [11] |
Kilcoyne J, McCoy A, Burrell S, et al. Effects of temperature, growth media, and photoperiod on growth and toxin production of Azadinium spinosum[J]. Marine Drugs. DOI:10.3390/md17090489 (  0) 0) |
| [12] |
Hui W, Zhang B, Song X, et al. High antioxidant capability interacts with respiration to mediate two Alexandrium species growth exploitation of photoperiods and light intensities[J]. Harmful Algae, 2019, 82: 26-34. DOI:10.1016/j.hal.2018.12.008 (  0) 0) |
| [13] |
Li G, Talmy D, Campbell D A. Diatom growth responses to photoperiod and light are predictable from diel reductant generation[J]. Journal of Phycology, 2017, 53(1): 95-107. DOI:10.1111/jpy.12483 (  0) 0) |
| [14] |
Zhang H, Gu B, Zhou Y, et al. Multi-omics profiling reveals resource allocation and acclimation strategies to temperature changes in a marine dinoflagellate[J]. Applied and Environmental Microbiology, 2022, 88(17): e01213-22. (  0) 0) |
| [15] |
王帅, 梁英. 盐胁迫对盐生杜氏藻生长及叶绿素荧光特性的影响[J]. 中国海洋大学学报(自然科学版), 2015, 45(3): 33-38. Wang S, Liang Y. Effects of salt stress on the growth and chlorophyll fluorescence of Dunaliella salina[J]. Periodical of Ocean University of China, 2015, 45(3): 33-38. DOI:10.16441/j.cnki.hdxb.20140045 (  0) 0) |
| [16] |
Quynh T N B, Kim H, Ki J. Low salinity causes oxidative stress and modulates specific antioxidant gene expression in the toxic dinoflagellate Alexandrium pacificum[J]. Journal of Applied Phycology, 2022, 34(5): 2437-2447. DOI:10.1007/s10811-022-02813-z (  0) 0) |
| [17] |
Songserm R, Nishiyama Y, Sanevas N. Light influences the growth, pigment synthesis, photosynthesis capacity, and antioxidant activities in Scenedesmus falcatus[J]. Scientifica, 2024, 2024: 1898624. (  0) 0) |
| [18] |
David H, Laza-Martinez A, Kromkamp J C, et al. Physiological response of Prorocentrum lima (Dinophyceae) to varying light intensities[J]. Fems Microbiology Ecology. DOI:10.109315emsec/fix166 (  0) 0) |
| [19] |
Navarro J M, Munoz M G, Contreras A M. Temperature as a factor regulating growth and toxin content in the dinoflagellate Alexandrium catenella[J]. Harmful Algae, 2006, 5(6): 762-769. DOI:10.1016/j.hal.2006.04.001 (  0) 0) |
| [20] |
Tillmann U, Krock B, Taylor B B. Azadinium caudatum var. margalefii, a poorly known member of the toxigenic genus Azadinium (Dinophyceae)[J]. Marine Biology Research, 2014, 10(10): 941-956. DOI:10.1080/17451000.2013.866252 (  0) 0) |
| [21] |
Takahashi K, Lum W M, Benico G, et al. Toxigenic strains of Azadinium poporum (Amphidomataceae, dinophyceae) from Japan and Vietnam, with first reports of A. poporum (ribotype A) and A. trinitatum in Asian Pacific[J]. Phycological Research, 2021, 69(3): 175-187. DOI:10.1111/pre.12455 (  0) 0) |
| [22] |
Fu Z, Piumsomboon A, Punnarak P, et al. Diversity and distribution of harmful microalgae in the Gulf of Thailand assessed by DNA metabarcoding[J]. Harmful Algae, 2021, 106: 102063. DOI:10.1016/j.hal.2021.102063 (  0) 0) |
| [23] |
Gu H, Zeng N, Liu T, et al. Morphology, toxicity, and phylogeny of Alexandrium (dinophyceae) species along the coast of China[J]. Harmful Algae, 2013, 27: 68-81. DOI:10.1016/j.hal.2013.05.008 (  0) 0) |
| [24] |
Feng L, Sun X, Zhu F, et al. Nanoplastics promote microcystin synthesis and release from cyanobacterial Microcystis aeruginosa[J]. Environmental Science & Technology, 2020, 54(6): 3386-3394. (  0) 0) |
| [25] |
Grzebyk D, Béchemin C, Ward C J, et al. Effects of salinity and two coastal waters on the growth and toxin content of the dinoflagellate Alexandrium minutum[J]. Journal of Plankton Research, 2003, 25(10): 1185-1199. DOI:10.1093/plankt/fbg088 (  0) 0) |
| [26] |
Pan Y, Cembella A D, Quilliam M A. Cell cycle and toxin production in the benthic dinoflagellate Prorocentrum lima[J]. Marine Biology, 1999, 134(3): 541-549. DOI:10.1007/s002270050569 (  0) 0) |
| [27] |
Guerrini F, Pezzolesi L, Feller A, et al. Comparative growth and toxin profile of cultured Ostreopsis ovata from the Tyrrhenian and Adriatic Seas[J]. Toxicon, 2010, 55(2-3): 211-220. DOI:10.1016/j.toxicon.2009.07.019 (  0) 0) |
| [28] |
Dai X, Bill B D, Adams N G, et al. The effect of temperature and salinity on growth rate and azaspiracid cell quotas in two strains of Azadinium poporum (Dinophyceae) from Puget Sound, Washington State[J]. Harmful Algae, 2019, 89: 101665. DOI:10.1016/j.hal.2019.101665 (  0) 0) |
| [29] |
Shi J, Liu Y, Gu H, et al. Variation in the growth and toxin production of Gymnodinium catenatum under different laboratory conditions[J]. Marine Biology. DOI:10.1007/s00227-022-04115-x (  0) 0) |
| [30] |
Tong M, Kulis D M, Fux E, et al. The effects of growth phase and light intensity on toxin production by Dinophysis acuminata from the northeastern United States[J]. Harmful Algae, 2011, 10(3): 254-264. DOI:10.1016/j.hal.2010.10.005 (  0) 0) |
| [31] |
叶志林, 曹洁茹, 吴霓, 等. 温度, 光照和盐度对产麻痹性贝类毒素藻类生长及产毒的影响[J]. 海洋环境科学, 2018, 37(3): 321-325. Ye Z L, Cao J R, Wu N, et al. Effects of temperature, light intensity and salinity on growth and toxin production of paralytic shellfish poisoning toxins-producing dinoflagellates[J]. Marine Environmental Science, 2018, 37(3): 321-325. (  0) 0) |
| [32] |
Wang D, Zhang S, Zhang Y, et al. Paralytic shellfish toxin biosynthesis in cyanobacteria and dinoflagellates: A molecular overview[J]. Journal of Proteomics, 2016, 135: 132-140. DOI:10.1016/j.jprot.2015.08.008 (  0) 0) |
| [33] |
Vanucci S, Guerrini F, Milandri A, et al. Effects of different levels of N- and P-deficiency on cell yield, okadaic acid, DTX-1, protein and carbohydrate dynamics in the benthic dinoflagellate Prorocentrum lima[J]. Harmful Algae, 2010, 9(6): 590-599. DOI:10.1016/j.hal.2010.04.009 (  0) 0) |
2. Key Laboratory of Marine Environment and Ecology, Ministry of Education, Ocean University of China, Qingdao 266100, China
 2025, Vol. 55
2025, Vol. 55


