盐度影响着鱼类生存、生长发育、新陈代谢等生理活动,盐度是决定鱼类分布的重要非生物环境因子[1-3]。面对水环境中盐度的变化,广盐性鱼类进化出了复杂的渗透调节机制[4-5]。其中鳃作为直接接触水体的渗透调节器官,能够敏锐地感知水体的盐度变化并作出适应性调整,这不仅能控制离子运输,还能维持体液pH,排泄氨氮,进而维持内、外环境间的平衡[6-9]。研究表明,在海、淡水驯化过程中广盐性鱼类的鳃会发生适应性变化,其主要体现在鳃丝和鳃小片形态、离子细胞类型、数量和分布及酶活性等多方面的改变[10-14]。
E-钙黏蛋白(E-cadherin,Cdh1)是一种钙依赖性跨膜糖蛋白,在调节细胞间黏附、维持上皮细胞间的形态和极性中发挥着关键作用,常用作上皮标志物[15-19]。同时,Cdh1是组织稳态的重要调节因子,通过信号转导来控制细胞功能和发育的多个方面[20]。有研究表明,cdh1基因的表达受低氧诱导因子1(Hypoxia-inducible factor-1, HIF-1)调控,并可能通过影响鳃形态改变进而参与金鱼(Carassius auratus)对低氧环境的响应[21]。然而Cdh1在鱼类鳃盐度驯化过程中的作用尚未可知。
花鲈(Lateolabrax maculatus)是中国重要的海水养殖鱼类[22-23],广泛分布于中国沿海地区,能够在0~38盐度范围内生存及生长,其最高耐受盐度为45,其是研究鱼类渗透调控机制的理想模式动物[24-25]。本研究首先通过组织学观察并结合形态学指标的测量,解析了花鲈鳃组织在盐度驯化过程中的显微结构变化。同时,为探究盐度驯化过程中鳃形态重塑的潜在原因,本研究克隆注释了花鲈的cdh1基因,并通过实时荧光定量PCR、原位杂交及免疫荧光技术对不同盐度条件下花鲈鳃组织中Cdh1的表达模式进行了分析。此外,有研究表明,Cdh1介导的细胞间黏附需要钠钾ATP酶β亚基(Na, K-ATPase β-subunit,NKAβ)的参与,进而诱导上皮细胞极化,抑制细胞的迁移[26]。因此,本研究还对海水驯化过程中Cdh1与NKA蛋白的表达分布进行了共定位分析。研究结果为进一步解析广盐性硬骨鱼类盐度适应的生理及分子机制奠定了基础。
1 材料与方法 1.1 实验用鱼及盐度驯化实验实验用鱼由青岛市黄岛区鲁海丰海洋牧场提供。随机选取30尾活力好、体表无伤的健康花鲈成鱼(体长:(40.50±3.21) cm,体质量:(812.20±25.71) g),平均分配到6个400 L的塑化桶中,每桶5尾鱼,驯化3周,其中3桶海水(盐度:30.0±0.5,pH:8.3±0.3),3桶淡水(盐度:0±0.5,pH:7.5±0.3)。驯化期间每天9:00和16:30投喂配合饲料,投喂1 h后除去残饵和粪便,每隔1 d换水50%。驯化3周后开始进行盐度转换实验,迅速将海水组花鲈转入淡水,并标记为SW-FW组;淡水组花鲈转入海水,并标记为FW-SW组。其他实验条件,例如温度((16.0±0.5) ℃)、溶解氧((7.1±0.4) mg/L)等,在实验过程中保持不变。
1.2 样品采集选取4个时间点(0 h、1 d、3 d、7 d)分别从SW-FW组和FW-SW组的3个塑化桶中随机挑选3尾鱼,用MS-222(200 mg/L)麻醉后采取鳃组织,其中部分组织样品放入液氮中速冻后转移至-80 ℃超低温冰箱保存,用于RNA的提取;另一部分组织放入4% PFA(多聚甲醛,DEPC水配置)中固定12~24 h后换成70%酒精(DEPC水配置),于-20 ℃保存,用于石蜡切片的制备。
1.3 组织学观察将固定好的花鲈鳃组织放入电脑程控组织脱水机(PPDT-12C)中,进行乙醇脱水(70%乙醇40 min, 80%乙醇30 min, 95%乙醇30 min, 95%乙醇20 min, 100%乙醇15 min×2),二甲苯透明(1/2乙醇+1/2二甲苯混合液10 min, 二甲苯10 min, 二甲苯5 min)和浸蜡(石蜡60 min×3)。石蜡包埋后,用LEICA-RM201切片机进行连续切片,切片厚度为5 μm,置于38 ℃烘箱过夜。经苏木精-伊红(HE)染色,中性树胶封片后,用OLYMPUS BX53光学显微镜拍照并观察。
1.4 RNA的提取及反转录采用Trizol试剂(Invitrogen, 美国)提取花鲈鳃组织总RNA,用Biodropsis BD1000核酸分析仪和琼脂糖凝胶电泳检测RNA的完整度和浓度,利用HiScript© Ⅲ RT SuperMix for qPCR (+gDNA wiper)(诺唯赞,中国)试剂盒将RNA反转录为cDNA。
1.5 花鲈cdh1基因的鉴定从NCBI(http://www.ncbi.nlm.nih.gov/)数据库中检索并下载人(Homo sapiens)和斑马鱼(Danio rerio)的Cdh1氨基酸序列,利用TBLASTN(1e-5)对花鲈全长转录组数据(PRJNA515783)及参考基因组(PRJNA408177)进行检索,获得花鲈的cdh1基因序列。用open reading frame(ORF)Finder(https://www.ncbi.nlm.nih.gov/gorf/gorf.html)预测花鲈Cdh1的氨基酸序列,并通过BLASTP比对NCBI非冗余(NR)蛋白序列数据库进一步验证。通过ExPASy Prot-Param在线工具(https://web.expasy.org/protparam/)预测花鲈Cdh1蛋白的分子量(MW,kD)和等电点(pI)。通过DNAMAN 9.0软件将花鲈Cdh1序列与其他物种进行同源比对。
利用NCBI检索人、鼠、鸡(Gallus gallus)、非洲爪蟾(Xenopus laevis)、印度青鳉(Oryzias melastigma)、斑马鱼、尼罗罗非鱼(Oreochromis niloticus)、河鲈(Perca fluviatilis)、剑鱼(Xiphias gladius)、攀鲈(Anabas testudineus)、牙鲆(Paralichthys olivaceus)、黄鳝(Monopterus albus)、红鳍东方鲀(Takifugu rubripes)的Cdh1氨基酸序列,和花鲈Cdh1氨基酸序列一起进行系统进化分析。用MEGA 7.0软件的邻接法(NJ)分析并构建系统进化树。
1.6 实时荧光定量PCR(Quantitative Real-Time PCR,qPCR)检测cdh1基因的mRNA表达水平利用Primer-BLAST(https://www.ncbi.nlm.nih.gov/tools/primer-blast/)和Primer 5.0软件设计花鲈cdh1基因的特异性引物序列:Forward: ATGATGGACACCAGGGC; Reverse: CAGTGAGGTCAGGAATA。通过StepOnePlusTM Real-Time PCR系统(Applied Biosystems,USA),以花鲈18S作为内参基因(Forward: GGGTCCGAAGCGTTTACT; Reverse: TCACCTCTAGCGGCACAA),使用ChamQTMSYBR © Color qPCR Master Mix(High ROX Premixed)试剂盒(诺唯赞,中国),体系为10μL,反应程序为:95 ℃ 30 s,95 ℃ 10 s,60 ℃ 30 s,72 ℃ 30 s,40个循环。每个时间点的鳃组织样品有3个生物学重复,每个样品设3个技术重复,并采用2-ΔΔCt法[27]计算花鲈cdh1基因的相对表达水平。
1.7 原位杂交定位cdh1基因的表达分布PCR扩增获得探针模板,测序成功后使用DIG RNA labeling kit(SP6/T7)(Roche,德国)试剂盒进行体外转录,分别合成DIG标记的正义和反义探针。通过琼脂糖凝胶电泳检测探针的完整性,用BD1000核酸分析仪测定探针浓度。用石蜡包埋好的花鲈鳃组织,参照标准步骤进行原位杂交[28]。用NBT/BCIP显色液(Roche,德国)对胚胎进行显色后,用梯度乙醇脱水、二甲苯透明,中性树胶封片,晾干后用显微镜(OLYMPUS BX53)拍照观察。
1.8 免疫荧光共定位Cdh1和NKA蛋白用石蜡包埋好的花鲈鳃组织进行免疫荧光共定位。石蜡切片经过二甲苯脱蜡,梯度乙醇复水。参照标准步骤进行免疫荧光[29]。对切片进行二甲苯脱蜡、梯度乙醇复水后,用高压法对抗原进行修复。灭活酶试剂(3%的过氧化氢-甲醇)避光处理15 min后,封闭液(5%的BSA-PBST)37 ℃封闭30 min。用抗体稀释液将Na, K-ATPase Antibody(Cell Signaling Technology,USA)1∶400稀释后滴加在切片上,于37 ℃孵育1 h。将鼠兔通用二抗滴加在切片上,于37 ℃孵育1 h。用信号放大液稀释TSA单色荧光染料570,然后将染料滴加在切片上避光显色30~60 min。再次类似上述步骤处理后,用抗体稀释液将E-cadherin Antibody(Affinity Biosciences,USA)1∶400稀释后滴加在切片上,4 ℃避光孵育过夜。显色、洗涤、细胞核染色,脱水封片后用BX53F荧光显微镜(Olympus, 日本)观察并拍照。
1.9 数据处理所测得数据均用平均值±标准差(Mean±SD)表示,用软件SPSS 21进行单因素方差分析(One-way ANOVA);用Duncan法进行多重比较分析,当P< 0.05时认为差异具有统计学意义;用GraphPad Prism 8.0.2作图。
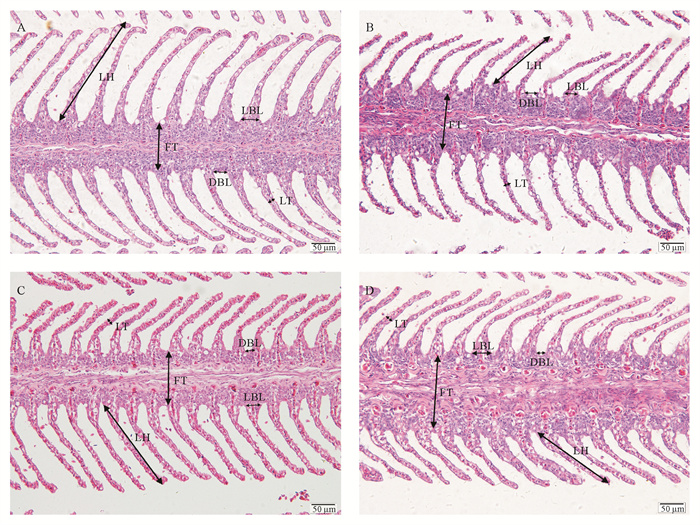
2 结果 2.1 盐度驯化中花鲈鳃组织形态的变化将鳃小片等分为3部分,从上至下分别为鳃小片的顶部、中部和底部,鳃小片之间的区域定义为相邻鳃小片之间的鳃丝上皮。组织学切片(见图 1)结合形态指标数据测量(见图 2)的分析结果表明,海水花鲈鳃中(SW 0 h)鳃丝和鳃小片较细(鳃丝:(80.44±1.74)μm,鳃小片:(7.50±0.32)μm),鳃小片较短((162.89±3.66) μm),鳃小片底部比较宽((42.55±0.61) μm),鳃小片之间的间距较大((45.65±0.99) μm)。由海水转移至淡水过程(SW-FW)中鳃丝和鳃小片逐渐变宽(鳃丝:(80.44±1.74) μm→(126.12±8.60) μm;鳃小片:(7.50±0.32) μm→(11.83±0.46) μm),鳃小片长度逐渐变大((162.89±3.66) μm→(190.73±3.42) μm),鳃小片之间的间距逐渐变小((45.65±0.99) μm→(28.13±0.89) μm),鳃小片底部宽度也逐渐变小((42.55±0.61) μm→(28.65±0.73) μm)。
|
(图A—D分别为淡水驯化前后4个时间点(0 h、1 d、3 d、7 d)的鳃组织。LH:鳃小片长度;LT:鳃小片宽度;FT:鳃丝宽度;DBL:鳃小片间距;LBL:鳃小片底部宽度。比例尺:50 μm。Figures A—D respectively show the gill tissues at four times (0 h, 1 d, 3 d, 7 d) before and after freshwater acclimation. LH: Gill lamellaes length; LT: Gill lamellaes width; FT: Gill filaments width; DBL: Gill lamellaes spacing; LBL: Gill lamellaes bottom width. Scale bar: 50 μm. ) 图 1 花鲈淡水驯化过程中(SW-FW)鳃组织的形态变化 Fig. 1 Gill tissue morphological changes of spotted sea bass during the acclimation to freshwater |
|
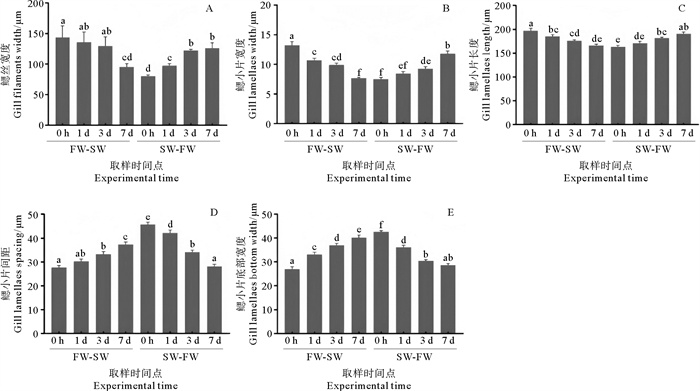
(FW-SW为淡水转移至海水,SW-FW为海水转移至淡水。每个实验组的数据都用平均值±标准差来表示,不同字母代表显著性差异(P< 0.05),n=30。FW-SW refers to the conversion of freshwater to seawater, SW-FW refers to the conversion of seawater to freshwater. Data were presented as mean±SD for each group tested. Different letters represent significant difference (P< 0.05), n=30. ) 图 2 盐度驯化对花鲈组织形态指标的影响 Fig. 2 Effects of salinity acclimation on gill morphological indices of spotted sea bass |
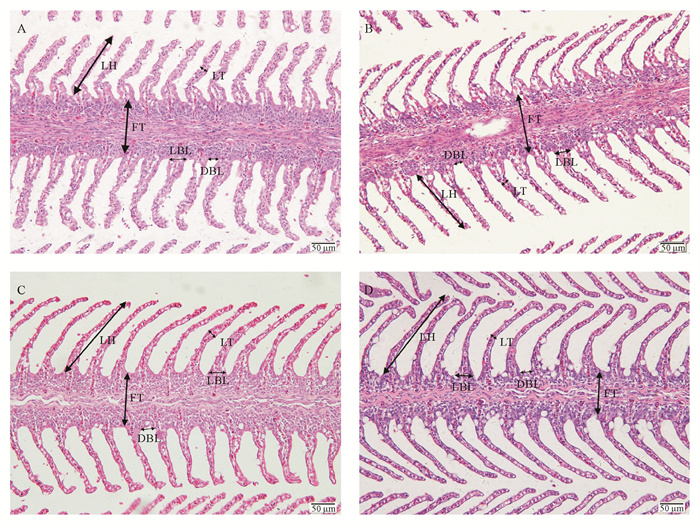
在淡水花鲈鳃(FW 0 h)中,鳃丝和鳃小片相对较粗(鳃丝:(143.62±18.85) μm;鳃小片:(13.17±0.65) μm),鳃小片较长((196.67±5.93) μm),鳃小片底部较窄((27.08±0.98) μm),鳃小片之间的间距也相对较小((27.59±0.95) μm)。在淡水转入海水过程(FW-SW)中,鳃丝和鳃小片逐渐变细(鳃丝:(143.62±18.85) μm→(95.40±5.24) μm;鳃小片:(13.17±0.65) μm→(7.64±0.17) μm),鳃小片长度变小((196.67±5.93) μm→(165.48±3.44) μm),底部宽度逐步变大((27.08±0.98) μm→(40.14±1.14) μm),鳃小片之间的间距也逐渐变大((27.59±0.95) μm→(37.33±1.10) μm)(见图 2和3)。
|
(图A—D分别为海水驯化前后4个时间点(0 h、1 d、3 d、7 d)的鳃组织。LH:鳃小片长度;LT:鳃小片宽度;FT:鳃丝宽度;DBL:鳃小片间距;LBL:鳃小片底部宽度。比例尺:50 μm。Figures A—D respectively show the gill tissues at four times (0 h, 1 d, 3 d, 7 d) before and after seawater acclimation. LH: Gill lamellaes length; LT: Gill lamellaes width; FT: Gill filaments width; DBL: Gill lamellaes spacing; LBL: Gill lamellaes bottom width. Scale bar: 50 μm. ) 图 3 花鲈海水驯化过程中(FW-SW)鳃组织的形态变化 Fig. 3 Gill tissue morphological changes of spotted sea bass during the adaption to seawater |
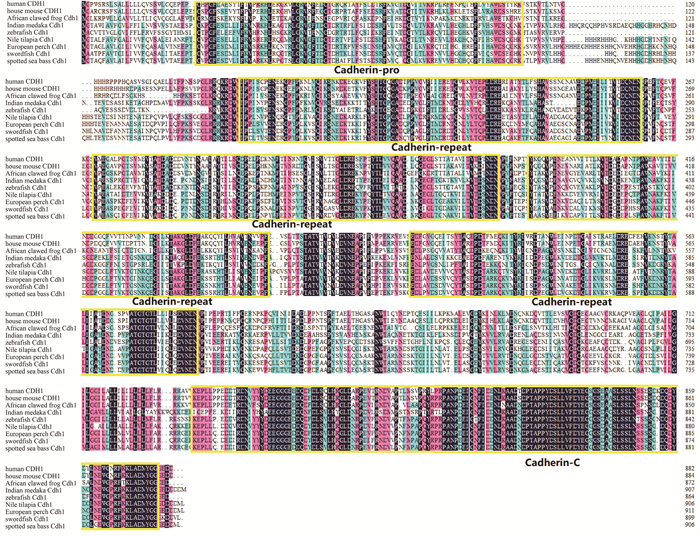
通过对花鲈参考基因组及转录组的筛选比对,鉴定出一个cdh1基因。该基因位于花鲈的13号染色体上,编码区全长2 721 bp,编码906个氨基酸,预测蛋白分子量为100.23 kD,等电点为4.82,具体信息见表 1。利用DNAMAN软件对花鲈和其他7种脊椎动物的Cdh1氨基酸序列进行同源比对(见图 4),结果显示花鲈的Cdh1与河鲈的Cdh1同源性最高,为78%,其次是剑鱼,同源性为77%,与人、鼠等高等脊椎动物的Cdh1同源性较低,仅为44%~50%。与其他硬骨鱼类及高等脊椎动物一样,花鲈Cdh1存在1个钙黏蛋白前结构域(Cadherin-pro),4个钙黏蛋白重复样结构域(Cadherin-repeat)和1个钙黏蛋白细胞质结构域(Cadherin-C)结构域。各个结构域较保守,其中钙黏蛋白细胞质结构域最保守。
|
|
表 1 花鲈cdh1基因序列信息统计 Table 1 Summary of sequence characteristics of cdh1 gene in spotted sea bass |
|
(Cadherin-pro为钙黏蛋白前结构域;Cadherin-repeat为钙黏蛋白重复样结构域;Cadherin-C为钙黏蛋白细胞质结构域。Cadherin-pro represents the cadherin prodomain, Cadherin-repeat represents the cadherin repeat-like domain, Cadherin-C represents the cadherin cytoplasmic domain. ) 图 4 花鲈与其他物种Cdh1氨基酸序列的多重比对 Fig. 4 Multiple alignment of the Cdh1 amino acid sequences between spotted sea bass and other species |
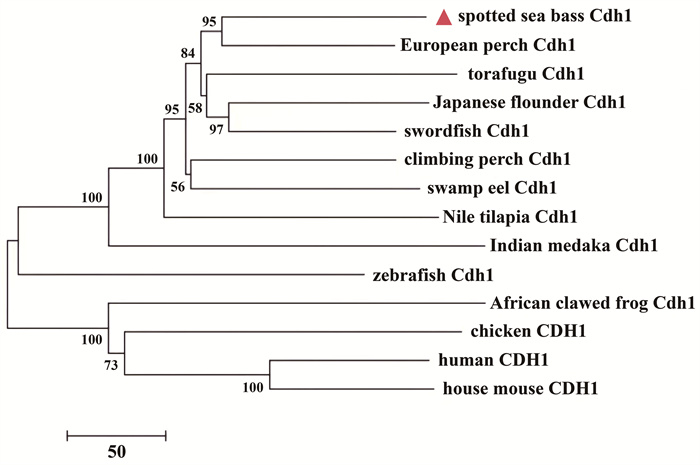
通过NCBI检索并下载了13种脊椎动物的Cdh1氨基酸序列,并与花鲈的Cdh1氨基酸序列一起,用MEGA软件进行了系统进化分析并构建了系统进化树,结果如图 5所示。人、鼠、鸡等高等脊椎动物的Cdh1聚为一支,另一支则由硬骨鱼类组成。该结果支持了花鲈cdh1基因的命名。
|
图 5 Cdh1的系统进化树 Fig. 5 Phylogenetic tree of Cdh1 |
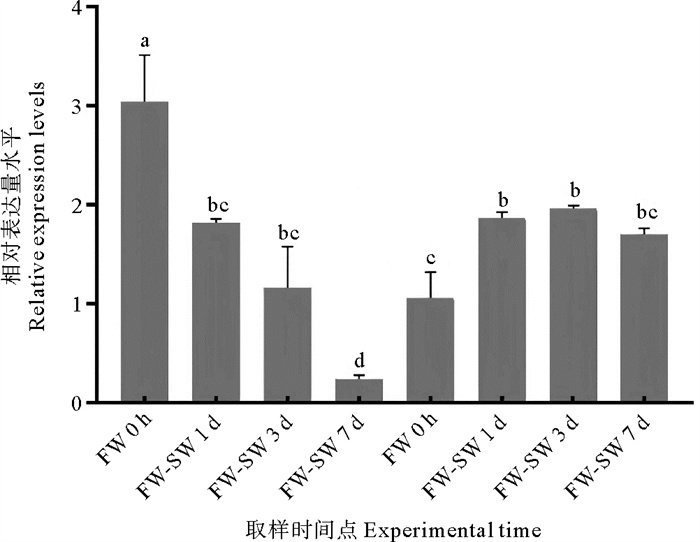
通过qPCR检测了海水和淡水驯化过程中,cdh1基因在花鲈鳃组织中的表达变化。结果如图 6所示,在海水驯化过程(FW-SW)中,cdh1基因的表达量呈逐渐下调的趋势:淡水转入海水1 d时,cdh1基因的表达量显著下调至淡水组的60%;3 d时下调至淡水组的38%;7 d时下调至淡水组的8%。在淡水驯化过程(SW-FW)中,cdh1基因的表达量显著上调,由海水转入淡水1、3和7 d时的表达量分别上调至海水组的1.86、1.96和1.60倍。淡水组(FW 0 h)花鲈鳃组织中cdh1的表达量显著高于海水组(SW 0 h),约为2.88倍。
|
(FW-SW:淡水转海水组,SW-FW:海水转淡水组。不同字母代表显著性差异(P< 0.05)。FW-SW refers to the conversion of freshwater to seawater, SW-FW refers to the conversion of seawater to freshwater. Different letters represents significant difference (P< 0.05). ) 图 6 花鲈cdh1基因在盐度驯化过程鳃组织中的相对表达水平 Fig. 6 Relative expression level of cdh1 gene in gill tissues of spotted sea bass during salinity acclimation |
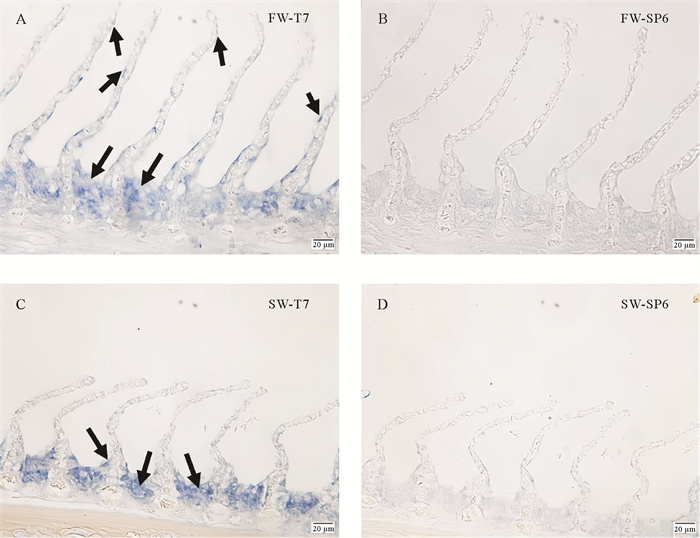
利用原位杂交技术对花鲈cdh1基因进行定位,结果如图 7所示。cdh1基因的信号在淡水组花鲈鳃小片上皮细胞较为均匀地分布(鳃小片的顶部、中部和底部均有分布),且在相邻鳃小片间的鳃丝上皮细胞中检测到大量信号(见图 7 A)。在海水组花鲈鳃中cdh1基因集中定位在鳃小片的底部及相邻鳃小片的鳃丝上皮细胞中(见图 7 C),而鳃小片上未检测到明显的阳性信号。
|
(FW为淡水组,SW为海水组,T7为反义探针,SP6为正义探针。图A、C分别代表花鲈cdh1基因的反义探针在淡水、海水鳃组织中的定位结果。图中黑色箭头所示为部分阳性信号。图B、D分别代表cdh1正义探针在淡水、海水鳃组织中的定位结果。比例尺:20 μm。FW represents freshwater group, SW represents seawater group, T7 represents antisense probe and SP6 represents sense probe. Figure A and C represent the localization results of antisense probes of cdh1 gene in freshwater and seawater gill tissues of spotted sea bass, respectively. The black arrow in figures shows some positive signals. Figure B and D (negative control) represent the localization results of cdh1 sense probe in freshwater and seawater gill tissues, respectively. Scale bar: 20 μm. ) 图 7 花鲈cdh1基因在海、淡水鳃组织中的原位杂交定位 Fig. 7 In situ hybridization of cdh1 gene in seawater and freshwater gills of spotted sea bass |
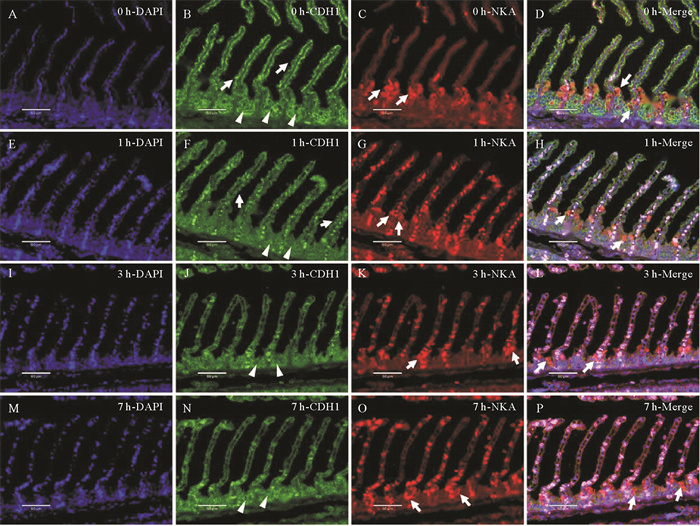
利用免疫荧光技术,检测了花鲈海水驯化过程中Cdh1蛋白在鳃中的表达分布情况,并进行了Cdh1与NKA蛋白的共定位分析。在淡水组花鲈鳃组织中,Cdh1阳性信号分布在鳃小片上皮(顶部、中部和底部)及相邻鳃小片之间的鳃丝上皮(见图 8 B)。在转入海水1 d时,相邻鳃小片之间鳃丝上皮的Cdh1信号未见明显变化,但鳃小片上(顶部、中部和底部)的信号明显减少(见图 8 F)。转入海水3 d时,除了相邻鳃小片之间的鳃丝上皮有少量阳性信号外,鳃小片上的信号几乎检测不到(见图 8 J)。转入海水7 d时,Cdh1的表达情况与3 d时无明显差异(见图 8 N)。
|
(绿色信号为Cdh1,红色信号为NKA,蓝色(DAPI)为细胞核,Merge图为三种信号的共定位。图中的白色三角符号和箭头所示均为部分阳性信号。比例尺:60 μm。Green signal represents Cdh1, red signal represents NKA, blue (DAPI) represents nucleus, and Merge diagram shows the co-localization of the three signals. The white triangle symbol and arrow in the figure are partial positive signals. Scale bar: 60 μm. ) 图 8 花鲈海水驯化过程鳃组织中Cdh1与NKA的免疫荧光共定位 Fig. 8 Immunofluorescence co-localization of Cdh1 and NKA in gill tissue of spotted sea bass during seawater acclimation |
同时,在淡水花鲈鳃组织中,NKA主要在鳃小片的中部和底部表达(见图 8 C)。淡水转入海水1 d时(见图 8 G),鳃小片上的NKA信号略有减少且表达位置主要在鳃小片底部;海水驯化3 d时(见图 8 K),NKA的表达位置更靠近鳃丝;而海水驯化7 d时(见图 8 O),NKA主要在鳃小片底部,靠近鳃丝上皮表达。总体而言,Cdh1的信号在淡水花鲈鳃上皮组织的分布要比NKA更广泛,二者不存在明显的共定位现象。
3 讨论广盐性鱼类的鳃是鱼体与水环境进行物质交换的媒介,也是鱼类第一道渗透调节线,是渗透调节的重要器官之一[30-31]。前期研究表明,海水、淡水环境下的花鲈鳃组织有显著的形态学差异[32]。本研究通过组织学切片对盐度驯化过程中花鲈鳃组织的形态结构变化进行了探究,发现在淡水驯化过程中,鳃丝和鳃小片逐渐变宽,鳃小片之间的间距逐渐变小,且鳃小片逐渐变长,而鳃小片底部的宽度逐渐变小;海水驯化过程中的变化则相反。这与王艳等[33]对不同盐度下欧洲鲈(Dicentrarchus labrax)鳃组织显微结构的研究结果一致。此外在虹鳟(Oncorhynchus mykiss)[34]、珍珠龙胆石斑鱼(Epinephelus lanceolatus♂×E. fuscoguttatus♀)[35]、中华鲟(Acipenser sinensis)[30]、鲻鱼(Mugil cephalus)[36]、红鳍东方鲀[37]以及大麻哈鱼(Oncorhynchus keta)[4]等硬骨鱼类的研究中,不同盐度下的鳃都观察到类似的形态学重塑现象。鳃组织之所以在盐度驯化过程中发生适应性变化,可能是因为在低渗环境中需要通过增加鳃丝和鳃小片宽度、增加鳃小片的长度以及缩短鳃小片之间的间距来增大与水的接触面积,这有利于从水环境中摄取无机盐离子,从而保持渗透压平衡,适应低渗环境。而在高渗环境中外界渗透压升高,使得鳃丝和鳃小片出现一定程度的萎缩,鱼体消耗的氧气及能量增加,鳃小片之间的间距增大有利于加快其与水体的水氧交换,从而更好地适应高渗环境[38]。
Cdh1是一种进化保守的大型单通道跨膜糖蛋白,通过调控Ca2+依赖性的细胞黏附[15-16], 在组织形成、细胞极化和发育等方面来维持上皮表型,是多种器官形态发生的关键分子[39-40]。基于此,本研究通过对cdh1基因的克隆及表达模式分析,探究了其在花鲈应对盐度驯化时的鳃形态重塑过程中的潜在作用。序列分析结果表明,花鲈Cdh1蛋白各个结构域较为保守,其中钙黏蛋白细胞质结构域最保守。钙黏蛋白的细胞质结构域诱导聚集,是钙黏蛋白介导的细胞间黏附强度的关键决定因素[16]。本研究利用qPCR检测了花鲈cdh1基因在盐度驯化时鳃组织中的表达模式,结果显示cdh1基因在淡水鳃组织中的表达量显著高于在海水鳃组织中的表达量,并在海水驯化过程中表达量呈逐渐下调的趋势,而在淡水驯化过程中的表达趋势刚好相反。利用原位杂交技术检测了花鲈cdh1基因海水、淡水鳃组织中的定位模式,结果显示cdh1基因在淡水鳃组织中定位于几乎全部的鳃小片上皮及相邻鳃小片之间的鳃丝上皮,而在海水鳃组织中只在相邻鳃小片之间的鳃丝上皮有明显的阳性信号,二者之间呈现出明显差异。这表明海水、淡水鳃组织的显微结构差异可能与上皮细胞极性的变化有关。
有研究表明,钠钾ATP酶在Cdh1介导的上皮极性的发展、细胞的侵袭性和运动性的抑制中起关键作用[26]。同时,我们先前报道的编码NKAβ蛋白的nkaβ1b基因与本研究中cdh1在盐度驯化过程中的表达变化趋势一致[41],因此,本研究对花鲈海水驯化过程中Cdh1和NKA蛋白在鳃中的表达分布进行了共定位分析。结果显示,Cdh1定位于淡水花鲈鳃小片上皮及相邻鳃小片之间的鳃丝上皮,且在海水驯化过程鳃小片上的信号逐渐减少直至消失。NKA在花鲈淡水鳃组织中定位于鳃小片的中部和底部,海水驯化过程中NKA表达位置沿鳃小片逐渐下移,最后仅定位在鳃小片底部上皮。以上结果表明,在海水驯化过程中,鳃小片上皮细胞极性逐渐消失,而在淡水驯化过程中,鳃小片上皮细胞极性逐渐建立。推测鳃小片上皮细胞极性的消失和建立是花鲈适应海水和淡水环境的重要过程,可能与海水、淡水鳃组织的显微结构差异显著相关。另外,NKA与Cdh1不存在共定位关系说明在盐度驯化过程中鳃上皮Cdh1的表达分布不受NKA的直接调控。
4 结语本研究发现花鲈在盐度驯化过程中存在显著的鳃形态重塑现象,在淡水驯化中鳃丝、鳃小片宽度和鳃小片长度增加,鳃小片底部宽度及相邻鳃小片之间的间距减小,而上述形态学指标在海水驯化过程中呈相反的变化趋势。同时,花鲈盐度驯化过程中Cdh1的表达水平和分布均出现了显著改变。在海水驯化过程中,鳃小片上的Cdh1信号逐渐减少直至消失,推测其介导的上皮细胞极性改变在花鲈鳃形态重塑中起着重要作用,但这一改变不受NKA的直接调控,其具体的作用机制尚有待进一步研究。
| [1] |
冉凤霞, 金文杰, 黄屾, 等. 盐度变化对鱼类影响的研究进展[J]. 西北农林科技大学学报(自然科学版), 2020, 48(8): 10-18. Ran F X, Jin W J, Huang S, et al. Research progress on the effects of salinity change on fish[J]. Journal of Northwest A&F University (Natural Science Edition), 2020, 48(8): 10-18. (  0) 0) |
| [2] |
林浩然. 鱼类生理学[M]. 广州: 中山大学出版社, 2011: 205-221. Lin H R. Fish Physiology[M]. Guangzhou: SunYat-sen University Press, 2011: 205-221. (  0) 0) |
| [3] |
Hwang P P, Lee T H, Lin L Y. Ion regulation in fish gills: Recent progress in the cellular and molecular mechanisms[J]. American Journal of Physiology-Regulatory, Integrative and Comparative Physiology, 2011, 301(1): 28-47. DOI:10.1152/ajpregu.00047.2011 (  0) 0) |
| [4] |
李培伦, 刘伟, 王继隆, 等. 盐度对大麻哈鱼幼鱼存活率、鳃ATP酶活力及其组织结构的影响[J]. 水生生物学报, 2020, 44(3): 562-569. Li P L, Liu W, Wang J L, et al. Effects of salinity on survival rate, gill ATPase activity and gill structure ofjuveniles chum salmon[J]. Acta Hydrobiologica Sinica, 2020, 44(3): 562-569. (  0) 0) |
| [5] |
Madsen S S, Engelund M B, Cutler C P. Water transport and functional dynamics of aquaporins in osmoregulatory organs of fishes[J]. The Biological Bulletin, 2015, 229(1): 70-92. DOI:10.1086/BBLv229n1p70 (  0) 0) |
| [6] |
Giari L, Manera M, Simoni E, et al. Changes to chloride and rodlet cells in gills, kidney and intestine of Dicentrarchus labrax(L.) exposed to reduced salinities[J]. Journal of Fish Biology, 2006, 69(2): 590-600. DOI:10.1111/j.1095-8649.2006.01130.x (  0) 0) |
| [7] |
Wood C M, Shuttleworth T J. Cellular and Molecular Approaches to Fish Ionic Regulation[M]. San Diego, CA: Academic Press, 1995.
(  0) 0) |
| [8] |
Leguen I, Prunet P. Effect of hypotonic shock on cultured pavement cells from freshwater or seawater rainbow trout gills[J]. Comparative Biochemistry and Physiology A, 2004, 137: 259-269. DOI:10.1016/j.cbpb.2003.09.027 (  0) 0) |
| [9] |
Evans D H, Piermarini P M, Choe K P. The multifunctional fish gill: Dominant site of gas exchange, osmoregulation, acid-base regulation, and excretion of nitrogenous waste[J]. Physiological Reviews, 2005, 85: 97-177. DOI:10.1152/physrev.00050.2003 (  0) 0) |
| [10] |
Dabom K, Cozzi R R F, Marshall W S. Dynamics of pavement cell-chloride cell interactions during abrupt salinity change in Fundulus heteroclitus[J]. Journal of Experimental Biology, 2001, 204(11): 1889-1899. DOI:10.1242/jeb.204.11.1889 (  0) 0) |
| [11] |
尹飞, 孙鹏, 彭士明, 等. 低盐度胁迫对银鲳幼鱼肝脏抗氧化酶、鳃和肾脏ATP酶活力的影响[J]. 应用生态学报, 2011, 22(4): 1059-1066. Yin F, Sun P, Peng S M, et al. Effects of low salinity stress on the antioxidant enzyme activities in juvenile Pampus argenteus liver and the ATPase activities in its gill and kidney[J]. Chinese Journal of Applied Ecology, 2011, 22(4): 1059-1066. (  0) 0) |
| [12] |
刘娟娟, 王京数, 赵珣, 等. 不同盐度和驯养时间中华鲟子二代幼鱼鳃的显微结构变化[J]. 水生态学杂志, 2015, 36(1): 60-65. Liu J J, Wang J S, Zhao X, et al. Microstructure changes in the gill epithelia of second filial Acipenser sinensis juvenile acclimated to various salinities for different time[J]. Journal of Hydroecology, 2015, 36(1): 60-65. (  0) 0) |
| [13] |
王雯, 区又君, 温久福, 等. 不同盐度对斜带石斑鱼幼鱼血清离子浓度和激素水平的影响及其与鳃MRCs渗透调节功能的关系[J]. 水产学报, 2017, 41(9): 1383-1391. Wang W, Ou Y J, Wen J F, et al. Effects of various salinities stress on the relationship between concentrations of ions, hormones in serum and gill mitochondrion-rich cells osmotic regulations of Epinephelus coioides junveniles[J]. Journal of Fisheries of China, 2017, 41(9): 1383-1391. (  0) 0) |
| [14] |
温久福, 蓝军南, 曹明, 等. 盐度对花鲈幼鱼鳃、脾及肌肉组织结构的影响[J]. 渔业科学进展, 2020, 41(1): 112-118. Wen J F, Lan J N, Cao M, et al. Effects of salinity on the histological structure of the gills, spleen, and muscle in Lateolabrax maculatus juveniles[J]. Progress in Fishery Science, 2020, 41(1): 112-118. (  0) 0) |
| [15] |
Takeichi M. The cadherins: Cell-cell adhesion molecules controlling animal morphogenesis[J]. Development, 1988, 102: 639-655. DOI:10.1242/dev.102.4.639 (  0) 0) |
| [16] |
Gumbiner B M. Regulation of cadherin-mediated adhesion in morphogenesis[J]. Nature Reviews, Molecular Cell Biology, 2005, 6: 622-634. DOI:10.1038/nrm1699 (  0) 0) |
| [17] |
Armesto P, Campinho M A, Rodríguez-Rúa A, et al. Molecular characterization and transcriptional regulation of the Na+/K+ATPase α subunit isoforms during development and salinity challenge in a teleost fish, the Senegalese sole (Solea senegalensis)[J]. Journal of Comparative Physiology B: Biochemical, Systemic, and Environmental Physiology, 2014, 175: 23-38. (  0) 0) |
| [18] |
Meigs T E, Fedor-Chaiken M, Kaplan D D, et al. Galpha12 and Galpha13 negatively regulate the adhesive functions of cadherin[J]. Journal of Biological Chemistry, 2002, 277(27): 24594-24600. DOI:10.1074/jbc.M201984200 (  0) 0) |
| [19] |
Gumbiner B M. Cell adhesion: The molecular basis of tissue architecture and morphogenesis[J]. Cell, 1996, 84(3): 345-357. DOI:10.1016/S0092-8674(00)81279-9 (  0) 0) |
| [20] |
Bruner H C, Derksen P W B. Loss of E-cadherin-dependent cell-cell adhesion and the development and progression of cancer[J]. Cold Spring Harbor Perspectives in Biology, 2018, 10(3): a029330. DOI:10.1101/cshperspect.a029330 (  0) 0) |
| [21] |
王华, 刘梦琦, 胡诗蒙, 等. 低氧对金鱼鳃形态重塑过程中EMT途径的影响[J]. 浙江师范大学学报(自然科学版), 2021, 44(1): 69-74. Wang H, Liu M Q, Hu S M, et al. Effect of hypoxia on cell adhesion in the gill remodeling of goldfish[J]. Journal of Zhejiang Normal University (Natural Sciences), 2021, 44(1): 69-74. (  0) 0) |
| [22] |
陈大刚, 张美昭. 中国海洋鱼类[M]. 青岛: 中国海洋大学出版社, 2015: 985-986. Chen D G, Zhang M Z. Marine Fishes of China[M]. Qingdao: China Ocean University Press, 2015: 985-986. (  0) 0) |
| [23] |
孟晓梦. 花鲈(Lateolabrax sp. )耳石形态的地理变异[D]. 青岛: 中国海洋大学, 2007. Meng X M. Regional Differences in Otolith Morphology of the Sea Bass[D]. Qingdao: Ocean University of China, 2007. (  0) 0) |
| [24] |
Wang H L, Wen H S, Li Y, et al. Evaluation of potential reference genes for quantitative RTPCR analysis in spotted sea bass (Lateolabrax maculatus) under normal and salinity stress conditions[J]. Peer J, 2018, 6: e5631. DOI:10.7717/peerj.5631 (  0) 0) |
| [25] |
Zhang X Y, Wen H S, Wang H L, et al. RNA-Seq analysis of salinity stress-responsive transcriptome in the liver of spotted sea bass (Lateolabrax maculatus)[J]. PLoS One, 2017, 12(3): e0173238. DOI:10.1371/journal.pone.0173238 (  0) 0) |
| [26] |
Rajasekaran S A, Palmer L G, Quan K, et al. Na, K-ATPase β-subunit is required for epithelial polarization, suppression of invasion, and cell motility[J]. Molecular Biology of the Cell, 2017(12): 2. (  0) 0) |
| [27] |
Livak K J, Schmittgen T D. Analysis of relative gene expression data using real-time quantitative PCR and the 2(-Delta Delta C(T)) Method[J]. Methods, 2001, 25(4): 402-414. DOI:10.1006/meth.2001.1262 (  0) 0) |
| [28] |
Zhou Y Y, Qi X, Wen H S, et al. Identification, expression analysis, and functional characterization of motilin and its receptor in spotted sea bass (Lateolabrax maculatus)[J]. General and Comparative Endocrinology, 2019, 277: 38-48. DOI:10.1016/j.ygcen.2019.02.013 (  0) 0) |
| [29] |
Ding T, Shi Y, Duan W, et al. Immunohistochemical characterization and change in location of branchial ionocytes after transfer from freshwater to seawater in the euryhaline obscure puffer, Takifugu obscurus[J]. Journal of Comparative Physiology B: Biochemical, Systemic, and Environmental Physiology, 2020, 190: 585-596. DOI:10.1007/s00360-020-01298-x (  0) 0) |
| [30] |
秦少宗, 冷小茜, 罗江, 等. 中华鲟幼鱼渗透调节器官组织结构在海水条件下的适应性调整[J]. 渔业科学进展, 2021, 42(4): 82-89. Qin S Z, Leng X Q, Luo J, et al. Adaptive adjustment of osmotic organ structure of juvenile Chinese sturgeon in seawater conditions[J]. Progress in Fishery Science, 2021, 42(4): 82-89. (  0) 0) |
| [31] |
El-Leithy A A A, Hemeda S A, Abd El Naby W S H, et al. Optimum salinity for Nile tilapia (Oreochromis niloticus) growth and mRNA transcripts of ion-regulation, inflammatory, stress and immunerelated genes[J]. Fish Physiology and Biochemistry, 2019, 45(2): 1217-1232. (  0) 0) |
| [32] |
Wang L Y, Zhang X Y, Wen H S, et al. Integrated miRNA and mRNA analysis in gills of spotted sea bass reveals novel insights into the molecular regulatory mechanism of salinity acclimation[J]. Aquaculture, 2023, 575: 739778. DOI:10.1016/j.aquaculture.2023.739778 (  0) 0) |
| [33] |
王艳, 胡先成. 不同盐度下鲈鱼稚鱼鳃的显微结构观察[J]. 海洋科学, 33, 33(12): 138-142. Wang Y, Hu X C. Microscopical observation on the gill structure of juvenile Lateolabrax japonicus under different salinities[J]. Marine Sciences, 33, 33(12): 198-142. (  0) 0) |
| [34] |
Shen A C Y, Leatherland J F. Histogenesis of the pituitary in rainbow trout (Salmo gairdneri) in different ambient salinities particular reference to the rostral pars distalis[J]. Cell and Tissue Research, 1978, 189(2): 355-363. (  0) 0) |
| [35] |
刘龙龙, 罗鸣, 陈傅晓, 等. 盐度对珍珠龙胆石斑鱼幼鱼生长及鳃肾组织学结构的影响[J]. 大连海洋大学学报, 2019, 34(4): 505-510. Liu LL, Luo M, Chen F X, et al. Effects of salinity on growth, and gill and kidney histological structures of juvenile pearl gentian grouper[J]. Journal of Dalian Ocean University, 2019, 34(4): 505-510. (  0) 0) |
| [36] |
于娜, 李加儿, 区又君, 等. 不同盐度下鲻鱼幼鱼鳃和肾组织结构变化[J]. 生态科学, 2012, 31(4): 424-428. Yu N, Li J E, Ou Y J, et al. Structural changes in gill and kidney of juvenile grey mullet under different salinity[J]. Ecological Science, 2012, 31(4): 424-428. (  0) 0) |
| [37] |
孙梦蕾, 蒋洁兰, 王莉苹, 等. 低盐胁迫下红鳍东方鲀幼鱼鳃、肾和肠组织结构的变化[J]. 广东海洋大学学报, 2016, 36(6): 38-43. Sun M L, Jiang J L, Wang L P, et al. Structural changes in gill, kidney and intestine of juvenile Takifugu rubripes under low salinity treatment[J]. Journal of Guangdong Ocean University, 2016, 36(6): 38-43. (  0) 0) |
| [38] |
Wood C M, Eom J. The osmorespiratory compromise in the fish gill[J]. Comparative Biochemistry and Physiology. Part A, Molecular & Integrative Physiology, 2021, 254: 110895. (  0) 0) |
| [39] |
Halbleib J M, Nelson W J. Cadherins in development: Cell adhesion, sorting, and tissue morphogenesis[J]. Genes & Development, 2006, 20: 3199-3214. (  0) 0) |
| [40] |
Lien W H, Klezovitch O, Vasioukhin V. Cadherin-catenin proteins in vertebrate development[J]. Current Opinion in Cell Biology, 2006, 18: 499-506. (  0) 0) |
| [41] |
Zhang X, Wen H S, Qi X, et al. Na+-K+-ATPase and nka genes in spotted sea bass (Lateolabrax maculatus) and their involvement in salinity adaptation[J]. Comparative Biochemistry and Physiology. Part A, Molecular & Integrative Physiology, 2019, 235: 69-81. (  0) 0) |
 2024, Vol. 54
2024, Vol. 54


