静脉用药调配中心(pharmacy intravenous admixture service, PIVAS)是在符合国际标准,依据药物特性设计的层流环境下,按照静脉用药调配的要求,由受过专业培训的药学或护理技术人员,严格按照操作规程,进行静脉用药集中调配,为临床提供优质的成品输液和药学服务的场所[1-2],其已成为医院感染管理的重点部门之一。文献[3-4]报道,操作不规范、净化环境不达标或输送过程中污染是导致成品输液污染的主要因素。作为输送成品输液的重要工具,转运药箱传递于PIVAS洁净区和病区非无菌区域之间,循环使用,是潜在的污染源,其洁净度关系到患者的成品输液安全。2010年我国卫生部颁布的《静脉用药集中调配质量管理规范》指出,每周一次采用75%乙醇擦拭消毒成品输送密闭容器[5]。而其他关于转运药箱的清洁消毒相关文献报道较少。在实际工作中,采用75%乙醇喷洒后再用专用清洁布擦拭消毒药箱操作不便,可能存在交叉污染等问题。本研究基于某院现状,通过对若干清洁消毒方法的筛选试用,选择使用一次性医用消毒湿巾对输送药箱进行擦拭清洁消毒[6],旨在根据随时间转运药箱染菌量变化情况,探讨一次性医用消毒湿巾对转运药箱的清洁消毒效果,并指导科室制定相应的清洁消毒频次。
1 材料与方法 1.1 试验材料试验用物包括转运药箱、一次性医用消毒湿巾[主要成分为无纺布浸润季铵盐消毒剂,浸润液复合季铵盐含量(w/v)为0.18%~0.22%,pH值7.0~8.0]、棉拭子、无菌洗脱液、无菌试管等。
1.2 方法 1.2.1 试验方法随机选取PIVAS正常使用中的64个转运药箱(规格25 cm×15 cm×15 cm),用一次性医用消毒湿巾进行擦拭清洁消毒,一张消毒湿巾擦拭一个药箱,避免交叉污染。如输送药箱表面有明显污渍,应先用一张消毒湿巾去除污物,再取另一张消毒湿巾进行擦拭消毒。每个药箱擦拭时间为5 min。
1.2.2 检测方法与标准分别于清洁消毒后的0、12、24、36、48 h对药箱进行目视检测并采样进行微生物学检测。目视法:肉眼观察清洁消毒后的药箱表面,包括其内部、底部、外部、把手边缘等部位,无污物、无药液残留痕迹为合格;采样及微生物学检测:用5 cm×5 cm的灭菌规格板放在被检测药箱表面,用浸有含0.3%吐温和0.3%卵磷脂中和剂的无菌洗脱液的棉拭子一支,在规格板内横竖往返各涂抹5次,并随之转动棉拭子,连续采样4个规格板面积,剪去手接触部分,将棉拭子放入装有10 mL无菌检验洗脱液的试管内,立即送微生物室,37℃恒温培养48 h,进行细菌计数及菌种鉴定。64个药箱分为4组,分别于0、12、24、36、48 h检测箱内底部、箱内侧面、箱外侧面、箱把手4个部位,共为320个样本。以检测细菌菌落数≤5 CFU/cm2,无致病菌生长为合格(Ⅱ类)[7-8]。染菌率为细菌检测阳性的标本数占总标本数的比率。
1.3 统计学方法应用SPSS 21.0统计学软件进行数据分析,计数资料以率表示,采用行×列表资料的χ2检验进行比较。计量资料以均数±标准差(x±s)表示,采用随机分组设计资料的方差分析进行比较。P≤0.05为差异具有统计学意义。
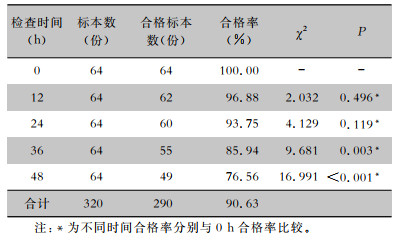
2 结果 2.1 清洁消毒后不同时间药箱洁净度目测合格情况清洁消毒后不同时间药箱洁净度目测合格率比较,差异有统计学意义(χ2=26.851,P<0.01),并呈下降趋势(χ趋势2=25.098,P<0.01)。进一步进行组间两两比较,12、24 h分别与0 h目测合格率比较,差异均无统计学意义(均P>0.05);而36、48 h与0 h目测合格率比较,差异均有统计学意义(均P<0.05)。见表 1。
| 表 1 清洁消毒后不同时间药箱洁净度目测合格率比较 Table 1 Comparison of qualified rate of visual inspection for the cleanliness of medicine boxes at different time after cleaning and disinfection |
|
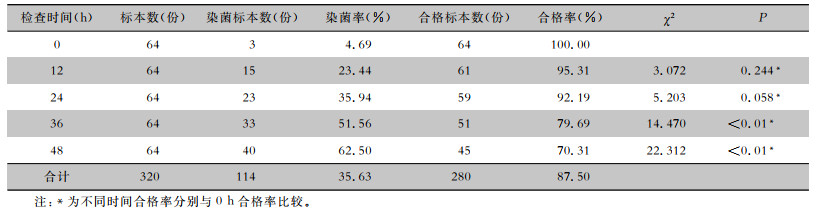
清洁消毒后不同时间药箱的微生物检测合格率比较,差异有统计学意义(χ2=34.857,P<0.01),并呈下降趋势(χ趋势2=32.811,P<0.01)。清洁消毒后(0 h),药箱表面的染菌率为4.69%,但均低于5 CFU/cm2,合格率为100%。12、24 h合格率分别与0 h比较,差异均无统计学意义(均P>0.05)。而清洁消毒36、48 h后,药箱表面的染菌率均>50%,药箱合格率均低于80%;清洁消毒36、48 h后合格率与0 h比较,差异均有统计学意义(均P<0.01)。见表 2。
| 表 2 清洁消毒后不同时间药箱的染菌率和微生物检测合格率比较 Table 2 Comparison of bacterial contamination rate and microbial detection qualified rate of medicine boxes at different time after cleaning and disinfection |
|
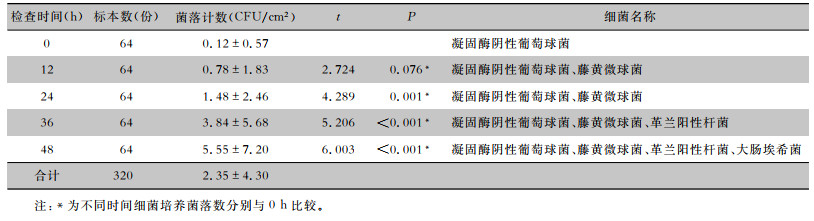
清洁消毒后不同时间药箱细菌培养菌落数比较,差异有统计学意义(F=20.648,P<0.01)。共检测出4种细菌,包括凝固酶阴性葡萄球菌、藤黄微球菌、革兰阳性杆菌、大肠埃希菌。15%的标本检出2种及以上的混合菌。而清洁消毒48 h后,在儿科药箱把手处检测出大肠埃希菌(12 CFU/m2)。见表 3。
| 表 3 清洁消毒后不同时间药箱细菌培养菌落数及细菌种类 Table 3 Bacterial colony count and bacterial species of medicine boxes at different time after cleaning and disinfection |
|
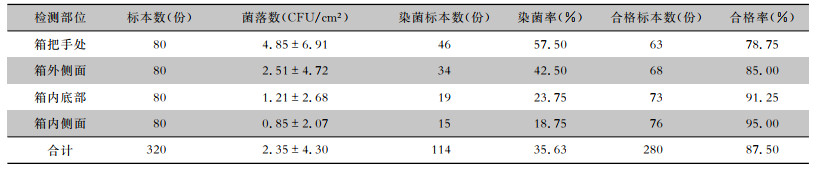
药箱不同检测部位的微生物检测合格率比较,差异有统计学意义(χ2=11.200,P=0.011)。与箱内侧面和箱内底部比较,箱把手处和箱外侧面的染菌率较高,而微生物检测合格率低。见表 4。
| 表 4 清洁消毒后不同部位药箱的染菌率和微生物检测合格率比较 Table 4 Comparison of bacterial contamination rate and microbial detection qualified rate of different sites of medicine boxes after cleaning and disinfection |
|
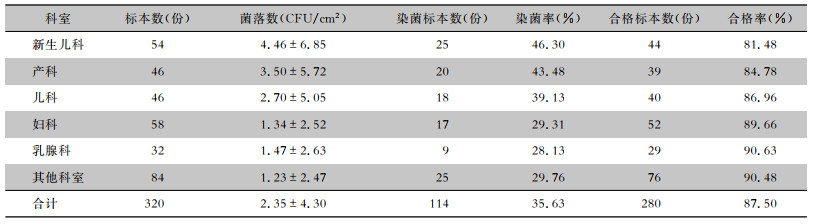
不同科室药箱的微生物检测合格率比较,差异无统计学意义(χ2=3.324,P=0.650)。药箱染菌率位于前三的科室为新生儿科(46.30%)、产科(43.48%)、儿科(39.13%)。见表 5。
| 表 5 清洁消毒后不同科室药箱的染菌率和微生物检测合格率比较 Table 5 Comparison of bacterial contamination rate and microbial detection qualified rate of medicine boxes in different departments after cleaning and disinfection |
|
医院感染管理贯穿于PIVAS日常工作的各个方面。该院PIVAS于2012年成立,承担全院18个临床病区的输液调配工作,每日平均配置4 200余袋静脉输入液体,目前在使用的转运药箱共132个。由于该院PIVAS每日输送成品输液量较多,且转运药箱有大、中、小三种规格,目前很难做到转运药车全封闭式输送。到达临床病区后,通常病区治疗护士未立刻打开药箱取药,空药箱暴露于临床病区长达数小时后,再由输送员收回PIVAS循环使用,大大增加了转运药箱被污染的概率[9]。文献[10-11]报道,配置好的输液瓶口不经任何处理直接暴露于病区治疗室环境中4 h后染菌率高达76.54%,存在被金黄色葡萄球菌、唾液链球菌、人葡萄球菌等多种细菌污染的现象。而同样作为潜在的感染源,如果转运药箱清洁消毒不彻底或未及时进行消毒,将极大地增加静脉输液的感染风险,对患者用药安全造成威胁[12]。
该院为妇女儿童专科医院,患者主要以婴幼儿为主,常需用输液泵严格控制输液量和输液速度,以及用于肠外营养液的输入等。多用20 mL或50 mL一次性注射器配置所需液体和药物至临床病区;与输液袋相比,一次性注射器针头容易松动或挤压导致漏液,药品污染风险相对较高,这就对转运药箱的清洁度提出了更高的要求。
文献[4, 13]报道,与传统采用75%乙醇擦拭消毒比较,采用医用消毒湿巾清洁消毒与其消毒效果相当,且价格低廉,操作简便,可减少配置人员职业损害,提高实施人员消毒执行率和满意度。本研究结果表明,清洁消毒后(0 h),目视法和微生物检测法检测结果显示合格率均为100%。说明选用一次性医用消毒湿巾对转运药箱进行擦拭清洁消毒效果可靠。清洁消毒24 h内,转运药箱有较少药液残留及肉眼可见污物,微生物检测合格率为90%以上,未检测出致病菌,维持效果良好。而随着时间延长,至48 h时,目视法和微生物检测法检测结果合格率均显著下降,染菌率>50%,并在转运药箱的把手处检测出大肠埃希菌。药箱把手和箱外侧面的染菌率较高,新生儿科、产科、儿科等科室的药箱染菌率明显高于其他科室,可能与该院是妇女儿童专科医院,上述三类科室成品输液量多,以及药箱使用较频繁有关。综合以上结果,该院PIVAS将转运药箱的清洁消毒时间确定为每24 h一次,对成品输液量较多,药箱使用频繁的临床科室,如新生儿科、产科、儿科,可适当增加转运药箱的清洁消毒频次。重点注意转运药箱接触频繁部位,如药箱把手处的清洁消毒。加强PIVAS工作人员的医院感染管理相关知识培训,强化预防医院感染的意识。当班药师每次回收由临床病区转运回PIVAS的药箱时,在药箱把手处等接触频繁部位表面使用75%乙醇进行消毒,并检查每个药箱表面是否有药液残留及肉眼可见污物等,如发现问题药箱,立即放入待清洁区,不可再继续使用。每月采用荧光标记法抽查转运药箱的清洁消毒情况,并进行微生物监测,做好登记。
PIVAS是临床静脉用药集中调配的重要场所,成品输液的质量直接关系到患者的用药安全[14-17]。作为将成品输液传递于PIVAS洁净区和病区非无菌区域的重要工具,转运药箱是引起成品输液微生物的潜在危险因素,医疗机构应重视其污染情况,制定合理的清洁消毒方法和频次,预防医院感染的发生。
| [1] |
冷萍, 李静, 刘晓英, 等. 精细化管理对静脉用药调配中心医院感染防控的效果[J]. 中国感染控制杂志, 2018, 17(4): 347-350. |
| [2] |
赵德斌, 杨发建, 王长林, 等. 静脉用药调配中心药品瓶口不同消毒方法的对比研究[J]. 现代医药卫生, 2019, 35(12): 1912-1914. DOI:10.3969/j.issn.1009-5519.2019.12.054 |
| [3] |
朱文靖, 邱季. 我院静脉用药调配中心成品输液问题原因分析及对策[J]. 临床医药实践, 2018, 27(9): 694-697, 708. |
| [4] |
邵玲君, 黄秀良. 静脉输液过程中的医院感染控制[J]. 中华医院感染学杂志, 2010, 20(7): 978-979. |
| [5] |
中华人民共和国国家卫生和计划生育委员会. 卫生部办公厅关于印发《静脉用药集中调配质量管理规范》的通知[EB/OL]. (2010-04-23)[2020-04-18]. http://www.nhc.gov.cn/zwgkzt/wsbysj/201004/46963.shtml.
|
| [6] |
张珊红, 兰丽华. 医用消毒湿巾对血透机表面消毒效果的研究[J]. 实用临床护理学电子杂志, 2019, 4(26): 105, 140. |
| [7] |
中华人民共和国国家卫生和计划生育委员会. 医疗机构环境表面清洁与消毒管理规范: WS/T 512-2016[S]. 北京: 中国标准出版社, 2017.
|
| [8] |
中华人民共和国国家质量监督检验检疫总局, 中国国家标准化管理委员会. 医院消毒卫生标准: GB 15982-2012[S]. 北京: 中国标准出版社, 2012.
|
| [9] |
徐萍, 罗建华, 阮大山, 等. 三家医院门急诊环境下输液配置微生物污染情况比较分析[J]. 儿科药学杂志, 2014, 20(6): 47-49. |
| [10] |
穆殿平, 徐彦贵, 杨荣兰, 等. 输液瓶口不同处置方法染菌情况研究[J]. 中国医院药学杂志, 2015, 35(13): 1242-1245. |
| [11] |
孔琳姝, 赵宜男, 郭治伟. 双阀易折式输液袋加药瓶口无覆盖对液体染菌的影响[J]. 中国实用医药, 2019, 14(19): 143-145. |
| [12] |
叶建林, 华燕. 静脉用药调配中心微生物监测分析[J]. 中国医药导报, 2011, 8(35): 166-167. DOI:10.3969/j.issn.1673-7210.2011.35.074 |
| [13] |
邱素红, 薛莲, 刘颖, 等. 配液中心摆药筐清洁消毒方法的对比研究[J]. 中华医院感染学杂志, 2016, 26(23): 5508-5510. |
| [14] |
王雅蘋, 潘淑曼, 林小芳, 等. 两种擦拭消毒方法对静脉用药配置台面消毒效果观察[J]. 中国消毒学杂志, 2018, 35(1): 74-75. |
| [15] |
秦雄妹. 医用消毒湿巾与75%乙醇纱布在物表消毒的效益-成本比较[J]. 抗感染药学, 2017, 14(2): 338-340. |
| [16] |
胡小骞, 吴贻乐, 李若洁, 等. 某医疗机构医护人员工作服细菌污染监测及干预研究[J]. 安徽预防医学杂志, 2020, 26(1): 34-37. |
| [17] |
张国兵, 赵红英, 沈晓飞, 等. 静脉用药调配中心医院感染管理的现状与模式探讨[J]. 中华医院感染学杂志, 2017, 27(12): 2837-2840. |



