随着医疗技术的不断提升,肝癌患者在进行外科切除术后围手术期病死率明显降低[1]。但肝癌切除术后感染仍然是威胁患者生命的重要原因。研究[2-4]表明,患者手术后感染并发症的发生率可超过50%。尤其对于接受肝癌切除术的患者,术后感染对发病率、病死率、住院时间、住院费用和长期治疗效果有显著影响[5]。因此预防术后感染的发生是改善患者临床结局的关键环节。
研究[6-11]表明,患者伴有高龄、超重状态、肝功能状态、低蛋白血症、糖尿病、手术时间长、术中输血和失血、引流时间延长是肝癌外科切除术后患者发生感染的易感因素,其中一些危险因素仍然存在争议。目前可以有效预测肝癌患者外科术后引发感染的方法尚且不足,故探讨相关危险因素,建立肝癌切除术后预测模型对减少围手术期感染发生率,提高肝癌患者外科切除术后生存质量至关重要。
1 对象与方法 1.1 研究对象选取2017年2月—2019年10月苏州大学附属第一医院普通外科收治的施行肝癌外科切除术的患者。纳入标准:(1)年龄18~85岁;(2)接受肝癌外科手术;(3)肝功能Child分级为A或B。排除标准:(1)严重的基础疾病,危害患者生命;(2)围手术期存在感染。本研究经患者或家属知情同意,且经医院伦理委员会审核批准。
1.2 研究方法采用回顾性研究方法,调查内容包括患者的性别、年龄、糖尿病、ASA评分、手术相关信息、实验室检查、术后引流情况等。收集术后感染患者的相关信息,包括发热、术后放射性诊断、实验室检查、引流液的性状、切口周围情况等。ASA评分由临床经验丰富的麻醉医生在手术前进行评定。
1.3 诊断标准本研究中,肝癌患者外科切除术后的感染分别为肺部感染、手术部位感染、腹腔感染及泌尿系统感染。医院感染诊断标准参照2001年卫生部颁发的《医院感染诊断标准(试行)》[12]判定。
1.4 模型验证另选取2020年1—6月100例施行肝癌外科切除患者建立验证组,将验证组的数据代入构建的风险评分模型中生成相应分值,利用ROC的曲线下面积(AUC)评价模型的判别效度。
1.5 统计学方法应用SPSS 19.0软件对数据进行分析,计量资料采用x±s表示,计数资料采用例数和百分比表示,单因素分析采用χ2检验,logistic回归方程构建风险预测模型,利用ROC的AUC评价模型预测效果。P≤0.05为差异有统计学意义。
2 结果 2.1 患者一般情况共纳入患者310例,其中男性249例,女性61例,年龄33~82岁,平均年龄(57.02±10.62)岁。外科手术后发生医院感染45例,医院感染发病率为14.52%。手术部位感染15例(占33.33%),肝周围感染12例(占26.67%),其他远处部位感染18例(占40.00%)。
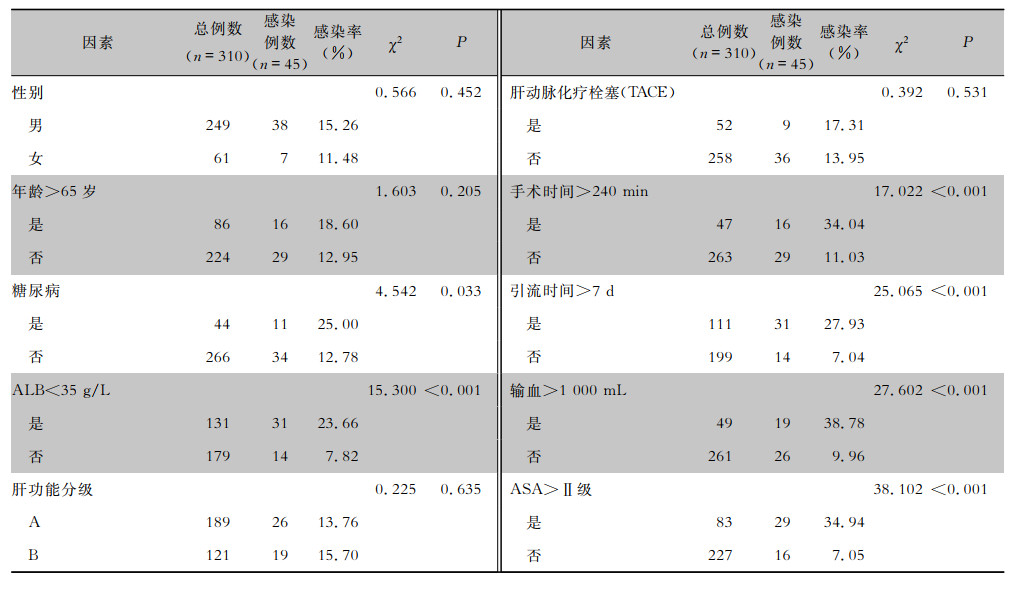
2.2 肝癌患者外科切除术后感染的危险因素分析 2.2.1 单因素分析将可能影响患者术后发生感染的危险因素进行单因素分析,结果显示糖尿病、血清清蛋白(ALB)<35 g/L、手术时间>240 min、引流时间>7 d、输血>1 000 mL、ASA>Ⅱ级是肝癌患者发生术后感染的危险因素。见表 1。
| 表 1 肝癌患者外科切除术后感染危险因素单因素分析 Table 1 Univariate analysis on HAI in liver cancer patients after hepatectomy |
|
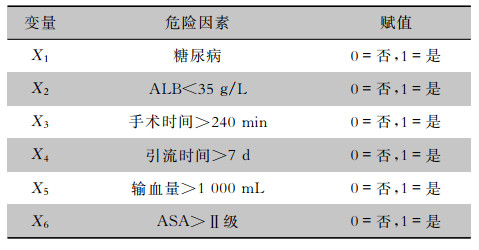
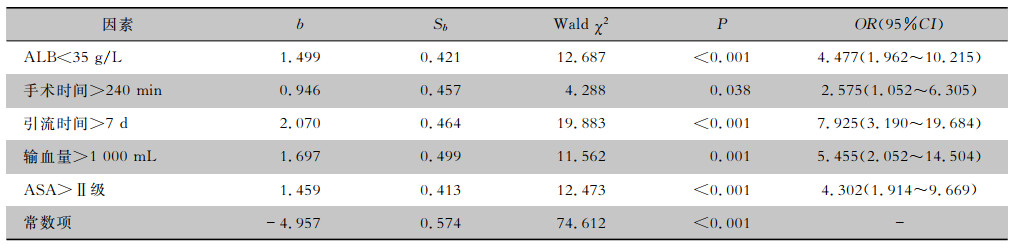
将上述单因素分析中P<0.05的因素代入多因素logistic回归分析(前进法),赋值见表 2。结果显示ALB<35 g/L、手术时间>240 min、引流时间>7 d、输血量>1 000 mL、ASA>Ⅱ级是肝癌患者外科切除术后感染的独立危险因素,见表 3。回归方程为:logitP=-4.957+0.605X1+1.499X2+0.946X3+2.070X4+1.697X5+1.459X6。
| 表 2 肝癌患者外科切除术后感染的危险因素赋值表 Table 2 Assignment of risk factors for post-operative infection in liver cancer patients after hepatectomy |
|
| 表 3 肝癌患者外科切除术后感染危险因素多因素分析 Table 3 Multivariate analysis on liver cancer patients after hepatectomy |
|
似然比χ2值(likelihood ratio chi-square)=90.455,P<0.001,表示该logistic回归模型具有统计学意义。Wald检验(χ2=120.934,P<0.001),表示该logistic回归方程的系数具有统计学意义。
2.3.2 对logistic回归模型进行拟和优度检验本研究采用Hosmer-Lemeshow检验进行模型的拟和优度检验,结果显示模型拟和良好(χ2=6.057,P=0.417)。
2.3.3 ROC曲线对肝癌患者外科切除术后感染风险预测模型的效果分析绘制ROC曲线,并计算ROC的AUC,根据AUC来评价该模型的判别能力。本研究AUC为0.904,95%CI为0.864~0.944,可以认为此模型具有较好的判别效果。Youden指数最大值为该预测模型的最佳临界值,本研究Youden指数为0.655,灵敏度为0.889,特异度为0.766。见图 1。
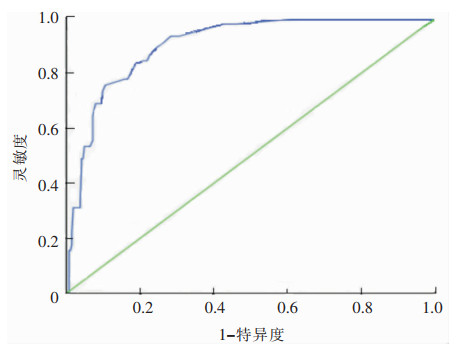 |
| 图 1 logistic回归模型ROC曲线图 Figure 1 ROC curve of logistic regression model |
另选取2020年1—6月施行肝癌外科切除术的患者100例建立验证组,代入前期成功建模的公式,以相同的方法绘制ROC曲线,结果显示AUC为0.930,Sb为0.024,95%CI为0.90~1.05,见图 2。提示已建立的风险评分模型在验证组同样具有较好的判别效度。
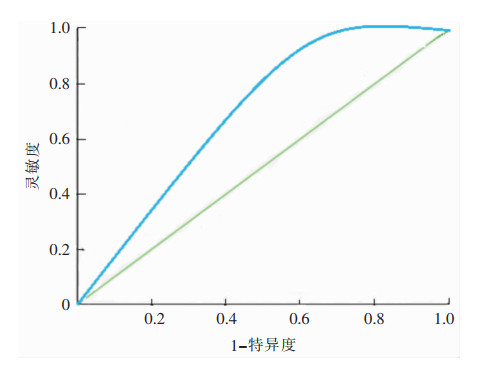 |
| 图 2 ROC曲线评价风险评分模型的判别效度 Figure 2 Discriminant validity of risk scoring model evaluated by ROC curve |
目前,治疗肝癌最有效的手段是手术切除,但相关研究[3, 7, 13-14]表明,肝癌患者术后手术切口感染(SSI)的发生率为2.1%~19.1%,严重影响患者的预后。本研究中肝癌患者外科切除术后感染发生率为14.52%。尽管SSI不可能降低为0,但目前SSI仍然是患者生命质量的重要威胁。本次研究目的是通过建立预测模型有效识别感染风险系数较高的患者,医务人员可改变治疗方法来有效预防患者术后感染,减轻患者痛苦,降低医疗成本。
本研究多因素分析结果表明,肝癌患者外科切除术后发生感染的独立危险因素为低蛋白血症(ALB<35 g/L)、手术时间>240 min、引流时间>7 d、输血量>1 000 mL、ASA评分>Ⅱ级。
低蛋白血症患者是营养不良和肝功能不全的重要标志,肝癌患者常伴有低蛋白血症。研究[15-16]表明,低蛋白血症对肝癌患者的发病率和病死率有很大的预测价值,分析原因可能与手术部位胶原合成减少和肉芽组织形成导致的组织愈合受损有关,也可能与低蛋白血症导致组织水肿,引发手术部位灌注不足[17-18]。此外,渗透压降低、手术部位液体积聚为细菌的生长繁殖提供培养基[19]。因此,肝癌患者在施行外科切除术前,应加强围手术期护理,提高营养支持,提高血清蛋白水平,减少术后感染的发生。
本研究表明,ASA评分越高,患者术后感染的发生率越高,与相关研究[15]结果一致。ASA分级是美国麻醉医师协会根据患者体质和对手术危险性进行分类的系统。ASA评分越高,患者术前基础条件越差,手术和麻醉危险程度越高,术后发生并发症的概率越大。手术时间越长,患者术后感染发生率越高[20-21]。手术时间反映手术的复杂程度,手术时间越长,切口和组织暴露的时间越长,被细菌污染的概率增加。术中大量输血会使体内循环血量急剧增加,造成酸碱平衡紊乱,且输入异体血液制品,容易诱发免疫反应,激活中性粒细胞,释放炎性因子,从而引起肺损伤。肝癌患者自身营养条件较差,容易发生肺水肿,从而增加感染风险[9]。
肝癌患者行肝切除术后切口创面大,渗出液多,需常规放置引流管进行引流。引流期间如引流量过多或引流液较黏稠时,易导致引流管堵塞或引流时间延长,增加患者感染风险[22-23]。医护人员应加强导管留置期间的护理,尽早拔除不必要的导管。
logistic回归模型是一种概率型的广义线性回归模型,其对相关研究样本资料的要求较少,既不要求研究的样本数据类型符合正态分布,也不要求自变量符合正态分布,现已应用于医院感染防控相关的许多研究中。本研究以患者相关因素为自变量,以是否发生感染为因变量构建回归模型,使用AUC大小对模型的判别效果进行评价。ROC曲线结合综合灵敏度和特异度两个指标,全面、客观评价模型判别准确性。通过模型整体的判别分析,本研究logistic风险预测模型ROC的AUC为0.904,95%CI为0.864~0.944,表明此logistic回归模型判别能力良好。
通过危险因素建立预测模型,可以有效筛选发生术后感染的高危人群,提醒临床医务人员加强围手术期护理,术前改善患者自身营养情况,术中提升团队配合能力,缩短手术时间,减少输血,术后及时反馈,拔除不必要的导管,最大程度降低感染风险,提高肝癌患者生存质量。
| [1] |
Khan AS, Garcia-Aroz S, Ansari MA, et al. Assessment and optimization of liver volume before major hepatic resection: current guidelines and a narrative review[J]. Int J Surg, 2018, 52: 74-81. DOI:10.1016/j.ijsu.2018.01.042 |
| [2] |
Garwood RA, Sawyer RG, Thompson L, et al. Infectious complications after hepatic resection[J]. Am Surg, 2004, 70(9): 787-792. |
| [3] |
Uchiyama K, Ueno M, Ozawa S, et al. Risk factors for postoperative infectious complications after hepatectomy[J]. J Hepatobiliary Pancreat Sci, 2011, 18(1): 67-73. DOI:10.1007/s00534-010-0313-1 |
| [4] |
Sadamori H, Yagi T, Shinoura S, et al. Risk factors for major morbidity after liver resection for hepatocellular carcinoma[J]. Br J Surg, 2013, 100(1): 122-129. |
| [5] |
Haruki K, Shiba H, Fujiwara Y, et al. Negative impact of surgical site infection on long-term outcomes after hepatic resection for colorectal liver metastases[J]. Anticancer Res, 2013, 33(4): 1697-1703. |
| [6] |
Moreno Elola-Olaso A, Davenport DL, Hundley JC, et al. Predictors of surgical site infection after liver resection: a multicentre analysis using national surgical quality improvement program data[J]. HPB (Oxford), 2012, 14(2): 136-141. DOI:10.1111/j.1477-2574.2011.00417.x |
| [7] |
Yang T, Tu PA, Zhang H, et al. Risk factors of surgical site infection after hepatic resection[J]. Infect Control Hosp Epidemiol, 2014, 35(3): 317-320. DOI:10.1086/675278 |
| [8] |
胡兴龙, 王胜智, 吴敏良, 等. 原发性肝癌患者术后医院感染病原学特点及危险因素分析[J]. 中华医院感染学杂志, 2017, 27(20): 4588-4591. |
| [9] |
刘清, 惠永丰, 卜稳平, 等. 肝癌患者肝部分切除术后感染相关因素分析[J]. 中华医院感染学杂志, 2017, 27(16): 3719-3721. |
| [10] |
Kurmann A, Wanner B, Martens F, et al. Hepatic steatosis is associated with surgical-site infection after hepatic and colorectal surgery[J]. Surgery, 2014, 156(1): 109-116. DOI:10.1016/j.surg.2014.02.020 |
| [11] |
Nanashima A, Arai J, Oyama S, et al. Associated factors with surgical site infections after hepatectomy: predictions and countermeasures by a retrospective cohort study[J]. Int J Surg, 2014, 12(4): 310-314. DOI:10.1016/j.ijsu.2014.01.018 |
| [12] |
中华人民共和国卫生部. 医院感染诊断标准(试行)[J]. 中华医学杂志, 2001, 81(5): 314-320. DOI:10.3760/j:issn:0376-2491.2001.05.027 |
| [13] |
Okabayashi T, Nishimori I, Yamashita K, et al. Risk factors and predictors for surgical site infection after hepatic resection[J]. J Hosp Infect, 2009, 73(1): 47-53. DOI:10.1016/j.jhin.2009.04.022 |
| [14] |
吴增华, 徐艳, 胡倩倩, 等. 运用风险评估方法降低重症医学科医院感染发病率[J]. 中国感染控制杂志, 2019, 18(3): 238-242. |
| [15] |
Kokudo T, Uldry E, Demartines N, et al. Risk factors for incisional and organ space surgical site infections after liver resection are different[J]. World J Surg, 2015, 39(5): 1185-1192. DOI:10.1007/s00268-014-2922-3 |
| [16] |
王莹, 邓澜, 谈宜斌, 等. 基于风险矩阵的重症医学科医院感染风险评估指标体系[J]. 中国感染控制杂志, 2018, 17(10): 913-917. |
| [17] |
Ward MW, Danzi M, Lewin MR, et al. The effects of subclinical malnutrition and refeeding on the healing of experimental colonic anastomoses[J]. Br J Surg, 1982, 69(6): 308-310. |
| [18] |
Testini M, Margari A, Amoruso M, et al. The dehiscence of colorectal anastomoses: the risk factors[J]. Ann Ital Chir, 2000, 71(4): 433-440. |
| [19] |
Runyon BA. Low-protein-concentration ascitic fluid is predisposed to spontaneous bacterial peritonitis[J]. Gastroenterology, 1986, 91(6): 1343-1346. DOI:10.1016/0016-5085(86)90185-X |
| [20] |
胡森懋, 李善平, 卢菊芳, 等. 直肠癌患者术后切口感染的相关危险因素分析[J]. 中华医院感染学杂志, 2016, 26(17): 4026-4028. |
| [21] |
Ogihara S, Yamazaki T, Inanami H, et al. Risk factors for surgical site infection after lumbar laminectomy and/or discectomy for degenerative diseases in adults: a prospective multicenter surveillance study with registry of 4027 cases[J]. PLoS One, 2018, 13(10): e0205539. DOI:10.1371/journal.pone.0205539 |
| [22] |
李辉, 于淼, 刘成科, 等. 肝癌患者肝脏部分切除术后感染的影响因素分析[J]. 中华医院感染学杂志, 2017, 27(24): 5611-5614. |
| [23] |
王煜, 王锋, 张爱芸, 等. 肝癌肝切除术后感染的病原学特征与影响因素分析[J]. 中国普通外科杂志, 2019, 28(6): 762-767. |



