磺胺类抗菌药物是指具有对氨基苯磺酰胺结构的一类药物的总称,是现代医学中常用的一类抗菌药物。临床研究表明,磺胺类药物在体内的代谢时间较长,长期使用可能在人体中蓄积,导致人体机能损害,可诱使病原体产生抗药性[1]。另外,磺胺类药物半衰期较短,但由于频繁地被使用并进入环境,形成环境中抗生素的“假持续”现象,对人体安全及整个生态系统构成了长期潜在风险[2 – 3]。为探讨人体内磺胺类抗生素的暴露状况及其对人群健康影响,需建立相应的分析技术来测量人体内抗生素残留的内暴露剂量[4 – 5]。目前,磺胺类药物检测研究主要集中在食品样品[6 – 7] 和环境样品[8 – 9],方法包括光谱法[10]、化学发光法[6]、高效液相色谱法(high performance liquid chromatography,HPLC)[11]、高效液相色谱 – 串联质谱法(high performance liquid chromatography tandem mass spectrometry,HPLC/MS/MS) [7 – 8]及超临界流体色谱法(supercritical fluid chro-matography,SFC)[12] 等。本研究采用固相萃取技术结合超高效液相色谱 – 串联质谱(ultra-performance liquid chromatography/tandem mass spectrometry,UPLC/MS/MS),拟建立一种同时检测尿液中16 种磺胺类抗菌药物的分析方法,旨在为磺胺类抗生素的暴露特征和污染现状,评估其对人群的潜在危害提供技术支撑。结果报告如下。
1 材料与方法 1.1 主要仪器与试剂超高效液相色谱仪、XEVO-TQD四极杆串联质谱仪、BEH C18色谱柱(美国Waters公司);超纯水仪(美国Millipore公司);EXTRA全自动固相萃取仪(上海屹尧仪器科技发展有限公司);水浴氮吹仪(美国Organomationg公司);Oasis PRiME HLB(200 mg、6 mL)固相萃取柱(美国Waters公司)。甲醇、乙腈、乙酸铵均为色谱纯(德国Merck公司);无水硫酸氢二钠、磷酸二氢钾(上海国药集团化学试剂有限公司):乙二胺四乙酸四钠盐(ethylenediaminetetraacetic acid,EDTA)(上海阿拉丁生化科技股份有限公司);β – 葡糖苷酸酶(helix pomatia),含 β – 葡糖苷酸酶 ≥ 100 000单位/mL(美国Sigma公司);16种磺胺混合标准:磺胺醋酰(sulfacetamide)、磺胺嘧啶(sulfadiazine)、磺胺甲噻二唑(sulfamethizole)、磺胺二甲异恶唑(sulfisoxazole)、磺胺噻唑(sulfathiazole)、磺胺甲基异恶唑(sulfamethoxazole)、磺胺氯哒嗪(sulphachlorpyridazine)、磺胺甲基嘧啶(sulfamerazine)、磺胺吡啶(sulfapyridine)、磺胺间甲氧嘧啶(sulfamonomethoxine)、磺胺对甲氧嘧啶(sulfameter)、磺胺邻二甲氧嘧啶(sulfadoxine)、磺胺甲氧哒嗪(sulfamethoxypyridazine)、磺胺二甲嘧啶(sulfamethazine)、磺胺苯吡唑(sulfaphenazole)、磺胺间二甲氧嘧啶(sulfadimethoxine)(100 mg/mL)(美国o2si公司)。
1.2 液相色谱条件色谱柱:Waters BEH C18(2.1 × 100 mm,1.7 μm),流动相:母液,1 mol/L乙酸铵溶液pH = 5;A:母液稀释100倍水溶液;B:母液稀释100倍甲醇溶液,梯度洗脱:0到0.25 min,2 % B;0.25到12.25 min,2 % B升至99 % B;12.25 min到13.00 min,99 % B;13.00到13.01 min,99 % B到2 % B;13.01到15 min,2 % B,流速:0.45 mL/min,柱温:35 ℃,进样量:10 μL。
1.3 质谱条件(表1)| 表 1 16种化合物的MRM方法参数及参考保留时间 |
离子源:ESI+,采集方式:多反应监测模式(MRM),毛细管电压:3.0 kV,离子源温度:150 ℃,脱溶剂气温度:600 ℃,脱溶剂气流速:1 000 L/h,锥孔气:50 L/h。
1.4 样品前处理 1.4.1 酶消解提取准确量取1.00 mL尿液样品,加入0.5 mL磷酸盐缓冲溶液(pH = 6.5)、10 μL β – 葡糖苷酸酶,震荡混匀后37 ℃恒温水浴过夜。
1.4.2 固相萃取净化在提取液中加入若干盐酸,调节样品pH = 2,然后加入20 mg EDTA,混匀,固相萃取净化。Oasis PRiME HLB(200 mg、6 mL)固相萃取柱经20 mL甲醇,6 mL水,6 mL pH = 2的水依次活化(注意保证小柱不干),将上述样品提取液转入活化好的固相萃取柱,流速为1 mL/min,然后用10 mL水清洗小柱(洗去EDTA),干燥10 min后,用5 mL甲醇以2 mL/min洗脱,收集全部洗脱液,氮气吹至近干,用液相流动相(A液:B液为9:1)定容至1.0 mL,旋涡混匀后,过0.22 μm滤膜,上机测定。
2 结果与讨论 2.1 液相色谱-质谱条件优化 2.1.1 液相色谱条件优化分别比较了常用溶剂水、甲醇、乙腈、甲酸和乙酸铵等不同配比的流动相体系及其梯度对磺胺类抗生素离子化及分离度的影响,结果表明,分别含0.01 mol/L乙酸铵的甲醇-水作为流动相,以优化好的梯度洗脱条件,16种磺胺类抗生素可以获得良好的分离效果及质谱响应,各组分保留时间在0.75~4.42 min。
2.1.2 质谱条件优化(图1)
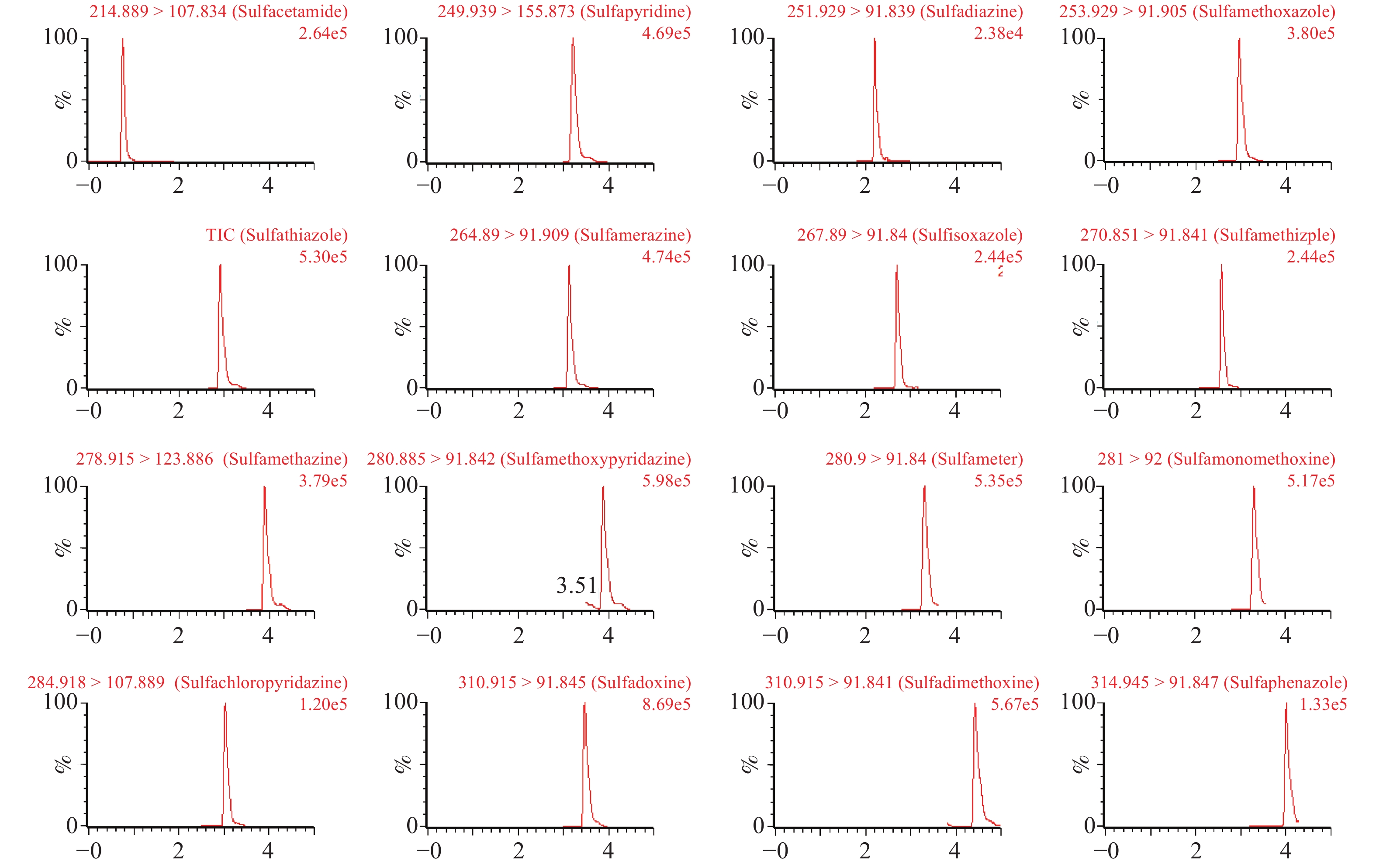
|
图 1 加标浓度为100 ng/mL的16种磺胺类抗菌药物的MRM色谱图 |
磺胺类抗生素具有仲氨基或叔氨基的化学电离性质,在ESI源的正离子化模式下电离,可获得较高丰度的[M+H]+母离子。在ESI+模式下分别对16种磺胺类抗生素的单标准溶液采用仪器工作站Masslynx附带的MS Tune及Intellistart方式进行质谱条件优化。
2.2 提取条件优化尿液中所含磺胺类抗生素与葡萄糖醛酸结合形成葡萄糖醛酸甙缀合物,需经酶水解处理,使其游离释放后再行提取。分别比较 β – 葡糖苷酸酶水解尿样时所需温度、时间、用量及pH等条件,结果表明,在pH = 6.5、37 ℃环境中,10 μL β – 葡糖苷酸酶水解尿样12 h以上,样品中各组分可以完全释放。
2.3 固相萃取条件优化 2.3.1 pH影响分别在pH = 2、4、7、9、12的溶液环境下萃取各组分的回收率,结果显示,16种抗生素中,磺胺醋酰、磺胺嘧啶、磺胺甲噻二唑、磺胺二甲异恶唑、磺胺噻唑、磺胺甲基异恶唑、磺胺氯哒嗪、磺胺甲基嘧啶、磺胺间甲氧嘧啶、磺胺对甲氧嘧啶、磺胺邻二甲氧嘧啶、磺胺甲氧哒嗪12个化合物在碱性条件几乎检测不到,酸性条件下才有响应,磺胺吡啶、磺胺二甲嘧啶、磺胺苯吡唑、磺胺间二甲氧嘧啶4个化合物在碱性条件下也有明显响应,但其回收率也小于酸性条件,16种抗生素在pH = 2条件下萃取,回收率均为最佳。
2.3.2 EDTA用量影响尿样中金属离子能与磺胺类抗生素形成络合物,干扰固相萃取,降低萃取效率,为抑制其干扰,需在样品中加入EDTA。分别加入0、5、10、20 mg EDTA时,结果显示,加入20 mg EDTA,各组分的回收率最大。
2.3.3 SPE小柱、洗脱溶剂用量影响Oasis PRiME HLB固相萃取小柱,能够去除蛋白、盐等95 %以上的基质干扰物。为保证洗脱完全,且避免杂质干扰过大,选择甲醇作为洗脱剂。不同洗脱体积(2、3、4、5、10 mL)回收率结果显示,洗脱溶剂大于5 mL时,化合物回收率升高并不明显。
2.3.4 上机前定容溶剂影响最终上机前定容溶剂对部分磺胺类抗生素的保留时间有影响,使用甲醇 – 水(1 : 1)定容时,磺胺醋酰的保留时间偏离很大,而使用液相流动相(A液 : B液为9 : 1)定容,尿液样品中各组分的保留时间未发生变化。
2.4 线性范围、检出限、定量限(表2)| 表 2 16种磺胺类抗生素回收率、精密度和检出限(n = 6) |
取16种磺胺混合标准,用空白样品提取液配制浓度为0、5、10、50、100、500、1 000 ng/mL基质混合标准工作溶液,用峰面积对标准溶液中各被测组分的浓度绘制工作曲线。结果显示,16种磺胺抗生素的浓度在5~1 000 ng/mL范围内时,线性关系良好,相关系数(r)均 > 0.99。在标准添加的最低质量浓度点5 ng/mL,16种磺胺类抗生素的信噪比(S/N)均大于10,并且具有较好的回收率,确定各组分的定量限为5 ng/mL;以信噪比为3估算检出限,16种磺胺的检出限为0.3~1.7 ng/mL。选用母乳喂养的新生儿尿液,分别添加10、100和500 ng/mL的16种磺胺类抗生素混合标准溶液,按前述方法处理样品,液相色谱 – 质谱测定并计算其回收率和精密度,结果见 表2。
3 小 结本研究所建立的同时测定尿液中16种磺胺类抗生素残留的固相萃取 – 超高效液相色谱 – 串联质谱(solid-phase extraction (SPE)- UPLC-MS/MS)方法准确度和精密度较高,定性确证准确,并且整个实验流程较简单、快速,适用于尿液中多种痕量磺胺类抗菌药物残留量的同时测定。
| [1] | 李俊锁, 邱月明, 王超. 兽药残留分析[M]. 上海: 上海科学技术出版社, 2002: 228-229. |
| [2] | Golet EM, Xifra I, Siegrist H, et al. Environmental exposure assessment of fluoroquinolone antibacterial agents from sewage to soil[J]. Environ Sci Teehno1, 2003, 37(15): 3243–3249. DOI:10.1021/es0264448 |
| [3] | Brown KD. Pharmaceutically active compounds in residential and hospital effluent, municipal wastewater, and the Rio Grande in Albuquerque, New Mexico. Water Resources Program [R]. Publication No. W RP-9, 2004: 1-56. |
| [4] | Tuerk J, Reinders M, Dreyer D, et al. Analysis of antibiotics in urine and wipe sample from environmental and biological monitoring – comparison of HPLC with UV-, single MS- and tandem MS-detection[J]. Journal of Chromatography B, 2006, 831(1 – 2): 72–80. DOI:10.1016/j.jchromb.2005.11.030 |
| [5] | Cazorla-Reyes R, Romero-González R, Frenich AG, et al. Simul-taneous analysis of antibiotics in biological samples by ultra high performance liquid chromatography-tandem mass spectrometry[J]. Journal of Pharmaceutical and Biomedical Analysis, 2014, 89(4): 203–212. |
| [6] | 代婷婷, 林华萍, 段婕, 等. 毛细管区带电泳化学发光法测定食品中残留的磺胺类药物[J]. 分析化学, 2016, 44(05): 747–753. |
| [7] | 孟哲, 石志红, 吕运开, 等. 超高效液相色谱-高分辨四级杆飞行时间质谱法快速筛查乳制品中磺胺类与氟喹诺酮类药物[J]. 分析化学, 2014, 42(10): 1493–1500. DOI:10.11895/j.issn.0253-3820.140299 |
| [8] | 李晓晶, 黄聪, 于鸿, 等. 土壤中11种磺胺类兽用抗生素的超高效液相色谱 – 串联质谱测定法[J]. 环境与健康杂志, 2013, 30(05): 437–439. |
| [9] | 周爱霞, 苏小四, 高松, 等. 高效液相色谱测定地下水、土壤及粪便中4种磺胺类抗生素[J]. 分析化学, 2014, 42(03): 397–402. |
| [10] | 潘乐. 微波消解 – 原子吸收光谱法测定药品中的磺胺甲恶唑[J]. 光谱实验室, 2012, 29(06): 3662–3665. DOI:10.3969/j.issn.1004-8138.2012.06.088 |
| [11] | 欧阳燕玲, 谢维平, 黄盈煜, 等. 动物源食品磺胺类药物残留GPC法测定[J]. 中国公共卫生, 2009, 25(05): 610–611. DOI:10.3321/j.issn:1001-0580.2009.05.070 |
| [12] | 陈海, 李胜迎, 刘大伟, 等. 新型超临界流体色谱仪在磺胺药物分析中的应用研究[J]. 重庆科技学院学报: 自然科学版, 2017, 19(06): 68–71. |
 2019, Vol. 35
2019, Vol. 35


